патфиз ответы. 1. Патофизиология, задачи и методы ее изучения. Патофизиология, как теоретическая и методологическая база современной клинической медицины
 Скачать 0.63 Mb. Скачать 0.63 Mb.
|
|
Признаки: местные (покраснение, припухлость, жар, боль, нарушение ф-ций) и общие (лихорадка, увелич СОЭ, лейкоцитоз, изменение белков плазмы) Воспаление – это процесс, который проявляется не только ярко выраженными местными признаками, но и весьма характерными и нередко существенными изменениями во всем организме. Из факторов, обусловливающих взаимосвязь местных и общих изменений при воспалении, наряду с образующимися и циркулирующими в крови аутокоидами (кинины, цитокины, компоненты системы комплемента, простагландины, интерфероны и др.), большое значение имеют так называемые реактанты “острой фазы”. Эти вещества неспецифичны для воспаления, они появляются после разнообразных повреждений тканей, в том числе после повреждения при воспалении. Наибольшее значение из них имеют С-реактивный белок, a2-макроглобулин, a1 - гликопротеид, гаптоглобин, трансферрин, аппоферритин. Большинство реактантов «острой фазы» синтезируются макрофагами, гепатоцитами и другими клетками. 44. Фагоцитоз и воспаление. Барьерная роль воспалительной реакции (И.И.Мечников). Эмигрирующие лейкоциты участв в синтезе БАВ, а так же в фагоцитозе. Фагоцитоз – защитно-приспособит р-ция орг, закл в разрушении м/о, поврежд кл-ок и инородных частиц. Фагоцитарной активностью обладают нейстрофилы, лимфоциты, моноциты, тканевые макрофаги. Стадии: хемотаксис, адгезия, активация мембраны, образование фагосомы, лизис, выброс продуктов деградации. Воспаление является своеобразным биологическим и механическим барьером, при помощи которого обеспечиваются локализация и элиминация флогогена и (или) поврежденной им ткани и ее восстановление или же возмещение тканевого дефекта. Свойства биологического барьера достигаются путем адгезии, умерщвления и лизиса бактерий, деградации поврежденной ткани. Функция механического барьера осуществляется за счет выпадения фибрина, свертывания лимфы в очаге, блокады кровеносных и лимфатических сосудов, размножения соединительнотканных клеток на границе поврежденной и нормальной ткани (демаркация). Все это препятствует всасыванию и распространению микробов, токсинов, продуктов нарушенного обмена и распада.
Воспалительный очаг выполняет не только барьерную, но и дренажную функцию: с экссудатом из крови в очаг выходят продукты нарушенного обмена, токсины. Как уже указывалось, воспаление влияет на формирование иммунитета. 45. Медиаторы воспаления. Классификация. Влияние медиаторов на воспалительный процесс. Медиаторы воспаления различаются 1) по времени их активности: ранние и поздние; 2) по точке приложения: влияющие на сосуды или на клетки и 3) по происхождению: гуморальные (плазменные) и клеточные. Источниками медиаторов воспаления могут быть белки крови и межклеточной жидкости, все клетки крови, клетки соединительной ткани, нервные клетки, неклеточные элементы соединительной ткани. Различают преформированные и вновь образующиеся медиаторы. Преформированные медиаторы синтезируются постоянно без всякого повреждения, накапливаются в специальных хранилищах и высвобождаются немедленно после повреждения (например - гистамин). Синтез других медиаторов начинается после повреждения, как ответная мера. Такие медиаторы называются вновь образующимися (например простагландины). Повреждение ткани сопровождается активацией специальных протеолитических систем крови, что ведет к появлению в очаге воспаления различных пептидов, выполняющих роль медиаторов воспаления. Вазоактивные кинины образуются так же при активации фибринолитической системы активированным фактором Хагемана, который превращает циркулирующий в крови неактивный плазминоген в активный фермент плазмин. Плазмин расщепляет фибрин (а своевременное переваривание фибрина необходимо для успешного заживления ран). При этом образуются пептиды, способные расширять сосуды и поддерживать увеличенную сосудистую проницаемость. Плазмин активирует систему комплемента. Система комплемента, включающая около 20 различных белков, активируется кроме фактора Хагемана еще двумя путями: классическим - это комплекс антиген-антитело и альтернативным - это липополисахариды микробных клеток. В воспалении участвуют С3а и С5а компоненты комплемента, которые опсонизируют и лизируют бактерии, вирусы и патологически измененные собственные клетки; способствуют дегрануляции тучных клеток и базофилов с высвобождением медиаторов. Компоненты комплемента вызывают также адгезию, агрегацию и дегрануляцию клеток крови, выход лизосомальных ферментов, образование свободных радикалов, ИЛ-1, стимулируют хемотаксис, лейкопоэз и синтез иммуноглобулинов. Медиаторы плазменного и клеточного происхождения взаимосвязаны и действуют по принципу аутокаталитической реакции с обратной связью и взаимным усилением. 46. Понятие о лихорадке, этиология и патогенез. Лихорадка (от лат. febris) - типовой патологический процесс, характеризующийся активной задержкой тепла в организме вследствие смещения на более высокий уровень «установочной точки» центра теплорегуляции под действием пирогенных факторов. В 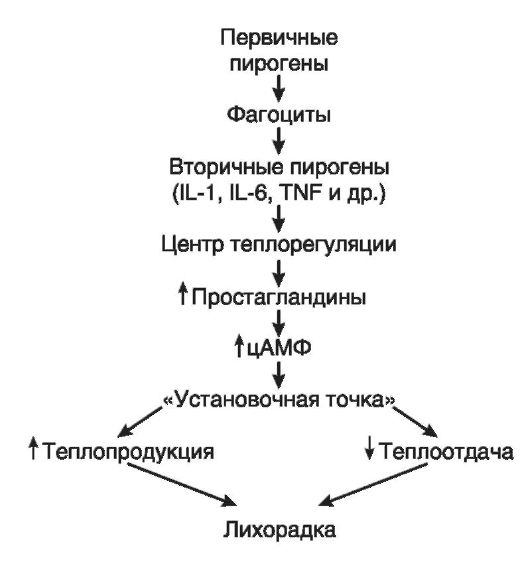 процессе возникновения и развития лихорадки основная роль отводится так называемым пирогенным веществам (от греч. pyros - огонь, pyretos - жар). Они подразделяются на первичные и вторичные. Первичный пироген - это главный этиологический фактор для развития лихорадки, а вторичный пироген - это основное звено патогенеза лихорадки. процессе возникновения и развития лихорадки основная роль отводится так называемым пирогенным веществам (от греч. pyros - огонь, pyretos - жар). Они подразделяются на первичные и вторичные. Первичный пироген - это главный этиологический фактор для развития лихорадки, а вторичный пироген - это основное звено патогенеза лихорадки.Инфекционные пирогены основном представляют собой термостабильные липополисахариды бактериальных мембран. При неинфекционной лихорадке первичными пирогенами являются продукты распада нормальных и патологически измененных тканей и лейкоцитов, иммунные комплексы, фрагменты комплемента. Первичные пирогены, как инфекционные, так и неинфекционные, сами по себе не могут вызвать характерную для лихорадки перестройку теплорегуляции. Их действие опосредуется через образование вторичных пирогенов, которые в состоянии такую перестройку вызвать. Образование вторичных пирогенов является основным патогенетическим фактором в развитии лихорадки независимо от вызывающей ее причины. Свойствами вторичных пирогенов обладают IL-1 и IL-6, фактор некроза опухолей (TNF) α; менее выраженное пирогенное действие оказывают интерферон, катионные белки и гранулоцитарномакрофагальный колониестимулирующий фактор (ГМ-КСФ). Цепь патогенеза лихорадки: 1) внедрение экзогенных пирогенов в организм, 2) взаимодействие экзопирогенов с фагоцитами организма, 3) активация фагоцитов, 4) выделение активированными фагоцитами эндопирогенов - ИЛ-1, 5) воздействие ИЛ-1 на центр терморегуляции (в 1-ю очередь на термоустановочную точку), 6) повышение возбудимости холодочувствительных нейронов и снижение возбудимости теплочувствительных нейронов, 7) индукция усиленного синтеза простагландина Е2 в нервных клетках гипоталамуса и возбуждение симпатоадреналовых структур, 8) ограничение теплоотдачи (за счет спазма поверхностных сосудов) и повышение теплопродукции, 9) повышение температуры тела до нового уровня регулирования. 4 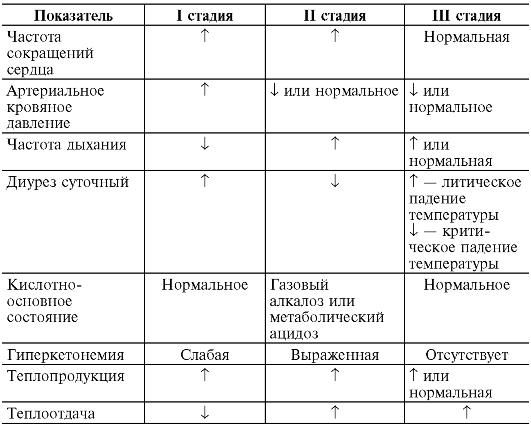 7.Стадии лихорадки, отношение между теплопродукцией и теплоотдачей в каждую из них. Изменение функции органов и систем при лихорадке. 7.Стадии лихорадки, отношение между теплопродукцией и теплоотдачей в каждую из них. Изменение функции органов и систем при лихорадке.Стадии лихорадки: 1) Stadium incrementi - стадия подъема температуры тела – характ ознобом (спазм сосудов кожи и пониж темп кожи на 10-12 гр, что вызыв разждраж холод рец и ответную р-цию на холод – дрожь) – повышение теплопродукции и понижение теплоотдачи 2) Stadium fastigii - стадия стояния высокой температуры – характ жаром – равновесие между теплоотдачей и теплопродукцией 3) Stadium decrementi - стадия снижения температуры и возврат ее к норме – характ обильным потоотделением – повышение теплоотдачи и понижение теплопродукции: критическое(резкое снижение) и литическое(постепенное) <----Изменение ф-ции органов и систем 48. Классификация лихорадки по степени подъема температуры. Виды температурных кривых. В зависимости от продолжительностилихорадка может быть эфемерной (1-3 дня), острой (до 15 дней), подострой (до 1,5 месяца) и хронической (более 1,5 месяца). По степени подъематемпературы различают лихорадку субфебрильную (37,1-37,9 °С), умеренную (38-39,5 °С), высокую (39,6- 40,9 °С) и гиперпиретическую (41 °С и выше). Последний вид лихорадки наблюдается, в частности, при столбняке и менингите. Температурыне кривые 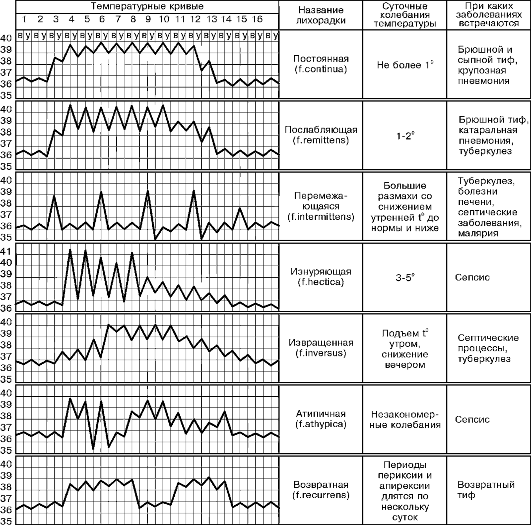 49. Роль воспаления и лихорадки в инфекционном процессе. Биологическое значение лихорадки - в основном создание более высокого температурного фона для обменных процессов, что ведет к повышению уровня защитных реакций: 1) активирование ферментов, 2) усиление фагоцитоза. Известно, что биохимические процессы протекают значительно быстрее при температуре 39 градусов, чем при 36. Это одна из приспособительных реакций организма Воспаление является своеобразным биологическим и механическим барьером, при помощи которого обеспечиваются локализация и элиминация флогогена и (или) поврежденной им ткани и ее восстановление или же возмещение тканевого дефекта. Свойства биологического барьера достигаются путем адгезии, умерщвления и лизиса бактерий, деградации поврежденной ткани. Функция механического барьера осуществляется за счет выпадения фибрина, свертывания лимфы в очаге, блокады кровеносных и лимфатических сосудов, размножения соединительнотканных клеток на границе поврежденной и нормальной ткани (демаркация). Все это препятствует всасыванию и распространению микробов, токсинов, продуктов нарушенного обмена и распада.
Воспалительный очаг выполняет не только барьерную, но и дренажную функцию: с экссудатом из крови в очаг выходят продукты нарушенного обмена, токсины. Как уже указывалось, воспаление влияет на формирование иммунитета. 50. Определения понятия «аллергия». Аллергены, их классификация, пути проникновения в организм. Аллерген – в-во, вызывающее аллергию. Классификация аллергенов: экзоаллергены и эндоаллергены. Экзоаллергены: 1) инфекционные: а) бактериальные, б) вирусы, в) грибки, 2) неинфекционные а) пыльца цветущих растений, пух тополя, одуванчик, амброзия, хлопок, б) бытовые - домашняя и библиотечная пыль, как продукт жизнедеятельности домашнего клеща, специфичны для конкретной квартиры, в) пищевые продукты - особенно у детей - коровье молоко, куриные яйца, шоколад, цитрусовые, земляника, рыбы, крабы, омары, злаковые, г) лекарственные препараты - особенно лечебные сыворотки. д) продукты химического синтеза. Эндоаллергены: 1) естественные (первичные): хрусталик и сетчатка глаза, ткани нервной системы, щитовидной железы, мужских половых желез, 2) вторичные (приобретенные), индуцированные из собственных тканей под влиянием внешних воздействий: инфекционные: а) промежуточные (поврежденная под действием микроба ткань); б) комплексные (микроб+ткань, вирус+ткань); неинфекционные: холодовые, ожоговые, при облучении 51. Классификация аллергических реакций их общий патогенез, стадии. Понятие о десенсибилизации. Аллергия — иммунная реакция организма на какие-либо вещества антигенной или гаптенной природы, сопровождающаяся повреждением структуры и функции клеток, тканей и органов. Классификация аллергических реакций по Джеллу и Кумбсу: I. Анафилактический (реагиновый, ГНТ). Взаимодействие аллергена с фиксированными на клетках-мишенях (тучные клетки) IgE приводит к активации тучных клеток и высвобождению медиаторов аллергии (гистамин, серотонин, гепарин, производные арахидоновой к-ты, простогландины).Анафилактический шок – IgG4. Аллергены: пыльца растений, пищевые продукты, лек-ва. Заболевания: атопическая бронхиальная астма, поллиноз, анафилактический шок, аллергический коньюктивит, ринит, крапивница, отек Квинке. II. Цитотоксический. Связан с образованием IgG (кроме IgG4) и IgM-антител к детерминантам, имеющимся на собственных клетках (первичные или вторичные компоненты клеток). Заболевания: гемолитическая анемия, тромбоцитопения, агранулоцитоз, лейкоцитопения III. Иммунокомплексный (гистотоксический). Связан с образованием комплексов аллергенов с IgG- или IgM-антителами и с повреждающим действием этих комплексов на ткани организма. Заболевания: дерматит, сывр\ороточная болезнь, ревматоидный артрит, аллергич гломерулонефрит. IV. Клеточно-опосредованный (ГЗТ). Связан с образованием сенсабилизированных лимфоцитов (Т-эффекторов). ///////////////V. Рецепторно-опосредованой стимуляции Стадии аллергических реакций: 1)иммунологическая – охватывает изменения в иммунной системе при попадании аллергена 2)патохимическая – образование БАВ(медиаторов аллергии) 3)патофизиологическая – патогенное действие медиаторов на клетки, ткани и органы организма с клиническими проявлениями. 52.Реагиновый тип аллергии, его характеристика. Клинические проявления. Бронхиальная астма, ринит, конъюктивит, кожный зуд, крапивница, анафилаксия, отек Квинке 53.Цитотоксический тип аллергии, его характеристика, особенности патофизиологической стадии. Гемолитическая анемия, тромбоцитопения, агранулоцитоз, лейкоцитопения 54. Иммунокомплексный тип аллергии, его характеристика, клинические проявления. Дерматит, сывр\ороточная болезнь, ревматоидный артрит, аллергич гломерулонефрит. 55. Клеточно-опосредованный тип аллергии, его стадии, клинические проявления. Туберкулез,р-ция Манту, бруцеллез 56.Лекарственная аллергия, механизм ее возникновения. Анафилактический шок. Лекарственная аллергия — это побочное действие лекарств, основу которого составляют специфические иммунологические механизмы, что отличает лекарственную аллергию от других побочных действий лекарств (передозировка, идиосинкразия, образование токсических метаболитов и др.). Выраженными аллергическими свойства- ми обладают чужеродные сыворотки, гормоны, ферменты, белковые препараты из крови человека. Однако большинство лекарственных препаратов — это относительно простые химические соединения небелковой природы (гаптены). Для сенсибилизирующего действия они должны превратиться в полные антигены, что достигается путем образования химической (ковалентной) связи с белком-носителем. В развитии лекарственной аллергии определенное значение имеет генетическая предрасположенность. Кроме того, фактором, предрасполагающим к лекарственной аллергии, может стать дисфункция иммунной системы, связанная с длительным применением лекарства В развитии лекарственной аллергии могут участвовать все четыре типа иммунологического повреждения. Проявления лекарственной аллергии весьма разнообразны: от легких реакций (в виде кожной сыпи) до тяжелых системных проявлений (таких, как анафилактический шок). Одним из частых симптомов аллергической реакции на лекарства (чаще всего на применение антибиотиков пенициллинового ряда, сульфаниламидов, барбитуратов) является лекарственная лихорадка, которая исчезает через 48 ч после отмены препарата. Другое довольно частое проявление лекарственной аллергии — различные поражения кожи: зуд, сыпь (эритематозная, папулезная, экзематозная), которые могут быть обнаружены спустя неделю после начала приема препарата и не исчезают в течение 3 — 4 дней после его отмены. При профессиональном контакте рабочих фармацевтических предприятий, медицинских работников, а также при местном применении лекарств (мази) нередко развивается аллергическая реакция в виде контактного дерматита. Анафилактический шок – острая системная аллергическая реакция немедленного типа, развивающаяся в результате парентерального введения аллергена в организм на фоне сенсабилизации. Анафилактический шок характеризуется быстро развивающимся периферическим сосудистым коллапсом, повышением проницаемости сосудов, спазмом гладкой мускулатуры, расстройством ЦНС. Основу патогенеза анафилактического шока составляет I тип иммунного повреждения, обусловленный антителами, относящимися к IgE. В результате освобождения медиаторов падает сосудистый тонус, повышается сосудистая проницаемость, развивается спазм гладкой мускулатуры и как результат развивается коллапс, отек гортани, легких, мозга, спазм бронхов, кишечника и т. д. 57.Аллергические заболевания человека (бронхиальная астма, сывороточная болезнь), патогенез и методы предупреждения. Сывороточная болезнь — аллергическое заболевание, развивающееся в ответ на введение в организм чужеродной (гетеро- и гомологичной) сыворотки или препаратов, приготовленных на ее основе. Частота сывороточной болезни зависит от дозы белкового препарата и степени его очистки. Причиной возникновения сывороточной болезни являются антитоксические сыворотки (противостолбнячная, противодифтерийная, антирабическая, антилимфоцитарная), переливание крови, плазмы, яд насекомых и т. п. В развитии сывороточной болезни участвует несколько механизмов, из которых ведущим является повреждающее действие иммунных комплексов. Одновременно с введением сыворотки идет образование антител, относящихся к реагинам, которые включают аллергическую реакцию I типа, приводящую к повышению проницаемости сосудов. Профилактика: - назначение сыворотки строго по показаниям; - постановка проб на чувствительность к сывороткам; - использование «чистых сывороток»; - смена сывороток; - ограничение контакта с аллергенами; Бронхиальная астма — это хроническое заболевание легких, характеризующееся приступообразными нарушениями бронхиальной проходимости, клиническим выражением которых являются приступы экспираторного (с затруднением выдоха) удушья. Бронхиальной астмой страдает около 3 % населения земного шара. Принято различать атопическую (неинфекционно-аллергическую) бронхиальную астму и инфекционно- аллергическую. Атопическая бронхиальная астма обусловлена аллергенами неинфекционной природы (домашняя пыль, пыльца растений, перхоть животных, различные химические соединения и др.). Инфекционно- аллергическая бронхиальная астма тесно связана с хроническими воспалительными респираторными заболеваниями (бронхит, пневмония и др.). Аллергизацию организма вызывает микрофлора дыхательных путей (вирусы, бактерии, грибы и др.). Бронхиальная астма характеризуется сложным патогенезом, включающим иммунологические и неиммунологические механизмы. Значительная роль в развитии заболевания отводится аллергической предрасположенности. Существенную роль в патогенезе бронхиальной астмы играют иммунологические повреждения (I — IV типов), причем эти повреждения встречаются в различной комбинации. В формировании обструкции бронхов важное значение имеют дисгормональные сдвиги. Поскольку в регуляции бронхиального тонуса участвует симпатическая и парасимпатическая иннервация, дисбаланс функционального состояния этих отделов вегетативной нервной системы играет большую роль в патогенезе бронхиальной астмы. Основным звеном патогенеза заболевания, по общему мнению, являются повышенная чувствительность и реактивность бронхов. 58. Зависимость углеводного обмена от нервно-эндокринной регуляции. Гипергликемия причины и механизм развития, последствия. Нервная регуляция, подтверждением которой является «сахарный укол» - раздражение дна четвертого желудочка приводит к повышению уровня глюкозы в крови. Эндокринная регуляция при участии гормонов гипофиза, щитовидной железы, поджелудочной железы и надпочечников: Инсулин- снижается содержание глюкозы в крови Глюкагон- казывает гипергликемическое действие Адреналин - обладает гипергликемическим эффектом Тироксин, трийодтиронин - оказывают гипергликемическое действие Кортизон, кортизол, дезоксикортикостерон (глюкокортикоиды) –обладают гипергликемическим действием Кортикотропин, соматотропин – повышают уровень глюкозы в крови Гипергликемии (концентрация глюкозы в крови более 5,5 ммоль/л) Различают следующие типы гипергликемий. *Физиологические гипергликемии. Это быстрообратимые состояния. Нормализация уровня глюкозы в крови происходит без каких-либо внешних корригирующих воздействий. К ним относятся:
1. Алиментарная гипергликемия. Обусловлена приемом пищи, содержащей углеводы. Концентрация глюкозы в крови нарастает вследствие ее быстрого всасывания из кишечника. Активация секреции гормона β-клетками островков Лангерганса поджелудочной железы начинается рефлекторно, сразу после попадания пищи в полость рта и достигает максимума при продвижении пищи в двенадцатиперстную кишку и тонкий кишечник. Пики концентраций инсулина и глюкозы в крови совпадают по времени. Таким образом, инсулин не только обеспечивает доступность углеводов пищи к клеткам организма, но и ограничивает повышение концентрации глюкозы в крови, не допуская потерю ее с мочой. 2. Нейрогенная гипергликемия. Развивается в ответ на эмоциональный стресс и обусловлена выбросом в кровь большого количества катехоламинов, образующихся в мозговом веществе надпочечников и реализующих свои гипергликемические эффекты (см. табл. 12-2). Освобождающаяся глюкоза быстро выходит в кровь, обусловливая гипергликемию. Физиологический смысл этого феномена состоит в обеспечении срочной мобилизации резерва углеводов для использования их в качестве источников энергии (окисления) в предстоящей повышенной двигательной активности в условиях стресса. *Патологические гипергликемии. Причинами их развития являются: 1) нейроэндокринные расстройства, когда нарушены соотношения уровня гормонов гипо- и гипергликемического действия. Например, при заболеваниях гипофиза, опухолях коры надпочечников, при феохромоцитоме, гиперфункции щитовидной железы; при недостаточной продукции инсулина, глюкагономе; 2) органические поражения центральной нервной системы, расстройства мозгового кровообращения различной этиологии; 3) нарушения функций печени при циррозе; 4) судорожные состояния, когда происходит расщепление гликогена мышц и образование лактата, из которого в печени синтезируется глюкоза;
5) действие наркотических веществ (морфин, эфир), возбуждающих симпатическую нервную систему и тем самым способствующих развитию гипергликемии. 59. Эндокринная регуляция углеводного обмена. Гипогликемия причины и механизм развития, последствия. Эндокринная регуляция при участии гормонов гипофиза, щитовидной железы, поджелудочной железы и надпочечников: Инсулин- снижается содержание глюкозы в крови Глюкагон- аказывает гипергликемическое действие Адреналин - обладает гипергликемическим эффектом Тироксин, трийодтиронин - оказывают гипергликемическое действие Кортизон, кортизол, дезоксикортикостерон (глюкокортикоиды) –обладают гипергликемическим действием Кортикотропин, соматотропин – повышают уровень глюкозы в крови Гипогликемии(конц глюкозы в крови менее 3,3 ммоль/л) Патогенез гипогликемийможет быть связан с недостаточным поступлением глюкозы в кровь, ускоренным выведением ее из крови либо комбинацией этих факторов. Различают физиологическую и патологическую гипогликемию. Физиологическая гипогликемия. Выявляется при тяжелой и длительной физической нагрузке; длительном умственном напряжении; у женщин в период лактации; развивается сразу вслед за алиментарной гипергликемией благодаря компенсаторному выбросу в кровь инсулина. Патологическая гипогликемия (гиперинсулинизм). Чаще возникает у больных сахарным диабетом в связи с передозировкой инсулина при лечении. Причиной ее могут быть также: аденома островковых клеток поджелудочной железы (инсулома); синдром Золлингера- Эллисона (аденома или карцинома поджелудочной железы, которая, по-видимому, развивается из α-клеток островков Лангерганса, ответственных за выделение глюкагона и гастрина). Патологическая гипогликемия (без гиперинсулинизма). Выявляется: при патологии почек, сопровождающейся снижением порога для глюкозы, что приводит к потере глюкозы с мочой; нарушении всасывания углеводов; заболеваниях печени, сопровождающихся торможением синтеза гликогена и глюконеогенеза (острые и хронические гепатиты); недостаточности надпочечников (дефицит глюкокортикоидов); гипоавитаминозе В1, галактоземиях и при печеночных формах гликогенозов; голодании или недостаточном питании (алиментарная гипогликемия); недостаточности механизмов регуляции углеводного обмена у новорожденных. 60. Cахарный диабет, этиология и патогенез. Виды. Сахарный диабет — группа эндокринных заболеваний, связанных с нарушением усвоения глюкозы и развивающихся вследствие абсолютной или относительной (нарушение взаимодействия с клетками-мишенями) недостаточности гормона инсулина, в результате чего развивается гипергликемия — стойкое увеличение содержания глюкозы в крови. Заболевание характеризуется хроническим течением, а также нарушением всех видов обмена веществ: углеводного, жирового, белкового, минерального и водно-солевого. Панкреатическая недостаточность (1-й тип диабета) - инсулинозависимый диабет. Причина- разрушение островков Лангерганса поджелудочной железы и критическое снижение уровня инсулина в крови Массовая гибель эндокринных клеток поджелудочной железы может иметь место в случае вирусных инфекций, онкологических заболеваний, панкреатита, токсических поражений поджелудочной железы, стрессовых состояний, различных аутоиммунных заболеваний, при которых клетки иммунной системы вырабатывают антитела против β-клеток поджелудочной железы, разрушая их. У человека это заболевание зачастую является генетически детерминированным и обусловленным дефектами ряда генов. Эти дефекты формируют предрасположенность к аутоиммунной агрессии организма к клеткам поджелудочной железы и отрицательно сказываются на регенерационной способности β-клеток. В основе аутоиммунного поражения клеток лежит их повреждение любыми цитотоксическими агентами. Данное поражение вызывает выделение аутоантигенов, которые стимулируют активность макрофагов и Т-киллеров, что в свою очередь, приводит к образованию и выделению в кровь интерлейкинов в концентрациях, оказывающих токсическое действие на клетки поджелудочной железы. Также клетки повреждаются находящимися в тканях железы макрофагами. Также провоцирующими факторами могут являться длительная гипоксия клеток поджелудочной железы и высокоуглеводистая, богатая жирами и бедная белками диета, что приводит к снижению секреторной активности островковых клеток и в перспективе к их гибели. После начала массивной гибели клеток запускается механизм их аутоиммунного поражения. Внепанкреатическая недостаточность (2-й тип диабета) - инсулинонезависимый диабет При этом типе диабета инсулин производится в нормальных или даже в повышенных количествах, однако нарушается механизм взаимодействия инсулина с клетками организма (инсулинорезистентность) Главной причиной инсулинрезистентности является нарушение функций мембранных рецепторов инсулина при ожирении — рецепторы становятся неспособными взаимодействовать с гормоном в силу изменения их структуры или количества. Также при некоторых видах диабета 2-го типа может нарушаться структура самого инсулина (генетические дефекты). Кроме ожирения, факторами риска являются: пожилой возраст, курение, употребление алкоголя, артериальная гипертония, хроническое переедание, малоподвижный образ жизни. Доказана генетическая предрасположенность к диабету 2-го типа. При сахарном диабете 2 типа часто наблюдается нарушение циркадных ритмов синтеза инсулина и относительно длительное отсутствие морфологических изменений в тканях поджелудочной железы. В основе заболевания лежит ускорение инактивации инсулина или же специфическое разрушение рецепторов инсулина на мембранах инсулин-зависимых клеток. Ускорение разрушения инсулина зачастую происходит при наличии портокавальных анастомозов и, как следствие, быстрого поступления инсулина из поджелудочной железы в печень, где он быстро разрушается. Разрушение рецепторов к инсулину является следствием аутоиммунного процесса, когда аутоантитела воспринимают инсулиновые рецепторы как антигены и разрушают их, что приводит к значительному снижению чувствительности к инсулину инсулинзависимых клеток. Эффективность действия инсулина при прежней концентрации его в крови становится недостаточной для обеспечения адекватного углеводного обмена. 61. Диабетическая кома, механизм развития, проявление, последствие. Она характеризуется потерей сознания, глубокими расстройствами обмена веществ и нарушениями рефлекторной деятельности. |
