Лекции Лаборант школы (химия). 1 посуда лабораторная
 Скачать 1.87 Mb. Скачать 1.87 Mb.
|
МеркуриметрияМеркуриметрия– метод объемного анализа, основанный на приме- нении в качестве титрованного раствора Hg(NO3)2. Ионы Hg2+ при взаимо- действии с галогенидами, цианидами или роданидами образуют слабодис- социированные соединения, например: Hg2+ + 2Cl- → HgCl2 Титрование проводят в кислой среде. В качестве индикатора приме- няют либо дифенилкарбазон, либо нитропруссид натрия. При титровании с дифенилкарбазоном в точке эквивалентности титруемый раствор приобре- тает фиолетово-синее окрашивание. В присутствии нитропруссида натрия раствор титруют до появления неисчезающей мути — нитропруссида рту- ти: Hg2+ + [Fe(CN)5NO]2- = Hg[Fe(CN)5NO] Меркуриметрический метод имеет те же преимущества по сравне- нию с аргентометрическим методом, что и меркурометрия, но соли ртути ядовиты. Электрохимические методыФизические и физико-химические методы исследования широко применяют для контроля производства и управления технологическими процессами, при оценке качества готовых продуктов, и др. Наибольшее распространение получили методы: электрохимические, оптические, реологические, хроматографические, радиометрические. Помимо методов титрования в присутствии индикатора, применяют- ся электрохимические методы. В процессе электрохимического титрова- ния наблюдение ведут не за изменением окраски раствора, т.к. в этом слу- чае индикатор не применяется, а за изменением электрохимических пока- зателей титруемого раствора: электропроводностьюпри кондуктометрическом титровании; окислительно-восстановительнымпотенциаломпри потенциомет- рическом титровании. При этом титрование ведут обычным способом, но вместо визуаль- ного наблюдения изменения окраски, пользуются приборами. Достоинстваэлектрохимическихметодов: высокая чувствительность; быстрота выполнения; объективность полученных результатов. КондуктометрияКондуктометрические методы анализа основаны на измерении элек- тропроводности водных растворов электролитов (кислот, щелочей, солей). Прямая кондуктометрия – метод, позволяющий непосредственно определять концентрацию электролита путем измерения электропроводно- сти раствора с известным качественным составом; Кондуктометрическое титрование – метод анализа, основанный на определении содержания вещества по излому кривой титрования. Кривую строят по измерениям удельной электропроводности анализируемого рас- твора, меняющейся в результате химических реакций в процессе титрова- ния; Хронокондуктометрическое титрование – основано на определении содержания вещества по затраченному на титрование времени, автомати- чески фиксируемого на диаграммной ленте регистратора кривой титрова- ния. Кондуктометрия. Если в раствор с электролитом поместить два электрода и соединить их с источником тока, то через раствор пойдѐт электрический ток, величина которого определяется законом Ома: U 1 I L R , R. Электропроводностью называется способность веществ (металлов, газов, жидкостей и др.) проводить электрический ток под воздействием внешнего источника электрического поля. Различают следующие виды электропроводности: Электронная – осуществляется электронами металлов, сплавов, по- лупроводников, некоторых солей – проводники I рода; Ионная – осуществляется ионами (газы, растворы электролитов) – проводники II рода; Смешанная – осуществляется электронами и ионами в зависимости от условий. Электропроводность – величина обратная сопротивлению. Элек- тропроводность раствора зависит от его концентрации, от размеров и рас- положения электродов. На практике измеряют удельную электропровод- ность, которая представляет собой электропроводность раствора, заклю- чѐнного между пластинами – электродами, площадью 1 см2 и отстающими друг от друга на 1 см. Переносчиком тока в растворе являются ионы, на которые распада- ются молекулы при диссоциации в водных растворах электролитов. Ионы в растворе находятся в беспорядочном движении. Когда к электродам подводят напряжение, в растворе возникает электрический ток, под дей- ствием которого начинается движение ионов в определѐнном направлении, т.е. через раствор начинает протекать ток. Это свойство используется для определения концентрации веществ в растворах электролитов. Чем выше концентрация или подвижность ионов, тем выше удельная электропроводность раствора. Применениепрямойкондуктометрии Определение концентрации раствора электролита с известным качественным составом (метод градуировочного графика, метод стандарт- ных добавок). Кондуктометрический детектор в хроматографии. 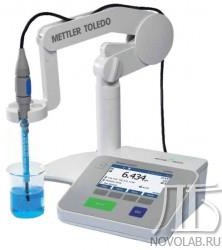 Определение физико-химических констант. Определение физико-химических констант.Рис. 34. Стационарный кондуктометр S230-USP/EP SevenCompact Примером применения метода прямой кондуктометрии является ме- тодикаопределенияудельнойэлектропроводностипаровогоконденсата. Измерение удельной электропроводности парового конденсата. Про- изводится на приборе «Индикатор солесодержания». Его работа основана на зависимости электропроводности раствора от концентрации растворѐн- ных солей (солесодержания). Перед измерением производится калибровка прибора по стандартному раствору NaCl. Поместив пробу конденсата в соответствующий датчик и измерив удельную электропроводность в дан- ном растворе, находят солесодержание, используя калибровочные кривые по NaCl. |
