Монография исследование водорослей.. Во́доросли. Аутентичного материала
 Скачать 2.99 Mb. Скачать 2.99 Mb.
|
§
164
Примечание: различия статистически достоверны по сравнению с группой до лечения при^-р^О^-р^ДИ. Количество общих фосфолипидов (ФЛ) после лечения относительно таковых показателей до лечения увеличилось на 22% (р<0,05). Таким образом, лечение БТ+статин+фуколам способствовало снижению уровня атерогенного холестерина в плазме крови. После проведенного курса лечения базовой терапией с аторвастатином (10 мг) и «Фуколамом» (БТ+статин 10 мг+фуколам) в плазме крови больных ИБС отмечалось изменение липидного состава по сравнению с таковыми величинами до лечения (рис. 7.5). Это проявлялось в снижении ТГ на 9% (16,37±0,29%; р<0,001) и увеличении количества ЭЖК на 9% (15,73±0,44%; р<0,05). 15 ■ 2 10 ■ с с > Е- 5 ■ 5S О IS i -10 ■ m s ^ -15 ■ -20 ■ ЭЖК сжк П ТГ ХС эхе Рис. 7.5. Изменения липидного состава плазмы крови у больных ИБС после лечения БТ+статин 10 мг+фуколам по сравнению со 2-й группой (до лечения). *** — р<0,001 В то же время количество неэтерифицированного ХС снизилось на 11% (16,80±0,43%; р<0,001), а ЭХС на 17% (26,07±0,90%; р<0,001). Исследование фосфолипидного состава плазмы крови после курса лечения БТ+статин 10 мг+фуколам показало изменения их количественных характеристик (рис. 7.6). 165
ФХ а ФС ФЭ ЛФХ л см Рис. 7.6. Изменения в содержании фосфолипидных фракций в плазме крови после лечения БТ+статин (10 мг)+фуколам по сравнению со 2-й группой (до лечения). * — р<0,05; *** — р<0,001 Так, в плазме крови увеличилось количества ФХ на 11% (р<0,001), что составляло 45,11±0,71% при одновременном снижении ЛФХ на 26% (р<0,001) и СМ на 18% (р<0,001), что, соответственно, составляло 10,94±0,32% и 12,29±0,31%. Количество ФЭ возросло на 36% (р<0,001), тогда как ЛФЭ снизилось на 34% (р<0,001), что, соответственно, составляло 8,49±0,33% и 5,93±0,17%. Следует отметить увеличение метаболически активных фракций: количество ФС на 50% (р<0,001), ФИ на 17% (р<0,05), ДФГ на 11% (р<0,05) (5,51±0,33%; 6,14±0,22%; 5,59±0,17%, соответственно). То есть, после проведенного курса лечения БТ+статин+фуколам была купирована дислипопротеинемия, нормализовался уровень холестерина, триглицеридов и фосфолипидов в плазме крови. Влияние лечения базовой терапией с фуколамом (БТ+фуколам) на липидный состав плазмы крови больных ИБС Как видно из таблицы 7.3, в плазме крови больных после лечения отмечалось статистически достоверное увеличение общих фосфолипидов на 24% (р<0,01), снижение общего холестерина на 20% (р<0,01), ХС ЛПНП на 27% (р<0,01). Величина ХС ЛПВП оставалась на уровне контроля. 166 Таблица 7.3 Биохимические показатели плазмы крови больных ИБС до и после лечения (М±т)
Примечание: различия статистически достоверны по сравнению со 2-й группой (до лечения) при:г- р<0,05;2- р<0,01. После проведенного курса лечения базовой терапией с фуколамом (БТ+фуколам) в плазме крови больных ИБС отмечались изменения количественных характеристик фракций нейтральных липидов (ТГ, ХС, ЭХС) по сравнению с таковыми величинами до лечения (2 группа) (рис. 7.7). 15 1 10 >• О. I- JS «N I-О >s S X х 01 ю s -5 ■ •10 •15 эжк ежк ТГ эхе Рис. 7.7. Изменения липидного состава плазмы крови у больных ИБС после лечения БТ+фуколам по сравнению со 2-й группой (до лечения). ** — р<0,01; *** — р<0,001 Так, количество ТГ снизилось на 11% (р<0,01), что составляло 16,06±0,46%. При этом количество неэтерифицированного холестерина (ХС) уменьшилось на 11 % (17,41 ±0,45%; р<0,01) при одновременном снижении ЭХС на 13% (27,37±0,29%; р<0,001). Таким образом, лечение по схеме БТ+фуколам сопровождалось снятием дислипопротеинемии, снижением атерогенного холестерина (ЭХС и ХС 167 ЛПНП), увеличением общих фосфолипидов. Исследование фосфолипидного состава плазмы крови после курса лечения БТ+фуколам по сравнению с таковыми показателями до лечения показало изменения их количественных характеристик (рис. 7.8). 100 1 80 >- о. I- >s I-О 35 5 X 01 X ш м 60 40 20 -20 -40 ФС ФХ П Л ФЭ см ЛФХ п ЛФЭ дфг ФИ Г| п__N Рис. 7.8. Изменения в содержании фосфолипидных фракций в плазме крови после лечения БТ+фуколам по сравнению со 2-й группой (до лечения). ** — р<0,01; *** — р<0,001 Увеличение количества ФХ на 9% (р<0,001) сопровождалось снижением ЛФХ на 27% (р<0,001) и СМ на 19% (р<0,001). Это, соответственно, составляло 43,97±0,95%, 11,19+0,35% и 12,67±0,33%. Количество ФЭ возросло на 34% (р<0,001), тогда как ЛФЭ снизилось на 30% (р<0,001), что, соответственно, составляло 8,83±0,22% и 6,08±0,11%. Среди метаболически активных фракций количество ФС увеличилось на 84% (р<0,001), ФИ на 7%, ДФГ на 15% (р<0,001) (5,71±0,32%; 5,73±0,09%; 5,82±0,13%, соответственно). В результате после проведенного курса лечения по схеме БТ+фуколам нормализовалось соотношение фосфолипидных фракций в плазме крови. Таким образом, введение фуколама в терапию больных ИБС способствует снятию дислипопротеинемии, снижению атерогенного холестерина, нормализации уровней триглицеридов, восстановлению соотношения фракций нейтральных липидов и фосфолипидов. 168 Сравнительная оценка влияния схемы лечения на изменения липид-ных фракций в плазме крови больных ИБС Было проведено сравнение процентных отклонений, вычисленных между исследованными показателями до лечения и после лечения с использованием двух схем лечения (БТ+статин+фуколам и БТ+фуколам). Как видно на рисунке 7.9, лечение БТ+статин+фуколам и БТ+фуколам по сравнению с таковыми показателями до лечения показало различные эффекты их действия. Так, при лечении БТ+статин+фуколам более значительно снизилось количество ХС (на 11%, р<0,001) и ЭХС (на 17%, р<0,001), отмечалось также снижение ТГ (на 9%, р<0,01), то есть, схема лечения БТ+статин+фуколам эффективно влияла на обмен холестерина. При лечении БТ+фуколам отмечалось более значительное снижение ТГ (на11%,р<0,01). О. 35 eg 15 -10 - 5 - 0 -5 -10 -15 -20 ежк 1 эжк в Шстатин+фуколам Нфуколам ХС 1 эхе Рис. 7.9. Изменения липидного состава плазмы крови у больных ИБС после лечения БТ+статин+фуколам и БТ+фуколам по сравнению со 2-й группой (до лечения). ** - р<0,01; *** - р<0,001 Эта схема лечения также влияла на обмен холестерина: снижение ХС на 8% (р<0,001), ЭХС на 13% (р<0,001). То есть, направленность в восстановлении нарушенных биохимических параметров при использовании обеих видов терапии была одинаковой, а отличия отмечались только в степени ее выраженности. Как видно на рисунке 7.10, лечение БТ+статин+фуколам и БТ+фуколам по сравнению с таковыми показателями до лечения показало одинаковую направленность в изменении фосфолипидных фракций, однако степень выраженности этих изменений различалась. 169 100 80
^ -20 -40 QD Статин+фуколам H фуколам ФЭ ФХ ЛФХ 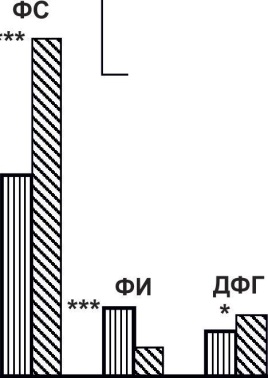 ЛФЭ Рис. 7.10. Изменения фосфолипидного состава плазмы крови у больных ИБС после лечения БТ+статин+фуколам и БТ+фуколам по сравнению со 2-й группой (до лечения). * - р<0,05; ** - р<0,01; *** - р<0,001 Так, при лечении БТ+статин+фуколам более значительно увеличилось количество ФХ (на 11%), ФЭ (на 36%, р<0,001), ФИ (на 17%, р<0,001) и снизилось количество ЛФЭ (на 34%, р<0,001). При лечении БТ+фуколам отмечалось более значительное снижение ЛФХ (на 27%, р<0.001), СМ (на 19%, р<0,001), а также увеличение ФС (на 84%, р<0,001) и ДФГ (на 15%, р<0,01). Эти результаты свидетельствуют о том, что обе схемы лечения восстанавливали этерифицирующую функцию печени, что способствовало преобразованию ТГ в фосфолипиды. Кроме того, «Фуколам», входящий в состав обеих схем лечения, снижал активность фосфолипаз и этим предотвращал разрушение фосфолипидных фракций. Таким образом, введение «Фуколама» в схему лечения способствовало восстановлению в соотношении липопротеинов в плазме крови, что обусловливало увеличение возможности выведения холестерина из мембран липопротеинами высокой плотности. В то же время снижение доли холестерина в мембранах способствовало замещению его на фосфолипидные фракции, в частности ФХ и ФЭ. Данный феномен определяет «Фуколам» не только как гипохолестеринемическое средство, но и как эффективное средство для восстановления структуры мембран, нарушенных при ИБС. 170 —♦— статин 10 мг +фуколам ■ фуколам Динамика изменений клинико-биохимических показателей липид-ного спектра крови пациентов с ИБС II-IIIФК в течение 6 месяцев на фоне приема препаратов На рисунке 7.11 представлены результаты эффективности длительного применения «Фуколама» с использованием двух схем лечения (БТ + статин + фуколам и БТ+фуколам) у больных ИБС II—III ФК с дислипидемией. Динамика снижения уровня общего ХС была более выражена в группе 2. Через 3,6 месяцев от начала лечения снижение общего ХС в группе 2а составило 30% (р<0,001),34%(р<0,001), а В до 1 мес 3 глее б мес группе 26 - 17% (р<0,001), D _ 1t n r/ r Рис. 7.11. Динамика изменении в содержании 24% (р<0,001). Более заметные изменения общего ХС в сыворотке крови пациентов после лечения (1 месяц) и последующего профилактического применения препаратов (3 и 6 месяцев) проявились в содержании ХС-ЛПНП. Так, через 3, 6 месяцев в группе 2а снижение ХС-ЛПНП составило: 49% (р<0,001), 47% (р<0,001), в группе 26 - 22% (р<0,001), 31% (р<0,01), при этом сохранилась тенденция снижения, как и у общего ХС (рис. 7.12). -♦— статин 10 мг +фуколам -■- фуколам 4,5 4 3,5 ■ 1 2,5 ■ О 1.5 Ж 1 0,5 ■ 1 мес 3 мес 6 мес Рис. 7.12. Динамика изменений в содержании ХС - ЛПНП в сыворотке крови после лечения (1 месяц) и последующего профилактического применения препаратов (3 и 6 месяцев) Европейские липидологи считают, что следует добиваться снижения ХС-ЛПНП при ИБС до 2,6 ммоль/л и ниже, что практически было достигнуто в группе 2а через 3 месяца и пролонгировано до 6 месяцев. 171 Рис. 7.13. Динамика изменений в содержании не- ЛПВП в сыворотке крови после лечения (1 месяц) и последующего профилактического применения препаратов (3 и 6 месяцев) Уровень ХС ЛПВП в динамике в течение б месяцев значительно не менялся. Интересным представляется и такой показатель, как содержание не-ЛПВП холестерина (рис. 7.13). Существуют доказательства, что уровень не-ЛПВП холестерина может —♦— статин ю мг +фуколам —■— фуколам рассматриваться как более сильный предиктор сердечно-сосудистых заболеваний, чем уровень ХС-ЛПНП (Liu et al., 2005; Pischon et al., 2005), особенно у пациентов, принимающих статины (Gotto et al., 2000). Особенно важно учитывать содержание не-ЛПВП холестерина в случае, когда уровень ХС-ЛПНП низкий или умеренный. Отмечается снижение содержания не-ЛПВП холестерина в процессе приема препаратов и через 3, б месяцев в 2а группе составило: 43% (р<0,001), 46% (р<0,001); в 26 — 24% (р<0,001), 29,5% (р<0,001). В данном исследовании практически кривые показателей ХС-ЛПНП и не-ЛПВП холестерина практически идентичны. Немалую роль в развитии атеросклеротического процесса играет соотношение компонентов общего холестерина (ОХС) и ЛПВП (липопротеи-нов высокой плотности). Для того чтобы это соотношение было более наглядным, используют ориентировочный показатель - индекс атерогенности, чаще его называют коэффициент атерогенности (КА). Исследования показали, что при приеме препаратов в группе 2а отмечалось значительное снижение КА до 3 месяца, но к 6 месяцу уровень его приблизился к норме, в группе 2 б происходило постепенное динамичное снижение КА до б месяца (рис. 7.14). Коэффициент атерогенности является ос- ■ статин 10 мг +фуколам - - фуколам Рис. 7.14. Динамика изменений в содержании КА в сыворотке крови после лечения (1 месяц) и последующего профилактического применения препаратов (3 и 6 месяцев) 172 -«— статин 10 мг чфуколам - - фуколам 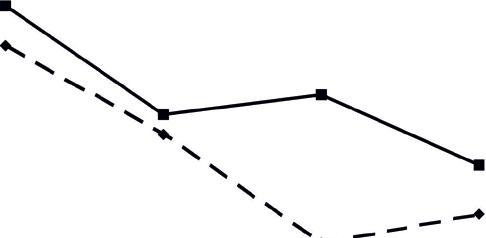 новным критерием, позволяющим следить за эффективностью лечения гиперхолестеринемии. Учитывая, что у пациентов данных групп уровень ХС-ЛПВП был в пределах нормы, снижение КА можно объяснить снижением концентрации общего ХС. Сравнение уровня атерогенных липидов было также оценено по содержанию апопротеина В (апо В) — белкового компонента, присутствующего в ЛПНП - веществах циркулирующих в крови, осуществляющих транспорт холестерина. Определение апо В позволяет оценить степень риска развития ИБС у пациентов. Этот тест полезен для выявления остаточного риска у пациентов, которые уже принимают липидснижающую терапию и | отреагировали уже снижением | ХС-ЛПНП. Сохранение высоких значений апо В на фоне терапии служит поводом для некото- и т/- до 1мес Змее бмес рои ее оптимизации. Контуры кривых показателей апоВ обеих Рис. 7Л5. дИНамика изменений в содержа-групп идентичны кривым пока- нии апо в в сыворотке крови после лечения зателям Л^-ЛИгШ фИС. /ЛЬ), ц месяц) и последующего профилактического Увеличение отношения апо В к применения препаратов (3 и 6 месяцев) апо А (более 1) служит одним из показателей атерогенного сдвига. Отношение апо В/апо А в сыворотке крови после 1 месяца лечения была различной: снижался риск развития ИБС в 2а группе, в то время как в 26 группе он оставался повышенным. При дальнейшем приеме препаратов отмечалось достоверное снижение соотношение апо В/апо А в сыворотке крови пациентов и к б месяцу составило для группы 2а - 26% (р<0,001), группы 26 -17% (рис. 7.16). Существенно коррелирует с сердечно-сосудистой заболеваемостью и такой показатель, как липопротеин(а) — ЛП(а), который указывает на высокий риск как атерогенных процессов, так —*— статин 10 мг +фуколам ■ -фуколам Рис. 7.16. Динамика изменений в содержании апо В/апо А в сыворотке крови после лечения (1 месяц) и последующего профилактического применения препаратов (3 и 6 месяцев) 173 —«— статин 10 мг +фуколам —■— фуколам и протромботических реакций. В отличие от ЛПНП, его уровень не зависит от уровня глюкозы в крови, наличия инсулинрезистентности и других факторов. Результаты, полученные в ходе исследования, показали снижение количества ЛП(а) в сыворотке крови в обеих группах, но при приеме системы статин 10 мг+«Фуколам» оно было более выражено. На рисунке 7.17 показана динамика снижения количества ЛП(а), положительный эффект отмечен как в группе 2а, так и 26, причем при приеме статин 10 мг+БАД «Фуколам» снижение его уровня более выражено. Концентрация ЛП (а) в сыворотке крови пациентов снижалась, но не пришла к норме. К б месяцу снижение ЛП(а) составило в группе 2а — 46,79%, в группе 26 - 30,19%. Считают, что ЛП(а) генетиче-ски детерминирована, и в на-Рис. 7.17. Динамика изменений в содержании стоящее время не существует ЛП(а) в сыворотке крови после лечения (1 месяц) лекарственных средств, СНИ-и последующего профилактического применения жающих ее, поэтому основная препаратов (Зиб месяцев) стратегия лечения пациентов с повышенной концентрацией ЛП(а) - устранение всех прочих факторов риска ИБС (высокая концентрация ЛПНП, курение, избыточная масса тела, артериальная гипертензия). Таким образом, гиполипидемическое действие «Фуколама» заключается в снижении общего ХС, ХС-ЛПНП, КА в уменьшении синтеза основного белка в составе атерогенных ЛПНП - апоВ. При этом выраженность гиполипидемического эффекта находится в прямой зависимости от степени исходной гиперлипидемии. Полученные данные позволяют говорить об эффективности «Фуколама» у больных ИБС со стабильной стенокардией напряжения П-Ш ФК. Наибольший гиполипидемический эффект достигается при комплексном применении фуколам с БТ, включающей аторвастатин 10 мг. Поэтому при лечении дислипидемий можно рекомендовать не повышать концентрацию статинов, учитывая нежелательные побочные их эффекты и высокую стоимость, а использовать в качестве дополнительного гиполипидемического средства фуколам. Исходя из результатов клинического исследования БАД «Фуколам» может быть рекомендована для широкого использования в качестве профилактического и дополнительного средства к базисной терапии при различных формах ИБС, а, учитывая ранее полученные данные о 174 гепатопротекторнои, антикоагулянтнои, иммуномодулирующеи активности фуколама, это позволит улучшить эффективность проводимых лечебных и профилактических мероприятий. Динамика изменений нейтральных липидов в плазме крови после лечения через Зиб месяцев с применением аторвастатина (10 мг) с «Фуколамом» (статин 10 мг+фуколам) или «Фуколама» На рисунке 7.18 показано, что сразу после лечения отмечалось более эффективное снижение ТГ при БТ+фуколам (на 11%). Далее, через 3 мес величина ТГ в обеих группах была, в среднем одинаковой, в пределах 16,58—16,65%. Через 6 мес количество ТГ при лечении «Фуколамом» незначительно повысилось в пределах 3% (16,25% и 16,79%). Кроме того, эти величины достоверно не отличались —♦— статин 10 мг + фуколам ■ - фуколам 17 5 16,8 s | 16,6 I 16,4 1 16,2 16 15,8 15,6 и после лечения 3 мес после лечения 6 мес после лечения —*— статин 10 мг-+фуколам * - фуколам Рис. 7.18. Динамика изменений в содержании тригли-церидов (ТГ) в плазме крови после лечения и последующего профилактического применения препаратов 0Т контрольного значения (16,00±0,58%). Динамика изменений количества свободных жирных кислот и эфиров жирных кислот была практически одинаковой приобеих схемах терапии и не имела статистически достоверных отличий от контрольных показателей как до лечения, так и после него. При исследовании динамики величины неэтерифи-цированного холестерина (ХС) в плазме крови в течение 6 мес после лечения следует отметить большее снижение ЭТОЙ фрак- Рис. 7.19. Динамика изменений в содержании холе-ЦИИ при приеме системы стерина (ХС) в плазме крови после лечения и после -статин+фуколам (рис. 7.19). дующего профилактического применения препаратов Величина ХС снизилась с 16,80±0,43% после лечения до 15,05±0,23% через 3 мес и до 15,43±0,39% через 6 мес. При приеме «Фуколама» величина ХС составляла 17,41±0,45% после лечения, через 3 мес - 16,36±0,56% и через 6 мес - 16,81%. То есть, 18 ! 17,5 " 17 | 16,5 I 16 1 15,5 I 15 $ 14,5 и 14 13,5 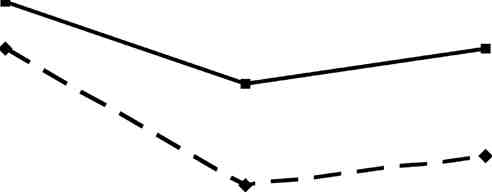 после лечения 3 мес после лечения б мес после лечения 175 при использовании схемы статин+фуколам произошло снижение ХС на 19% через 3 мес и на 8% через б мес после лечения, тогда как при приеме «Фуколама» снижение ХС составляло через 3 и б мес в среднем на 6%. При сравнении полученных значений ХС через 3 и б мес с контрольными величинами следует отметить, что лечение с применением статина сопровождалось стойким удерживанием величины неэтерифицирован-ного холестерина (ХС) в плазме крови ниже контроля на 13-15%. При применении лечения БТ+фуколам значения ХС после лечения были в пределах контрольных величин, которые поддерживались в течение б мес применения фуколама. При исследовании динамики величины эфиров холестерина (ЭХС) в плазме крови следует отметить, что через 3 мес эта величина была одинаковой как при приеме системы статин+фуколам, так и фуколама (26,84+0,45% и 26,92+0,56%, соответственно) (рис. 7.20). 27,5 27,25 —♦— статин 10 мг +фуколам —■— фуколам после лечения 3 мес после лечения 6 мес после лечения Рис. 7.20. Динамика изменений в содержании эфиров холестерина (ЭХС) в плазме крови после лечения и последующего профилактического применения препаратов Через 6 мес величины ЭХС сохранились на уровне зафиксиро-ваных через 3 мес приема препаратов. Таким образом, применение статина+фуколам и «Фуколама» после лечения в течение 6 мес сопровождалось сохранением показателей нейтральных липидов на уровне величин, которых имели место после лечения. Применение статина стойко удерживало величину ХС и ЭХС ниже контрольного уровня на 10-15%. Динамика изменений фосфолипидного состава плазмы крови после лечения в течение 6 мес с применением аторвастатина (10 мг) с фуколамом (статин 10 мг+фуколам) или фуколама Изучение динамики изменений фосфолипидных фракций в плазме крови после лечения в течение 6 мес показало, что прием больными 176 системы статин 10 мг + фуколам или только фуколам сохраняет исследованные величины на уровне таковых, которые были зарегистрированы при выписке из стационара. Так, если после лечения БТ+статин 10 мг + фуколам в плазме крови пациентов количество фосфатидилхолина (ФХ) было на уровне 45,11+0,71%, то через 3 и 6 мес его величина была в пределах 44,33—44,69% (рис. 7.21). При приеме фуколама величина ФХ как после лечения, так и через 3 и 6 мес была в пределах 44%. 45 ■ 44,8 | 44,6 £ 44,4 1 44,2 | 44 I 43,8 43,6 43,4 —♦— статин 10 мг + фуколам —■— фуколам после лечен! 3 мес после лечения 6 мес после лечен! Рис. 7.21. Динамика изменений в содержании фосфатидилхолина (ФХ) в плазме крови после лечения и последующего профилактического применения препаратов Изучение динамики величины лизофосфатидилхолина (ЛФХ) (рис. 7.22) в плазме крови пациентов показало, что при приеме системы статин 10 мг + фуколам происходило сохранение этой фракции через и 3 и 6 мес (11,00+0,18% и 11,21+0,17%, соответственно) на уровне, зафиксированной после выписки (10,94+0,32%). —♦— статин 10 мг + фуколам - фуколам 11,8 -1 11,6 ■ ? 11,4 ' после лечения 3 мес после лечения 6 мес после лечения Рис. 7.22. Динамика изменений в содержании лизофосфатидилхолина (ЛФХ) в плазме крови после лечения и последующего профилактического применения препаратов 177 При приеме фуколама содержание ЛФХ в плазме крови через 3 и б мес (11,62±0,42% и 11,10±0,20%) также было на уровне величин после лечения (11,19±0,35%). Динамика изменений в содержании сфингомиелина (СМ) в плазме крови пациентов после лечения в течение 3 и б мес показала плавное колебание величины этой фракции как при приеме системы статин 10 мг + фуколам, так и фуколама (рис. 7.23). —*— статин 10 мг + фуколам —■—фуколам после лечения 3 мес после лечения 6 мес после лечения Рис. 7.23. Динамика изменений в содержании сфингомиелина (СМ) в плазме крови после лечения и последующего профилактического применения препаратов Так, при приеме системы статин 10 мг +фуколам количество СМ составляло 3 и б мес практически одинаковую величину — 13,50±0,32%. При приеме фуколама количество СМ через б мес составляло 12,92±0,34%, что соответствовало таковому уровню после лечения (12,67±0,33%) и соответствовали контрольным величинам. Динамика изменений в содержании фосфатидилэтаноламина (ФЭ) относительно таковых величин после лечения при приеме системы статин 10 мг + фуколам и фуколама до 3 мес была практически одинаковой (в среднем, 8,50±0,20%). Че- —♦— статин 10 мг + фуколам —■— фуколам рез б мес количество ФЭ у первых немного снизилось до 7,81±0,18% (рис. 7.24). В то же время эти величины сохранялись на уровне таковых после лечения и соответствовали контроль- после лечения 3 мес после лечения 6 мес после лечения ным показателям. Рис. 7.24. Динамика изменений в содержании фосфати- При исследовании дина-дилэтаноламина (ФЭ) в плазме крови после лечения и по- МИКИ В содержании ЛИЗО-следующего профилактического применения препаратов фосфатидилэтаноламина (ЛФЭ) в плазме крови па-
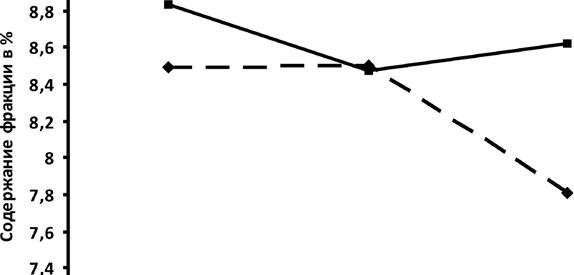 178 циентов, принимавших систему статин 10 мг + фуколам было замечено, что через 3 и 6 мес после лечения значения данной фракции были в пределах 5,90—5,97%, что соответствовало контрольным значениям (рис. 7.25). При применении фуколама величина ЛФЭ в плазме крови оставалась на уровне таковой после лечения, то есть в пределах 6,10±0,26%. £ 5,85 —♦— статин 10 мг + фуколам ■ - фуколам после лечения 3 меспосле лечен! 6 плес после лечения Рис. 7.25. Динамика изменений в содержании лизофосфатидилэтаноламина (ЛФЭ) в плазме крови после лечения и последующего профилактического применения препаратов Величина фосфатидилсерина (ФС) в плазме крови пациентов обеих групп была практически идентичной как через 3 мес, так и через б мес и сохранялась на уровне таковой, зафиксированной после лечения (рис. 7.26). —•— статин 10 мг + фуколам • ■ фуколам
после лечения 3 мес после лечения 6 мес после лечения Рис. 7.26. Динамика изменений в содержании фосфатидилсерина (ФС) в плазме крови после лечения и последующего профилактического применения препаратов При исследовании динамики изменений в содержании фосфатидили-нозита (ФИ) в плазме крови пациентов через 3 мес после приема системы статин 10 мг + фуколам было отмечено снижение этого показателя с 6,14±0,22% после лечения до 5,64±0,28%, а затем опять увеличение до 5,92±0,20% через 6 мес. (рис. 8.27). Однако эти колебания были недостоверны относительно контроля, а также относительно таковых после лечения. При исследовании динамики изменений количества ФИ в плазме крови (рис. 26) при приеме фуколама отмечается его увеличение через 3 мес до 179 —♦— статин Юмг + фуколам —■—фуколам  N- после лечения 3 мес после лечения 6 мес после лечения Рис. 7.27. Динамика изменений в содержании фосфатидилинозита (ФИ) в плазме крови после лечения и последующего профилактического применения препаратов 6,12±0,25% (5,73±0,09% после лечения), а затем снижение до 5,65±0,26% через б мес. Однако эти колебания были статистически не достоверны по сравнению как с контролем, так и с таковыми после лечения. Динамика изменений количества дифосфатидилглицерина (ДФГ) в плазме крови пациентов практически совпадала как при приеме системы сатин 10 мг + фуколам, так и при приеме фуколама (рис. 7.28). ♦■ ■ статин 10 мг + фуколам - фуколам 6,3 ' Ж 6,2 ■ " 6,1 ■ |
