|
|
ШПОРЫ БХ 2 ИТОГОВАЯ. Эндергонические процессы, протекающие с увеличением свободной энергии. Катаболические превращения
Вопрос 36.сфинголипиды. строение и роль.
Сфинголипиды
Аминоспирт сфингозин, состоящий из 18 атомов углерода, содержит гидроксильные группы и аминогруппу. Сфингозин образует большую группу липидов, в которых жирная кислота связана с ним через аминогруппу. Продукт взаимодействия сфингозина и жирной кислоты называют "церамид"). В церамидах жирные кислоты связаны необычной (амидной) связью, а гидроксильные группы способны взаимодействовать с другими радикалами. Церамиды отличаются радикалами жирных кислот, входящих в их состав. Обычно это жирные кислоты с большой длиной цепи - от 18 до 26 атомов углерода. Существует 3 основных типа сфинголипидов:
Церамиды — это наиболее простые сфинголипиды. Они содержат только сфингозин, соединённый с жирнокислотным ацильным остатком.
Сфингомиелины содержат заряженную полярную группу, такую как фосфохолин или фосфоэтаноламин.
Гликосфинголипиды содержат церамид, эстерифицированный по 1-гидрокси-группе остатком сахара. В зависимости от сахара гликосфинголипиды подразделяются нацереброзиды и ганглиозиды.
Цереброзиды содержат в качестве остатка сахара глюкозу или галактозу.
Ганглиозиды содержат трисахарид, причём один из них всегда сиаловая кислота.
Биол. роль сфинголипидов разнообразна. Известно, что они участвуют в формировании мембранных структур аксонов, синапсов и др. клеток нервной ткани, опосредуют в организме механизмы узнавания, рецепторные взаимодействия, межклеточные контакты и др. жизненно важные процессы.
Это наиболее распространенные сфинголипиды. В основном они находятся в мембранах животных и растительных клеток. Особенно богата ими нервная ткань. Сфингомиелины обнаружены также в ткани почек, печени и других органов. При гидролизе сфингомиелиныобразуют одну молекулу жирной кислоты, одну молекулу двухатомного ненасыщенного спирта сфингозина, одну молекулу азотистого основания(чаще это холин) и одну молекулу фосфорной кислоты. Общую формулу сфингомиелинов можно представить так:
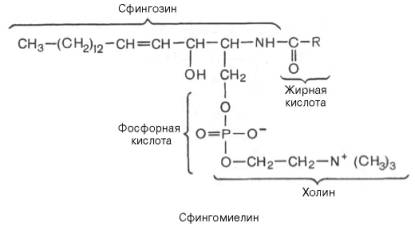
Вопрос 37. Гликолипиды широко представлены в тканях, особенно в нервной ткани, в частности в мозге. Главной формой гликолипидов в животных тканяхявляются гликосфинголипиды. Последние содержат церамид, состоящий из спирта сфингозина и остатка жирной кислоты, и один или несколько остатков сахаров. Простейшими гликосфинголипидами являются галактозилцерамиды и глюкозилцерамиды.
Галактозилцерамиды – главные сфинголипиды мозга и других нервных тканей, но в небольших количествах встречаются и во многих других тканях. В состав галактозилцерамидов входит гексоза (обычно это D-галактоза), которая связана эфирной связью с гидроксильной группой аминоспиртасфингозина. Кроме того, в составе галактозилцерамида имеется жирная кислота. Чаще всего это лигноцериновая, нервоновая или це-реброноваякислота, т.е. жирные кислоты, имеющие 24 углеродных атома.
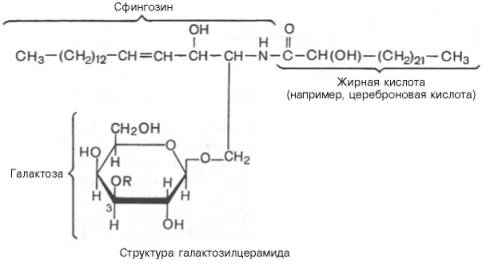
Существуют сульфогалактозилцерамиды, которые отличаются от га-лактозилцерамидов наличием остатка серной кислоты, присоединенного к третьему углеродному атому гексозы. В мозге млекопитающих сульфо-галактозилцерамиды в основном находятся в белом веществе, при этом содержание их в мозге намного ниже, чем галактозилцерамидов.
Глюкозилцерамиды – простые гликосфинголипиды, представлены в тканях, отличных от нервной, причем главным образом глюкозил-церамидами. В небольших количествах они имеются в ткани мозга. В отличие от галактозилцерамидов у них вместо остатка галактозы имеется остаток глюкозы. Более сложными гликосфинголипидами являются ганглиозиды, образующиеся из гликозилцерамидов. Ганглиозиды дополнительно содержат одну или несколько молекул сиаловой кислоты. В тканях человека доминирующей сиаловой кислотой является нейраминовая. Кроме того, вместо остаткаглюкозы они чаще содержат сложный олигосахарид. Ганглиозиды в больших количествах находятся в нервной ткани. Они, по-видимому, выполняют рецепторные и другие функции. Одним из простейших ганглиозидов является гематозид, выделенный из стромы эритроцитов. Он содержит церамид(ацилсфингозин), одну молекулу глюкозы, одну молекулу N-ацетилнейраминовой кислоты.
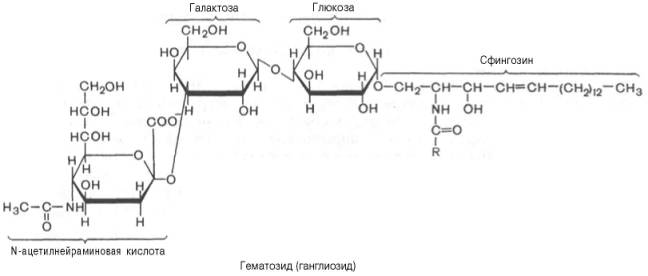
Вопрос 38. ХОЛЕСТЕРОЛ - важный компонент мембран и регулятор свойств гидрофобного слоя. Производные холестерола (жёлчные кислоты) необходимы для переваривания жиров. Стероидные гормоны, синтезируемые из холестерола, участвуют в регуляции энергетического, водно-солевого обменов, половых функций.В организме человека это основной стероид, остальные стероиды - его производные. Растения, грибы и дрожжи не синтезируют холестерол, но образуют разнообразные фитостеролы и микостеролы, не усваиваемые организмом человека. Бактерии не способны синтезировать стероиды. Холестерол входит в состав мембран и влияет на структуру бислоя, увеличивая её жёсткость. Из холестерола синтезируются жёлчные кислоты, стероидные гормоны и витамин D3. Нарушение обмена холестерола приводит к развитию атеросклероза. Холестерол представляет собой молекулу, содержащую 4 конденсированных кольца, обозначаемые латинскими буквами А, В, С, D, разветвлённую боковую цепь из 8 углеродных атомов в положении 17, 2 "ангулярные" метильные группы (18 и 19) и гидроксильную группу в положении 3. Присоединение жирных кислот сложноэфирной связью к гидроксильной группе приводит к образованию эфиров холестерола. В неэтерифицированной форме холестерол входит в состав мембран различных клеток. Гидроксильная группа холестерола обращена к водному слою, а жёсткая гидрофобная часть молекулы погружена во внутренний гидрофобный слой мембраны. В крови 2/3 холестерола находится в этерифицированной форме и 1/3 - в виде свободногохолестерола. Эфиры холестерола служат формой его депонирования в некоторых клетках (например, печени, коры надпочечников, половых желёз). Из этих депо холестерол используется для синтеза жёлчных кислот и стероидных гормонов.
Вопрос 39. ПЕРЕВАРИВАНИЕ ТАГ,ХОЛЕСТЕРИНА,ФОСФОЛИПИДОВ панкреатической липазой.
Панкреатическая липаза выделяется в полость тонкой кишки из поджелудочной железы вместе с белком колипазой. Колипаза попадает в полость кишечника в неактивном виде и частичным протеолизом под действием трипсина превращается в активную форму. Колипаза своим гидрофобным доменом связывается с поверхностью мицеллы эмульгированного жира. Другая часть молекулы способствует формированию такой конформации панкреатической липазы, при которой активный центр фермента максимально приближен к своим субстратам - молекулам жиров, поэтому скорость реакции гидролиза жира резко возрастает. Панкреатическая липаза гидролизует жиры преимущественно в положениях 1 и 3, поэтому основными продуктами гидролиза являются свободные жирные кислоты и 2-моноацилглицеролы (β-моноацилглицеролы). Молекулы 2-моноацилглицеролов также обладают детергентными свойствами и способствуют эмульгированию жиров.
В переваривании глицерофосфолипидовучаствуют несколько ферментов, синтезирующихся в поджелудочной железе. Фосфолипаза А2 гидролизует сложноэфирную связь у второго атома углерода глицерола, превращая глицерофосфолипиды в соответствующие лизофосфолипиды. ФосфолипазаA2 секретируется в кишечник в виде профермента и активируется уже в полости кишечника путём частичного протеолиза. Для проявления активности фосфолипазыA2 необходимы ионы кальция. Жирная кислота в положении 1 отщепляется под действием лизофосфолипазы, а глицерофосфохолин гидролизуется далее до глицерола, холина и фосфорной кислоты, которые всасываются. Лизофосфолипиды - эффективные эмульгаторы жира, ускоряющие его переваривание.
Переваривание эфиров холестерола
В составе пищи холестерол находится в основном в виде эфиров. Гидролиз эфиров холестерола происходит под действием холестеролэстеразы - фермента, который также синтезируется в поджелудочной железе и секретируется в кишечник. Продукты гидролиза (холестерол и жирные кислоты) всасываются в составе смешанных мицелл. Следствие этого нарушение переваривания и всасывания жиров у детей более опасно, чем у взрослых.
Всасывание продуктов гидролиза липидов в тонком кишечнике.
Образование смешанных мицелл.
Продукты гидролиза липидов - жирные кислоты с длинным углеводородным радикалом, 2-моноацилглицеролы, холестерол, а также соли жёлчных кислот образуют в просвете кишечника структуры, называемые смешанными мицеллами. Смешанные мицеллы построены таким образом, что гидрофобные части молекул обращены внутрь мицеллы, а гидрофильные - наружу, поэтому мицеллы хорошо растворяются в водной фазе содержимого тонкой кишки. Стабильность мицелл обеспечивается в основном солями жёлчных кислот. Мицеллы сближаются со щёточной каймой клеток слизистой оболочки тонкого кишечника, и липидные компоненты мицелл диффундируют через мембраны внутрь клеток. Вместе с продуктами гидролиза липидов всасываются жирорастворимые витамины A, D, Е, К и соли жёлчных кислот. Наиболее активно соли жёлчных кислот всасываются в подвздошной кишке. Жёлчные кислоты далее попадают через воротную вену в печень, из печени вновь секретируются в жёлчный пузырь и далее опять участвуют в эмульгировании жиров. Этот путь жёлчных кислот называют "энтерогепатическая циркуляция". Каждая молекула жёлчных кислот за сутки проходит 5- 8 циклов, и около 5% жёлчных кислот выделяется с фекалиями. Всасывание жирных кислот со средней длиной цепи, образующихся, например, при переваривании липидов молока, происходит без участия смешанных мицелл. Эти жирные кислоты из клеток слизистой оболочки тонкого кишечника попадают в кровь, связываются с белком альбумином и транспортируются в печень.
Вопрос 40.ЖЕЛЧНЫЕ КИСЛОТЫ.
Жёлчные кислоты синтезируются в печени из холестерола. Часть жёлчных кислот в печени подвергается реакции конъюгации - соединения с гидрофильными молекулами (глицином и таурином). Жёлчные кислоты обеспечивают эмульгирование жиров, всасывание продуктов их переваривания и некоторых гидрофобных веществ, поступающих с пищей, например жирорастворимых витаминов и холестерола. Жёлчные кислоты также всасываются, через юротную вену попадают опять в печень и многократно используются для эмульгирования жиров. Этот путь называют энтерогепатической циркуляцией жёлчных кислот.
Синтез жёлчных кислот
В организме за сутки синтезируется 200- 600 мг жёлчных кислот. Первая реакция синтеза - образование 7-α-гидроксихолестерола - является регуляторной. Фермент 7-α-гидроксилаза, катализирующий эту реакцию, ингибируется конечным продуктом - жёлчными кислотами. 7-α-Гидроксилаза представляет собой одну из форм цитохрома Р450 и использует кислород как один из субстратов. Один атом кислорода из О2 включается в гидроксильную группу в положении 7, а другой восстанавливается до воды. Последующие реакции синтеза приводят к формированию 2 видов жёлчных кислот: холевой и хенодезоксихолевой, которые называют "первичными жёлчными кислотами".
Конъюгирование жёлчных кислот
Конъюгирование - присоединение ионизированных молекул глицина или таурина к карбоксильной группе жёлчных кислот; усиливает их детергентные свойства, так как увеличивает амфифильность молекул.
Конъюгация происходит в клетках печени и начинается с образования активной формы жёлчных кислот - производных КоА. Затем присоединяется таурин или глицин, и в результате образуется 4 варианта конъюгатов: таурохолевая и таурохенодезоксихолевая, гликохолевая или гликохенодезоксихолевая кислоты (они значительно более сильные эмульгаторы, чем исходные жёлчные кислоты). Конъюгатов с глицином образуется в 3 раза больше, чем с таурином, так как количество таурина ограничено. Продукты гидролиза жиров всасываются в основном в верхнем отделе тонкого кишечника, а соли жёлчных кислот - в подвздошной кишке. Около 95% жёлчных кислот, попавших в кишечник, возвращается в печень через воротную вену, затем опять секретируются в жёлчь и повторно используются в эмульгировании жиров. Этот путь жёлчных кислот называют энтерогепатической циркуляцией. В сутки всего реабсорбируется 12-32 г солей жёлчных кислот, так как в организме имеется 2-4 г жёлчных кислот, и каждая молекула жёлчной кислоты проходит этот крут 6-8 раз. Часть жёлчных кислот в кишечнике подвергается действию ферментов бактерий, которые отщепляют глицин и таурин, а также гидроксильную группу в положении 7 жёлчных кислот. Жёлчные кислоты, лишённые этой гидроксильной группы, называют вторичными. Вторичные жёлчные кислоты: дезоксихолевая, образующаяся из холевой, и литохолевая, образующаяся из дезоксихолевой, хуже растворимы, медленнее всасываются в кишечнике, чем первичные жёлчные кислоты. Поэтому с фекалиями в основном удаляются вторичные жёлчные кислоты. Однако реабсорбированные вторичные жёлчные кислоты в печени опять превращаются в первичные и участвуют в эмульгировании жиров. За сутки из организма выводится 500-600 мг жёлчных кислот. Путь выведения жёлчных кислот одновременно служит и основным путём выведения холестерола из организма. Для восполнения потери жёлчных кислот с фекалиями в печени постоянно происходит синтез жёлчных кислот из холестерола в количестве, эквивалентном выведенным жёлчным кислотам. В результате пул жёлчных кислот (2-4 г) остаётся постоянным.
Нарушения переваривания и всасывания жиров. Стеаторея.
Нарушение переваривания жиров может быть следствием нескольких причин. Одна из них - нарушение секреции жёлчи из жёлчного пузыря при механическом препятствии оттоку жёлчи. Это состояние может быть результатом сужения просвета жёлчного протока камнями, образующимися в жёлчном пузыре, или сдавлением жёлчного протока опухолью, развивающейся в окружающих тканях. Уменьшение секреции жёлчи приводит к нарушению эмульгирования пищевых жиров и, следовательно, к снижению способности панкреатической липазы гидролизовать жиры. Нарушение секреции сока поджелудочной железы и, следовательно, недостаточная секреция панкреатической липазы также приводят к снижению скорости гидролиза жиров. В обоих случаях нарушение переваривания и всасывания жиров приводит к увеличению количества жиров в фекалиях - возникает стеа-торея (жирный стул). В норме содержание жиров в фекалиях составляет не более 5%. При стеаторее нарушается всасывание жирорастворимых витаминов (A, D, E, К) и незаменимых жирных кислот, поэтому при длительно текущей стеаторее развивается недостаточность этих незаменимых факторов питания с соответствующими клиническими симптомами. При нарушении переваривания жиров плохо перевариваются и вещества нелипидной природы, так как жир обволакивает частицы пищи и препятствует действию на них ферментов.
41.РЕСИНТЕЗ. ХИЛОМИКРОНЫ. АПОПРОТЕИНЫ И Т.Д
Ресинтезтаг в кишечнике. После всасывания продуктов гидролиза жиров жирные кислоты и 2-моноацилглицеролы в клетках слизистой оболочки тонкого кишечника включаются в процесс ресинтеза с образованием триацилглицеролов. Жирные кислоты вступают в реакцию этерификации только в активной форме в виде производных коэнзима А, поэтому первая стадия ресинтеза жиров - реакция активации жирной кислоты:
HSКоА + RCOOH + АТФ → R-CO
КоА + АМФ + Н4Р2О7.
Реакция катализируется ферментом ацил-КоА-синтетазой (тиокиназой). Затем ацилКоА участвует в реакции этерификации 2-моноацилглицерола с образованием сначала диацилгли-церола, а затем триацилглицерола. Реакции ресинтеза жиров катализируют ацилтранеферазы. В реакциях ресинтеза жиров участвуют, как правило, только жирные кислоты с длинной углеводородной цепью. В ресинтезе жиров участвуют не только жирные кислоты, всосавшиеся из кишечника, но и жирные кислоты, синтезированные в организме, поэтому по составу ре-синтезированные жиры отличаются от жиров, полученных с пищей. Однако возможности "адаптировать" в процессе ресинтеза состав пищевых жиров к составу жиров организма человека ограничены, поэтому при поступлении с пищей жиров с необычными жирными кислотами, например бараньего жира, в адипоцитах появляются жиры, содержащие кислоты, характерные для бараньего жира (насыщенные разветвлённые жирные кислоты). В клетках слизистой оболочки кишечника происходит активный синтез глицерофосфолипидов, необходимых для формирования структуры липопротеинов - транспортных форм липидов в крови.
Транспорт жиров. Липиды в водной среде (а значит, и в крови) нерастворимы, поэтому для транспорта липидов кровью в организме образуются комплексы липидов с белками - липопротеины. Все типы липопротеинов имеют сходное строение - гидрофобное ядро и гидрофильный слой на поверхности (рис. 8-18). Гидрофильный слой образован белками, которые называют апопротеинами, и амфифильными молекулами липидов- фосфолипидами и холестеролом. Гидрофильные группы этих молекул обращены к водной фазе, а гидрофобные части - к гидрофобному ядру липопротеина,в котором находятся транспортируемые липиды. Некоторые апопротеины интегральные и не могут быть отделены от липопротеина, а другие могут свободно переноситься от одного типа липопротеина к другому. Апопротеинывыполняютнесколькофункций:
Формируют структуру липопротеинов;
взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов;
служат ферментами или активаторами ферментов, действующих на липопротеины.
Образование хиломикронов.
Жиры, образовавшиеся в результате ресинтеза в клетках слизистой оболочки кишечника, упаковываются в ХМ. Основной апопротеин в составе ХМ - белок апоВ-48. Этот белок закодирован в том же гене, что и белок ЛПОНП - В-100, который синтезируется в печени. В кишечнике в результате посттранскрипционных превращений "считывается" последовательность мРНК, которая кодирует только 48% от длины белка В-100, поэтому этот белок называется апоВ-48. Белок апоВ-48 синтезируется в шероховатом ЭР и там же гликозилируется. Затем в аппарате Гольджи происходит формирование ХМ, называемых "незрелыми". По механизму экзоцитоза они выделяются в хилус, образующийся в лимфатической системе кишечных ворсинок, и через главный грудной лимфатический проток попадают в кровь. В лимфе и крови с ЛПВП на ХМ переносятся апопротеины Е (апоЕ) и С-П (апоС-П); ХМ превращаются в "зрелые". ХМ имеют довольно большой размер, поэтому после приёма жирной пищи они придают плазме крови опалесцирующий, похожий на молоко, вид. ХМ транспортируют жир к различным тканям, где он утилизируется, поэтому концентрация ХМ в крови постепенно снижается, и плазма опять становится прозрачной. ХМ исчезают из крови в течение нескольких часов.
Липопротеинлипазы. В крови триацилглицеролы, входящие в состав зрелых ХМ, гидролизуются ферментом липопротеин-липазой, или ЛП-липазой. ЛП-липа-за связана с гепарансульфатом (гетерополисаха-ридом), находящимся на поверхности эндотелиальных клеток, выстилающих стенки капилляров кровеносных сосудов. ЛП-липаза гидролизует молекулы жиров до глицерола и 3 молекул жирных кислот. На поверхности ХМ различают 2 фактора, необходимых для активности ЛП-липазы - апоС-П и фосфолипиды. АпоС-П активирует этот фермент, а фосфолипиды участвуют в, связывании фермента с поверхностью ХМ. ЛП-липаза синтезируется в клетках многих тканей: жировой, мышечной, в лёгких, селезёнке, клетках лактирующей молочной железы. Изоферменты ЛП-липазы в разных тканях отличаются по значению Кm: ЛП-липаза жировой ткани имеет в 10 раз более высокое значение Кm, чем, например, ЛП-липаза сердца, поэтому гидролиз жиров ХМ в жировой ткани происходит в абсорбтивный период. Жирные кислоты поступают в адипоциты и используются для синтеза жиров. В постабсорбтивном состоянии, когда количество жиров в крови снижается, ЛП-липаза сердечной мышцы продолжает гидролизовать жиры в составе ЛПОНП, которые присутствуют в крови в небольшом количестве, и жирные кислоты используются этой тканью как источники энергии, даже при низкой концентрации жиров в крови. ЛП-липазы нет в печени, но на поверхности клеток этого органа имеется другой фермент - печёночная липаза, не действующая на зрелые ХМ, но гидролизующая жиры в ЛППП, которые образуются из ЛПОНП.
Гиперхиломикронемия, гипертриглицеролемия.
После приёма пищи, содержащей жиры, развивается физиологическая гипертриглицеролемия и, соответственно, гиперхиломикронемия, которая может продолжаться до нескольких часов.
Скорость удаления ХМ из кровотока зависит от:
активности ЛП-липазы;
присутствия ЛПВП, поставляющих апопротеины С-II и Е для ХМ;
активности переноса апоС-II и апоЕна ХМ.
Генетические дефекты любого из белков, участвующих в метаболизме ХМ, приводят к развитию семейнойгиперхиломикронемии - гиперлипопротеинемии типа I. У таких больных в постабсорбтивном периоде концентрация триацилглицеролов повышена (более 200 мг/дл), плазма крови по виду напоминает молоко и при оставлении на холоде (+4 °С) в ней всплывают белые жирные хлопья, что характерно для гипертриглицеролемии и гиперхиломикронемии. В тяжёлых случаях при этом заболевании происходит отложение триацилглицеролов в коже и сухожилиях в виде ксантом, у пациентов рано нарушается память, появляются боли в животе из-за сужения просвета сосудов и уменьшения кровотока, нарушается функция поджелудочной железы, что часто бывает причиной смерти больных. Если концентрация триацилглицеролов в крови превышает 4000 мг/дл, то липиды откладываются в сетчатке глаза, однако это не всегда влияет на зрительную функцию. При лечении гиперхиломикронемий необходимо прежде всего
снизить потребление жиров с пищей, так как ХМ транспортируют экзогенные жиры. |
|
|
 Скачать 2.83 Mb.
Скачать 2.83 Mb.