ШПОРЫ БХ 2 ИТОГОВАЯ. Эндергонические процессы, протекающие с увеличением свободной энергии. Катаболические превращения
 Скачать 2.83 Mb. Скачать 2.83 Mb.
|
|
Вопрос 54. Биосинтез холестерина и его этапы. Регуляция. Реакции синтеза холестерола происходят в цитозоле клеток. Это один из самых длинных метаболических путей в организме человека. Сложный путь синтеза холестерола можно разделить на 3 этапа Первый этап заканчивается образованием мевалоната (мевалоновой кислоты). Две молекулы ацетил-КоА конденсируются ферментом тиолазой с образованием ацетоацетил-КоА. Фермент щдроксиметилглутарил-КоА-синтаза присоединяет третий ацетильный остаток с образованием ГМГ-КоА (3-гидрокси-3-метилглутарил-КоА). Эта последовательность реакций сходна с начальными стадиями синтеза кетоновых тел (см. рис. 8-33). Однако реакции синтеза кетоновых тел происходят в митохондриях печени, а реакции синтеза холестерола - в цитозоле клеток. Следующая реакция, катализируемая ГМГ-КоА-редуктазой, является регуляторной в метаболическом пути синтеза холестерола. В этой реакции происходит восстановление ГМГ-КоА до мевалоната с использованием 2 молекул NADPH. Фермент ГМГ-КоА-редуктаза - гликопротеин, пронизывающий мембрану ЭР, активный центр которого выступает в цитозоль.На втором этапе синтеза мевалонат превращается в пятиуглеродную изопреноидную структуру, содержащую пирофосфат - изопентенилпирофосфат. Продукт конденсации 2 изопреновых единиц - геранилпирофосфат. Присоединение ещё 1 изопреновой единицы приводит к образованию фарнезилпирофосфата - соединения, состоящего из 15 углеродных атомов. Две молекулы фарнезилпирофосфата конденсируются с образованием сквалена - углеводорода линейной структуры, состоящего из 30 углеродных атомов.На третьем этапе синтеза холестерола сквален через стадию образования эпоксида ферментом циклазой превращается в молекулу ланостерола, содержащую 4 конденсированных цикла и 30 атомов углерода. Далее происходит 20 последовательных реакций, превращающих ланостерол в холестерол. На последних этапах синтеза от ланостерола отделяется 3 атома углерода, поэтому холестерол содержит 27 углеродных атомов. У холестерола имеется насыщенная разветвлённая боковая цепь из 8 углеродных атомов в положении 17, двойная связь в кольце В между атомами углерода в положениях 5 и 6, а также гидроксильная группа в положении 3. В организме человека изопентенилпирофосфат также служит предшественником убихинона (KoQ) и долихола, участвующего в синтезе гликопротеинов. Регуляция ключевого фермента синтеза холестерола (ГМГ-КоА-редуктазы) происходит разными способами. Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы (рис. 8-67). При увеличении соотношения инеулин/глюкагон этот фермент дефосфорилируется и переходит в активное состояние. Действие инсулина осуществляется через 2 фермента:
Следовательно, в абсорбтивный период синтез холестерола увеличивается. В этот период увеличивается и доступность исходного субстрата для синтеза холестерола - ацетил-КоА (в результате приёма пищи, содержащей углеводы и жиры, так как ацетил-КоА образуется при распаде глюкозы и жирных кислот). В постабсорбтивном состоянии глюкагон через протеинкиназу А стимулирует фосфорилирование ГМГ-КоА-редуктазы, переводя её в неактивное состояние. Это действие усиливается тем, что одновременно глюкагон стимулирует фосфорилирование и инактивацию фосфатазы ГМГ-КоА-редуктазы и фосфорилирование киназы ГМГ-КоА-редуктазы, удерживая, таким образом, ГМГ-КоА-редуктазу в фосфорилированном неактивном состоянии. В результате синтез холестерола в постабсорбтивном периоде и при голодании ингибируется. Ингибирование синтеза ГМГ-КоА-редуктазы. Конечный продукт метаболического пути (холестерол) снижает скорость транскрипции гена ГМГ-КоА-редуктазы, подавляя таким образом собственный синтез. В печени активно идёт синтез жёлчных кислот из холестерола, поэтому и жёлчные кислоты (как конечные продукты синтеза) подавляют активность гена ГМГ-КоА-редуктазы (рис. 8-67). Так как молекула ГМГ-КоА-редуктазы существует около 3 ч после синтеза, то ингибирование синтеза этого фермента кочечным продуктом метаболического пути (холестеролом) является эффективной регуляцией. 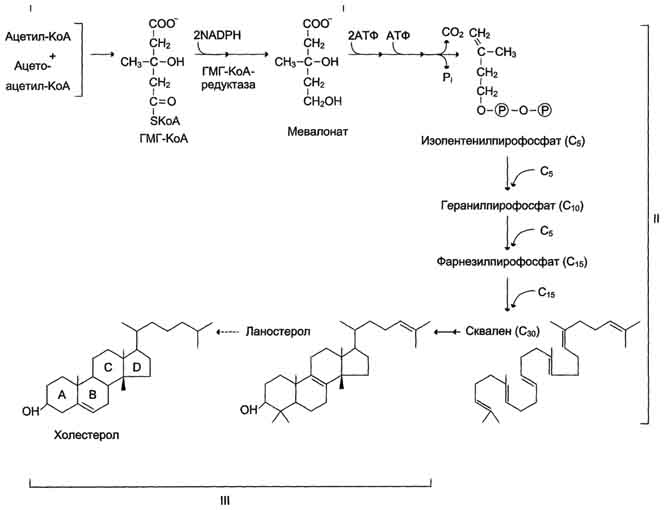 Вопрос 55. ЛПНП и ЛПВП как транспортные формы холестерина в крови, их роль в обмене холестерина. Атерогенные и атерогенные ЛП. Рецепторы ЛПНП. Вопрос 55. ЛПНП и ЛПВП как транспортные формы холестерина в крови, их роль в обмене холестерина. Атерогенные и атерогенные ЛП. Рецепторы ЛПНП.На ЛППП, оставшиеся в крови, продолжает действовать ЛП-липаза, и они превращаются в ЛПНП, содержащие до 55% холестерола и его эфиров. Апопротеины Е и С-II реносятся обратно в ЛПВП. Поэтому основным апопротеином в ЛПНП служит апоВ-100. Апопротеин В-100 взаимодействует с рецепторами ЛПНП и таким образом определяет дальнейший путь холестерола. ЛПНП - основная транспортная форма холестерола, в которой он доставляется в ткани. Около 70% холестерола и его эфиров в крови находится в составе ЛПНП. Из крови ЛПНП поступают в печень (до 75%) и другие ткани, которые имеют на своей поверхности рецепторы ЛПНП. Рецептор ЛПНП - сложный белок, состоящий из 5 доменов и содержащий углеводную часть рецепторы ЛПНП синтезируются в ЭР и аппарате Гольджи, а затем экспонируются на поверхности клетки, в специальных углублениях, выстланных белком клатрином. Эти углубления называют окаймлёнными ямками. Выступающий на поверхность N-концевой домен рецептора взаимодействует с белками апоВ-100 и апоЕ; поэтому он может связывать не только ЛПНП, но и ЛППП, ЛПОНП, остаточные ХМ, содержащие эти апопротеины. Клетки тканей содержат большое количество рецепторов ЛПНП на своей поверхности: например, на одной клетке фибробласта имеется от 20 000 до 50 000 рецепторов. Из этого следует, что холестерол поступает в клетки из крови в основном в составе лпнп. Если количество холестерола, поступающего в клетку, превышает её потребность, то синтез рецепторов ЛПНП подавляется, что уменьшает поток холестерола из крови в клетки. При снижении концентрации свободного холестерола в клетке, наоборот, активируется синтез ГМГ-КоА-редуктазы и рецепторов ЛПНП. В регуляции синтеза рецепторов ЛПНП участвуют гормоны: инсулин и трийодтиронин (Т3), полрвые гормоны. Они увеличивают образование рецепторов ЛПНП, а глюкокортикоиды(в основном кортизол) уменьшают. Эффекты инсулина и Т3, вероятно, могут объяснить механизм гиперхолестеролемии и увеличение риска атеросклероза при сахарном диабете или гипотиреозе. ЛПВП выполняют 2 основные функции: они поставляют апопротеины другим ЛП в крови и участвуют в так называемом "обратном транспорте холестерола". ЛПВП синтезируются в печени и в небольшом количестве в тонком кишечнике в виде "незрелых липопротеинов" - предшественников ЛПВП. Они имеют дисковидную форму, небольшой размер и содержат высокий процент белков и фосфолипидов. В печени в ЛПВП включаются апопротеины А, Е, С-II, фермент ЛХАТ. В крови апоС-II и апоЕ переносятся с ЛПВП на ХМ и ЛПОНП. Предшественники ЛПВП пракгически не содержат холестерола и ТАГ и в крови обогащаются холестеролом, получая его из других ЛП и мембран клеток. Для переноса холестерола в ЛПВП существует сложный механизм. На поверхности ЛПВП находится фермент ЛХАТ - лецитишхолестерол-ацилтрансфераза. Этот фермент превращает холестерол, имеющий гидроксильную группу, выступающую на поверхность липопротеинов или мембран клеток, в эфиры холестерола. Радикал жирной кислоты переносится от фосфатидилхолита(лецитина) на гидроксильную группу холестерола. Реакция активируется апопротеином A-I, входящим в состав ЛПВП. Гидрофобная молекула, эфира холестерола перемещается внутрь ЛПВП. Таким образом, частицы ЛПВП обогащаются эфирами холестерола. ЛПВП увеличиваются в размерах, из дисковидных небольших частиц превращаются в частицы сферической формы, которые называют ЛПВП3, или "зрелые ЛПВП". ЛПВП3 частично обменивают эфиры холестерола на триацилглицеролы, содержащиеся в ЛПОНП, ЛППП и ХМ (рис. 8-70). В этом переносе участвует "белок, переносящий эфиры холестерина" (он также называется aпoD). Таким образом, часть эфиров холестерола переносится на ЛПОНП, ЛППП, а ЛПВП3 за счёт накопления триацилглицеролов увеличиваются в размерах и превращаются в ЛПВП2. ЛПОНП под действием ЛП-липазы превращаются сначала в ЛППП, а затем в ЛПНП. ЛПНП и ЛППП захватываются клетками через рецепторы ЛПНП. Таким образом, холестерол из всех тканей возвращается в печень в основном в составе ЛПНП, но в этом участвуют также ЛППП и ЛПВП2. Практически весь холестерол, который должен быть выведен из организма, поступает в печень и уже из этого органа выделяется в виде производных с фекалиями. Путь возвращения холестерола в печень называют "обратным транспортом" холестерола. Вопрос 56. Эйкозаноиды. Биосинтез, строение, номентклатура, биологические функции. Ингибиторы синтеза эйкозаноидов. Эйкозаноиды – биологически активные вещества , синтезируемые большинством клеток из полиеновых жк, содержащих 20 углеродных атомов. Эйкозаноиды, включающие в себя простагландины, тромбоксаны, лейкотриены и ряд других веществ, - высокоактивные регуляторы клеточных функций. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как "гормоны местного действия", влияя на метаболизм продуцирующей их клетки по аугокзэинному механизму, и на окружающие клетки - по паракринному механизму. Эйкозаноиды участвуют во многих процессах: регулируют тонус ГМК и вследствие этого влияют на АД, состояние бронхов, кишечника, матки. Эйкозаноиды регулируют секрецию воды и натрия почками, влияют на образование тромбов. Разные типы эйкозаноидов участвуют в развитии воспалительного процесса, происходящего после повреждения тканей или инфекции. Такие признаки воспаления, как боль, отёк, лихорадка, в значительной мере обусловлены действием эйкозаноидов. Избыточная секреция эйкозаноидов приводит к ряду заболеваний, например бронхиальной астме и аллергическим реакциям. Хотя субстраты для синтеза эйкозаноидов имеют довольно простую структуру (полистовые жирные кислоты), из них образуется большая и разнообразная группа веществ. Наиболее распространены в организме человека простагландины, которые впервые были выделены из предстательной железы, откуда и получили свое название. Позже было показано, что и другие ткани организма синтезируют простагландины и другие эйкозаноиды. Структура и номенклатура простагландинов и тромбоксанов . Простагландины обозначают символами, например PG А, где PG обозначает слово "простагландин", а буква А обозначает заместитель в пятичленном кольце в молекуле эйкозаноида. Каждая из указанных групп простагландинов состоит из 3 типов молекул, отличающихся по числу двойных связей в боковых цепях. Число двойных связей обозначают нижним цифровым индексом, например, PG Е2. Число двойных связей в боковых цепях простагландинов зависит от структуры предшественника - полистовой кислоты, из которой образовались простагландины. Две двойные связи полиеновой кислоты используются при образовании кольца в молекуле простагландина, а количество оставшихся двойных связей в радикалах, связанных с кольцом, определяет серию простагландина: 1 - если одна двойная связь, 2 - если две двойные связи и 3 - если в радикалах имеются три двойных связи. PG I - простациклины. Имеют 2 кольца в своей структуре: одно пятичленное, как и другие простагландины, а другое - с участием атома кислорода. Их также подразделяют в зависимости от количества двойных связей в радикалах (PG I2, PG I3). Тромбоксаны. В отличие от простагландинов, тромбоксаны синтезируются только в тромбоцитах, откуда и происходит их название, и стимулируют их агрегацию при образовании тромба. Тромбоксаны имеют шестичленное кольцо, включающее атом кислорода (рис. 8-46). Так же, как и другие эйкозаноиды, тромбоксаны могут содержать различное число двойных связей в боковых цепях, образуя ТХ А2, или ТХ A3, отличающиеся по активности. ТХ В2 - продукт катаболизма ТХ А2 и активностью не обладает. Циклооксигеназный путь: синтез простагландинов и тромбоксанов . Активация фосфолипаз. Синтез проетагландинов начинается только после отделения полиеновых кислот от фосфолипида мембраны под действием ферментов (рис. 8-47). Активация фосфолипаз, ассоциированных с мембранами, происходит под действием многих факторов: гормонов, гистамина, цитокинов, механического воздействия. Связывание стимулирующего агента с рецептором может активировать или фосфолипазу А2 или фосфолипазу С. Это зависит от типа клетки и типа рецепторов. После отделения арахидоновой кислоты от фосфолипида она выходит в цитозоль и в различных типах клеток превращается в разные эйкозаноиды. В клетках имеется 2 основных пути превращения арахидоновой кислоты: циклооксигеназный, приводящий к синтезу простагландинов, простациклинов и тромбоксанов, и липоксигеназный, заканчивающийся образованием лейкотриенов или других эйкозаноидов (рис. 8-48). Синтез простагландинов. Фермент, катализирующий первый этап синтеза простагландинов, называется PG Н2 синтазой и имеет 2 каталитических центра. Один из них называют циклооксигеназой, другой - пероксидазой. Этот фермент представляет собой димер гликопротеинов, состоящий из идентичных полипептидных цепей. Фермент имеет гидрофобный домен, погружённый в липидный слой мембран ЭР, и каталитический домен, обращённый в полость ЭР. В активном центре циклооксигеназы находится тирозин (385), в активном центре пероксидазы - простетическая группа - гем. В организме имеются 2 типа циклооксигеназ (PG Н2 синтаз). Циклооксигеназа 1 - конститутивный фермент, синтезирующийся с постоянной скоростью. Синтез циклооксигеназы 2 увеличивается при воспалении и индуцируется соответствующими медиаторами - цитокинами. Оба типа циклооксигеназ катализируют включение 4 атомов кислорода в арахидоновую кислоту и формирование пятичленного кольца. В результате образуется нестабильное гидропероксидпроизводное, называемое PG G2. Гидропероксид у 15-го атома углерода быстро восстанавливается до гидроксильной группы пероксидазой с образованием PG Н2. До образования PG Н2 путь синтеза разных типов простагландинов одинаков. Дальнейшие превращения PG Н2 специфичны для каждого типа клеток. Например, PG Н2 в клетках ГМК может быть восстановлен под действием PG E синтазы с образованием PG Е2 или под действием PG D синтазы с образованием PG D2. В тромбоцитах содержится фермент тромбоксансинтаза, превращающий тот же исходный PG Н2 в ТХ А2 обладающий сильным сосудосуживающим действием. В клетках эндотелия под действием фермента простациклинсинтазы из PG Н2 синтезируется PG I2 (простациклин), имеющий сосудорасширяющее действие. Воспаление - реакция организма на повреждение или инфекцию, направленная на уничтожение инфекционного агента и восстановление повреждённых тканей. Продукция медиаторов воспаления - эйкозаноидов, гистамина, кининов) - активируется каскадами реакций, запускающимися при внедрении инфекционных агентов или повреждении тканей. Многие эйкозаноиды выполняют функцию медиаторов воспаления и действуют на всех этапах воспаления. В результате увеличивается проницаемость капилляров, транссудат и лейкоциты проходят через сосудистую стенку. Лейкотриен В4 и липоксин А4 являются мощными факторами хемотаксиса; взаимодействуя с рецепторами, стимулируют движение лейкоцитов в область воспаления и секрецию ими лизосомальных ферментов и фагоцитоз чужеродных частиц.На семейства эйкозаиоидов, синтезируемых в организме, влияет состав жирных кислот пищи. Если с пищей поступает больше эйкозапентаеновой кислоты (20:5, ю-3), в большом количестве содержащейся в рыбьем жире, то эта кислота включается преимущественно в фосфо-липиды мембран (вместо арахидоновой) и после действия фосфодипазы А2 служит основным субстратом для синтеза эйкозаноидов. Это имеет существенное влияние на свёртывание крови. Аспирин - препарат, подавляющий основные признаки воспаления. Механизм противовоспалительного действия аспирина стал понятен, когда обнаружили, что он ингибирует циклооксигеназу. Следовательно, он уменьшает синтез медиаторов воспаления и, таким образом, уменьшает воспалительную реакцию. Циклооксигеназа необратимо ингибируется путём ацетилирования серина в положении 530 в активном центре (рис. 8-54). Однако эффект действия аспирина не очень продолжителен, так как экспрессия гена этого фермента не нарушается и продуцируются новые молекулы фермента. Другие нестероидные противовоспалительные препараты (например, ибупрофен и ацетаминофен) действуют по конкурентному механизму, связываясь в активном центре фермента, и также снижают синтез простагландинов. Вопрос 57. Липиды биомембран. Их роль. Участие фосфолипаз в обмене фосфолипидов. Биомембраны состоят из липидов, белков и углеводов. Соотношение этих компонентов варьирует от одной мембраны к другой. Разнообразие мембранных липидов и их относительное содержание в различных мембранах. Видно, что в количественном отношении преобладают фосфолипиды, затем следуют гликолипиды и холестерин. Триацилглицерины (нейтральные жиры) в мембранах не обнаружены. Холестерин найден почти исключительно в эукариотических клетках. Мембраны животных клеток содержат холестерина гораздо больше, чем мембраны растений, в которых холестерин обычно заменен другими стеринами. У прокариот за несколькими исключениями вообще нет холестерина. Внутренняя митохондриальная мембрана эукариот также почти полностью лишена холестерина. Фосфолипиды - большой класс липидов, получивший своё название из-за остатка фосфорной кислоты, придающего им свойства амфифильности. Благодаря этому свойству фосфолипиды формируют бислойную структуру мембран, в которую погружены белки. Клетки или отделы клеток, окружённые мембранами, отличаются по составу и набору молекул от окружающей среды, поэтому химические процессы в клетке разделены и ориентированы в пространстве, что необходимо для регуляции метаболизма. Стероиды, представленные в животном мире холестеролом и его производными, выполняют разнообразные функции. Холестерол - важный компонент мембран и регулятор свойств гидрофобного слоя. Производные холестерола (жёлчные кислоты) необходимы для переваривания жиров. Стероидные гормоны, синтезируемые из холестерола, участвуют в регуляции энергетического, водно-солевого обменов, половых функций. Кроме стероидных гормонов, многие производные липидов выполняют регуляторные функции и действуют, как и гормоны, в очень низких концентрациях. Например, тромбоцитактивирующий фактор - фосфолипид особой структуры - оказывает сильное влияние на агрегацию тромбоцитов в концентрации 10-12 М; эйкозаноиды, производные полиеновых жирных кислот, вырабатываемые почти всеми типами клеток, вызывают разнообразные биологические эффекты в концентрациях не более 10-9 М. Из приведённых примеров следует, что липиды обладают широким спектром биологических функций.Расщепление фосфолипидов идет гидролитическим путем при участии ферментов фосфолипаз, поступающих в двенадцатиперстную кишку с соком поджелудочной железы. Фосфолипаза А1 катализирует расщепление сложноэфирной связи между ацилом и первым атомом углерода глицерола.Фосфолипаза А2 катализирует гидролиз сложноэфирной связи между ацилом и вторым атомом углерода глицерола. Фосфолипаза С катализирует гидролитический разрыв связи между третьим атомом углерода глицерола и остатком фосфорной кислоты, а фосфолипаза Д ДД сложноэфирной связи между остатком фосфорной кислоты и остатком аминоспирта. В результате действия этих четырех ферментов фосфолипиды расщепляются до свободных жирных кислот, глицерола, фосфорной кислоты и аминоспирта или его аналога, например, аминокислоты серина, однако часть фосфолипидов расщепляется при участии фосфолипазы А2 только до лизофосфолипидов и в таком виде может поступать в стенку кишечника. Вопрос 58. Холестерол - стероид, характерный для животных организмов. основное место синтеза - печень-более 50% х., в тонком кишечнике - 15- 20%, остальной х. синтезируется в коже, коре надпочечников, половых железах. В сутки в организме синтезируется около 1 г х.; с пищей поступает 300-500 мг. функций: входит в состав всех мембран клеток и влияет на их св-ва, исходный субстрат в синтезе жёлчных кислот и стероидных гормонов. Предшественники в метаболическом пути синтеза х. превращаются также в убихинон - компонент дыхательной цепи и долихол, участвующий в синтезе гликопротеинов. за счёт своей гидроксильной группы может образовывать эфиры с жирными кислотами. Этерифицированный х.преобладает в крови. Х. и его эфиры - гидрофобные молекулы, поэтому они транспортируются кровью только в составе разных типов ЛП. Нарушения обмена х. приводят к одному из наиболее распространённых заболеваний - атеросклерозу. Накопление х. в организме приводит к развитию желчнокаменной болезни. Пути поступления х.: с пищей извне и процесс синтеза собственного х. в печени из ацитилКоА. холестерол поступает в клетки из крови в основном в составе лпнп Пути использования и выведения х.: вывед с фекалиями, синт Д3, выдел с кожнми покровами, синт стероидн гормонов, синтез и вывед желчных к-т. Определение содержания общего х. в сыворотке крови: свободный х. образуется при гидролизе эфиров холестерина ферментом холестролэстеразой. Х. окисляют кислородом воздуха с ферментом холестеролоксидазой с образованием перекиси водорода. образуется окрашивание продукта блягодаря окислению перекисью водорода хромогенных субстратов. В ФЭКе измеряют оптическую плотность проб. Клиническое значение. Повышение уровня х. в крови — один из основных факторов риска атеросклероза. Развитие ГЛП может быть обусловлено генетическими аномалиями и факторами среды, а также такими заболеваниями, как сахарный диабет, патология печени, почек, гормональными нарушениями. липидограмма позволяет как диагностировать нарушения липидного обмена, так и оценить риск развития атеросклероза и ишемической болезни сердца. Норма ХС в крови: Содержание холестерина в крови человека может варьировать от 3,6 ммоль/л до 7,8 ммоль/л. Оптимальный уровень: менее 5 ммоль/л Слегка высокий уровень холестерина: между 5 и 6,4 ммоль/л Умеренно высокий уровень холестерина: между 6,5 и 7,8 ммоль/л Очень высокий уровень холестерина: выше 7,8 ммоль/л |
