Патфиз ч.1. Патфиз ч. Гл. 1 Введение в предмет Гл. 2 Общая нозология
 Скачать 9.21 Mb. Скачать 9.21 Mb.
|
|
Общая управляемая гипотермия • Область применения Выполнение операций в условиях значительного снижения или даже временного прекращения кровообращения. Это получило название операций на так называемых «сухих» органах: сердце, мозге и некоторых других. Наиболее широко общая искусственная гибернация используется при операциях на сердце для устранения дефектов его клапанов и стенок, а также на крупных сосудах, что требует остановки кровотока. • Преимущества Существенное возрастание устойчивости и выживаемости клеток и тканей в условиях гипоксии при сниженной температуре. Это даёт возможность отключить орган от кровоснабжения на несколько минут с последующим восстановлением его жизнедеятельности и адекватного функционирования. • Диапазон температуры † Обычно используют гипотермию со снижением ректальной температуры до 30–28 °C. При необходимости длительных манипуляций создают более глубокую гипотермию с использованием аппарата искусственного кровообращения, миорелаксантов, ингибиторов метаболизма и других воздействий. При проведении продолжительных операций (несколько десятков минут) на «сухих» органах выполняют «глубокую» гипотермию (ниже 28 °C), применяют аппараты искусственного кровообращения и дыхания, а также специальные схемы введения ЛС и средств для наркоза. † Наиболее часто для общего охлаждения организма применяют жидкость с температурой +2–12 °C, циркулирующую в специальных «холодовых» костюмах, одеваемых на пациентов или в «холодовых» одеялах, которыми их укрывают. Дополнительно используют также ёмкости со льдом и воздушное охлаждение кожных покровов пациента. • Медикаментозная подготовка С целью устранения или снижения выраженности адаптивных реакций организма в ответ на снижение его температуры, а также для выключения стрессреакции непосредственно перед началом охлаждения пациенту дают общий наркоз, вводят нейроплегические вещества, миорелаксанты в различных комбинациях и дозах. В совокупности указанные воздействия обеспечивают значительное снижение обмена веществ в клетках, потребления ими кислорода, образования углекислоты и метаболитов, предотвращают нарушения КЩР, дисбаланса ионов и воды в тканях. • Эффекты медицинской гибернации При гипотермии 30–28 °C (в прямой кишке) † не наблюдается жизненно опасных изменений функции коры головного мозга и рефлекторной деятельности нервной системы; † снижается возбудимость, проводимость и автоматизм миокарда; † развивается синусовая брадикардия, † уменьшаются ударный и минутный выбросы сердца, † понижается АД, † снижается функциональная активность и уровень метаболизма в органах и тканях. Локальная управляемая гипотермия Локальная управляемая гипотермия отдельных органов или тканей (головного мозга, почек, желудка, печени, предстательной железы и др.) применяется при необходимости проведения оперативных вмешательств или других лечебных манипуляций на них: коррекции кровотока, пластических процессов, обмена веществ, эффективности ЛС и др
Инфекционный процесс (инфП) — типовой патологический процесс, возникающий в организме человека под действием микроорганизмов. ИнфП представляет собой комплекс взаимосвязанных изменений: функциональных, морфологических, иммунобиологических, биохимических и других, лежащих в основе развития конкретных инфекционных болезней (инфБ). ИнфБ по распространённости устойчиво удерживают третье место в мире (после болезней сердечно-сосудистой системы и онкологических заболеваний). Крупные эпидемии и пандемии инфБ уносили многие миллионы жизней: от эпидемии чумы в средние века погибла треть населения Европы; в XVIIXVIII веках натуральной оспой ежегодно заболевало около 10 млн. человек. Вместе с тем в этот период: • Выработаны принципы борьбы с эпидемиями (например, сжигание одежды больных, трупов умерших, изоляция пациентов). • Открыты возбудители основных инфБ человека (сибирской язвы, дифтерии, столбняка и др.). • Установлено, что патогенные для человека бактерии способны вырабатывать токсины, с действием которых связано развитие инфекционного процесса. Аргументом в пользу важной роли бактериальных токсинов в развитии инфБ явилась высокая клиническая эффективность использования для их лечения сывороток, что способствовало существенному снижению летальности от инфБ. В России в настоящее время ежегодно регистрируется более 30 млн. больных инфБ, включая грипп и острые респираторные заболевания. Общей тенденцией является изменение спектра регистрируемых инфБ. Параллельно с увеличением доли заболеваний, вызываемых условнопатогенными бактериями, появились принципиально новые возбудители (ВИЧинфекция, прионные инфекции, геморрагические лихорадки из группы арбовирусных инфекций и пр.). ТЕРМИНОЛОГИЯ Выделяют следующие виды инфП. • Сепсис — тяжёлая генерализованная форма инфП, обусловленная размножением микроорганизмов в крови и нередко в других биологических жидкостях организма. • Септикопиемия — инфП, характеризующийся вторичным развитием гнойных очагов в различных тканях и органах у пациентов с сепсисом. • Бактериемия, вирусемия — наличие в крови бактерий и/или вирусов без признаков их размножения. Является одним из этапов развития ряда инфП. • Микстинфекция — инфП, вызванный одновременно двумя и более возбудителями. • Реинфекция — повторное (после выздоровления пациента) возникновение инфП, вызванного тем же микроорганизмом. • Суперинфекция — повторное инфицирование организма тем же возбудителем до периода выздоровления. • Вторичная инфекция — инфП, развивающийся на фоне уже имеющейся (первичной) инфБ, вызванной другим микроорганизмом. ЭТИОЛОГИЯ Организм человека — идеальный объект для роста и размножения микробов. Он обеспечивает достаточно высокую стабильность основных параметров внутренней среды (температуры, электролитного состава, рН и др.) и лёгкую доступность питательных веществ для микроорганизмов. ВЗАИМООТНОШЕНИЯ МАКРО И МИКРООРГАНИЗМОВ Макро и микроорганизмы могут находится в различных отношениях: паразитизма, мутуализма и комменсализма (табл. 7–1). Таблица 7–1. Основные формы симбиоза макро и микроорганизма
Паразитизм — форма антагонизма, при которой микроорганизм использует макроорганизм как источник питания и объект постоянного или временного обитания. Мутуализм — форма взаимовыгодного сосуществования микро и макроорганизма (например, бактерии из группы кишечной микрофлоры и организм). Комменсализм — форма взаимоотношения микро и макроорганизма, при которой жизнедеятельность микробов в макроорганизме не наносит последнему вреда (например, нормальная микрофлора кишечника, кожи, слизистых оболочек). ВИДЫ ВОЗБУДИТЕЛЕЙ К возбудителям инфБ относятся простейшие, грибы, бактерии, вирусы и прионы. Каждый из вышеуказанных возбудителей инфБ обусловливает специфические черты инфП. В значительной мере они определяются природой микроорганизма. СВОЙСТВА ВОЗБУДИТЕЛЕЙ Классическая модель инфП наиболее типична для бактериальных инфекций. В отличие от этого, развитие инфП при вирусных инфекция имеет существенные особенности в связи с тем, что вирусы являются «генетическими паразитами». Важным свойством микроорганизмовпаразитов является их патогенность — способность вызывать определённую инфБ. ПАТОГЕННОСТЬ Патогенность — видовой признак (присущий представителям одного и того же вида возбудителя). Этот признак закреплён в генетической программе микроорганизма и, следовательно, передается по наследству. Свойство патогенности означает способность микроорганизма: • проникать в макроорганизм, • размножаться в нём, • вызывать болезнь с патогенезом, характерным для данного возбудителя. Мерой патогенности является фенотипическое свойство — вирулентность. ВИРУЛЕНТНОСТЬ Вирулентность — свойство, характеризующее степень болезнетворности данного микроорганизма. Она зависит как от характеристик микроорганизма, так и от восприимчивости макроорганизма. ФАКТОРЫ ПАТОГЕННОСТИ Факторы патогенности перечислены на рис. 7–1. 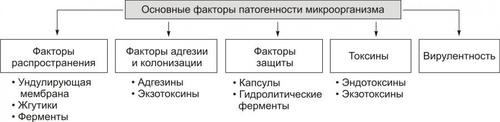 Рис. 7–1. Основные факторы патогенности микроорганизмов. Факторы распространения Факторы распространения обеспечивают или облегчают проникновение возбудителя во внутреннюю среду организма и распространение в ней. К ним относятся: • ферменты (например, гиалуронидаза, коллагеназа, нейраминидаза); • жгутики (например, у холерного вибриона, кишечной палочки, протея); • ундулирующая мембрана (например, у спирохет и некоторых простейших). Факторы адгезии и колонизации Факторы адгезии и колонизации способствуют попадающим в организм хозяина микроорганизмам взаимодействовать со специфическими рецепторами клеток, обеспечивая тем самым возможность паразитирования, размножения и образования колоний. • Адгезивные молекулы — поверхностные химические структуры микробных клеток белковой или полисахаридной природы. Различные адгезины обеспечивают прочность взаимодействия микробов с определёнными клетками макроорганизма. • Колонизация — размножение и образование большого количества однородных микробов (колоний). Этому способствуют также многие экзотоксины. Факторы защиты К факторам защиты возбудителя от бактерицидных механизмов организма хозяина относятся: • капсулы, механически защищающие микроб от фагоцитоза (таким свойством обладают, например, возбудители сибирской язвы, гонореи, туберкулёза); • факторы, угнетающие различные стадии фагоцитоза и реакции иммунитета (например, каталаза, содержащаяся у отдельных штаммов стафилококка разрушает H2O2 и тем самым угнетает процесс переваривания микробов в фагоците; протеаза гидролизует Ig; коагулаза стимулирует свёртывание белков плазмы крови, в том числе — АТ). Токсины Токсины — вещества, оказывающие повреждающее действие на клетки и ткани организма хозяина (рис. 7–2). 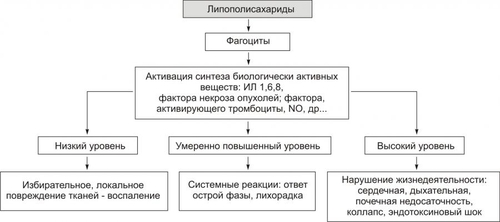 Рис. 7–2. Дозозависимые эффекты биологически активных веществ, образующихся под действием ЛПС. Описано более 50 разновидностей бактериальных токсинов. По происхождению в макроорганизме их подразделяют на эндогенные (эндотоксины) и экзогенные (экзотоксины). Эндотоксины Эндотоксины — вещества, выделяемые бактериями в среду обитания при их разрушении. Образование токсинов контролируется генами хромосом или/и плазмидами (например, Col, F, R), которые включают в себя tox–транспозоны или фаги. • Эндотоксин обладает классическими признаками, характерными для ядов (например, токсическое действие в минимальных дозах, взаимодействие со специфическими рецепторами, селективность действия, термостабильность и др.). • Эндотоксины являются липополисахаридами (ЛПС). Они относятся к основным структурным компонентам внешней мембраны практически всех грамотрицательных бактерий (в том числе и непатогенных для человека). Биологическая активность эндотоксина определяется его гидрофобным компонентом — липидом А. • Механизм действия ЛПС in vivo не носит специфического характера. † При попадании в организм ЛПС поглощается фагоцитами (лейкоцитами, макрофагами, купферовскими клетками и др.). † Указанные клетки активируются, синтезируют и секретируют в окружающую среду значительное количество БАВ липидной и белковой природы: Пг, активирующий тромбоциты фактор (PAF), лейкотриены, ИЛ, ИФН, ФНОα, колониестимулирующие факторы и др. † В крови эндотоксин взаимодействует с ЛПВП и белком, связывающим его. Этот липопротеинсвязывающий белок катализирует перенос его же мономерной формы на мембрану клеткимишени (моноциты, нейтрофилы). † На клеточной мембране происходит связывание липопротеинсвязывающего белка с CD14. Этот белок выполняет функцию «рецептора–мусорщика», ответственного за удаление молекулы эндотоксина с поверхности клетки с помощью эндоцитоза, а также презентирует молекулы эндотоксина «истинному» рецептору. Описаны также другие мембранные белки, выполняющие функцию рецептора для ЛПС. • Повреждающий эффект ЛПС реализуется при участии ИЛ 1–8, ФНО, PAF. • В настоящее время выделен ряд критических этапов, воздействие на которые способно подавить активацию клетокмишеней и блокировать патогеное действие эндотоксинов. Экзотоксины Экзотоксины — вещества, выделяемые в окружающую среду (т.е. секретируемые) микроорганизмами в процессе их жизнедеятельности. В зависимости от объекта воздействия в эукариотических клетках, экзотоксины условно подразделяют на мембранотоксины и токсины, влияющие на внутриклеточные структуры. • Действующие на цитолемму мембранотоксины обеспечивают повышение её проницаемости и/или деструкцию. К основным мембранотоксинам относят: † порообразующие неферментные вещества (могут приводить к апоптозу T-лимфоцитов), † соединения, оказывающие прямое ферментативное повреждение мембран (нейраминидаза, гиалуронидаза, фосфолипазы, сфингомиелиназы и пр.); † токсины, оказывающие детергентный эффект на липидный слой мембран (они содержат амфифильные соединения типа лизофосфолипидов). • Влияющие на внутриклеточные структуры токсины. В молекуле экзотоксинов этой подгруппы имеется две функционально различные части: рецепторная и каталитическая. Каждая из них ответственна за определённый этап взаимодействия с эукариотической клеткой. • Взаимодействие экзотоксинов с клетками протекает в четыре этапа: (1) связывания с рецептором, (2) интернализации, (3) перемещения в цитозоле, (4) внутриклеточных эффектов (табл. 7–2). Таблица 7–2. Этапы взаимодействия экзотоксинов микробов с клеткоймишенью
• Экзотоксины обладают исключительно высокой специфичностью действия. Благодаря этому они обеспечивают развитие синдромов, характерных для действия именно данного токсина (ботулизма, столбняка, дифтерии и пр.). Инфицирующая доза Инфицирующая доза — минимальное количество жизнеспособных возбудителей, необходимых для развития инфБ. От величины инфицирующей дозы микроба может зависеть тяжесть течения инфП, а в случае условнопатогенных бактерий — возможность его развития. Величина инфицирующей дозы в большой мере зависит от вирулентных свойств возбудителя. Между этими двумя характеристиками существует обратная зависимость: чем выше вирулентность, тем ниже инфицирующая доза и наоборот. Известно, что для такого высоковирулентного возбудителя как чумная палочка (Yersinia pestis) инфицирующая доза может колебаться от одной до нескольких микробных клеток; для Shigella dysenteriae (палочка ГригорьеваШига) — около 100 микробных клеток. В отличие от этого, инфицирующая доза низковирулентных штаммов может быть равна 105–106 микробных клеток. УСЛОВИЯ ВОЗНИКНОВЕНИЯ ИНФЕКЦИИ Они определяются входными воротами инфекции, путями её распространения в организме, механизмами противоинфекционной резистентности. ВХОДНЫЕ ВОРОТА Входные ворота инфекции — место проникновения микробов в макроорганизм. Такими воротами могут быть: • кожные покровы (например, для возбудителей малярии, сыпного тифа, кожного лейшманиоза), • слизистые оболочки дыхательных путей (для возбудителей гриппа, кори, скарлатины и др.), • слизистые оболочки ЖКТ (например, для возбудителей дизентерии, брюшного тифа), • слизистая оболочка мочеполовых органов (для возбудителей гонореи, сифилиса и др.), • стенки кровеносных и/или лимфатических сосудов, через которые возбудитель поступает в кровь или лимфу (например, при укусах членистоногих и животных, инъекциях и хирургических вмешательствах). Входные ворота могут определять нозологическую форму заболевания. Так, внедрение стрептококка в области миндалин вызывает ангину, через кожу — рожу или пиодермию, в области матки — эндометрит. ПУТИ РАСПРОСТРАНЕНИЯ БАКТЕРИЙ Известны следующие пути распространения бактерий в организме: • по межклеточному пространству (благодаря бактериальной гиалуронидазе или дефектам эпителия), • по лимфатическим капиллярам — лимфогенно, • по кровеносным сосудам — гематогенно, • по жидкости серозных полостей и спинномозгового канала. Большинство возбудителей имеет тропность к определённым тканям макроорганизма. Это определяется наличием молекул адгезии у микробов и специфических рецепторов у клеток макроорганизма, что ведёт к присоединению бактерий к рецепторам клетокмишеней. МЕХАНИЗМЫ ПРОТИВОИНФЕКЦИОННОЙ РЕЗИСТЕНТНОСТИ Существуют эффективные защитные системы, препятствующие проникновению возбудителей в организм, их размножению и реализации их патогенных эффектов. Особенно велика роль факторов, тормозящих проникновение патогенных или условнопатогенных бактерий. В качестве примера в табл. 7–3 представлены основные защитные факторы ЖКТ. Таблица 7–3. Основные защитные факторы желудочнокишечного тракта
Учитывая наличие защитных факторов макроорганизма, попадание в него инфекционного агента не означает обязательного и, тем более, немедленного развития инфБ. В зависимости от условий инфицирования и состояния защитных систем, инфП может вообще не развиться или протекать в форме бактерионосительства. В последнем случае какиелибо системные ответные реакции организма (включая иммунные) не выявляются. ОБЩИЙ ПАТОГЕНЕЗ Взаимодействие микроорганизмов и фагоцитов В механизме развития инфП ключевую роль играет взаимодействие возбудителей болезней и фагоцитов. Результат этого взаимодействия во многом определяет особенности течения инфП. В классическом варианте защитная роль фагоцитов состоит в поглощении и уничтожении микроорганизмов. Однако возбудители некоторых инфБ обладают резистентностью к эффекторным механизмам фагоцитов и даже способны размножаться в них (табл. 7–4). Таблица 7–4. Некоторые виды микроорганизмов, размножающихся в макрофагах
Вирусы могут проникать в фагоцитирующие клетки, изменяя их функциональную активность. В табл. 7–5 представлены данные о влиянии некоторых патогенных для человека вирусов на жизнедеятельность лейкоцитов. Таблица 7–5. Влияние вирусов на функциональную активность полиморфноядерных лейкоцитов in vivo и in vitro
|
