конспект лекций.Химия(органическая химия).dos. конспект лекций.Химия(органическая химия). Конспект лекций по дисциплине для студентов, обучающихся по специальностям и направлениям 050100. 62Естественнонаучное образование
 Скачать 1.49 Mb. Скачать 1.49 Mb.
|
|
Изомерия. 1. Структурная Для диеновхарактерны следующие виды: а) различное строение углеродной цепи (для углеводородов с числом атомов углерода ≥ 4); б) различное расположение кратной связи (для углеводородов с числом атомов углерода ≥ 4); в) межклассовая. Межклассовыми изомерами алкадиенов могут быть алкины, циклоалкены. 2. Геометрическая изомерия: Геометрическая изомерия характерна для сопряженных диенов, у которых в концевых СН2-группах атомы водорода замещены на другие атомы или радикалы: 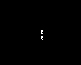  транс, цис-изомер цис, цис-изомер Сопряженные алкадиены могут существовать в двух пространственных формах (конформациях):  s-цис-формаs-транс-форма s-транс-формастабильнее (95%)s-цис-формы. Строение алкадиенов. Строение изолированных диенов практически не отличается от алкенов. В кумулированных диенах центральный атом углерода находится в sр-гибридизации, что и определяет пространственную форму этих соединений. Кумулированные диены не стабильны и при нагревании изомеризуются в алкины. В молекуле сопряженных диенов π-электроны двойных связей взаимодействуют друг с другом (π, π-сопряжение), что приводит к изменению порядка и длины как простой σ-связи С-С, так и двойной связи С=С, увеличению стабильности молекулы. Физические свойства. Бутадиены - бесцветные газообразные вещества с характерными запахами, изопрен - легкокипящая жидкость с приятным запахом. Диены по физическим свойствам близки к алкенам. Химические свойства сопряженных диенов. Для сопряженных диенов известны все реакции, характерные для алкенов (присоединение, окисление, полимеризация). Наиболее характерным типом реакций являются реакции электрофильного присоединения (гидрирование, галогенирование, гидрогалогенирование, гидратация и др.), особенность которых состоит в том, что возможно образование продуктов 1,2- и 1,4-присоединения (по двойной связи и концам сопряженной цепи). Соотношение изомерных продуктов присоединения определяется температурным режимом, полярностью растворителя, характером реагента. Как правило, при низких температурах преобладают продукты 1,2-присоединения, при более высоких температурах и в полярных растворителях - 1,4-присоединения.  1,2-присоединение 1,4-присоединение 1,2-присоединение 1,4-присоединениеВ реакциях электрофильного присоединения сопряженные диены более активны, чем алкены. Полимеризацию (радикальную, ионную) сопряженных диенов осуществляют для синтеза синтетических каучуков. Синтетический каучук, по свойствам подобный натуральному, получают и координационной полимеризацией изопрена на катализаторах Циглера-Натта. Сопряженным диенам свойственна реакция присоединения с образованием шестичленного цикла (реакция Дильса-Альдера, диеновый синтез): диен диенофил продукт 1,4-присоединения Z: Н, -NO2, -C≡N, -COOH, -CHO и другие электроноакцепторные группы. Многие полученные соединения обладают высокой биологической активностью и широко используются как лекарственные препараты, средства защиты растений. Знаете ли вы, что -В 1861 году при нагревании природного каучука без доступа воздуха английским ученым К.Уильямсоном получен и назван первый диен - изопрен. -Группа ученых под руководством Сергея Васильевича Лебедева - профессора Военно-медицинской академии г.Ленинграда в 1926 году впервые получила синтетический каучук. -В 1928 году два немецких химика-органика Отто Пауль Дильс и Курт Альдер открыли реакцию циклоприсоединения к сопряженным диенам. В 1950 году за это открытие ученые удостоены Нобелевской премии. -Каучук - сок дерева гевеи (от начала индийских слов: сао - дерево, chu -течь, плакать). -В 1932 году началось мировое производство синтетического каучука, крупнейшие промышленные производители - Германия, США. -Мировое производство каучуков приближается к 10 млн тонн в год. Из них изготавливают около 50 тыс. различных изделий. -В 1939 году Ч. Гудьир при нагревании каучука с серой получил продукт, который в 1943 году Т. Гэнкок назвал резиной , а процесс - вудканизацией. -Производные диенов - терпены широко представлены в природе, многие являются составной частью эфирных масел, придающих растениям специфический аромат (например, лимонен в кожуре цитрусовых). 3. Алкины Алкины – углеводороды состава CnH2n-2, содержащие одну тройную углерод-углеродную связь. Номенклатура. Названия алкинов образуют, заменяя суффикс «ан» в названии соответствующего алкана на суффикс «ин». Тривиальное название первого представителя гомологического ряда - ацетилен. По рациональной номенклатуре алкинам дают названия как производным ацетилена, полученным в результате замещения одного или двух атомов водорода на алкильные радикалы. Например, пропин СН3-С≡СН по рациональной номенклатуре будет иметь название - метилацетилен. Нахождение алкинов в природе. Ацетилен и его гомологи мало распространены в природе. Более распространены полиины, которые обнаружены в некоторых растениях. В составе природных полиинов содержится от двух до пяти тройных углерод-углеродных связей. Получение алкинов. В промышленных масштабах получают, в основном, ацетилен. 1. Пиролиз метана и алканов: 2. Гидролиз карбида кальция: CaC2 + 2H2O → C2H2 + Ca(OH)2 3. Дегидрогалогенирование вицинальных и геминальных дигалогенидов: отщепление галогеноводорода происходит под действием спиртового раствора щелочи:  4. Алкилирование ацетилена и алкинов: НС≡СNа + R-Сl → НС≡С-R + NаСl R-С≡С- MgCl + R-Сl → R-С≡С-R + MgCl2 Изомерия. 1. Структурная Для алкинов характерны следующие виды: а) различное строение углеродной цепи (для углеводородов с числом атомов углерода ≥ 5); б) различное расположение кратной связи (для углеводородов с числом атомов углерода ≥ 4; в) межклассовая. Межклассовыми изомерами алкинов могут быть алкадиены, циклоалкены. Строение алкинов. Атомы углерода алкинов, образующие тройную связь, находятся в состоянии sр-гибридизации. Тройная связь представляет комбинацию σ-С-С (перекрывание sр - sр - орбиталей) и двух π-С-С связей (боковое перекрывание р-р-орбиталей). Молекула ацетилена имеет линейное строение, углы между связями соответствуют 1800, в молекулах гомологов и их изомеров присутствует только фрагмент линейной структуры. Тройная связь, по сравнению с двойной, короче и более поляризуема. Увеличение электроотрицательности атома углерода в sр-гибридизации приводит к более высокой, по сравнению с алкенами, поляризации σ-С-Н-связи. Молекула ацетилена неполярна, но при введении одной алкильной группы появляется значительный, по сравнению с этиленовыми углеводородами, дипольный момент: δ+ δ- Физические свойства. Алкины представляют собой бесцветные газы или жидкости, начиная с С17 - твердые вещества. Поскольку для алкинов характерны значительные дипольные моменты, они, по сравнению с алканами и алкенами, имеют более высокие температуры кипения и плавления, относительную плотность. Алкины нерастворимы воде, однако хорошо растворяются в органических малополярных растворителях. Например, ацетилен хорошо растворяется в ацетоне. Ацетилен термодинамически неустойчивое соединение, при сжижении легко разлагается на углерод и водород. Химические свойства. Химические свойства алкинов определяются наличием С≡С-связи, для которой, как и для двойной углерод-углеродной связи, характерны реакции присоединения электрофильных и нуклеофильных реагентов, реакции окисления и полимеризации. Алкины с концевой тройной связью вступают в реакции замещения водорода при тройной связи, который обладает слабыми кислотными свойствами. Таким образом, молекулы алкинов содержат два основных реакционных центра – С≡С-связь и подвижный водород: Реакции электрофильного присоединения. В реакциях электрофильного присоединения ацетилен и его гомологи по сравнению с алкенами проявляют меньшую реакционную способность, что обусловлено особенностями в строении тройной связи. Реакции протекают ступенчато (присоединение первой молекулы реагента, а затем - второй), при этом присоединение молекулы электрофила сопровождается образованием как одного геометрического изомера (стереоселективное присоединение), так и образованием смеси геометрических изомеров. Реакции присоединения к алкинам резко ускоряет присутствие в реакционной среде катализатора - соли меди (I) или ртути (II). Поэтому многие реакции присоединения к тройной связи рассматриваются как реакции нуклеофильного присоединения (вода, спирты, карбоновые кислоты и другие). В реакциях присоединения реакционная активность ацетилена по сравнению с другими алкинами мала. а) присоединение галогенов:  Взаимодействие с молекулой галогена происходит как стереоселективное транс-присоединение (образование транс-изомера). Реакция с бромом является качественной реакцией для обнаружения как двойной, так и тройной связи. б) присоединение галогеноводородов:  Присоединение галогеноводородов происходит по правилу Марковникова с образованием гем-дигалогенопроизводных. в) присоединение воды. В кислой среде в присутствии солей ртути (II) алкины взаимодействуют с водой с образованием карбонильных соединений (реакция М.Г. Кучерова, 1881г.). Присоединение воды происходит в соответствии с правилом Марковникова с образованием неустойчивых ненасыщенных спиртов (енолов), которые в условиях реакции быстро изомеризуются (правило А.П. Эльтекова, 1887г.) в более стабильные карбонильные соединения (кетоны):  Из ацетилена образуется уксусный альдегид: г) реакции винилирования. В реакциях присоединения спиртов, карбоновых кислот, циаоноводорода и т.д. к алкинам образуются соединения с двойной углерод-углеродной связью (винильные производные):  При этом получают простые и сложные эфиры, акрилонитрилы, которые в промышленном масштабе используются в качестве мономеров в реакциях полимеризации (например, при получении поливинилового эфира, поливинилацетата, полиакрилонитрила). Реакции по связи С-Н: а) кислотные свойства. Ацетилен и алкины с концевой тройной связью вследствие высокой электроотрицательности sр-гибридизованного атома углерода проявляют кислотные свойства за счет связи С-Н (СН-кислотность). Ряд кислотности: При взаимодействии с металлами, сильными основаниями образуются соли – ацетилениды, при этом связь С-металл в зависимости от природы металла имеет различную полярность: Ацетилениды щелочных металлов легко разлагаются водой. Реакцию алкинов с магнийорганическими соединениями (реактив Гриньяра) открыл Ж. Иоцич (1902 г.), в результате взаимодействия получают углеводороды: С ионами некоторых тяжелых металлов образуются нерастворимые в воде, иногда окрашенные, соли: R-C≡CH + [Ag(NH3)2]OH → R-C≡CAg↓ + 2NH3 + H2O R-C≡CH + [Сu(NH3)2]Сl → R-C≡CCu↓ + NH4Cl + NH3 Реакции используются как качественные на концевую тройную связь. Ацетилениды меди и серебра термически нестабильные вещества, при нагревании легко разлагаются: АgC≡CAg → 2Ag + 2С. Ацетилениды используются в различных органических синтезах. б) взаимодействие с карбонильными соединениями. Ацетилен и алкины с концевой тройной связью в присутствии щелочей присоединяются к карбонильной группе альдегидов и кетонов с образованием ненасыщенных спиртов: НС≡СН + Н2С=О → НС≡С-Н2С-ОН → НО-Н2С-НС≡С-Н2С-ОН пропаргиловый спирт бутин-2-диол-1,4 Реакции окисления и восстановления. Алкины, как и алкены, легко окисляются различными по силе окислителями (см. «Алкены»). Реакция с перманганатом калия в нейтральной или слабощелочной среде (реакция Вагнера) является качественной реакцией на ненасыщенный характер углеводородов. При полном окислении (горении) ацетилена в избытке кислорода выделяется огромное количество энергии. Гидрирование (восстановление) ацетиленовых углеводородов протекает с образованием алкенов, а затем алканов. Каталитическое гидрирование (катализаторы: Ni, Pt, Pd) происходит нестереоселективно, при этом образуются как цис-, так и транс-алкены. Восстановление водородом в других условиях (например, в присутствии щелочного металла в спирте или цинка в соляной кислоте) преимущественно образуются транс-алкены:  Димеризация, циклоолигомеризация и полимеризация. В присутствии катализаторов ацетилен и алкины могут образовывать димеры, циклические тримеры и тетрамеры, линейные полимеры: а) в присутствии ионов меди (I) в кислой среде  б) циклоприсоединение  в) полимеризация  цис-полиацетилен, красного цвета, менее устойчив; транс-полиацетилен, синего цвета, более устойчив. Применение: Основные направления применения алкинов - органический синтез,сырье для производства синтетических каучуков и других полимеров, сварка и резка металлов. Знаете ли вы, что -В 1836г. из карбида кальция впервые получил ацетилен и изучил некоторые его свойства английский химик Э.Дэви. -В 1860-х годах пиролизом метана получил углеводород состава С2Н2 и дал название «ацетилен» французский химик Марселен Бертло. -В середине 19 века получены ацетилениды серебра и меди, калия и натрия. -В 1895 г. французский химик Анри Ле Шаталье провел и изучил реакцию горения ацетилена в избытке кислорода. -Катализатор (активированный уголь) в реакции образования бензола открыт русским химиком Николаем Дмитриевичем Зелинским. -В 1931г. американский ученый Юлиус Артур Ньюленд получил винилацетилен и совместно с коллегой Уоллесом Хьюмом Карозерсом разработал технологию получения хлоропрена и хлоропренового каучука. -С 1906г. ацетилен широко используется для автогенной сварки и резки металлов, температура ацетилен-кислородного пламени около 30000С. Первый сварочный аппарат изготовлен в США в 1904г. -Полиацетилены - вещества с высокой электропроводностью («органические металлы»). В 1976 г. в лаборатории японского ученого Хидэки Сиракавы обнаружена сверхпроводимость материала, полученного обработкой полиацетилена парами иода (в миллиард раз лучше полиацетилена), область применения таких материалов - токопроводящие полимеры электронных и звуковоспроизводящих устройств. ЛЕКЦИЯ 8. АРЕНЫ (АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ) План 1. Классификация ароматических углеводородов. 2. Гомологический ряд моноциклических аренов, номенклатура, получение. 3. Изомерия, строение бензола и его гомологов. 4. Свойства аренов. Аренами называют богатые углеродом циклические углеводороды, которые содержат в молекуле бензольное ядро и обладают особыми физическими и химическими свойствами. Арены по числу бензольных колец в молекуле и способа соединения циклов подразделяют на моноциклические (бензол и его гомологи) и полициклические (с конденсированными и изолированными циклами) соединения. Арены бензольного ряда можно рассматривать как продукты замещения атомов водорода в молекуле бензола на алкильные радикалы. Общая формула таких аренов СnH2n-6. В названии монозамещенных аренов указывают название радикала и цикла (бензол): бензол метилбензол (толуол) этилбензол. В более замещенных аренах положение радикалов указывают наименьшими цифрами, в дизамещенных аренах положение радикалов называют: 1,2 - орто (o-)-, 1,3 - мета (м-)- и 1,4 - пара (п-)-:  1,3-диметилбензол 1,2-метилэтилбензол м-диметилбензол (м-ксилол) о-метилэтилбензол (о-ксилол) Для аренов широко распространены тривиальные названия (некоторые названия указаны в скобках). |
