|
|
лекции токса. Лекции по токсикологической химии
ГРУППА ВЕЩЕСТВ, ИЗОЛИРУЕМЫХ ИЗ БИОЛОГИЧЕСКОГО МАТЕРИАЛА ЭКСТРАКЦИЕЙ И СОРБЦИЕЙ. (подгруппа «Лекарственные средства»)
Номенклатура и классификация.
К группе веществ, изолируемых из биологического материала экстракцией и сорбцией (их еще называют «нелетучие» яды), относятся соединения кислотного, нейтрального и основного характера, различные по своему химическому строению. Номенклатура их очень велика и постоянно расширяется по мере синтеза новых соединений. Наибольшее токсикологическое значение в настоящее время имеют:
Вещества кислотного характера:
Органические кислоты: бензойная, салициловая, ацетилсалициловая, пикриновая.
Барбитураты: барбитал, фенобарбитал, барбамил, этаминал-Na, бутобарбитал, гексенал, бензонал, бензобамил, циклобарбитал и др.
Вещества нейтрального характера:
Небарбитуровые снотворные: ноксирон, тетридин.
Сердечные гликозиды.
Многоатомные фенолы: гидрохинон, пирогаллол.
Полинитропроизводные: м-динитробензол, динитротолуолы, тринитротолуол.
Производные анилина и п-аминофенола: фенацетин, п-фенилендиамин.
Вещества основного характера:
Алкалоиды: производные пиридина и пиперидина (жидкие алкалоиды), тропана (атропин, кокаин и др.), хинолина (хинин), изохинолина (опийные), индола (стрихнин, бруцин, резерпин), пурина (кофеин, теобромин, теофиллин), пирролизидина (платифиллин, саррацин), ациклические (эфедрин), стероидоподобные (вератрин) и неустановленного строения (аконитин).
Синтетические вещества основного характера: антипирин, амидопирин - производные пиразола, промедол - производное пиперидина, новокаин и дикаин - производные аминокислот ароматического ряда, изониазид, производные фенотиазина - аминазин и др., производные бензодиазепина и т.д.
При полном (общем, ненаправленном) судебно-химическом анализе обязательному исследованию в лабораториях БСМЭ подлежат, согласно Приказа МЗ СССР № 1021 от 25.12.73, следующие вещества:
Из веществ кислотного характера - производные барбитуровой кислоты.
Из веществ основного характера - алкалоиды: производные пиридина и пиперидина (никотин, пахикарпин), тропана, изохинолина (опийные алкалоиды), индола (стрихнин), производные фенотиазина, промедол.
Теоретические основы метода изолирования
Большинство «нелетучих» ядов, являясь слабыми кислотами или слабыми основаниями, способны существовать в водном растворе в виде ионизированных или неионизированных (молекулярных) форм в зависимости от рН среды. Степень ионизации вещества (слабой кислоты или слабого основания) и необходимое для этого значение рН могут быть определены из уравнения степени ионизации (уравнение Гендерсона):
100
% = ------------------------- для кислот
1+ antilog (рК - рН)
100
% = ------------------------- для оснований
1+ antilog (рН - рК)
где рК - показатель ионизации вещества (-lgК), численно равный значению рН, при котором в растворе в равновесной концентрации присутствуют ионизированная и неионизированная (молекулярная) формы (т.е. вещество ионизировано на 50%). Эта величина постоянная для данного вещества.
Для большинства слабых кислот и слабых оснований рК приведены в монографии Альберта и Сержента «Константы ионизации кислот и оснований». Сильные кислоты (HNO3 и др.) и сильные основания (NаОН) ионизированы на 100% в широком интервале рН.
На основании уравнения Гендерсона, зная рН раствора, всегда можно вычислить степень ионизации вещества и, наоборот, если необходимо достичь определенной степени ионизации, всегда можно рассчитать необходимое для этого значение рН.
Степень ионизации вещества всегда приходится учитывать при изолировании ядов из биологического материала, так как растворимость ионизированных и неионизированных форм различна в воде и органических растворителях.
Ионизированные формы, которым соответствуют соли кислот и оснований, как правило, хорошо растворимы в воде и ограниченно растворимы в неполярных органических растворителях (хлороформ и эфир).
Неионизированные (молекулярные) формы, которым соответствуют свободная кислота и основание, наоборот, хорошо растворимы в неполярных растворителях и ограниченно растворимы в воде.
Пользуясь различной растворимостью ионизированных и молекулярных форм «нелетучих» ядов в воде и органических растворителях легко сформулировать принцип их изолирования из биологического материала.
Изолирование «нелетучих» ядов из биологического материала основано на различной растворимости их ионизированной и молекулярной форм в воде и органических растворителях и на коэффициенте распределения молекулярной формы между водной и органической фазами.
С орг
Кр =-------------
С н2о
где Кр - коэффициент распределения молекулярной формы,
С - концентрации вещества в водной и органической фазах.
Очевидно, что, чем больше Кр, тем эффективнее идет экстракция.
В процессе изолирования «нелетучих» ядов из биологического материала взаимодействуют 3 компонента: яд, биологический материал и экстрагент.
При исследовании тканевого материала (внутренние органы трупа) изолирование состоит из двух стадий: извлечение яда из твердой фазы (объект) в водную и извлечение яда из водной фазы в органический растворитель.
Схематично это может быть представлено следующим образом:
I стадия экстракции II стадия экстракции
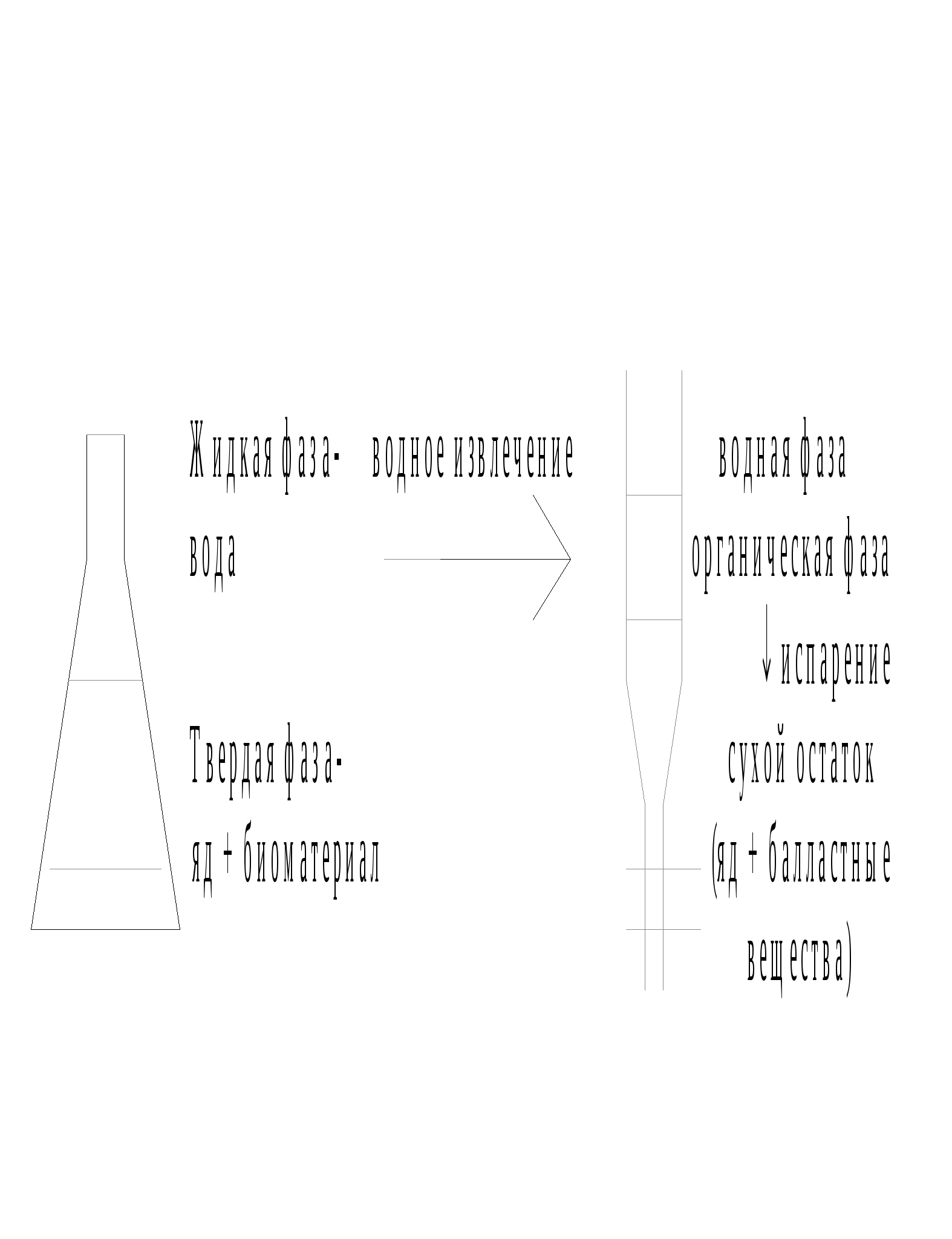
При исследовании биологических жидкостей (кровь, моча, промывные воды) необходимость в первой стадии изолирования отпадает и сразу проводится экстракция в органический растворитель.
Факторы, влияющие на эффективность изолирования «нелетучих» ядов из биоматериала.
Эффективность изолирования веществ на I и II стадиях определяется рядом факторов.
На первой стадии на эффективность изолирования вещества будут влиять такие факторы, как:
1) Растворимость яда в используемом экстрагенте.
Поскольку на первой стадии используются полярные растворители (вода), яд должен находиться в водорастворимом (ионизированном) состоянии, т.е. кислоты и основания должны присутствовать в виде своих солей, а степень ионизации 100%.
Необходимое для этого значение рН может быть рассчитано из уравнения степени ионизации Гендерсона. На практике пользуются более простым правилом. Для того, чтобы полностью перевести вещество в ионизированное состояние ( 100%), необходимо создать
рН = рК + 2(3) для кислот и
рН = рК - 2(3) для оснований
Отсюда очевидно, что для переведения кислот в ионизированное состояние (т.е. в их соли) нужна щелочная реакция среды. Так, если для барбитуратов рК =7-8,, то рН = рК + 2(3) = (7-8)+2(3) = 10 и выше.
Для оснований же требуется кислая реакция среды. Так, для атропина рН = рК - 2(3) = 9,6 - 3 = 6,6 и ниже.
Слабоосновные алкалоиды нацело ионизированы уже в сильно кислой среде, например, для кофеина рН 2,0 (рК 0,6)
Кислая реакция среды (рН2) приводит, кроме того, к разрушению комплексов алкалоидов с белками, в виде которых они находятся в биологическом материале, что увеличивает выход алкалоидов. Влияние рН на эффективность изолирования «нелетучих» ядов особенно выражено при использовании в качестве экстрагента воды, т.к. этанол в большинстве случаев является хорошим растворителем и для ионизированной, и для молекулярной форм кислот и оснований.
Экстрагент
Кроме реакции среды, на степень изолирования в значительной мере влияет природа экстрагента, его количество, время и кратность экстракции.
К экстрагенту предъявляются следующие основные требования:
-Способность легко проникать в клетки тканей.
-Высокая растворяющая способность (по отношению к яду).
-Селективность (по отношению к анализируемым соединениям). Селективный растворитель в какой-то мере исключает загрязнение вытяжки балластными веществами - жирами, белками, пигментами и другими.
В большей мере этим требованиям отвечает вода, несколько в меньшей степени - спирт, который является почти универсальным растворителем для лекарственных веществ. Основным недостатком этанола является способность экстрагировать совместно с анализируемыми веществами нормальные компоненты биоматериала (белки, жиры, пигменты), что усложняет анализ, приводя к дополнительным методам очистки и потерям значительных количеств искомых веществ.
Количество экстрагента обычно берется вдвое больше по отношению к весу органов (1:2). Большие количества экстрагента, хотя и увеличивают эффективность экстракции, приводят к разбавлению извлечения и усложнению последующих операций, связанных с концентрированием веществ в извлечении.
Время экстракции определяется моментом наступления равновесия в концентрациях вещества между твердой и жидкой фазами, что устанавливается экспериментально (по прекращению прироста концентрации вещества в экстрагенте ). Для воды оно меньше (около 2 часов) по сравнению с этанолом (более 4-6 часов).
Кратность экстракции приводит к увеличению выхода вещества за счет поступления новых порций растворителя. Для извлечения искомых соединений из внутренних органов возможны такие способы, как однократная и многократная экстракция, т.к. непрерывная экстракция требует специальной аппаратуры.
Немаловажную роль в экстракции играет и степень измельченности объекта, что обеспечивает максимальный доступ растворителя к искомому веществу (площадь соприкосновения твердой и жидкой фаз), но одновременно увеличивает количество соэкстрактивных веществ.
Вторая стадия изолирования «нелетучих» ядов заключается в выделении их из водного извлечения путем экстрагирования органическим растворителем, не смешивающимся с водой, при различных значениях рН среды. Этим достигается концентрирование вещества в извлечении и его частичная очистка от нормальных компонентов биоматериала (не растворимых в данном растворителе).
За счет экстрагирования веществ вначале из кислого, а затем из щелочного водного раствора, их можно разделить на 2 подгруппы:
Вещества, экстрагируемые органическими растворителями из кислого раствора (вещества кислотного, нейтрального и частично слабоосновного характера).
Вещества, экстрагируемые из щелочного раствора (вещества основного и частично слабоосновного характера).
Вещества со слабо выраженными основными свойствами могут частично перераспределяться из одной подгруппы в другую. К ним относятся производные пурина - кофеин, теобромин, теофиллин; опийные алкалоиды - папаверин, наркотин,; производные индола - бруцин, стрихнин; стероидоподобный алкалоид - вератрин, некоторые синтетические лекарственные средства - антипирин, амидопирин, промедол, производные фенотиазина (аминазин ) и др.
Для веществ нейтрального характера, не способных к ионизации, практически не требуется создания определенного значения рН, т.к. они экстрагируются органическим растворителем в молекулярной форме из любой среды. Разделение веществ на 2 подгруппы в значительной степени облегчает проведение последующего ненаправленного анализа с целью обнаружения неизвестного яда.
На второй стадии изолирования продолжают играть свою роль уже рассмотренные выше факторы, такие, как
1) растворимость яда, которая определяется степенью ионизации и регулируется рН среды.
2) природа экстрагента, его объем, время и кратность экстракции.
Если на первой стадии изолирования веществ данной группы мы стремились перевести их в ионизированное состояние и сделать водорастворимыми, то на второй стадии наша задача заключается в том, чтобы перевести вещества в неионизированную (молекулярную) форму (0), которая хорошо экстрагируется из водной фазы неполярным органическим растворителем. Необходимое для этого значение рН может быть рассчитано из уравнения, имеющего следующий вид:
рН = рК - 2(3) для кислот
рН = рК + 2(3) для оснований
Понятно, что для веществ кислого характера на этой стадии требуется создание кислой среды, а для основных – щелочной.
В качестве экстрагентов веществ из водной фазы подбирают неполярные органические растворители, которые:
а) не смешиваются с водой и по удельному весу (d) значительно отличаются от нее, что предотвращает образование эмульсий в процессе экстрагирования (d1,0)
б) имеют низкую температуру кипения, что облегчает их упаривание из экстракта
в) хорошо растворяют изолируемое вещество и обеспечивают высокий коэффициент распределения его между водной и органической фазами (Кр = С0/Св)
Коэффициент распределения можно увеличить, добавив в водную фазу электролит, который способствует вытеснению вещества из водной фазы в слой органического растворителя за счет понижения его растворимости в воде (разрушение сольватной оболочки молекул). В качестве электролита используют Na2SO4, (NH4)2SO4, NaCl.По данным проф. В.Ф.Крамаренко, наиболее подходящим электролитом при изолировании алкалоидов является сульфат аммония.
Наличие электролита в водной фазе приводит также к осаждению белков, что служит своеобразной очисткой полученного извлечения. Избыточное количество электролита, особенно при изолировании соединений кислотного характера, может привести к значительным потерям искомых веществ за счет их осаждения.
Исходя из перечисленных выше требований, наиболее подходящим экстрагентом для веществ кислотного характера является эфир, а для веществ основного характера - хлороформ.
Объем экстрагента, время и кратность экстракций.
Необходимый объем экстрагента при однократной экстракции можно рассчитать , исходя из уравнения степени экстракции (Е)
100 Кр
Е = ---------------------- %, где
Кр + Н2О/орг
Кр - коэффициент распределения
Н2О - объем водной фазы
орг - объем органической фазы
Время экстракции обычно не превышает 5 минут, т.к. экспериментально доказано, что за этот период времени большинство органических соединений переходит из водной в органическую фазу.
Кратность экстракции обычно составляет 2-3, что обеспечивает полноту извлечения вещества за счет поступления свежих порций растворителя.
ОБЩИЕ И ЧАСТНЫЕ МЕТОДЫ ИЗОЛИРОВАНИЯ
В зависимости от поставленной перед экспертом-химиком задачи, судебно-химическое исследование может носить общий или частный характер, т.е. анализ может быть ненаправленным (общим) или направленным (частным).
Частное исследование предусматривает проведение анализа на какое-то определенное вещество или группу веществ. Например, на производные барбитуровой кислоты, на алкалоиды или даже на одно конкретное вещество. При частном исследовании метод изолирования подбирается с учетом физико-химических свойств того соединения (или группы соединений), на которое производится анализ.
Общий анализ включает исследование на несколько групп веществ (3 группы), подлежащих обязательному судебно-химическому исследованию, в том числе и на группу «нелетучих» ядов. В этом случае используются общие для всей группы веществ ( универсальные) методы изолирования.
Общими методами изолирования «нелетучих» ядов являются;
Изолирование этанолом, подкисленным щавелевой кислотой (метод Стаса-Отто).
Изолирование водой, подкисленной щавелевой кислотой (метод Васильевой).
Оба метода вначале были разработаны для алкалоидов, а затем применены и к другим веществам.
Изолирование этанолом, подкисленным щавелевой кислотой
(метод Стаса-Отто)
В 1851 году во Франции произошло насильственное отравление Гюстава Фугни никотином. Он стал жертвой собственной сестры Лидии Фугни и ее мужа - графа Бокарме, которые совершили это преступление в погоне за наследством. Исследование внутренних органов погибшего было поручено бельгийскому химику Ж.С.Стасу, который применил для изолирования яда этанол, подкисленный щавелевой кислотой. Последующее извлечение алкалоида из водной фазы (после добавления гидроксида аммония для переведения его соли в основание) проводилось эфиром. В 1856 году братья Юлий и Роберт Ф.Отто ввели в метод Стаса еще одну операцию - очистку извлечения, исследуемого на алкалоиды, путем экстрагирования примесей эфиром из кислой водной вытяжки. В дальнейшем метод изолирования подкисленным спиртом, названный по имени авторов методом Стаса-Отто, претерпел серьезные изменения и стал применяться не только для алкалоидов, но и для многих других ядовитых и сильнодействующих веществ, имеющих токсикологическое значение.
Современная модификация метода состоит из этапов:
Настаивание измельченного объекта с этиловым спиртом, подкисленным щавелевой кислотой до рН2-3, в течение суток. Спирт берется в количестве, необходимом для покрытия объекта. Спиртовое извлечение сливается и вся операция повторяется трехкратно.
Упаривание объединенных спиртовых извлечений при температуре 40-500С до густого остатка, в который по каплям добавляют абсолютный этанол для коагуляции белков. Осадок отфильтровывают и всю операцию осаждения повторяют по мере необходимости до полного удаления белковых соединений.
Упаривание фильтрата при той же температуре до густого остатка и разбавление горячей водой для удаления смолистых веществ, жиров и пигментов. Осадок отфильтровывают.
Экстрагирование веществ кислого, нейтрального и слабоосновного характера из водного фильтрата хлороформом при рН=2 (трехкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием ( фракция А, «кислое» извлечение).
Подщелачивание оставшегося после разделения фаз водного слоя до рН 9-10, экстрагирование веществ сильноосновного и нейтрального характера (трехкратная экстракция) хлороформом, отделение органической фазы и концентрирование упариванием (фракция Б, «щелочное» извлечение).
Изолирование «нелетучих» ядов из биологического материала подкисленным спиртом (метод Стаса-Отто) проводится по следующей схеме:
100 г
органа

C2H5OH + H2C2O4
pH 2-3, 3 раза
по 24 часа
спиртовые извлечения
(соли алкалоидов, молекулярные формы кислот)

>t
40-50° C
густой остаток
 
C2H5OH абс.
осаждение белков
фильтрат
>t
40-50° C
густой остаток
 
H2O горячая
жиры, смолы,
пигменты,
фильтрат
pH
3
NH4OH
водная фаза
pH 9-10

CHCl3
3 раза
|
|
|
 Скачать 5.01 Mb.
Скачать 5.01 Mb.