Струков Патологическая анатомия. Литература для студентов медицинских институтов А. И. Струков В. В. Серов Патологическая анатомия Издание второе
 Скачать 16.97 Mb. Скачать 16.97 Mb.
|
|
Регенерация отдельных тканей и органов Регенерация крови происходит таким образом, что вначале возме- щается плазма за счет поступления в кровеносное русло тканевой жидкости, а затем — форменные элементы крови за счет поступления в кровоток ново- образованных клеток из кроветворной ткани. 163 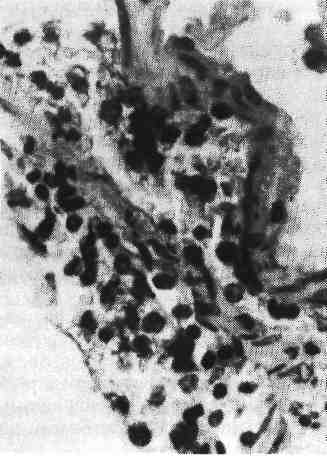 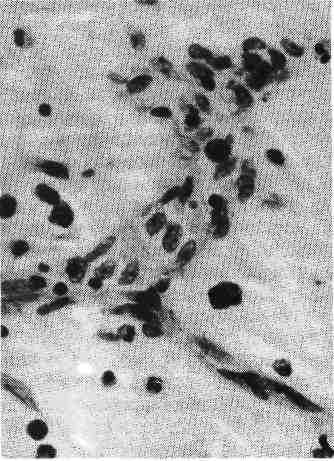 Рис. 100. Внекостномозговое кроветворение. Периваскулярное скопление молодых клеток крови. Рис. 101. Регенерация сосудов путем почкования. Гемопоэз в постэмбриональном периоде осуществляется в миелоидной и лимфоидной тка- нях, причем эритроциты, зернистые лейкоциты и тромбоциты образуются в красном костном мозге, лимфоциты — в лимфатических узлах, селезенке и лимфатических фолликулах ряда орга- нов, а моноциты, по-видимому, во всех кроветворных тканях. Источником образования фор- менных элементов крови служит единая полипотентная стволовая клетка, которая является об- щим предшественником всех трех ростков кроветворения и всех клеток иммунокомпетентной системы. Репаративная регенерация крови отличается от физиологиче- ской не только большей интенсивностью, но и тем, что кроветворение может происходить вне красного костного мозга — внекостномозговое, или экстрамедуллярное, кроветворение (рис. 100). При этом ак- тивный красный мозг появляется в длинных трубчатых костях на месте жиро- вого костного мозга (миелоидное превращение жирового костного мозга). Жировые клетки вытесняются растущими островками кроветворной ткани, которая заполняет костномозговой канал и выглядит сочной, темно- красной. В результате выселения из костного мозга стволовых клеток крове- творной ткани очаги экстрамедуллярного (гетеротопического) кроветворения появляются во многих органах и тканях — селезенке, печени, лим- фатических узлах, слизистых оболочках, жировой клетчатке и т. д. При больших кровопотерях репаративная регенерация крови оказывается недостаточной, поэтому широко пользуются переливанием (трансплантацией) донорской крови от живых людей или трупов. Регенерация крови может быть резко угнетена (например, при луче- вой болезни, апластической анемии, алейкии, агранулоцитозе) или извра- щена (например, при злокачественной анемии, полицитемии, лейкозе). В кровь при этом поступают незрелые, функционально неполноценные и бы- стро разрушающиеся форменные элементы. В таких случаях говорят о пато- логической регенерации крови. 164 Костный мозг обладает очень высокими пластическими свойствами и может восстанавливаться даже при значительных повреждениях. Лимфа- тические узлы хорошо регенерируют только в тех случаях, когда сохра- няются связи приносящих и выносящих лимфатических сосудов с окружающей их соединительной тканью. Регенерация ткани селезенки при повреждении бывает, как правило, неполной, погибшая ткань замещается рубцом. Возможности и формы регенерации к р о в ен о с н ы х и лимфатиче- ских сосудов в значительной мере зависят от их калибра. Микросо- суды обладают большей способностью регенерировать, чем крупные сосуды. Новообразование микрососудов может происходить путем почкования или аутогенно. При регенерации сосудов путем почкования (рис. 101) в их стенке появляются боковые выпячивания за счет усиленно делящихся эндоте- лиальных клеток (ангиобласты), которые образуют клеточные тяжи. В тяжах из эндотелия возникают просветы, тяжи превращаются в выстланные эндоте- лием трубки, в которые поступает кровь или лимфа из материнского сосуда. Другие элементы сосудистой стенки образуются за счет дифференцировки эн- дотелия и окружающих сосуд соединительнотканных клеток. В сосудистую стенку врастают нервные волокна, ответвляющиеся от предсуществующих не- рвов. Аутогенное новообразование сосудов состоит в том, что в соедини- тельной ткани появляются скопления недифференцированных клеток, между которыми возникают щели. В эти щели открываются предсуществующие ка- пилляры и изливается кровь. Клетки соединительной ткани, окружающие ще- ли, образуют эндотелиальную выстилку и другие элементы стенки сосуда. Крупные сосуды не обладают достаточными пластичными свойства- ми. Поэтому при повреждении их стенки (атеросклероз, артериит, аортит, аневризма, травма) восстанавливаются лишь структуры внутренней оболочки, ее эндотелиальная выстилка; элементы средней и наружной оболочек обычно замещаются соединительной тканью, что ведет нередко к сужению или обли- терации просвета сосуда. В связи с этим в настоящее время широкое распространение получила замена пораженного участка сосуда трансплантатом. Такой трансплантат представляет собой сосуд, взятый от трупа или изготовленный из синтетических материалов. С помощью сосудистых трансплантатов мож- но заменить большие участки пораженных сосудов (артерий, аорты) или создать новые крове- носные пути в обход пораженных сосудов (рис. 102). Регенерация соединительной ткани начинается с пролифера- ции молодых мезенхимальных элементов и новообразования микрососудов. Образуется молодая, богатая клетками и тонкостенными сосудами соедини- тельная ткань, которая имеет характерный вид. Это — сочная темно-красная ткань с зернистой, как бы усыпанной крупными гранулами поверхностью, что явилось поводом назвать ее грануляционной тканью. Гранулы пред- ставляют собой выступающие над поверхностью петли новообразованных тонкостенных сосудов, которые составляют основу грануляционной ткани. Между сосудами много недифференцированных лимфоцитоподобных клеток соединительной ткани, лейкоцитов, плазматических клеток и лаброцитов (рис. 103). В дальнейшем происходит созревание грануляционной тка- ни, в основе которого лежит дифференцировка клеточных элементов, волок- нистых структур, а также сосудов. Число гематогенных элементов уменьшает- ся, а фибробластов — увеличивается. С фибробластами связано образо- вание тропоколлагена и гликозаминогликанов соединительной ткани. В связи с синтезом фибробластами тропоколлагена в межклеточных пространствах образуются нежные аргирофильные волокна (см. рис. 103), а за- 165   Рис. 102. Сосудистый протез из пласт- массы, заменяющий часть брюшной аорты, и отходящие от нее крупные ветви, пораженные атеросклерозом и непроходимые для крови (по Д. С. Сар- кисову). Рис. 103. Грануляционная ткань. Меж- ду тонкостенными сосудами много недифференцированных клеток соеди- нительной ткани и аргирофильных волокон. Импрегнация серебром. тем и коллагеновые. Синтез фибробластами гликозаминогликанов при- водит к накоплению последних, особенно хондроитинсульфатов, в основном веществе соединительной ткани, которые расходуются на построение волок- нистых структур. По мере превращения (созревания) фибробластов в фи- броциты количество коллагеновых волокон увеличивается, они группи- руются в пучки. Одновременно уменьшается количество сосудов, они дифференцируются в артерии и вены. Созревание грануляционной ткани за- вершается образованием грубоволокнистой рубцовой ткани. Новообразование соединительной ткани происходит не только при ее по- вреждении, но и при неполной регенерации других тканей, а также при орга- низации (инкапсуляции), заживлении ран, продуктивном воспалении. Созревание грануляционной ткани может иметь те или иные отклоне- ния. Воспаление, развивающееся в грануляционной ткани, приводит к за- держке ее созревания, а чрезмерная синтетическая активность фибробла- стов — к избыточному образованию коллагеновых волокон с последующим резко выраженным их гиалинозом. В таких случаях возникает рубцовая ткань в виде опухолевидного образования синюшно-красного цвета, которая возвы- шается над поверхностью кожи в виде келоида. Келоидные рубцы обра- 166 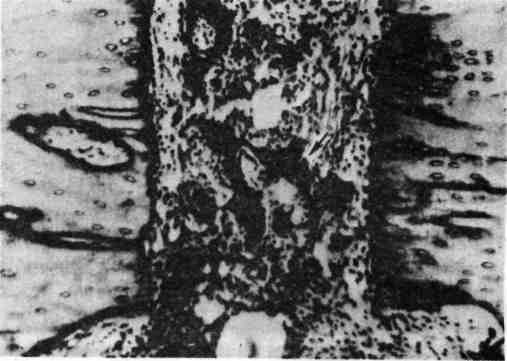 Рис. 104. Первичное костное сращение. Интермедиарная костная мозоль (показана стрелкой), спаивающая от- ломки кости (по Г. И. Лав- рищевой). зуются после различных травматических поражений кожи, особенно после ожогов. Регенерация жировой ткани происходит за счет новообразова- ния соединительнотканных клеток, которые затем превращаются в жировые путем накопления в цитоплазме липидов. Жировые клетки складываются в дольки, между которыми располагаются соединительнотканные прослойки с сосудами и нервами. Регенерация жировой, ткани может происходить также из ядросодержащих остатков цитоплазмы жировых клеток, которые путем на- копления капель липидов превращаются в зрелые жировые клетки. Регенерация костной ткани при переломе костей в значительной мере зависит от степени разрушения кости, правильной репозиции костных отломков, местных условий (состояние кровообращения, воспаление и т. д.). При неосложненном костном переломе, когда костные отломки непо- движны, может происходить первичное костное сращение (рис. 104). Оно начинается с врастания в область дефекта и гематомы между от- ломками кости молодых мезенхимальных элементов и сосудов. Возникает так называемая предварительная соединительнотканная мо- золь, в которой сразу же начинается образование кости. Оно связано с акти- вацией и пролиферацией остеобластов в зоне повреждения, но прежде всего в периосте и эндосте. В остеогенной фиброретикулярной ткани по- являются малообызвествленные костные балочки, число которых нарастает. Образуется предварительная костная мозоль. В дальней- шем она созревает и превращается в зрелую пластинчатую кость: так обра- зуется окончательная костная мозоль, которая по своему строе- нию отличается от костной ткани лишь беспорядочным расположением костных перекладин. После того как кость начинает выполнять свою функ- цию и появляется статическая нагрузка, вновь образованная ткань с помощью остеокластов и остеобластов подвергается перестрой - к е, появляется костный мозг, восстанавливаются васкуляризация и иннерва- ция. При нарушении местных условий регенерации кости (расстройство кро- вообращения), подвижности отломков, обширных диафизарных переломах происходит вторичное костное сращение (рис. 105). Для этого ви- да костного сращения характерно образование между костными отломками сначала хрящевой ткани, на основе которой строится костная ткань. Поэтому при вторичном костном сращении говорят о предварительной костно-хря- 167 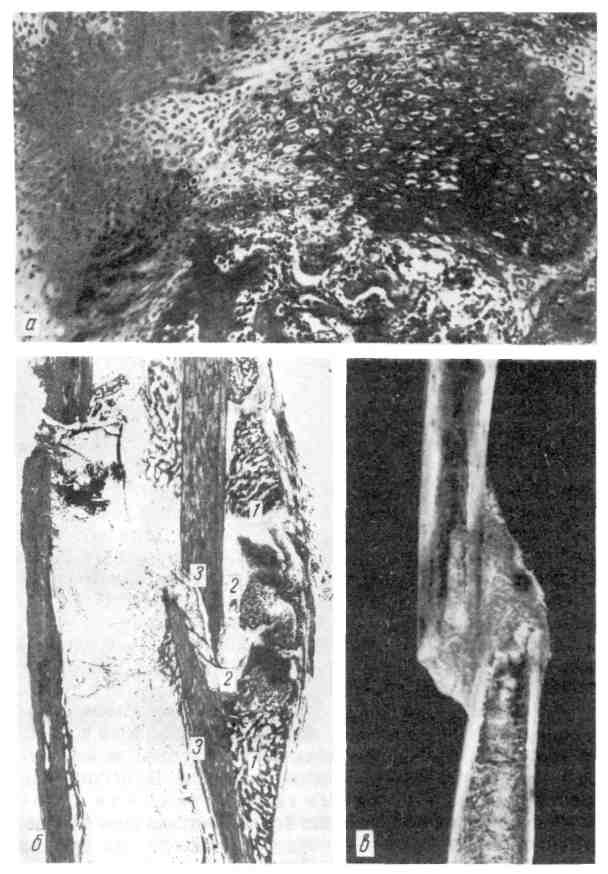 Рис. 105. Вторичное костное сращение (по Г. И. Лаврищевой). а — микроскопическая картина костно-хрящевой периостальной мозоли: участок костной ткани среди хрящевой; б — периостальная костно-хряшевая мозоль (гистотопограмма через 2 мес после операции): 1 — костная часть; 2 — хрящевая часть; 3 — отломки кости; в — периостальная мозоль, спаивающая смещенные отломки кости. щевой мозоли, которая со временем превращается в зрелую кость. Вто- ричное костное сращение по сравнению с первичным встречается значительно чаще и занимает больше времени. При неблагоприятных условиях регенерация костной ткани мо- жет быть нарушена. Так, при инфицировании раны регенерация кости задер- живается. Костные осколки, которые при нормальном течении регенераторно- го процесса выполняют функцию каркаса для новообразованной костной ткани, в условиях нагноения раны поддерживают воспаление, что тормозит регенерацию. Иногда первичная костно-хрящевая мозоль не дифференцирует- 168 ся в костную. В этих случаях концы сломанной кости остаются подвижными, образуется ложный сустав. Избыточная продукция костной ткани в ходе регенерации приводит к по- явлению костных выростов — экзостозов. Регенерация хрящевой ткани в отличие от костной происходит обычно неполно. Лишь небольшие дефекты ее могут замещаться новообразо- ванной тканью за счет камбиальных элементов надхрящницы — х о н д р о - б л а с т о в. Эти клетки создают основное вещество хряща, а затем превра- щаются в хрящевые клетки. Крупные дефекты хрящевой ткани замещаются рубцовой. Регенерация мышечной ткани, ее возможности и формы раз- личны в зависимости от вида этой ткани. Гладкие мышцы, клетки ко- торых обладают способностью к митозу и амитозу, при незначительных де- фектах могут регенерировать достаточно полно. Значительные участки повреждения гладких мышц замещаются рубцом. При этом в сохранившихся участках гладкие мышечные волокна подвергаются гипертрофии. Новообра- зование гладких мышечных волокон может происходить путем превращения (метаплазии) элементов соединительной ткани. Так образуются пучки гладких мышечных волокон в плевральных спайках, в подвергающихся организации тромбах, при дифференцировке сосудов. Регенерация поперечнополосатой мускулатуры проис- ходит лишь при сохранении сарколеммы. Внутри трубок из сарколеммы осуществляется регенерация саркоплазмы и ее органелл, в результате чего по- являются клетки, называемые миобласгами. Они вытягиваются, число ядер в них увеличивается, в саркоплазме постепенно дифференцируются мио- фибриллы, и трубки сарколеммы вновь превращаются в поперечнополосатые мышечные волокна. В последнее время регенерацию скелетных мышц связывают с клетка- ми-сателлитами, которые располагаются под сарколеммой, т. е. внутри мышечного волокна, и являются камбиальными. В случае травмы клет- ки-сателлиты начинают усиленно делиться, затем подвергаются дифференци- ровке и обеспечивают восстановление мышечных волокон. Если при повреждении мышцы целость сарколеммы нарушается, то на ме- сте травмы обычно образуется рубец. На концах разрывов волокон возни- кают колбообразные выбухания, которые содержат большое число ядер и на- зываются мышечными почками. Соединения мышечных почек с обоих концов разрыва и восстановления непрерывности волокна не происходит. Место разрыва заполняется грануля- ционной тканью, превращающейся в рубец (мышечная мозоль). Лишь при заполнении места травмы размельченной мышцей возможно полноценное восстановление мышечных волокон (А. Н. Студитский). Регенерация мышцы сердца человека, как и поперечнополосатой мускулатуры, заканчивается рубцеванием дефекта. Однако в сохранившихся мышечных волокнах происходит интенсивная гиперплазия ультраструктур, что ведет к гипертрофии волокон и восстановлению функции органа (рис. 106). Регенерация эпителия осуществляется в большинстве случаев до- статочно полно, так как он обладает высокой регенераторной способностью. Особенно хорошо регенерирует покровный эпителий. Восстановление многослойного плоского ороговевающего эпителия воз- можно даже при довольно крупных дефектах кожи. При регенерации эпидер- миса в краях дефекта происходит усиленное размножение клеток зародышево- го (камбиального) мальпигиева слоя. Образующиеся эпителиальные клетки сначала покрывают дефект одним слоем. В дальнейшем пласт эпителия ста- 169 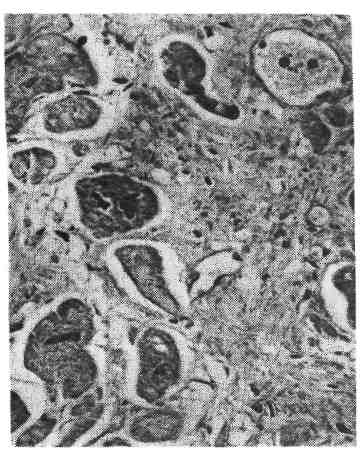 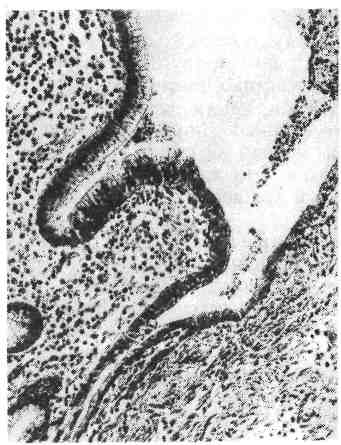 Рис. 106. Регенерационная гипертрофия миокарда. По периферии рубца гипертрофиро- ванные мышечные волокна. Рис. 107. Регенерация эпителия в дне хронической язвы желудка. новится многослойным, клетки его дифференцируются, и он приобретает все признаки эпидермиса, включающего в себя ростковый, зернистый, блестящий (на подошвах и ладонной поверхности кистей) и роговой слои. Созревание клеток сопровождается синтезом в их цитоплазме специфического для орого- вевающего эпителия белка — кератогиалина, превращающегося в элеи- дин и кератин. Однако регенераторные возможности покровного эпителия не безграничны. Большие де- фекты кожных покровов, например после ожогов, долго не эпителизируются. Для закрытия де- фекта в таких случаях используют как аутопластику, покрывая дефект слоем кожи, взятым у то- го же больного со здоровых участков, так и гомопластику. При нарушении регенерации эпителия кожи образуются незаживающие язвы, нередко с разрастанием в их краях атипичного эпителия, что может по- служить основой для развития рака кожи. Аналогичным образом регенерирует покровный эпителий сли- зистых оболочек (многослойный плоский неороговевающий, пере- ходный, однослойный призматический и многорядный мерцательный). Дефект слизистой оболочки восстанавливается за счет пролиферации клеток, высти- лающих крипты и выводные протоки желез. Недифференцированные упло- щенные клетки эпителия сначала покрывают дефект тонким слоем (рис. 107), затем эти клетки увеличиваются в объеме и принимают форму, свойственную клеточным структурам соответствующей эпителиальной выстилки. Парал- лельно частично или полностью восстанавливаются и железы слизистой обо- лочки (например, трубчатые железы кишки, железы эндометрия). Регенерация мезотелия брюшины, плевры и околосердечной сум- ки характеризуется делением сохранившихся клеток. На поверхности дефекта появляются сравнительно крупные кубические клетки, которые затем упло- 170 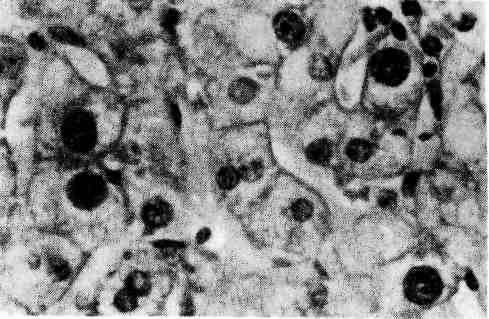 |
