Для заочников. Методические указания и контрольные задания для студентов заочников инженернотехнических (нехимических)
 Скачать 417.39 Kb. Скачать 417.39 Kb.
|
|
Пример 3. На основании стандартных теплот образования (см. табл. 5) и абсолютных стандартных энтропии веществ (табл. 7) вычислите  реакции, протекающей по уравнению реакции, протекающей по уравнениюСО (г) + Н2О (ж) = СО2 (г) + Н2 (г) Решение. 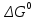 = = 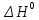 —Т —Т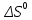 ; ; 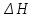 и и 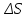 — функции состояния, поэтому — функции состояния, поэтому 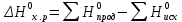 ; ;  . . (-393,51+0) – (-110,52 – 285,84) = +2,85 кДж; (-393,51+0) – (-110,52 – 285,84) = +2,85 кДж;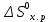 = (213,65 + 130,59) - (197,91 + 69,94) = + 76,39 = 0,07639 кДж/(моль∙К); = (213,65 + 130,59) - (197,91 + 69,94) = + 76,39 = 0,07639 кДж/(моль∙К); 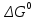 = +2,85 — 298∙0,07639 = — 19,91 кДж. = +2,85 — 298∙0,07639 = — 19,91 кДж.Пример 4. Реакция восстановление Fe203 водородом протекает по уравнению Fe 2О3 (к) + ЗН2 (г) = 2Fe (к) + ЗН2О (г); 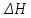 = + 96,61 кДж = + 96,61 кДжВозможна, ли эта реакция при стандартных условиях, если изменение энтропии ΔS=0,1387 кДж/(моль∙К)? При какой температуре начнется восстановление Fe203? Решение. Вычисляем ΔG0 реакции: ΔG = ΔH—TΔS = 96,61—298Х Х0,1387= +55,28 кДж. Так как ΔG>0, то реакция при стандартных условиях невозможна; наоборот, при этих условиях идет обратная реакция окисления железа (коррозия). Найдем, температуру, при которой ΔG = 0: ΔH = TΔS; Т=  696,5 К. 696,5 К.Следовательно, при температуре ≈ 696,5 К начнется реакция восстановления Fe203, Иногда эту температуру называют температурой начала реакции. Пример 5. Вычислите 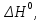 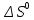 и и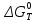 реакции, протекающей по уравнению реакции, протекающей по уравнениюFe 2О3 (к) + 3С = 2 Fe + 3СО Возможна ли реакция восстановления Fe 2О3 углеродом при температурах 500 и 1000 К? Решение. 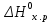 и и 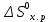 находим из соотношений (1) и (2) так же как в примере 3: находим из соотношений (1) и (2) так же как в примере 3: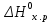 =[3(-110,52)+2∙ 0] – [-822,10+3∙ 0] = -331,56+822,10 =+490,54 кДж; =[3(-110,52)+2∙ 0] – [-822,10+3∙ 0] = -331,56+822,10 =+490,54 кДж;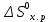 = (2∙ 27,2 + 3∙197,91) – (89,96 + 3∙5,69) = 541,1 Дж/К. = (2∙ 27,2 + 3∙197,91) – (89,96 + 3∙5,69) = 541,1 Дж/К.Энергию Гиббса при соответствующих температурах находим из соотношения 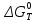 = ΔH—TΔS: = ΔH—TΔS: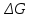 500 = 490,54 – 500 500 = 490,54 – 500 = +219,99 кДж; = +219,99 кДж;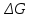 1000 = 490,54 – 1000 1000 = 490,54 – 1000 = -50,56 кДж. = -50,56 кДж.Так как 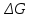 500 > 0, а 500 > 0, а 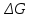 1000 < 0, то восстановление Fe 2О3 углеродом возможно при 1000К и не возможно при 500 К. 1000 < 0, то восстановление Fe 2О3 углеродом возможно при 1000К и не возможно при 500 К.Контрольные вопросы 101. Вычислите  для следующих реакция: для следующих реакция:а) 2NаF(к) + Cl2(г) = 2NаCl(к) + F2(г) б) PbO2 (к) + 2 Zn(к) = Pb(к) + 2 ZnО (к) Можно ли получить фтор по реакции (а) и восстановить PbO2 цинком по реакции (б)? Ответ: +313,94 кДж; -417,4 кДж. 102.При какой температуре наступит равновесие системы 4НCl (г)+О2 (г) 2Н2О (г)+2Сl2 (г); ΔН = -114,42 кДж? Хлор или кислород в этой системе является более сильным окислителем и при каких температурах? Ответ: 891 К. 103. Восстановление Fe304 оксидом углерода идет по уравнению Fe304 (к)+СО (г)=3FeO (к)+СО2 (г). Вычислите  и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях. Чему равно и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях. Чему равно 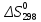 в этом процессе? Ответ: +24,19 кДж; +31,34 Дж/(моль-град). в этом процессе? Ответ: +24,19 кДж; +31,34 Дж/(моль-град).104. Реакция горения ацетилена идет по уравнению С2 Н2 (г) + 5/2О2 (г) = 2СО2 (г) + Н2О (ж) Вычислите  и и 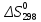 . Объясните уменьшение энтропии в результате этой реакции. Ответ; —1235,15 кДж; —216,15 Дж/(моль∙К). . Объясните уменьшение энтропии в результате этой реакции. Ответ; —1235,15 кДж; —216,15 Дж/(моль∙К).105. Уменьшается или увеличивается энтропия при переходах: а) воды в пар; б) графита в алмаз? Почему? Вычислите 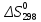 . ДЛЯ каждого превращения. Сделайте вывод о количественном изменении энтропии при фазовых и аллотропических превращениях. Ответ: а) 118,78 Дж/(моль∙К); б) —3,25 Дж/(моль∙К). . ДЛЯ каждого превращения. Сделайте вывод о количественном изменении энтропии при фазовых и аллотропических превращениях. Ответ: а) 118,78 Дж/(моль∙К); б) —3,25 Дж/(моль∙К).106. Чем можно объяснить, что при стандартных условиях невозможна экзотермическая реакция Н2 (г) + СО2 (г) = СО (г) + Н2О (ж); 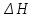 = — 2,85 к Дж = — 2,85 к ДжЗная тепловой эффект реакции и абсолютные стандартные энтропии соответствующих веществ, определите  этой реакции.Ответ:+19,91 кДж. этой реакции.Ответ:+19,91 кДж.107. Прямая или обратная реакция будет протекать при стандартных условиях в системе 2NO (г) + O2 (г) 2NO2 (г) ответ мотивируйте, вычислив  прямой реакции. Ответ: - 69,70 кДж. прямой реакции. Ответ: - 69,70 кДж.108. Исходя из значений стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ, вычислите  реакции, протекающей по уравнению реакции, протекающей по уравнениюNH3 (г) + Н Cl (г) = NH4Cl (к) Может ли эта реакция при стандартных условиях идти самопроизвольно. Ответ: —92,08 кДж. 109. При какой температуре наступит равновесие системы С  О (г) + 2Н2 (г) СН3ОН (ж); О (г) + 2Н2 (г) СН3ОН (ж); 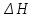 = - 128,05 кДж? = - 128,05 кДж?Ответ: ≈ 385,5 К. 110. При какой температуре наступит равновесие системы С  Н4 (г) + СО2 (г) 2СО (г) + 2Н2 (г); Н4 (г) + СО2 (г) 2СО (г) + 2Н2 (г); 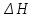 = + 247,37 кДж = + 247,37 кДжОтвет: = 961,9 К. 111. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите  реакции, протекающей по уравнению реакции, протекающей по уравнению4NH3(г) + 5О2 (г) = 4NO (г) + 6Н2О (г) Возможна ли эта реакция при стандартных условиях? Ответ: - 957,77кДж. 112. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите  реакции, протекающей по уравнению реакции, протекающей по уравнениюСО2 (г) + 4Н2 (г) = СН4 (г) + 2Н2О (ж) Возможна ли эта реакция при стандартных условиях? Ответ: -130,89 кДж. 113. Вычислите 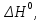 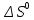 и и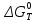 реакции, протекающей по уравнению реакции, протекающей по уравнениюFe 2О3 (к) + 3Н2 (г) = 2 Fe(к) = + 3Н2О (г) Возможна ли реакция восстановления Fe 2О3 водородом при температурах 500 и 2000 К? Ответ: +96,61 кДж; 138,83 Дж/К; 27,2 кДж; -181,0,5 кДж. 114. Какие из карбонатов: ВеСО3, СаСО3 или ВаСО3 —можно получить по реакции взаимодействия соответствующих оксидов с СО2? Какая реакция идет наиболее энергично? Вывод сделайте, вычислив  реакций. Ответ: +31,24 кДж; —130,17 кДж; — 216,02 кДж. реакций. Ответ: +31,24 кДж; —130,17 кДж; — 216,02 кДж.115. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите  реакции, протекающей по уравнению: реакции, протекающей по уравнению:СО (г) + ЗН2 (г) = СН4 (г) + Н2O (г) Возможна ли эта реакция при стандартных условиях? Ответ:-142,16 кДж. 116. Вычислите 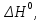 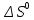 и и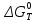 реакции, протекающей по уравнению реакции, протекающей по уравнениюTiO2 (к) + 2С(к) = Ti (к) + 2СО (г); Возможна ли реакция восстановления TiO2 углеродом при температурах 1000 и 3000 К? Ответ: +722,86 кДж; 364,84 Дж/К; +358,02 кДж; -371,66 кДж. 117. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите  реакции, протекающей по уравнению: реакции, протекающей по уравнению:С2Н4 (г) + 3О2 (г) = 2СО2 (г) + 2Н2O (ж) Возможна ли эта реакция при стандартных условиях? Ответ:-1331,21 кДж. 118. Определите, при какой температуре начнется реакция восстановления Fe304, протекающая по уравнению: Fe304 (к) + СО (г) = 3FeO (к) + СO2 (г); 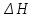 = + 34,55 кДж = + 34,55 кДж Ответ: 1102,4 К. 119. Вычислите, при какой температуре начнется диссоциация пентахлорида фосфора, протекающая по уравнению: РСl5 (г) = РСl3 (г) + Сl2 (г); 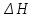 = + 92,59 кДж = + 92,59 кДж Ответ: 509 К. 120. Вычислите изменение энтропии для реакций, протекающих по уравнениям: 2СН4 (г) = С2Н2 (г) + ЗН2 (г); N2(г) + ЗН2 (г) = 2 NН 3 (г); С(графит) + О2 (г) = СО2 (г) Почему в этих реакциях 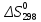 . >0; <0; ≈ 0? Ответ: 220,21 Дж/ К; -198,26 Дж/К; 2,93 Дж/К. . >0; <0; ≈ 0? Ответ: 220,21 Дж/ К; -198,26 Дж/К; 2,93 Дж/К.Химическая кинетика и равновесие Кинетика — учение о скорости различных процессов, в том числе химических реакций. Критерием принципиальной осуществимости реакций является неравенство ΔGp,T<0. Но это неравенство не является еще полной гарантией фактического течения процесса в данных условиях, не является достаточным для оценки кинетических возможностей реакции. Так,  Н2О(г) = —228,59 кДж/моль, и Н2О(г) = —228,59 кДж/моль, и  АlI0(к)= - 313,8 кДж/моль и, следовательно, при Т=298 К и р = 1,013∙ 105 Па возможны реакции, идущие по уравнениям: АlI0(к)= - 313,8 кДж/моль и, следовательно, при Т=298 К и р = 1,013∙ 105 Па возможны реакции, идущие по уравнениям:Н2 (г) + ½ О (г) = Н2O (г) (1) 2Аl (к) + 3I2 (к) = 2АlI3 (к) (2) Однако эти реакции при стандартных условиях идут только в Присутствии катализатора (платины для первой и воды для второй). Катализатор как бы снимает кинетический «тормоз», и тогда проявляется термодинамическая природа вещества. Скорость химических реакций зависит от многих факторов, основные из которых - концентрация (давление) реагентов, температура и действие катализатора. Эти же факторы определяют и достижение равновесия в реагирующей системе. Пример I. Во сколько раз изменится скорость прямой и обратной реакции в системе 2SО2 (г)+О2 (г) 2SО3 (г) если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы? Решение. Обозначим концентрации реагирующих веществ: [ SО2] = а, [О2]— b, [SO3] = c. Согласно закону действия масс скорости v примой и обратной реакции до изменения объема vпр = Ка 2 b; vобр = К1с2. После уменьшения объема гомогенной системы в три раза концен- трация каждого из реагирующих веществ увеличится в три раза[ SО2] = 3а, [О2]— 3b, [SO3] =3 c.. При новых концентрациях скорости примой и обратной реакции: v'пр (3а)2 (3 b)2 = 27 Ка 2 b; v'o6p = K1(Зс)2 = 9K1с2. Отсюда  Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной - только в девять раз. Равновесие системы сместилось в сторону образования SO3. Пример 2. Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70°С, если температурный коэффициент реакции равен 2. Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант - Гоффа по формуле  ; ; Следовательно, скорость реакции  при температуре 70°С больше скорости реакции при температуре 70°С больше скорости реакции  при температуре 300С в 16 раз. при температуре 300С в 16 раз. Пример 3. Константа равновесия гомогенной системы С  О (г) + Н2О (г) СО2 (г) + Н2 (г) О (г) + Н2О (г) СО2 (г) + Н2 (г)при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации: [СО]исх=3 моль/л, [Н2О]исх = 2 моль/л. Решение. При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы: vпр= К1[CО][ Н2О]; vобр = K2[CO2] [Н2]; 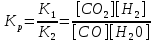 . .В условии задачи даны исходные концентрации, тогда как а выражение Кр входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрации [СО2]р = х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По стольку же молей (х моль/л) СО и Н2О расходуется для образования по х молей СО2 и Н2. Следовательно, равновесные концентрации всех четырех веществ [СО2]р = [Н2]р = х моль/л; [СО]р = (3 — х) моль/л; [Н2О]р = (2 — х) моль/л. Зная константу равновесия, находим значение х, а затем и исходные концентрации всех веществ: 1 = 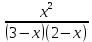 ; ;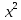 = 6 — 2х — Зх + х2; 5х = 6, х = 1,2 моль/л. = 6 — 2х — Зх + х2; 5х = 6, х = 1,2 моль/л. Таким образом, искомые равновесные концентрации: [СО2]р= 1,2 моль/л; [Н2]р= 1,2 моль/л; [CO]p = 3—1,2= 1,8 моль/л; [H2O]р =2—1,2 = 0,8 моль/л. Пример 4. Эндотермическая реакция разложения пентахлорида фосфора протекает по уравнению РСl5 (г) PCl3 (г) + Сl2 (г); ΔН = + 92,59 кДж Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону прямой реакции — разложения РСl5? Решение.Смещением или сдвигом химического равновесия называют изменение, равновесных концентраций реагирующих веществ и результате изменения одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу Ле Шателье: а) так как реакция разложения РСl5 эндотермическая (ΔН>0), то для смещения равновесия в сторону прямой реакции нужно повысить температуру; б) так как в данной системе разложение РСl5 ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации РСl5, так и уменьшением концентрации PCl3, или Сl2. |
