методичка химия. Методические указания и варианты контрольных заданий к самостоятельной работе студентов по дисциплине Аналитическая химия для студентов хтф направления
 Скачать 234 Kb. Скачать 234 Kb.
|
РАСЧЕТЫ РЕЗУЛЬТАТОВ ТИТРИМЕТРИЧЕСКОГО АНАЛИЗАВ титриметрическом анализе рассчитывают массу определяемого вещества по известным объемам реагирующих веществ и известной концентрации одного или нескольких рабочих растворов. Прямое титрование – наиболее распространенный и удобный прием, когда к анализируемому раствору добавляют рабочий раствор. Массу определяемого вещества m(A) определяют в данном случае по формуле (6) 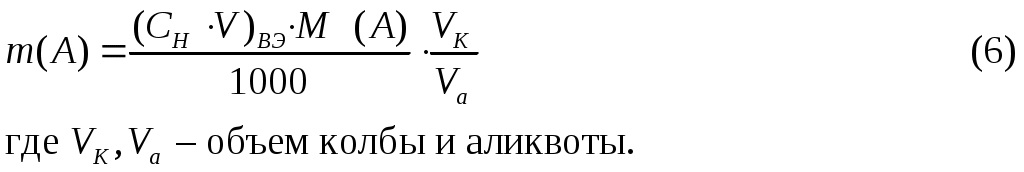 Титрование заместителя (косвенный метод) применяют, когда нет подходящей реакции или индикатора для прямого тестирования. В этом случае используют какую-либо реакцию, в которой анализируемое вещество замещают эквивалентным количеством другого вещества, а последнее титруют рабочим раствором. Массу определяемого вещества m(A) рассчитывают по формуле (6). Обратное титрование (титрование остатка) используют в тех случаях, когда прямое титрование невозможно или когда анализируемое вещество неустойчиво. При этом применяют два рабочих раствора. К раствору определяемого вещества (А) добавляют избыток рабочего раствора (В), а когда реакция заканчивается, остаток В титруют рабочим раствором С. Таким образом, масса определяемого вещества (А) рассчитывается в этом случае по формуле: Пример 3. При определении содержания CaO в образце мела навеску в 0,1500 г обработали 50,00 мл 0,0999 М HCI, избыток кислоты оттитровали 10,00 мл NaOH (К=1,01). Вычислить массовую долю CaO в образце мела. Решение: Из условия задачи видно, что определение CaO проводилось методом обратного титрования. Поэтому для расчета массы CaO в образце мела выбираем формулу (7): 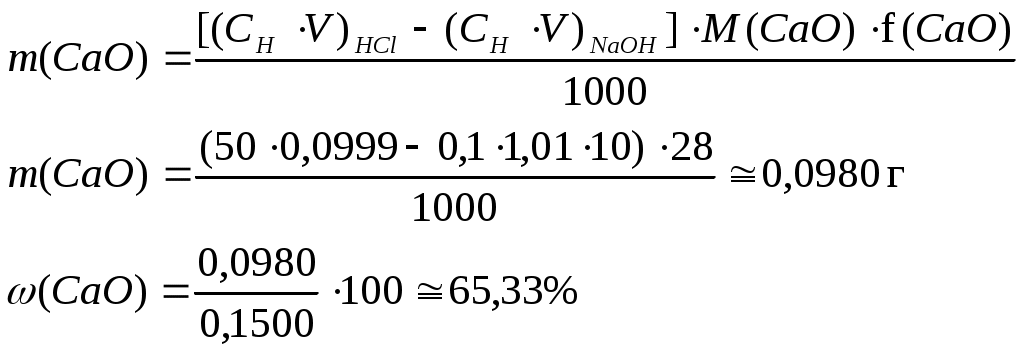 При выполнении расчетов следует учитывать некоторые математические правила. Если точность анализа не ограничивается заранее, то следует иметь в виду, что концентрация вычисляется до четвертой значащей цифры после запятой, процентное содержание – до сотых долей. Каждый результат не может быть точнее, чем это позволяют измерительные приборы, и математическими расчетами точность анализа повысить нельзя. Лишние цифры рекомендуется округлять. ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ И Если вещество удовлетворяет требованиям, предъявляемым к стандартным или исходным веществам, то из него можно приготовить рабочий раствор с точно известной концентрацией путем растворения точной навески вещества (m) в мерной колбе (V). |