Методичні вказівки для студентів 2 курсу фармацевтичного факультету
 Скачать 2.54 Mb. Скачать 2.54 Mb.
|
Заняття №17Дикарбонові кислотиАктуальність теми Дикарбонові кислоти відносяться до класу похідних вуглеводнів, до складу яких входять дві карбоксильні групи. Завдяки цьому дикарбонові кислоти вступають в ті ж самі реакції що і монокарбонові. Але завдяки наявності двох карбоксильних груп вони мають специфічні властивості, що залежать від взаємного розташування цих груп. Вивченню цих властивостей слід приділити достатньо уваги, оскільки дикарбонові кислоти мають важливе фармацевтичне значення. Відновні властивості щавелевої кислоти використовують в аналітичній практиці для встановлення титру калію перманганату. Нерозчинність кальцієвих солей щавелевої кислоти використовують для відкриття катіону кальцію. Рухливість атому гідрогену в малоновій кислоті та її похідному малоновому естері знайшла використання в органічному синтезі карбонових кислот та кетонів. Вивчення карбонових кислот уміння інтерпретувати їх хімічну будову і властивості необхідні студентові фармацевтичного факультету для вивчення таких дисциплін, як фармацевтична хімія, токсикологічна хімія, фармакологія. Вони дають змогу розробляти і удосконалювати нові методи синтезу лікарських речовин. ЦІЛІ НАВЧАННЯ Загальна ціль: Вміти визначати хімічні властивості дикарбонових кислот для застосування у фармацевтичних і токсикологічних дослідженнях. Конкретні цілі Вміти:
ЗМІСТ НАВЧАННЯ Основні теоретичні питання:
Граф логічної структури 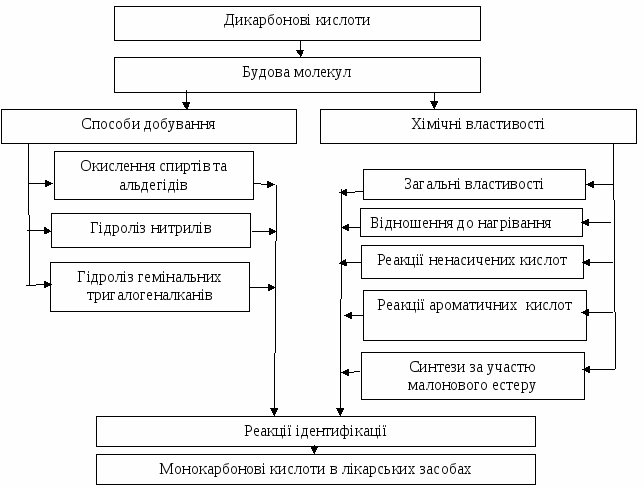 Джерела інформації Обов'язкова література:
Додаткова література: 1. Моррисон Р., Бойд Р. Органическая химия. Пер с англ. - М.: Мир, 1974. - 418 с. 2. Черных В.П., Руководство к лабораторным и семинарским занятиям по органической химии. - Харьков: Основа. - 1989. – 338с. 3. Степаненко Б.Н. Курс органической химии. В 2-х ч. - М.: Высшая школа, 1981. 453 с. 4. Некрасов В.В. Руководство к малому практикуму по органической химии. - М.:Химия, 1975. - 334 с. ОРІЄНТОВНА ОСНОВА ДІЇ (ООД) 1. Алгоритм складання синтезу за участю малонового естеру 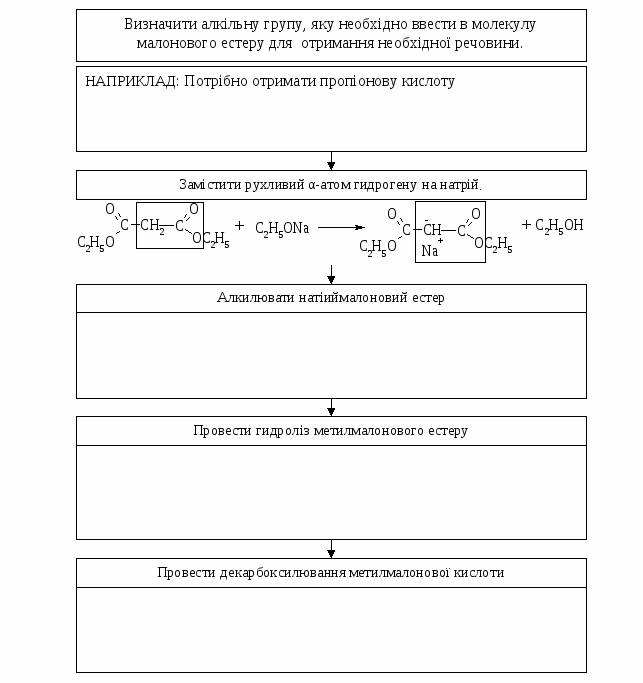 2. Інструкція з виконання лабораторних дослідів Хімічні властивості дикарбонових кислот Принцип методу: наявність в молекулах дикарбонових кислот двох карбоксильних групи може бути використана для реакцій ідентифікації сполук з відповідними функціональними групами. Ціль: за допомогою характерних реакцій практично довести хімічні властивості представників класу дикарбонових кислот . Обладнання та реактиви: штатив з пробірками, пальник, водні розчини мурашиної, оцтової, щавлевої, оксалатної і фумарової кислот, натрій форміат, 5% р-н CaCl2, баритова вода. Методика виконання: Опит 91. Отримання натрію оксалату із натрію формиату. В суху пробірку поміщають невелику кількість натрію форміату і нагрівають в полум’ї пальника до плавлення. Пробирку підносять отвором до полум’я пальника . Плав оксалату натрію зберігають для проведення оп. 92. Опит 92. Відкриття оксалатної кислоти у вигляді кальцієвої солі. В пробірку з плавом натрію оксалату, отриманого в оп. 91, додають 5-10 крап. Води. Каплю прозорого розчину наносять на предметне скло и додають 1 краплю 5% р-ну CaCl2. Опит 93. Розкладання оксалатної кислоти. В суху пробірку на 10-12мм поміщують оксалатну кислоту. Пробірку закривають пробкою з газовідвідною трубкою, кінець якої опускають в пробірку с 2мм баритової води. Пробірку з кислотою нагрівають. Спостерігають зміни в пробірці з баритовою водою. Опит 95. Відкриття оцтової та бензойної кислот реакцією з ферруму (III) хлоридом. В двох пробірках окремо в 0,5мл води розчиняють по декілька кристалів натрієвих солей оцтової та бензойної кислот. Додають по 2 краплі 1%-ного розчину ферруму(III) хлориду в кожну із пробірок. Спостерігають зміну кольору. Опит 96. Реакція карбонових кислот з натрію гідрокарбонатом. В пробірки окремо поміщають по 0,5 мл розчинів оцтової, бензойної та оксалатної кислот. Додають по краплям 5%-ний розчин натрію гідрокарбонату. Спостерігають бурхливе виділення бульбашок газу. Отриманий газ пропускають повз баритову воду. Опит 99. Возгонка саліцилової кислоти (“зимовий сад”). В хімічний стакан на 200 мл поміщають приблизно 2 г саліцилової кислоти і опускають ялицеву гілку. Стакан накривають чашкою Петрі, ставлять на сітку и нагрівають в полум’ї пальника . Хід роботи:
завдання для перевірки досягнення конкретних цілей навчання Тест 1 За будовою кислота э дикарбоновою. Знайдіть таку кислоту:
Тест 2 Завдяки особливостям будови кислота проявляє оптичну активність. Знайдіть таку кислоту: 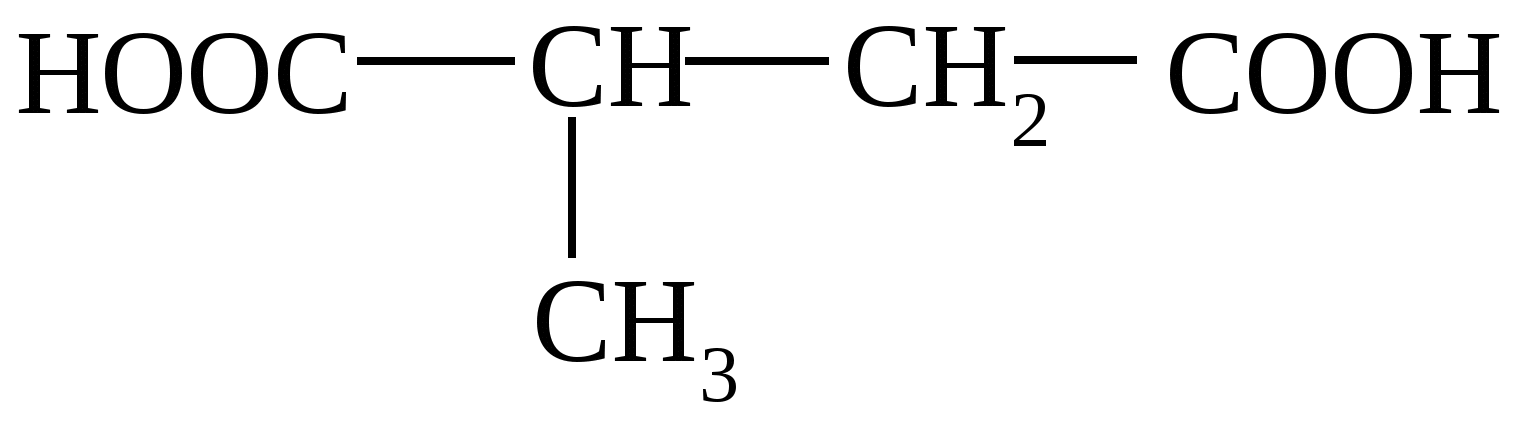 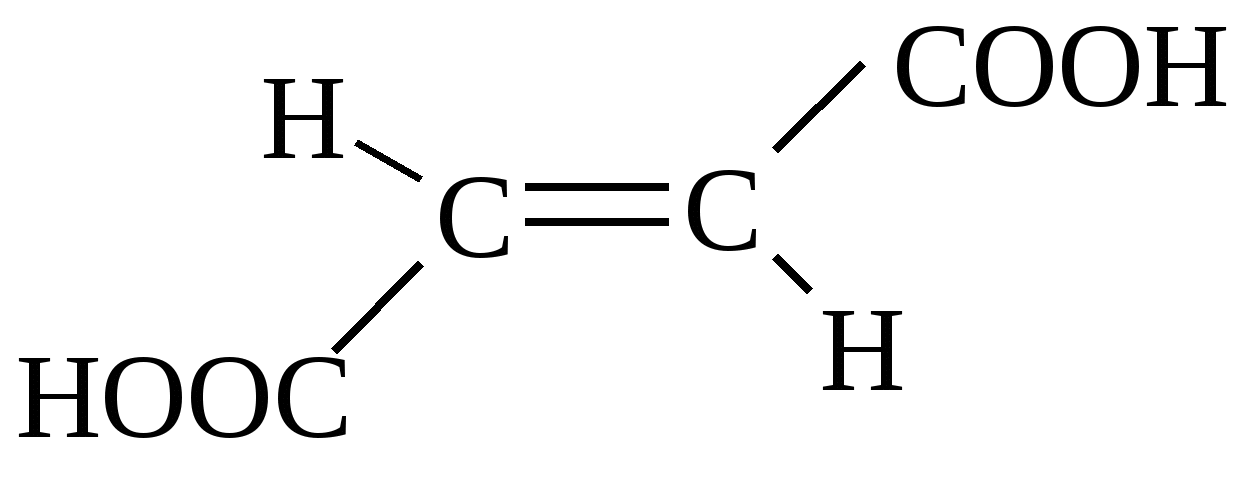 A. B. C. D. E. Тест 3 В результаті окислення невідомої сполуки утворюється фталева кислота за схемою. 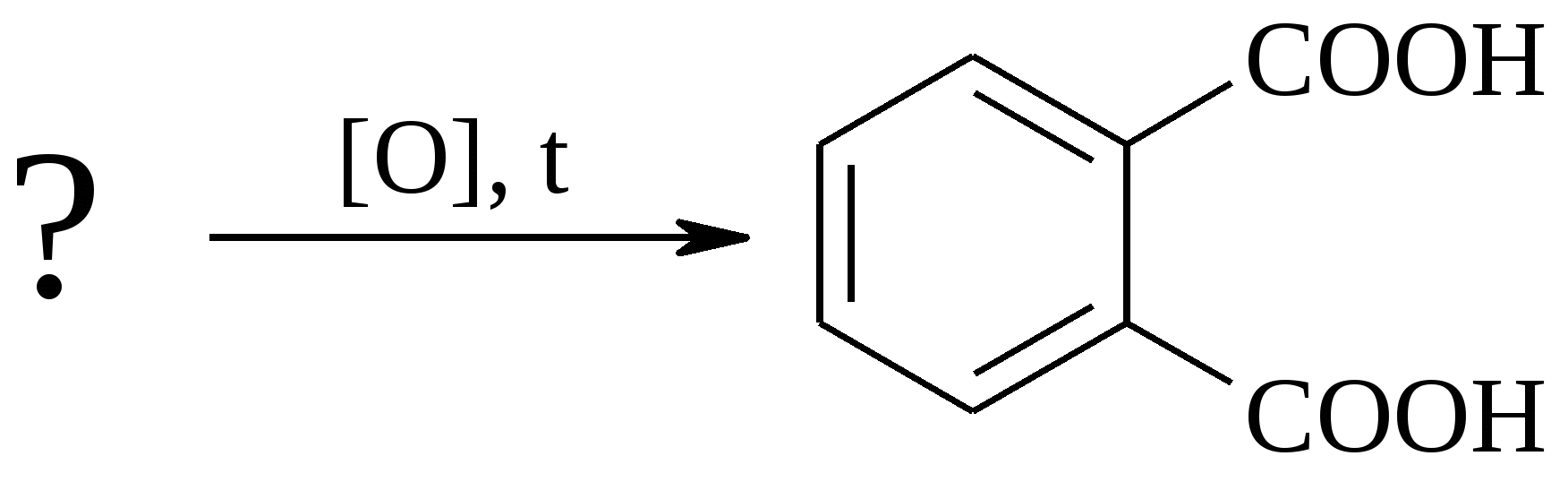 Знайдіть цю сполуку: 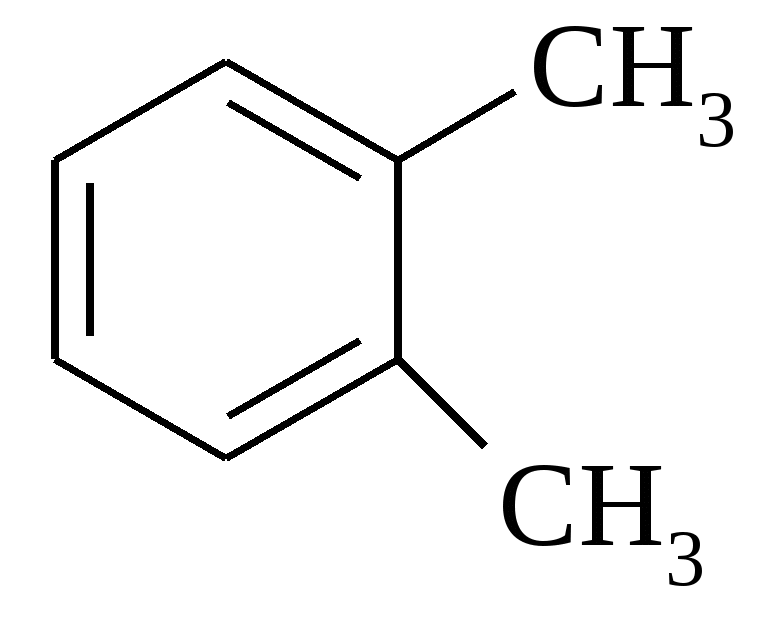 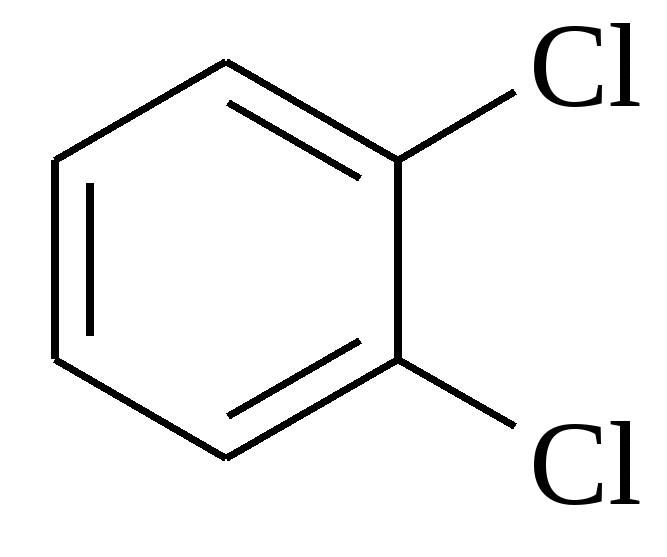 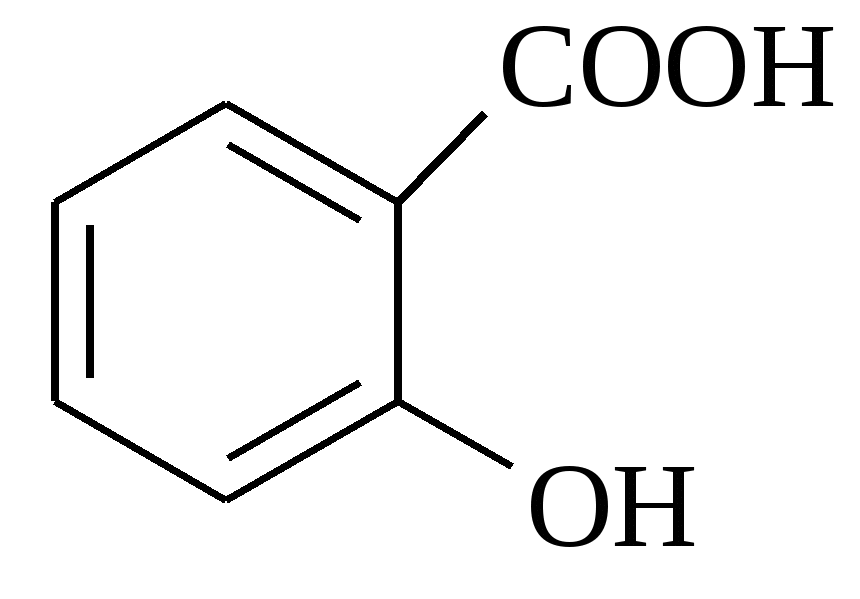 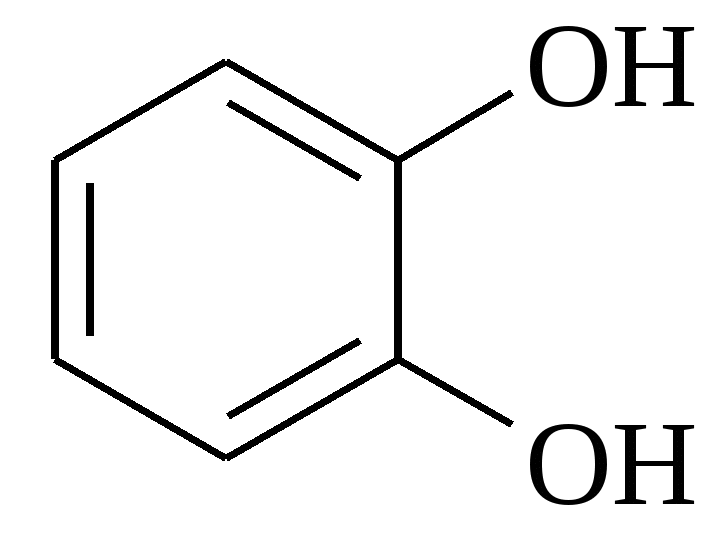 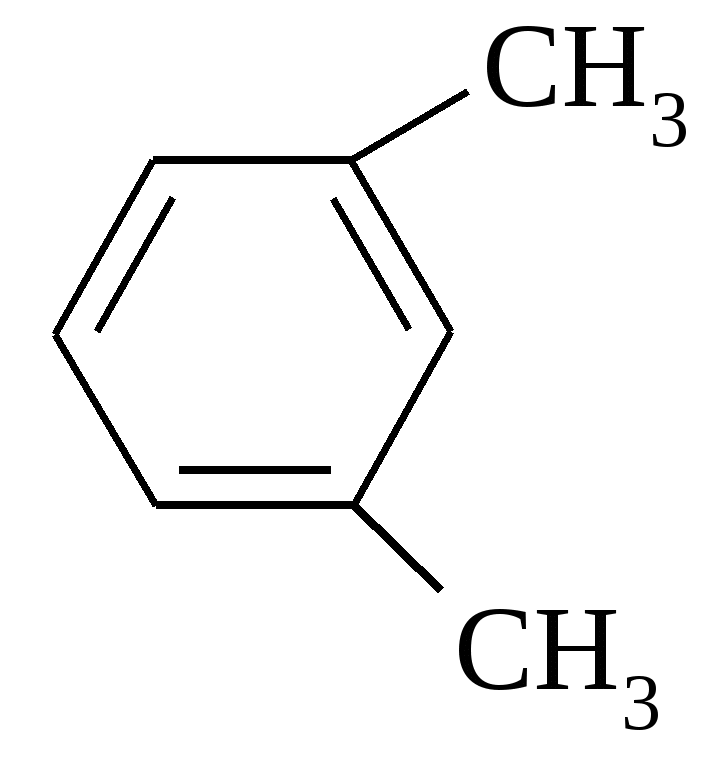 A. B. C. D. E. Тест 4 Вивчають хімічні властивості глутарової кислоти. З яким з запропонованих реагентів ця кислота не вступает в реакцию ?
Тест 5 Вивчають хімічні властивості дикарбонових кислот. При взаємодії з розчином FeCl3 утворює осад рожево-жовтого кольору. Знайдіть таку кислоту:
Еталони відповідей: 1.D, 2.B, 3.A, 4.E, 5.C. КОРОТКІ МЕТОДИЧНІ ВКАЗІВКИ ДО ПРОВЕДЕННЯ ПРАКТИЧНОГО ЗАНЯТТЯ На занятті перевіряється підготовленість студентів до проведення практичного заняття, проводиться інструктаж з техніки безпеки при роботі з хімічними реактивами. Перевіряється виконання домашнього завдання та під керівництвом викладача виконуються завдання для самостійної роботи. Потім студенти приступають до виконання лабораторної роботи, використовуючи при цьому інструкцію робочого журналу. Після виконання лабораторної роботи необхідно оформити протокол, зробити висновки до роботи, що перевіряє і контролює викладач. Проводиться підсумковий тестовий контроль за темою, підводяться підсумки роботи. |
