Проектирование хим. предприятий. Навчальний посібник до вивчення курсу основи проектування хімічних виробництв
 Скачать 6.93 Mb. Скачать 6.93 Mb.
|
|
Глава8 ТЕХНОЛОГИЧЕСКИЙ РАСЧЕТ ОСНОВНОЙ И ВСПОМОГАТЕЛЬНОЙ АППАРАТУРЫ 8.1. ОБЩИЕ ПОЛОЖЕНИЯ Задачей технологического расчета является определение размеров аппарата, обеспечивающих заданную производительность, и количества всех аппаратов, составляющих схему производства. Принципы расчетов оборудования периодического и непрерывного действия различны, хотя конечная их цель сводится к нахождению, преимущест- венно, объема аппарата или поверхности теплообмена. Геометрические размеры, например, реактора - это высота (Н) и диаметр (D). При этом диаметр реактора можно определить из соотношения 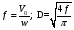 где V0 - объемная производительность, м3/с; w - скорость движения реакционной смеси, м/с; f - площадь сечения реактора, м2. Длина рабочей зоны реактора 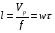 где Vp - объем реактора, м3; τ - среднее время пребывания реакционной смеси в аппарате, с. Объем реактора Vp = τV0 Исходными данными для технологического расчета химической аппаратуры являются: - предварительная аппаратурно-технологическая схема, предусматривающая характер выбранных аппаратов и их взаимосвязь в материальном потоке; - объемы перерабатываемого сырья, полупродуктов и готового продукта на каждой технологической стадии производства (в сутки, в час, в секунду). Количества перерабатываемых продуктов, полученных в материальном расчете, переводятся в соответствующие объемные величины; - длительность каждой стадии технологического процесса. Необходимо учесть возможность длительности отдельных стадий за счет усовершенствования процесса: введение более эффективно действующего инициатора или катализатора, изменение соотношения реагирующих компонентов, повышение эффективности перемешивания, обогрева и т.д.; - скорость протекания реакционной массы через аппарат в м/с или в других еди- ницах для реакторов непрерывного действия. Эта величина зависит от кинетики химической реакции, длительности аналогичной стадии периодического процес- са, вязкости реакционной смеси и, наконец, заданной степени конверсии исход- ных продуктов; - возможные соотношения длины (или высоты) аппаратов «идеального» вытеснения к их поперечному сечению. Для аппаратов «идеального» смешения и комбинированных типов необходимо заранее предполагать характер передачи реакционной смеси из одного аппарата (или секции) в другой. После завершения технологического расчета каждого аппарата необходимо дать обоснованный выбор конструкционного материала для его изготовления. 8.2. РАСЧЕТ ОБЪЕМОВ РЕАКТОРОВ 8.2.1. Основные положения химической кинетики Химическая кинетика - наука, изучающая протекание химических реакций во времени. Ее основным понятием является скорость химической реакции. Для гомогенных процессов под скоростью химической реакции понимают изменение количества одного из компонентов реакции в единицу времени в единице объема, т.е.: 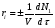 , ,где ri - скорость реакции по i-тому компоненту, моль/(м3 с); V - реакционный объем, м3; Ni - число молей i - того компонента, моль; τ — время, с. Знак плюс - для продуктов реакции, а знак минус - для реагентов (так как в резуль- тате реакции число молей продуктов увеличивается, а реагентов - уменьшается). Если реакция протекает без изменения объема, то 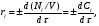 где Сi — концентрация i -того компонента, моль/м3. Вводя понятие степени превращения Хi определяемое соотношением 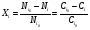 , ,где индекс «0» относится к начальному состоянию i - того компонента, получим 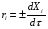 Для гетерогенных процессов скорость реакции - это изменение количества компо- нента в единицу времени, отнесенное к единице поверхности, где протекает хими- ческая реакция 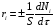 где S - «активная» поверхность, м2; ri - скорость реакции, моль/(м2∙с). Если в процессе реакции поверхность S постоянна, то скорость реакции можно от- нести к пропорциональным ей величинам: массе твердой фазы mτ, объему твердой фазы Vτ, реакционному объему Vp, т.е. 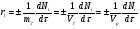 . .Единицы этих скоростей соответственно: моль/(кг∙с), моль/м3 Стехиометрия реакций дает следующие соотношения между скоростями реакции по компоненту и общей скоростью r, например для реакции: vAA = vBB; -vAA +vBB = 0; 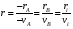 В отличие от скорости превращения вещества ri величина скорости простой химической реакции r всегда положительна. Основным законом химической кинетики является закон действующих масс, который гласит, что скорость реакции прямо пропорциональна произведению концентрации реагентов в степени, являющейся порядком реакции по данному реагенту, т.е. 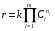 где k - константа скорости реакции, зависящая только от температуры; m - число реагентов; ni - порядок реакции по i-тому реагенту. Константа скорости реакции и ее порядок являются эмпирическими величинами и расчету практически не поддаются. Зависимость константы скорости реакции от температуры определяется известным уравнением Аррениуса: 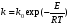 где k0 - предэкспоненциальный множитель, имеющий размерность константы ско- рости реакции; Е - энергия активации реакции, Дж/моль; R - универсальная газовая постоянная, Дж/(моль∙К); T - температура, К. Предэкспоненциальный множитель и энергия активации могут быть определены только опытным путем при обработке нескольких экспериментальных данных по константам скорости реакции, полученным при различных температурах. Считается, что энергия активации не зависит от температуры, что подтверждается экспериментом. Однако обычно ошибка в оценке энергии активации не может быть меньше 15 - 20% из-за сложности установления изотермического режима при проведении реакции, недостаточной точности измерения и регулирования температуры в реакционном пространстве. В узком интервале температур можно по двум точкам оценить температурную зависимость скорости реакции линейной функцией вида k = аТ + b. В химической кинетике принято разделя гь химические реакции на простые и слож ные. К простым относятся реакции, протекающие практически до конца в одну ста дию. Сложные реакции представляют некоторую совокупность простых и подраз- деляются на параллельные, последовательные и обратимые. Дальнейшее усложне- ние реакций приводит к комбинациям последних трех типов. Параллельные реакции имеют вид А →В; А →С. Скорость реакции в этом случае равна сумме скоростей отдельных реакций r = r1 + r2 = 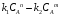 Последовательные реакции: А → В → С. скорость превращения компонента А rA = kА∙СА; скорость образования компонента С rC = kB∙СB скорость накопления компонента В rB = kАСА - kBСB. Обратимые реакции: А ↔ В. Если k1 - константа скорости прямой реакции, а k2 - обратной, то суммарная скорость r = rА - rB = 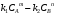 . .При равновесии r = 0 (rА = rB), поэтому выполняется условие, при котором КР = k1/k2, где КР - константа равновесия данной реакции. Со сложными реакциями связано понятие селективности (избирательности) процесса, так как часто желательно получение только одного, «целевого», продукта. Под дифференциальной селективностью понимают отношение скорости образования целевого продукта к общей скорости реакции, например, для параллельной реакции, если целевым является конечный продукт В, 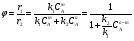 Дифференциальная селективность изменяется со временем, так как по мере увеличения степени превращения уменьшается концентрация реагентов. Интегральную (общую) селективность можно выразить отношением конечной концентрации целевого продукта СВк к сумме концентраций всех продуктов реакции. 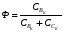 Соотношение между дифференциальной и интегральной селективностью определяется выражением 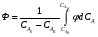 При кинетических расчетах не следует проводить операцию по исключению стехи ометрически зависимых реакций, так как она целесообразна только при материаль ных расчетах. 8.2.2. Расчет идеальных реакторов Реактор смешения периодического действия. Используя уравнение мате- риального баланса, можно получить общее характеристическое уравнение реакто ра идеального смешения периодического действия CA - (CA + dCA) - rAdτ = 0 где СА - концентрация ключевого реагента; rА - скорость химической реакции по этому компоненту. Из этого уравнения легко получить dτ = - (dCA/rA) Интегрируя это уравнение в пределах от 0 до τ и от СA0 до СA, получим время пре бывания реагентов в реакционном пространстве:  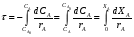 Здесь ХА - степень превращения ключевого реагента. Объем такого реактора будет определяться единовременной загрузкой реагентов, которая зависит от средней годовой производительности, поэтому V=G/ρ где V - объем реакционной зоны, м3; G - разовая загрузка реагентов в реактор, кг. Реактор смешения непрерывного действия. Для реактора идеального смешения непрерывного действия уравнение баланса массы будет иметь вид v0CA – v0(CA+dCA) - rAV = 0, где v0 - объемный расход (подача) реагентов, м3/с; V - объем реактора, м3. Так как в реакторе идеального смешения непрерывного действия rA=const, то 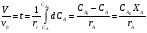 где t - условное время пребывания реагентов в зоне реакции. Объем реактора определится формулой V=v0∙t. Реактор вытеснения. Для реактора идеального вытеснения уравнение материального баланса аналогично реактору идеального смешения: v0СA - v0 (СA + dСA) - rAV = 0. После его интегрирования также получаем 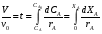 Объем реактора идеального вытеснения также определится формулой V = v0t При расчете объемов реактора вытеснения или смешения периодического действия приходится вычислять интегралы, подинтегральная функция которых может быть достаточно сложной. Поэтому в таком случае прибегают к численному интегрированию. Наиболее популярной для таких целей является формула Симпсона, которая имеет следующий вид: 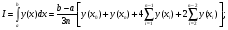 Здесь а и b - пределы интегрирования; n - четное число интервалов разбивки отрезка интегрирования. Расчет проводится в следующей последовательности: задаются точностью вычисления интеграла ε и вычисляют интеграл при n = 4. Затем n все время удваива- ется, пока не выполнится условие |J(n) – 1(2n) | < ε. Формула Симпсона легко программируется. Достаточно точными являются две следующие простые формулы: пятиточечная 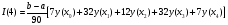 и семиточечная формула Уэддля 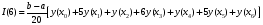 Задача расчета реальных реакторов в подавляющем большинстве случаев является весьма сложной, так как при этом требуется постановка специальных ис- следований по оценке эффективной диффузии компонентов реакции в конкретных технологических условиях. При наличии таких коэффициентов расчет можно провести по методикам, описанным в литературе. 8.3. ОПРЕДЕЛЕНИЕ ОБЪЕМОВ АППАРАТА Определение количества операций, совершаемых одним реактором в сутки, по формуле n = τ/t, где n - количество операций в сутки; τ - время работы реактора в сутки, ч; t - длительность стадии технологического процесса, ч. Значение n может быть найдено и другим путем: n = VC/VP, где VC - суточный объем перерабатываемых материалов, м3; VP - рабочая емкость всех аппаратов данной технологической стадии. Определение рабочей емкости всех аппаратов данной стадии: VP = VC/n. Расчет общего объема всех аппаратов: Vобщ = VP/φ где Vобщ - общий объем всех аппаратов данной технологической стадии; φ - коэффициент заполнения аппарата. Коэффициент заполнения φ имеет различные значения в зависимости от харак- тера процесса, осуществляемого в данном аппарате. При выборе коэффициента заполнения можно руководствоваться следующими данными, представленными в табл. 8.1. Таблица 8.1. Значения коэффициентов заполнения
Оптимальная емкость реактора выбирается в зависимости от конкретных условий проведения данного процесса. Необходимо использовать практические данные по объему аппарата существующего производства. Расчет количества аппаратов данной стадии определяется выражением К = Vобщ/V где К - количество аппаратов; Vобщ - общий объем одного аппарата (по каталогу), м3. Если проектируемый аппарат не предусмотрен каталогом, то объем аппарата выбирается по практическим соображениям. В любом случае после выбора аппарата дается краткое описание его конструктивных особенностей с указанием марки материала. Расчет объемов аппаратов непрерывного действия заключается в определении объ- ема перерабатываемых материалов, в час (или в секунду): Vчас = Vсут/24, м3/ч. Расчет рабочей емкости всех аппаратов: VP = Vчас τ где VP - рабочая емкость всех аппаратов, м3; τ - время пребывания реакционной массы в аппарате, ч. Расчет общей емкости всех аппаратов: Vобщ = VP /φ Выбор стандартного аппарата или конструирование нового заключается в следующем. Для аппаратов непрерывного действия - аппаратов «идеального» вытеснения - необходимо, прежде всего, определить соотношение между высотой (или длиной) аппарата и его поперечным сечением. При заданной скорости протекания реакционной массы можно рассчитать высоту (длину) аппарата идеального вытеснения по формуле: H = Wτ где Н - высота (длина) аппарата, м; τ - время пребывания реакционной массы в аппарате, с. Площадь поперечного сечения аппарата идеального вытеснения F = V/W. Количество аппаратов непрерывного действия определяется, как для периодических процессов: К = Vобщ/V где V - объем одного реактора, м3. В конце расчета следует привести подробное описание конструктивных особенностей и материала выбранного аппарата, а также описание пускового периода реактора до ввода его в непрерывный процесс. Для комбинированных аппаратов смешения каскадного и секционного типов основным вопросом технологического расчета является определение оптимального количества последовательно включенных аппаратов или секций, а также их рабочего объема. В тех случаях, когда имеется уравнение кинетики процесса и известны значения констант скорости реакций, используется аналитический метод расчета многосекционного реактора или каскада аппаратов. Ниже приводятся некоторые типовые примеры, иллюстрирующие методы определения объемов реакторов, которые характеризуют производство с заложенными в них различными химическими реакциями как с известными кинетическими уравнениями, так и без них. Пример 8.1. Рассчитать поликонденсатор дигликольтерефталата производи- тельностью 3 т/сут. Процесс периодический. Данные о работе аппарата при загрузке 1 т дигликольтерефталата приведены в табл. 8.2. Таблица 8.2. Режим работы реактора периодического действия (РПД)
Решение: VРПД = Gτ/(24x1040x0,4) = 2,11 м3 По ГОСТ 9931 - 61 объем РПД принимают равным 2,5 м3. Пример 8.2. Расчет продолжительности реакции с использованием кинетики реакции. В реакторе периодического действия протекает химический процесс, скорость которого определяется уравнением вида 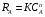 при n = 1 и при n = 1 и К= 0,000895 с-1. Начальная концентрация исходного продукта А равна 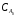 = 1 моль/л. Конечная степень превращения XА = 0,96. Требуется определить продолжительность реакции τ3. = 1 моль/л. Конечная степень превращения XА = 0,96. Требуется определить продолжительность реакции τ3.Решение: 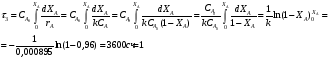 Далее подставляем τ3 в величину τn и заканчиваем расчет так же, как указано в примере 8.1. Пример 8.3. В реакторе вытеснения протекает реакция в газовой фазе по yравне- нию 4А → В + 6С при 648,89 К, скорость которой описывается выражением RA = 2,78 10 -3 СА. Степень превращения xA = 0,80. Давление в системе- 4,6 атм. Скорость подачи реагента А равна GА = 5,03 10-4 кмоль/с. Рассчитать объем РВНД. Решение: Объем РВНД находим по формуле 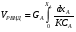 При постоянном давлении 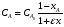 где 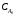 - начальная концентрация реагента; ε - коэффициент, учитывающий изме- - начальная концентрация реагента; ε - коэффициент, учитывающий изме-нение объема системы; ε = (7 - 4)/4 = 0,75 Подставляем соответствующие величины в первоначальную формулу 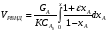 После интегрирования получаем следующее выражение: 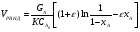 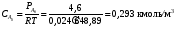 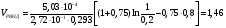 м3 м3По ГОСТ 13372 - 87 принимаем ближайший объем трубчатого реактора равным 1,6 м3 В том случае, когда неизвестны кинетические константы скорости реакции, время пребывания принимают по практическим данным (из регламента цеха). Ниже приводится пример расчета объема РВНД по принятому значению времени пребывания τ. Пример 8.4. Рассчитать объем РВНД для ежедневного производства 50 т этилацетата из уксусной кислоты. Исходные данные: время τ= 7270 с; плотность реагирующей смеси постоянна ρ = 120,56 кг/м3. Решение: Определяем объемную скорость реагирующей смеси для производства 50 т вещества: 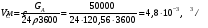 Определяем объем РВНД по уравнению VРВНД = Vc τ = 4,8∙10-3∙7270 = 34,8м3 По ГОСТ 13372 - 67 принимаем ближайший объем аппарата 40 м3. Пример 8.5. В РСНД проводится реакция типа А → В, которая характеризуется кинетическим уравнением RА = 5,55∙10-5∙СА, с-1. Необходимо получить 2,77 ∙10-5 кмоль/с вещества В из исходной смеси, содержащей вещество А в количестве 0,1 кмоль/м3. Степень превращения хА = 0,5. Требуется определить объем реактора смешения. Решение: Объем РСНД определяем по уравнению VРCНД = GA∙xA/RA Выражаем СА = СА0 (1 - хA). Определяем скорость подачи исходной смеси: GA = 2,77∙10-5/хА = 2,77∙10-5/0,5 = 5,54∙10-5 кмоль/с Подставляем указанные значения в первое уравнение и получаем искомое значение объема: VРCНД = (5,54∙10-5∙0,5)/( 5,54∙10-5∙0,1∙0,5) = 10м3 По ГОСТ 13372 - 67 принимаем объем РСНД, равным 10 м3. При выполнении проекта инженер-проектировщик обязан произвести технологические расчеты вспомогательной аппаратуры, всех транспортных устройств (ленточные и шнековые транспортеры, пневмотранспорт и др.), а также рассчитать необходимую производительность и выбрать соответствующие типы питателей, дозаторов, мерников, циклонов и т.д. Расчет соответствующего оборудования здесь не рассматривается, его можно най- ти в литературе по процессам и аппаратам химической технологии. |
