Phenylii salicylatis ana 0,25
 Скачать 231.24 Kb. Скачать 231.24 Kb.
|
|
7. Технология лекарственных форм с теоретическим обоснованием. Изготовление инъекционного раствора № 214. и № 308 и статьи ГФ Х1 «Инъекционные лекарственные формы». Рабочее № 309. ППК 214 от 16.07.97 г.В асептических условиях в 5мл воды очищенной по правилам работы с веществами списка А отвешивают и растворяют 0,1г атропина сульфата и 0,08 г натрия хлорида. Раствор фильтруют во флакон для отпуска через стерильный фильтр, промытый водой. Фильтр промывают 5 мл воды очищенной, с целью сохранения концентрации и объема раствора. Раствор проверяют на отсутствие механических включений, укупоривают «под обкатку» и стерилизуют при 100°С 30 минут. 8. Упаковка и оформление. Флакон из стеклодрота оформляют этикеткой с сигнальной полосой розового цвета, на которой указывают номера аптеки, рецепты, ФИО больного, способ применения . Флакон опечатывают, больному вместо рецепта выдают сигнатуру. 9. Оценка качества. -Упаковка и оформление соответствуют требованиям приказа МЗ РФ № 120 от 05.09.97 г. Капли укупорены герметично. - Отклонение в объеме ± 10% (от 9 до 11 мл) в соответствии с требованиями приказа МЗ РФ № 305 (от 16.10 97 г.). 10. Применяют в офтальмологии для достижения мидриатического эффекта. № 56. Recipe: Solutionis Novocaini 1% 25 мл Sterilisetur! Da. Signa: По 1 мл внутримышечно 2 раза в день. Характеристика лекарственной формы. Инъекционный раствор для внутримышечного введения, представляющий собой истинный водный раствор, в состав которого входит вещество сп. Б – новокаин, который в водных растворах подвержен реакции гидролиза, в связи, с чем его стабилизируют; раствор выдерживает термическую стерилизацию. Проверка доз и норм одноразового отпуска. В.р.д. внутримышечно 0,1 г; В.с.д. внутримышечно 0,1 г; Расчет разовой дозы: 1,0г новокаина – в 100 мл 1% раствора х г новокаина – в 1 мл 1% раствора x = 0,01 г Р.д. 0,01 г С.д. 0,01 2 = 0,02 г Дозы не завышены. Паспорт письменного контроля.
Технология лекарственной формы с теоретическим обоснованием. Изготовление инъекционного раствора 214 и № 308 и статьи ГФ ХI «Инъекционные лекарственные формы». Рабочее место № 309. ППК № 214. Новокаин является солью слабого азотистого основания и сильной кислоты хлористоводородной, в связи, с чем в его водных растворах протекает реакция гидролиза по следующему типу:   ВА + НОН ВОН + Н + + А – ВА + НОН ВОН + Н + + А – Прибавление к этому раствору свободной кислоты, т.е. избытка водородных ионов, подавляет гидролиз, вызывая сдвиг равновесия влево, в сторону недиссоциированного новокаина. Количество кислоты, необходимое для стабилизации определяется требованиями приказа МЗ РФ № 214 и составляет для 1% раствора новокаина 9 мл 0,1 М раствора кислоты хлористоводородной на 1 литр раствора новокаина (до рН 3,8 – 4,5). Учитывая максимальную концентрацию (%), при которой изменение объема укладывается в норму допустимого отклонения, для данного раствора новокаина равную 4,9%, КУО для расчетов не используют и приростом объема при растворении новокаина пренебрегают. Добавляемое количество стабилизатора – 0,225 мл также укладывается в нормы допустимых отклонений по приказу МЗ РФ 305 (для 25 мл 4%, т.е. 1мл). Воды для инъекций на этом основании берут 25 мл. В асептических условиях, в стерильной мерной колбе вместимостью 25 мл в части воды для инъекций растворяют 0,25 г новокаина, добавляют пипеткой 5 капель 0,1 М раствора кислоты хлористоводородной и доводят водой для инъекций до метки. Раствор фильтруют через стерильный бумажный фильтр с подложенным под него комочком стерильной медицинской, длинноволокнистой ваты в стерильный флакон нейтрального стекла вместимостью 30 мл. Изготовленный раствор подвергают полному химическому контролю до и после стерилизации. (Для этого во флакон из стеклодрота отливают 2-3 мл раствора. Флакон укупоривают «под обкатку», стерилизуют вместе с основным флаконом. После стерилизации раствор из флакона используют для проведения полного химического анализа.) Кроме того, флакон с раствором просматривают невооруженным глазом на отсутствие механических включений на белом и черном фоне, освещенном электрической лампочкой матового стекла мощностью 40 Вт. Причем, проверка на отсутствие механических включений проводится также дважды: до и после стерилизации. После первичной оценки на отсутствие механических включений и положительного химического анализа флакон укупоривают стерильной резиновой пробкой «под обкатку» или стерильной стеклянной пробкой со шлифом «под обвязку», пробку обвязывают пергаментной бумагой. На обвязке надписывают простым карандашом состав, концентрацию раствора и фамилию лица, изготовившего раствор. Проверяют качество укупорки и стерилизуют в паровом стерилизаторе при 120С в течение 8 мин. После стерилизации вторично поводят полный химический контроль, проверяют на отсутствие механических включений и качество укупорки. Упаковка и оформление. Флакон с готовым раствором в соответствии с требованиями приказа МЗ РФ № 120 от 05.09.97 г. оформляют этикеткой «Для инъекции», на которой, кроме общих для всех этикеток надписей, указывают «Раствор новокаина 1% 25 мл для внутримышечного введения по 1 мл 2 раза в день» и номер анализа. Предупредительные надписи: «Беречь от детей», «Хранить в защищенном от света месте». Наклеивают номер рецепта. Срок хранения раствора в аптеке составляет: если он изготовлен во флаконе со шлифом («под обвязку») – 2 суток; «под обкатку» – 30 суток при температуре не выше 25С, в защищенном от света месте. Оценка качества. Оформление соответствует требованиям приказа МЗ РФ №120 от 05.09.97г. Полный химический контроль № 214. Отклонение в объеме 4% (от 29 до 31 мл) в соответствии с требованиями приказа МЗ РФ № 305 от 16.10.97 г. - Стерильность, апирогенность. Применение. Обезболивающее. № 57. 1. Recipe: Solutionis Glucosi 5% 50 ml Sterilisetur! Da. Signa: Внутривенно, капельно. 4. Характеристика лекарственной формы. Инъекционный раствор для внутривенного капельного введения, представляющий собой истинный водный раствор лекарственного вещества – глюкозы, подвергающегося окислению и карамелизации. 6. Паспорт письменного контроля. Лицевая сторона Оборотная сторона Дата № 35 Глюкозы безводной Aquae pro injectionibus 47,5 ml 5 г на 100 мл раствора Solutio Vejbeli 2,5 ml 2,5 – 50 мл Glucosi 2,77 Глюкозы с влажностью 10% Объем 50 мл 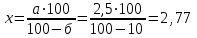 Простерилизовано! Приготовил (подпись) Стабилизатора Вейбеля Проверил (подпись) 5% от объема раствора на Отпустил (подпись) 100 мл – 5 мл 50 мл – 2,5 мл 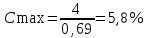 Воды для инъекций 50 – 2,5 = 47,5 мл 7. Технология лекарственной формы с теоретическим обоснованием. Изготовление инъекционного раствора № 214 и № 308 и статьи ГФ ХI «Инъекционные лекарственные формы». Рабочее место № 309 ППК № 214. При расчете Сmax (%) найдено, что 5% раствор глюкозы в количестве 50 мл можно готовить не учитывая КУО глюкозы. Растворы глюкозы при стерилизации, особенно во флаконах из щелочного стекла, подвергаются окислению и карамелизации. При этом наблюдается пожелтение, а иногда и побурение растворов. При выборе стабилизатора необходимо учитывать полифункциональный характер глюкозы. Она неустойчива в щелочной среде, под влиянием кислорода образуются оксикислоты: гликолевая, левулиновая, муравьиная и другие кислоты и оксиметилфурфурол. Для предотвращения этого процесса растворы глюкозы стабилизируют 0,1 М раствором кислоты хлороводородной до рН 3,0-4,1. Глюкоза неустойчива и в кислой среде – образуется Д – глюконовая кислота и ее лактоны в результате их окисления, особенно в процессе стерилизации, образуется 5-оксиметилфурфурол, вызывая пожелтение раствора, что связано с дальнейшей карамелизацией. Таким образом, в качестве стабилизаторов в раствор глюкозы вводят на 1 литр 0,2 г натрия хлорида и 0,1 М раствора кислоты хлороводородной до рН 3,0 – 4,1. В аптечных условиях используют готовый стабилизатор Вейбеля, в состав которого входят: Натрия хлорида 5,2 г Кислоты хлороводородной разведенной 4,4 мл Воды для инъекций до 1 литра. Этот стабилизатор добавляют в количестве 5% от объема раствора и независимо от его концентрации. В асептических условиях в стерильной подставке в воде для инъекций растворяют 2,77 г глюкозы, добавляют 2,5 мл раствора Вейбеля, затем раствор фильтруют через стеклянный фильтр с размером пор 10-16 мкм или стерильную фильтровальную бумагу с подложенным комочком стерильной длинноволокнистой медицинской ваты в стерильный флакон нейтрального стекла вместимостью 50 мл. Изготовленный раствор подвергают полному химическому контролю до и после стерилизации. (Для этого во флакон из стеклодрота отливают 2-3 мл раствора. Флакон укупоривают «под обкатку», стерилизуют вместе с основным флаконом. После стерилизации раствор из флакона используют для проведения полного химического анализа.) Кроме того, флакон с раствором просматривают невооруженным глазом на отсутствие механических включений на белом и черном фоне, освещенном электрической лампочкой матового стекла мощностью 40 Вт. Причем, проверка на отсутствие механических включений проводится также дважды: до и после стерилизации. Укупоривают и стерилизуют при 120С в течение 8 мин. Срок хранения 30 суток. 8. Упаковка и оформление. Флакон с готовым раствором в соответствии с требованиями приказа МЗ РФ № 120 от 05.09.97 г. оформляют этикеткой «Для инъекции», на которой, кроме общих для всех этикеток указывают «Раствор глюкозы 5% 50 мл для внутривенного, капельно» и номер анализа. Предупредительные надписи: «Беречь от детей», «Хранить в защищенном от света месте». Наклеивают номер рецепта. 9. Оценка качества. Оформление соответствует требованиям приказа МЗ РФ №120 от 05.09.97г. Полный химический контроль № 214 от 16.07.97г. Отклонение в объеме 4% (от 48 до 52 мл) в соответствии с требованиями приказа МЗ РФ № 305 от 16.10.97 г. - Стерильность, апирогенность. 10. Применение. Средство для парентерального питания (поддержание концентрации глюкозы в крови). № 58. 1. Recipe: Solutionis Acidi Ascorbinici 5% 50 мл Sterilisetur! Da. Signa: Для внутримышечного введения по 2 мл 1 раз в день. Характеристика лекарственной формы. Инъекционный раствор для внутримышечного введения, представляющий собой истинный водный раствор легкоокисляющегося лекарственного вещества – кислоты аскорбиновой, требующего стабилизации, выдерживающего термическую стерилизацию. Паспорт письменного контроля. Лицевая сторона Оборотная сторона Дата № 37 - Кислоты аскорбиновой Aquae pro injectionibus 48,1 ml 100 мл раствора – 5,0 г 50 мл – 2,5 г Natrii sulfitis anhydrici 0,1 - Натрия гидрокарбоната Natrii hydrocarbonatis 1,19 1000 мл раствора – 23,85 г Acidiascorbinici 2,5 50 мл – х Объем 50 мл x = 1,19 г |

