Практикум по бх. Практикум по биологической химии Для студентов лечебного и педиатрического
 Скачать 5.3 Mb. Скачать 5.3 Mb.
|
Тема 11.1. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1-глобулины | 2-глобулины | -глобулины | -глобулины |
| | | | |
ТЕМЫ ДЛЯ РЕФЕРАТИВНЫХ СООБЩЕНИЙ
Возрастная динамика белковых фракций. Эмбриоспецифические белки и их диагностическое значение.
Остаточный азот: его основные компоненты. Динамика уровня фракций остаточного азота в постнатальный период.
Лабораторная работа 1
Количественный метод определения содержания
остаточного азота крови по методу Аселя
Остаточный азот является суммарным показателем безбелкового азота крови. Он складывается из мочевины (около 50%), аминокислот (около 25%), эрготионеина (около 8%), креатина и креатинина (до 7,5%), пептидов, нуклеотидов и азотистых оснований (около 5%), мочевой кислоты (до 4%), аммиака и индикана (0,5%). Так как показатель включает различные низкомолекулярные азотсодержащие вещества, более информативным является определение отдельных фракций остаточного азота.
Принцип
Сжигание небелкового фильтрата с концентрированной серной кислотой дает переход азота органических веществ в сульфат аммония, который с реактивом Несслера образует продукты желто-оранжевого цвета. Интенсивность окраски прямо пропорциональна концентрации азота.
Материал исследования
Сыворотка крови.
Реактивы
1) Реактив Несслера (щелочной раствор йодистых солей ртути и калия), 2) 5% р-р NaOH, 3) лакмусовая бумага.
Стандартный раствор (NH4)2SO4, 26 ммоль/л.
Оборудование
Колбы Кьельдаля, песчаная баня, фотоэлектроколориметр.
Проведение анализа
1. Подготовительный этап (выполняет лаборант):
Осаждение белков: в центрифужную пробирку, содержащую 1,8 мл дистиллированной воды, вносят 0,2 мл сыворотки крови, приливают 1,0 мл 10% раствора ТХУ, центрифугируют или фильтруют через смоченный бумажный фильтр.
Для минерализации 1,0 мл надосадка переносят в термостойкую пробирку, приливают 3 капли концентрированной H2SO4 и 3 капли Н2О2. Осторожно упаривают и нагревают до получения бесцветного минерализата.
2. Цветная реакция
| | Опыт, мл | Стандарт, мл |
| Минерализат | 1,0 | –– |
| Стандартный раствор (NH4)2SO4 | –– | 1,0 |
| Раствор NaOH | Проверяя величину рН по лакмусовой бумажке, добавляют по каплям до тех пор, пока рН не станет нейтральной – в нейтральной среде лакмус синеет. N.B. Излишек щелочи вызывает помутнение раствора | |
| Дистил. вода Реактив Несслера | 8,0 2,0 | 8,0 2,0 |
| | Измеряют оптическую плотность опытной и стандартной проб против воды при 540 нм (зеленый светофильтр) | |
Расчет
Концентрация остаточного азота, ммоль/л =
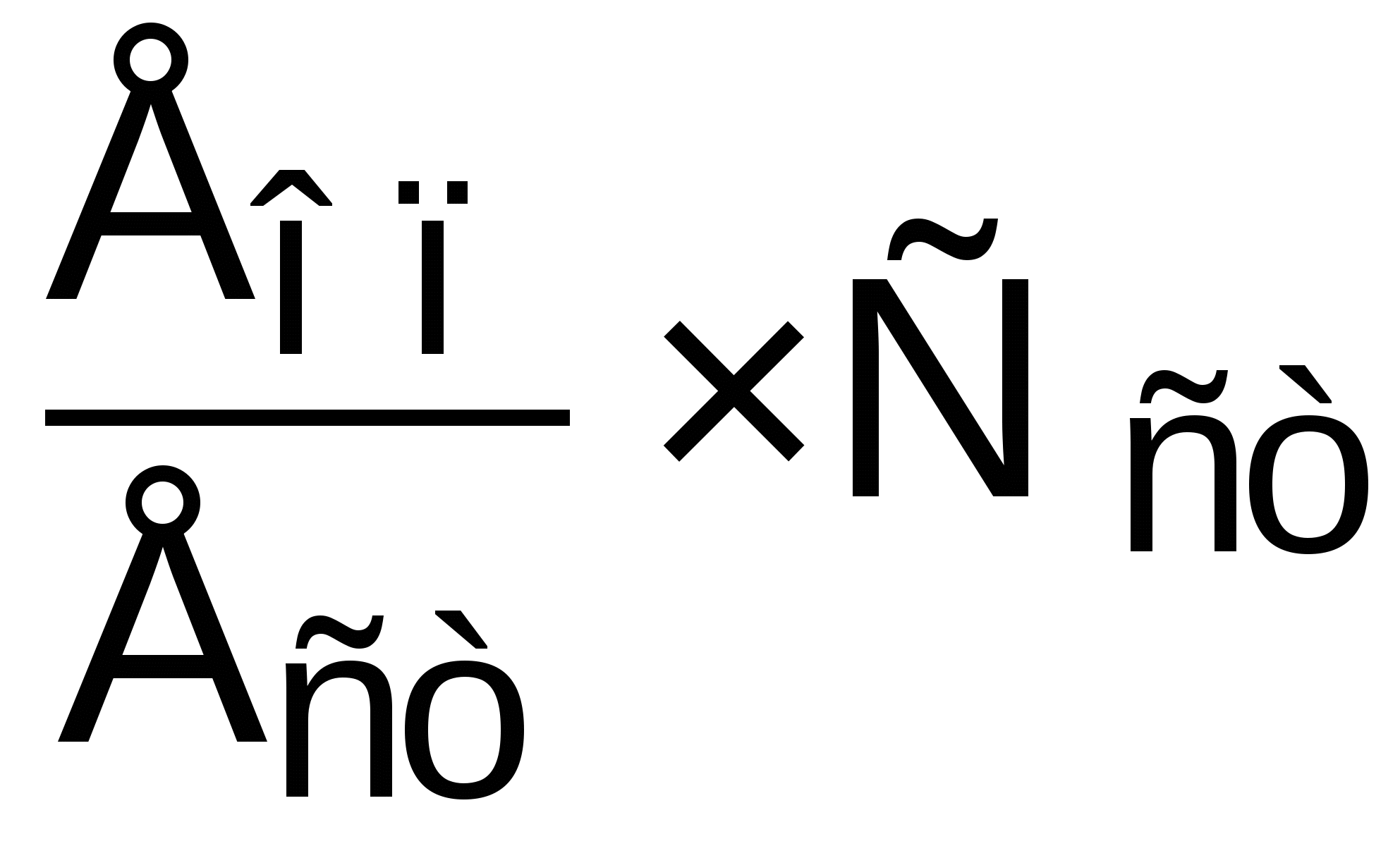 , где
, гдеЕоп и Ест – оптическая плотность опытной и стандартной проб,
Сст – концентрация стандартного раствора
Клинико диагностическое значение
Остаточный азот является показателем состояния белкового обмена.
Увеличение фракций остаточного азота (гиперазотемия) по своему характеру может быть абсолютной, связанной с действительным накоплением этих компонентов в крови, и относительной, связанной с дегидратацией. В свою очередь, абсолютная гиперазотемия может быть ретенционная (почечного и внепочечного происхождения) и продукционная:
ретенционная азотемия возникает в результате задержки выведения азотсодержащих веществ и различается на азотемии почечного происхождения (заболевания клубочков – нефриты, туберкулез почек, нефросклероз и др.) и внепочечного происхождения. Внепочечные гиперазотемии подразделяются на надпочечные (результат нарушения гемодинамики и падения фильтрационного давления при сердечно-сосудистой недостаточности, снижении артериального давления) и подпочечные (при гипертрофии или аденоме простаты, почечно-каменной болезни);
продукционная азотемия выявляется при всех состояниях, связанных с увеличением распада белков, от ретенционной ее отличает повышение содержания аминокислот в крови, а также одновременное накопление азотистых компонентов в крови и моче.
Уменьшение концентрации остаточного азота возникает при снижении содержания мочевины, аминокислот или других фракций.
Оформление работы
Записывают принцип методов и результаты анализа, отмечают клинико-диагностическое значение. Делают вывод о практическом значении метода и о возможных патологиях.
Лабораторная работа 2
Определение содержания общего белка
в сыворотке крови
Биуретовый метод
Принцип
Пептидная связь в щелочной среде образует с медью комплексное соединение (биуретовая реакция). Интенсивность развивающегося сине-фиолетового окрашивания пропорциональна содержанию белка.
Материал исследования
Сыворотка крови.
Реактивы
1) Биуретовый реактив: смесь р-ра CuSO4 и р-ра NaOH; 2) 0,9% р-р NaCl.
Стандартный раствор альбумина, 70 г/л.
Проведение анализа
| | Опыт, мл | Стандарт, мл |
| Сыворотка крови | 0,04 | –– |
| Стандартный р-р альбумина | –– | 0,04 |
| Биуретовый реактив | 3,0 | 3,0 |
| | Инкубируют 10 минут и измеряют оптическую плотность опытной и стандартной проб против воды при длине волны 540 нм (зеленый светофильтр) | |
Расчет
Концентрация общего белка сыворотки, г/л =
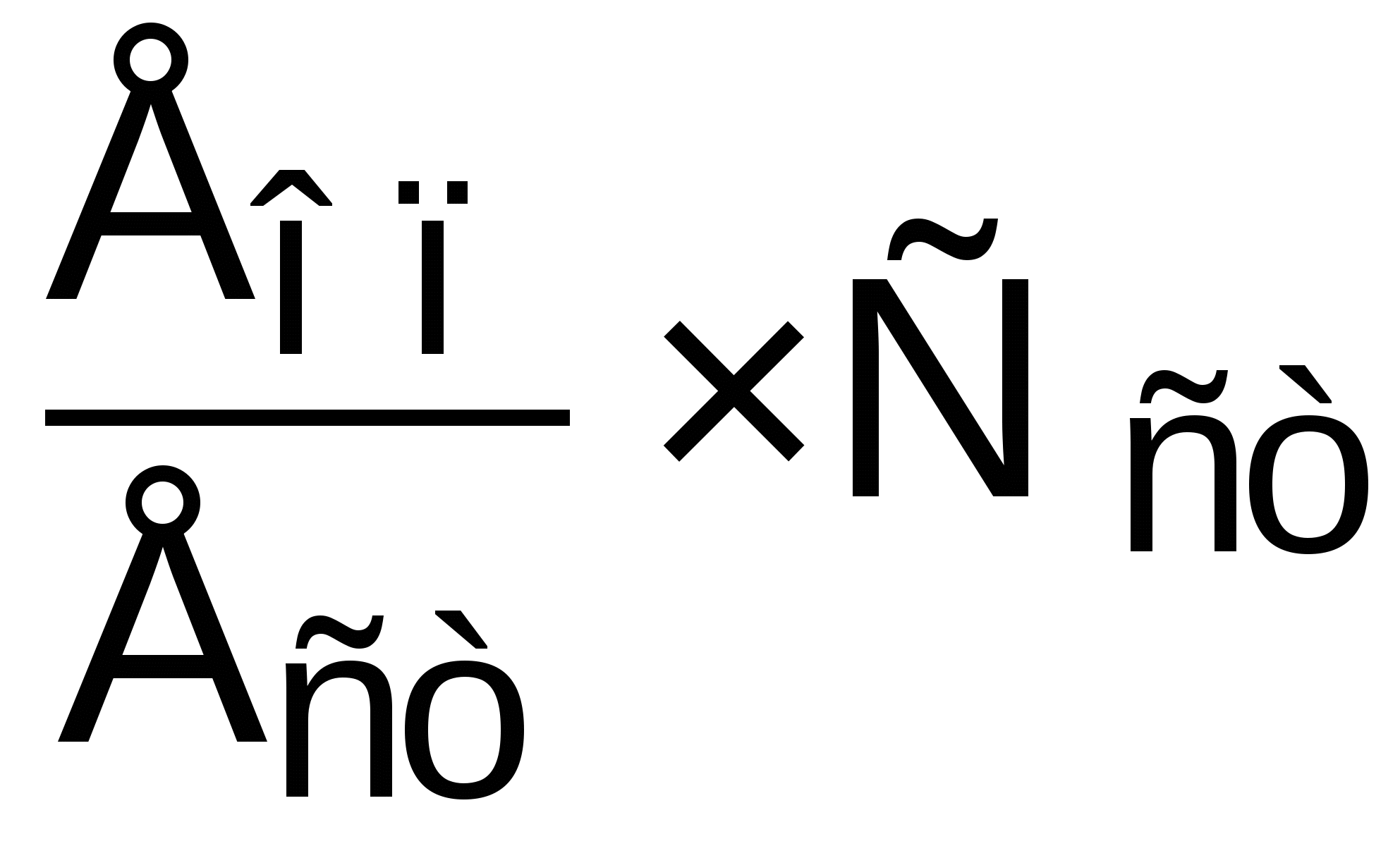 , где
, гдеЕоп и Ест – оптическая плотность опытной и стандартной пробы,
Сст – концентрация белка в стандартной пробе.
Нормальные величины
| Сыворотка крови | дети от 1 года до 3 лет | 54-85 г/л |
| | старшие дети и взрослые | 65-85 г/л |
Рефрактометрический метод
Принцип
При переходе из одной прозрачной среды (стекло) в другую (сыворотка крови) под наклоном к поверхности раздела двух фаз луч света преломляется. При этом отношение синуса угла падения к синусу угла преломления называется коэффициентом преломления (рефракции). В сыворотке крови величина рефракции зависит от количества и состава белков.
Материал исследования
Сыворотка крови.
Оборудование
Рефрактометр.
Реактивы
1. Проверяют нулевую точку прибора путем определения показателя преломления дистиллированной воды.
Для этого на чистую поверхность измерительной призмы капают 2-3 капли воды и опускают осветительную призму. Наводят окуляр на резкость. Поворотом рефрактометра к свету добиваются наилучшей освещенности шкалы и штриха. Вращением маховичка "И" границу светотени вводят в поле зрения окуляра. Вращают маховичок компенсатора "К" до исчезновения окраски границы светотеней. Наблюдая в окуляр, маховичком "И" наводят границу светотени точно на линию штриха.
Снимают отсчет по шкале. Показатель преломления дистиллированной воды равен 1,333.
2. Измерение показателя преломления сыворотки крови проводят аналогичным образом.
3. После проведения измерений поверхности призм очищают мягкой салфеткой.
Расчет
Зная показатель преломления, расчет проводят по таблице.
| Показатель преломления | Концентрация белка в сыворотке крови, г/л | Показатель преломления | Концентрация белка в сыворотке крови, г/л |
| 1,34500 1,34557 1,34575 1,34612 1,34650 1,34687 1,34724 1,34761 | 52,5 54,7 56,8 59,0 61,2 63,4 65,5 67,7 | 1,34798 1,34836 1,34870 1,34910 1,34947 1,34984 1,35021 | 69,8 72,0 74,2 76,3 78,5 80,6 82,8 |
Нормальные величины
| Сыворотка крови | дети от 1 года до 3 лет | 54-85 г/л |
| | старшие дети и взрослые | 65-85 г/л |
Клинико-диагностическое значение
Изменения концентрации общего белка в крови могут иметь как абсолютный, так и относительный характер. Изменения абсолютного характера являются следствием колебаний содержания белка в крови, в свою очередь относительные изменения зависят от объема крови, то есть наблюдаются при обезвоживании или гипергидратации.
Гиперпротеинемия
Истинное повышение концентрации белка в крови чаще всего связано с увеличением фракции глобулинов. Встречается при острых инфекциях (увеличение синтеза белков острой фазы), при хронических инфекциях (за счет глобулинемии), при миеломной болезни, лимфогрануломатозе, саркоидозе.
Относительная гиперпротеинемия вызывается потерями внутрисосудистой жидкости в результате профузных поносов (например, холере), усиленном потоотделении, неукротимой рвоте, несахарном диабете, тяжелых и обширных ожогах, генерализованных перитонитах.
Гипопротеинемия
Снижение концентрации белка в крови чаще всего связано с уменьшением фракции альбуминов крови.
Истинная (абсолютная) гипопротеинемия связана:
с недостаточным потреблением белка с пищей – заболевания желудочно-кишечного тракта, сужение пищевода при опухолях, частичное или полное голодание;
со снижением синтеза белка – несбалансированный аминокислотный состав пищи, хронические паренхиматозные гепатиты, интоксикации, злокачественные новообразования, лечение кортикостероидами;
с усиленным распадом белка – кахексия, тяжелые инфекции, длительные воспалительные процессы, лихорадочные состояния, тиреотоксикозы;
с потерей белка – нарушения проницаемости капиллярных стенок, кровоизлияния, ожоги, острые и хронические кровотечения, нефротический синдром.
Относительная гипопротеинемия связана с нарушением водного баланса – гипергидратация при гиперальдостеронизме, при почечной недостаточности со снижением экскреции солей, при использовании для питья морской воды, при неадекватных инфузиях солевых растворов.
Оформление работы
Указывают принцип метода, ход работы, нормальные величины и результаты исследования, отмечают клинико-диагностическое значение показателя и делают выводы о возможной патологии.
Лабораторная работа 3
Проведение проб на коллоидоустойчивость
белков сыворотки крови
Устойчивость белков сыворотки крови зависит от их заряда и наличия гидратной оболочки. Нарушение коллоидной устойчивости белков под влиянием различных агентов проявляется сначала склеиванием (коагуляцией) белковых молекул, а затем выпадением их в осадок. При этом в первую очередь осаждаются более крупные и менее заряженные белки – глобулины.
Осадочная проба Вельтмана в модификации Тайфля
Принцип
При добавлении к сыворотке крови раствора СаСl2 снижается коллоидная устойчивость белков вследствие уменьшения электрического заряда частиц при действии электролита. Вследствие этого при нагревании первыми выпадают в осадок -глобулины (иммуноглобулины).
Реактивы
0,5% р-р CaCl2.
Материал исследования
Сыворотка крови.
Проведение анализа
В химическую пробирку добавляют 0,1 мл сыворотки, 4,9 мл дистиллированной воды и 0,1 мл 0,5% раствора CaCl2. Встряхивают, нагревают в кипящей водяной бане или на спиртовке до однократного закипания и охлаждают.
Если хлопья в пробирке не обнаруживаются, то в нее добавляют еще 0,1 мл 0,5% раствора CaCl2 и раствор вновь нагревают до кипения. Процедуру повторяют до выпадения хлопьевидного осадка. Учитывают объем СaCl2, пошедший на образование хлопьевидного осадка сывороточных белков, и определяют состояние по коагуляционной ленте Вельтмана по схеме:
| N пробы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| CaCl2, мл | 1,0 | 0,9 | 0,8 | 0,7 | 0,6 | 0,5 | 0,4 | 0,3 | 0,2 | 0,1 |
| | Сдвиг влево. Обусловлен увеличением содержания сывороточных - и -глобулинов | | Сдвиг вправо. Обусловлен повышением содержания глобулинов | |||||||
| Клинико-диагностическое значение | Ревматизм, активный туберкулез, перитонит, нефроз, острые инфекции, опухоли, сахарный диабет | Фиброзы, гемолиз, повреждения печени (гепатит, цирроз, дистрофия), пневмония, плеврит, туберкулез, остеомиелит | ||||||||
Нормальные величины
| Сыворотка крови | 0,4-0,5 мл р-ра CaCl2 |
Тимоловая проба
Принцип
Сывороточные , глобулины и липопротеины осаждаются при рН 7,55 тимоловым реактивом вследствие образования глобулин-тимол-липидного комплекса.
Реактивы
Тимоловый буфер, рН 7,55 7,60.
Материал исследования
Сыворотка крови.
Проведение анализа
| | Опыт, мл |
| Сыворотка крови Тимоловый буфер | 0,05 3,0 |
| | Перемешивают и оставляют стоять 15 минут при комнатной температуре. Снова перемешивают и сравнивают с калибровочными пробами. Результат выражают в единицах помутнения S H (по авторам: Shank Haagland) |
Калибровочная шкала
В качестве калибровочных проб используются растворы с различной интенсивностью мутности. Перед использованием пробы необходимо тщательно перемешать.
| N пробы | Единицы помутнения, S H |
| 1 2 3 4 | 5 10 15 20 |
Нормальные величины
| Сыворотка крови | 0 4 ед.S H |
Клинико-диагностическое значение
Проба применяется для дифференциальной диагностики заболеваний печени. При поражении паренхимы печени (инфекционный и токсический гепатит) уже в преджелтушной стадии или при безжелтушной форме в 90 100% случаев тимоловая проба выше нормальных величин. У здоровых индивидов, при остальных заболеваниях печени или нарушении функции других органов тимоловая проба соответствует норме.
Как и все коагуляционные тесты, тимоловая проба является неспецифической реакцией. Вместе с тем она более приемлема для функционального исследования печени, чем другие коллоидные пробы.
Оформление работы
Указывают принцип метода, ход работы, нормальные величины и результаты исследования, отмечают клинико-диагностическое значение показателя и делают выводы о возможной патологии.
Лабораторная работа 4 (теоретически)
Электрофорез белков на бумаге и
ацетатцеллюлозных пленках
Принцип
Белковые молекулы, отрицательно заряженные при рН 6,8, перемещаются в электрическом поле постоянного тока: по направлению к аноду. Наиболее быстро перемещаются альбумины, затем по порядку 1-, 2 , - и глобулины.
На ход электрофореза влияет подвижность разделяемых веществ, находящаяся в зависимости от следующих факторов:
заряд (обычно зависит от pH), размеры и форма молекул веществ;
электрическое поле – скорость движения ионов белка прямо пропорциональна силе тока и напряжению и обратно пропорциональна сопротивлению (зависит от типа и размеров носителя и ионной силы буфера);
буферный раствор – состав, концентрация, pH и ионная сила (зависит от концентрации ионов и их заряда);
носитель – учитывается его гидрофильность, адсорбция веществ на молекулах носителя.
Материал исследования
Сыворотка крови.
Оборудование
Прибор для электрофореза, денситометр.
Проведение анализа (основные положения)
Образцы сыворотки равномерно наносят по линии старта на носитель (бумага, ацетатцеллюлозная пленка). Носитель помещают в прибор для электрофореза и подают электрический ток. Буферный раствор, двигаясь в электрическом поле, захватывает молекулы белка. Молекулы с наибольшим отрицательным зарядом и наименьшим размером, т.е. альбумины, двигаются быстрее остальных. Наиболее крупные и нейтральные ( глобулины) оказываются последними. Через некоторое время (устанавливается для каждого прибора индивидуально) электрофорез заканчивают.
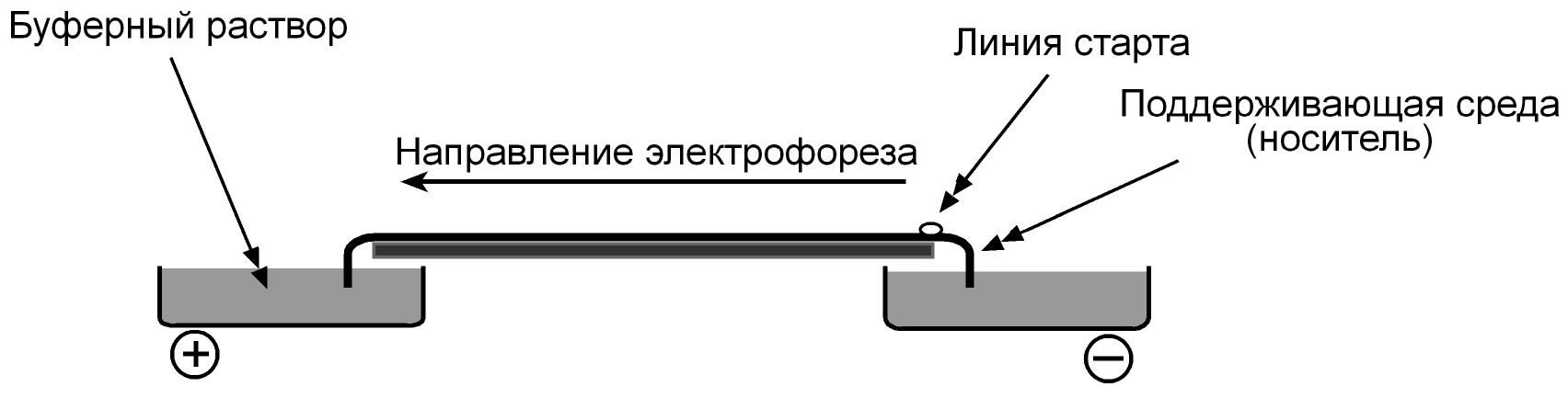 |
Полоски бумаги или ацетатцеллюлозной пленки отмывают от буферного раствора и окрашивают. В результате участки, содержащие белок, прокрашиваются, при этом площадь и интенсивность окраски зависят от содержания белковой фракции. В настоящее время количественный учет окрашенных зон на электрофореграмме проводят при помощи денситометра. Работа денситометра основана на пропускании луча света через движущуюся полоску носителя. При изменении интенсивности окраски носителя происходит "всплеск" и регистрируется наличие окрашенной зоны (белковой фракции). Параллельно современные приборы автоматически рассчитывают процентное соотношение белковых фракций.
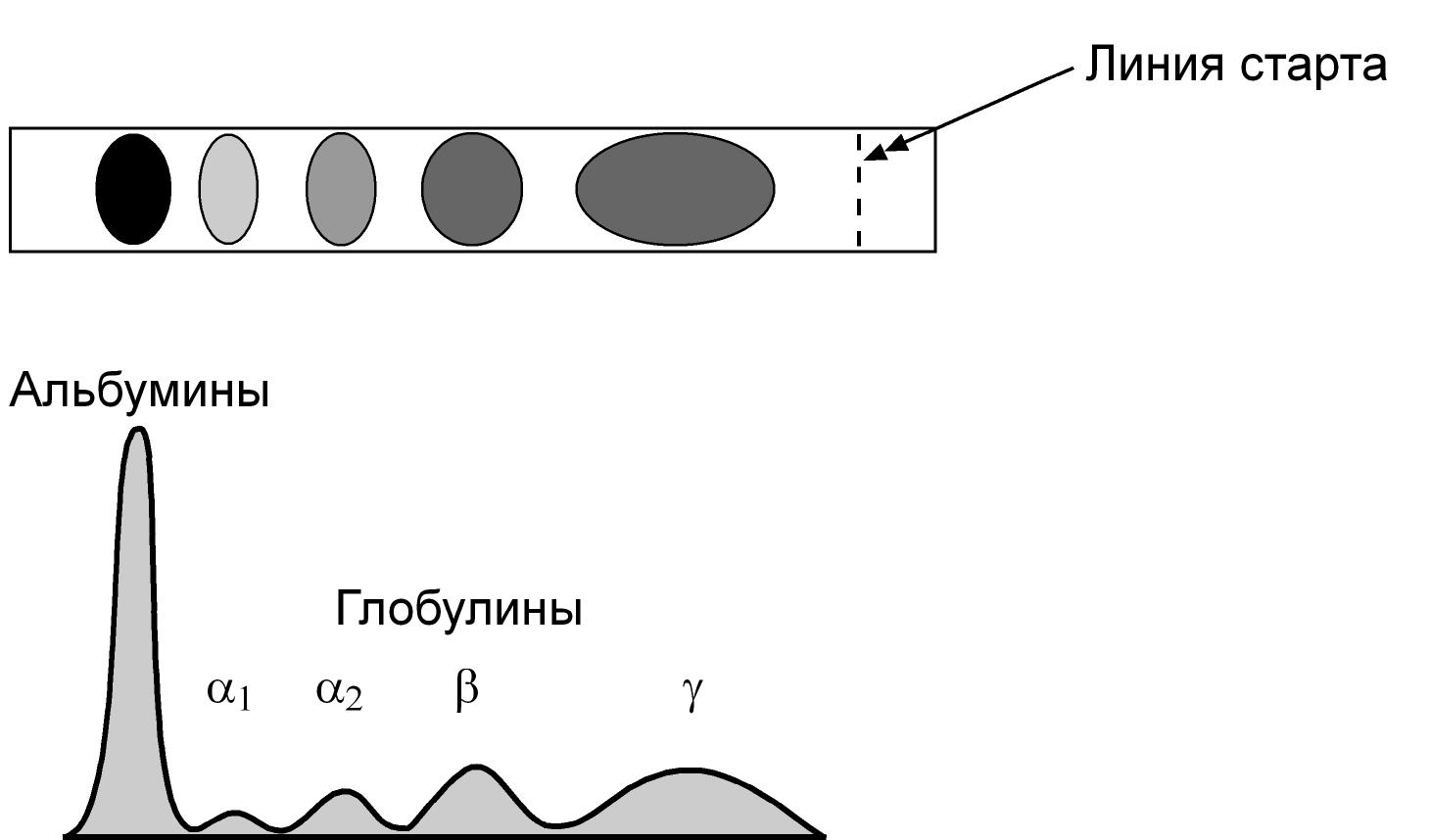
Клинико-диагностическое значение
 |
Альбумины
Снижение содержания альбуминовой фракции происходит при состояниях, характеризующихся:
пониженным синтезом альбуминов – при врожденной анальбуминемии, белковом голодании, нарушении всасывания, тяжелых поражениях печени (цирроз, дистрофии, некроз, активный гепатит, амилоидоз печени);
повышенным катаболизмом альбуминов – при лихорадке, кахексии, тяжелых инфекциях, панкреатите, коллагенозах, тиреотоксикозе, болезни Иценко-Кушинга (гипофункция надпочечников);
потерей альбумина через ожоговые поверхности, почки, желудочно-кишечный тракт;
воспалительными процессами, обусловленные выходом альбумина из кровотока в межклеточное пространство.
Концентрация альбумина <20 г/л сопровождается отеками.
-Глобулины
Повышение содержания 1- и 2-глобулиновой фракции связано с острыми и подострыми воспалительными процессами и некоторыми злокачественными опухолями, травмами, так как сюда входит большинство белков острой фазы (С реактивный белок, 2-макроглобулин, 1 гликопротеин, 1 антитрипсин, церулоплазмин, гаптоглобин).
-Глобулины
Большая доля белков -глобулиновой фракции является липопротеинами (ЛПОНП и ЛПНП), поэтому повышение этой фракции чаще всего связано с гиперлипопротеинемиями. Кроме того, влияние на динамику этой фракции оказывают трансферрин, гемопексин, компоненты системы комплемента.
-Глобулины
Содержание -глобулинов увеличивается при патологических состояниях, связанных с хроническими воспалительными процессами, так как класс содержит иммуноглобулины G, A и M.
