Лаб. практикум. Практикум по биологической химии методические указания к проведению лабораторных работ по биологической химии для студентов второго курса
 Скачать 1.02 Mb. Скачать 1.02 Mb.
|
Лабораторная работа №5Выделение муцина из слюны и открытие в нем углеводного компонентаМуцин – сложный белок – гликопротеин, обнаруживается в секретах слизистых желез. Гликопротеиды содержаться почти во всех тканях и жидкостях организма и носят общее название муцинов и мукоидов. Муцины встречаются в секретах слизистых желез. Мукоиды входят в состав различных тканей: костной (оссеомукоид), хрящевой (хондромукоид), соединительной (тендомукоид), а также яичного белка (овомукоид). В состав небелкового фрагмента гликопротеинов входят разнообразные моносахариды и их производные (глюкоза, галактоза, манноза, фруктоза, глюкозоамин, N-ацетилглюкозамин, галактозамин, нейраминовая кислота, глюкуроновая кислота), а также гетерополисахариды (гиалуроновая кислота, гепарин, хондроитинсульфат). Для качественного и количественного анализа используются углеводные компоненты, например глюкозоамин, галактозоамин. Гликопротеиды играют важную роль в организме, неся опорную и защитную функции. Качественные реакции на простетические группы гликопротеинов используются для выявления и количественного определения их в различном биологическом материале и лекарственных средствах (стекловидное тело, гонадотропины и др.). В клинической практике наиболее распространено суммарное определение гликопротеинов и мукопротеинов сыворотки крови по одному из входящих в них компонентов: гексозаминов, фукозе, сиаловым кислотам. Принцип метода. Из гексоз, входящих в состав гликопротеинов, в присутствии концентрированной серной кислоты образуется гидроксиметилфурфурол, который с α-нафтолом дает продукт конденсации красно-фиолетового цвета. 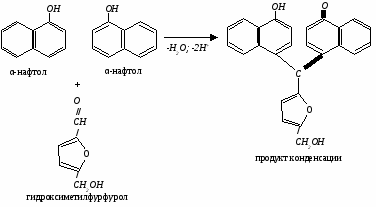 Исследуемый материал и реактивы 1. Слюна. 2. Уксусная кислота ледяная. 3. Спиртовой раствор α–нафтола (1%). 4. Серная кислота концентрированная. Ход работы В пробирку собирают 1-2 мл слюны и по каплям (10-20 капель) приливают концентрированную уксусную кислоту, помешивая содержимое пробирки стеклянной палочкой. Выпадает осадок муцина. Осторожно сливают жидкость из пробирки, а сгусток слегка высушивают фильтровальной бумагой. К муцину прибавляют 10-20 капель 1% спиртового раствора α–нафтола и по стенке пробирки, наклонив ее, осторожно наслаивают 20 капель концентрированной серной кислоты. При стоянии образуется красно-фиолетовое кольцо. Указания к оформлению лабораторной работы В тетради для лабораторных работ запишите ход работы, принцип метода, химизм реакции и сделайте выводы о природе простетической группы сложного белка муцина. Контрольные вопросы
биохимия ФЕРМЕНТовФерменты – биологические катализаторы белковой природы. Синтезируются в клетках организма. Каталитические свойства ферментов связаны с их способностью специфически активировать химические реакции. Работа, которую выполняют ферменты в качестве биологических катализаторов, необычайно эффективна. В некоторых случаях реакции под действием ферментов протекают более чем в миллион раз быстрее нежели в их отсутствие. Высокая каталитическая активность ферментов связана с тем, что они временно соединяются с субстратами, образуя фермент-субстратные комплексы. Ферменты могут быть как простыми (состоят только из аминокислот), так и сложными, т.е. в своем составе имеют небелковый компонент – кофермент. Коферментами могут быть ионы металлов, нуклеотиды, производные нуклеотидов и др. Лабораторная работа №6Количественное определение активности амилазы (по Вольгемуту)Для знакомства со свойствами ферментов используют в качестве объектов α-амилазу слюны. Она катализирует гидролиз крахмала и гликогена и является эндополиглюкозидазой, разрушающей α-1,4-гликозидные связи в молекуле этих полисахаридов. Фермент амилаза осуществляет гидролиз крахмала через промежуточные соединения (декстрины) до мальтозы Источником амилазы может быть слюна, содержащая α-амилазу. Гидролиз крахмала α-амилазой происходит через ряд стадий. Нерасщепленный крахмал с йодом дает синее окрашивание, декстрины в зависимости от размера их молекулы: амилодекстрины – фиолетовое; эритродекстрины – красное; арходекстрины и мальтоза – бесцветное (желтое окрашивание раствора связано с окраской самого раствора йода). Этим методом определяют активность амилазы в слюне, в сыворотке крови, в моче. Принцип метода. Метод заключается в том, что слюну разводят в определенной последовательности, после чего приливают одно и тоже количество раствора крахмала, находят наименьшее содержание фермента, которое полностью расщепляет все количество крахмала, затем производят пересчет на 1 мл слюны. Амилазная активность слюны выражается в количестве 0,1% раствора крахмала, которое гидролизуется 1 мл неразбавленной слюны при t = 38°C в течение 30 мин. В норме амилазная активность слюны Исследуемый материал и реактивы 1. Слюна в разведении 1:20. 2. Раствор крахмала (0,1%). 3. Раствор 0,1% йода в 0,2% йодистом калии. Ход работы Приготовить разведение слюны в 20 раз. Для этого в мерный цилиндр собирают 1 мл слюны (предварительно полость рта споласкивается водой) и доводят водой до метки 20 мл. Одновременно готовят ряд растворов с возрастающим разведением слюны. Для этой цели берут 11 пробирок, в которые за исключением пробирки №1 наливают по 1 мл дистиллированной воды. В пробирки №1 и №2 разливают по 1 мл слюны. После перемешивания жидкости из пробирки №2 отбирают 1 мл и вносят его в пробирку №3. Повторяют ту же операцию с жидкостью в пробирке №3 и т.д. В результате получают ряд с возрастающим разведением слюны. Затем в каждую из пробирок наливают по 2 мл 0,1%раствора крахмала и все содержимое пробирки перемешивают, ставят на 30 мин в водяную баню при температуре 38°С. После этого добавляют по несколько капель реактива Люголя (раствор J2 в KJ) в каждую пробирку и перемешивают. Жидкость в пробирках окрашивается в желтоватый, розовый и фиолетовый цвет. В розовый – благодаря наличию декстринов, а в фиолетовый – благодаря присутствию нерасщепившегося крахмала. Рассчитывают количество слюны в последней пробирке с желтоватой окраской. Если слюна в ней, например, была разведена в 320 раз, составляют следующую пропорцию и находят амилокластическую силу слюны: 1/320 мл слюны расщепила 2 мл 0,1% раствора крахмала 1 мл слюны расщепил Х мл 0,1 % раствора крахмала 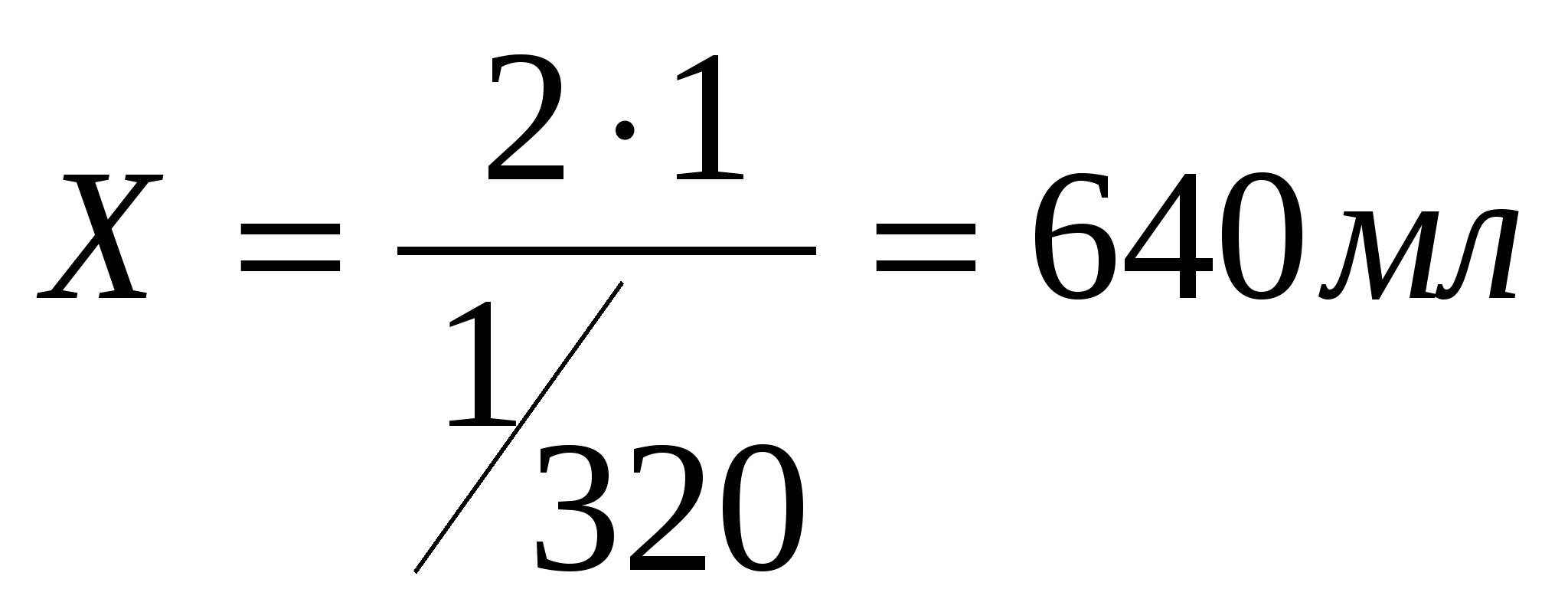 0,1% раствора крахмала. 0,1% раствора крахмала.Указания к оформлению лабораторной работы В тетради для лабораторных работ запишите ход работы, принцип метода, составьте таблицу для записи реакций окрашивания содержимого всех пробирок с йодом и рассчитайте амилокластическую силу слюны исследуемого.
Контрольные вопросы
|
