Лаб. практикум. Практикум по биологической химии методические указания к проведению лабораторных работ по биологической химии для студентов второго курса
 Скачать 1.02 Mb. Скачать 1.02 Mb.
|
Метод сахарной нагрузкиУглубленное изучение углеводного обмена производится методом сахарной нагрузки, при котором определение глюкозы в крови проводят через определенные промежутки времени. Эти данные являются более ценными, чем однократное определение содержания глюкозы в крови. Они позволяют выявить скрытые формы диабета и нарушение гликогенобразовательной функции печени. Показания для проведения теста на толерантность к глюкозе: ▪ Неоднозначные результаты однократных анализов крови натощак. ▪ Глюкозурия: панкреатическая и внепанкреатическая (первая связана с недостатком секреции или недостаточностью самого инсулина; внепанкреатическая глюкозурия развивается при поражении других органов внутренней секреции, ЦНС, при эмоциональном стрессе, заболеваниях почек, печени, избытке углеводов в диете, при беременности). ▪ Клинические признаки сахарного диабета или его осложнений при нормальной концентрации глюкозы крови натощак (скрытые формы диабета). Исследуемый материал и реактивы 1. Кровь. 2. Стандартный раствор глюкозы. 3. Раствор хлорида натрия (0,9%). 4. Раствор сернокислого цинка (5%). 5. Раствор едкого натра (0,3н). 6. Рабочий раствор фермента (глюкозооксидаза). 7. Дистиллированная вода. 8. Глюкоза (кристаллическая). 9. Кипяченая вода. 10. Скарификаторы. 11. Спирт. 12. Вата. Ход работы Утром натощак у пациента берут кровь из пальца и определяют в ней содержание глюкозы. После этого пациенту дают выпить 50 или 100г глюкозы в 200 мл теплой кипяченой воды (из расчета 1 г глюкозы на 1кг массы тела) в течение не более 5 мин. Глюкозу можно заменить сахарозой (из расчета 1,5г сахарозы на 1кг массы тела). Затем повторно исследуют содержание глюкозы в крови каждые 30 мин (иногда через 15 мин) в течение 2,5 ч (если было принято 50г глюкозы), в течение 3 ч (если было принято 100г глюкозы). У детей сахарную нагрузку проводят так же как у взрослых, изменяя только дозы вводимой глюкозы. На основании полученных данных строят график, откладывая на оси ординат содержание глюкозы в крови (в г/л), а на оси абсцисс – время взятия пробы (в мин или ч.). 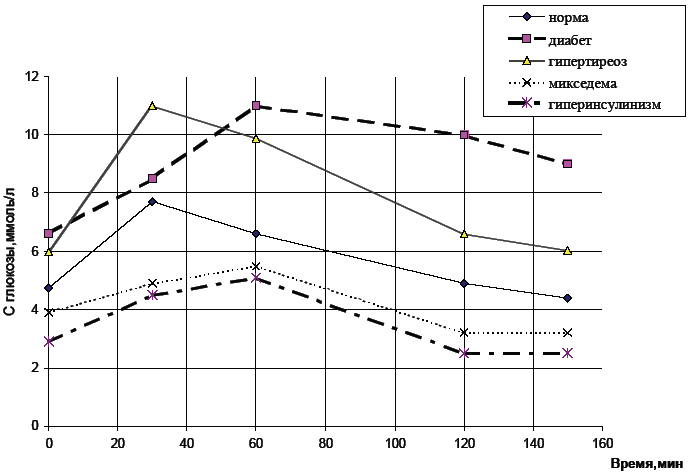 Анализ гликемических кривых У здорового человека уже через 15 мин после приема глюкозы наблюдается увеличение ее содержания в крови, которое между 30-й и 60-й минутами достигает максимального значения. Затем начинается снижение и к 120-й минуте содержание глюкоз достигает исходного уровня, отмечавшегося натощак, или с небольшими отклонениями в сторону как повышения, и так и снижения. Через 3 часа содержание глюкозы в крови достигает исходной цифры. Гликемические кривые отличаются от нормы (рис.1) при сахарном диабете (чрезвычайно высокая вершина сахарной кривой; повышенный уровень глюкозы остается через 3ч), аддисоновой болезни (низкие гипогликемические кривые до и после нагрузки, небольшой пик), поражении паренхимы печени, гипофункции щитовидной железы, тяжелых анемиях, заболеваниях центральной нервной системы, инфекционных болезнях токсических состояниях. Kлинико-диагностическое значение оценки гликемических кривых У больных с разными формами диабета нарастание гликемической кривой происходит медленнее, достигая через 60–150 мин. значительной величины (более чем в 1,8 раза превышая исходное значение), в большинстве случаев отмечается глюкозурия. Чем тяжелее заболевание, тем позже достигается максимум гликемии и тем он выше. Понижение кривой происходит очень медленно, чаще оно растягивается на 3–4 ч. Заболеваниям щитовидной железы, связанным с ее гиперфункцией, свойственны гликемические кривые с более быстрым, чем в норме, подъемом, что, возможно, вызвано более интенсивным обменом веществ и возбуждением симпатического отдела вегетативной нервной системы. Для больных с аденомой островков Лангерганса, гипотиреозом (микседемой), болезнью Аддисона характерен низкий исходным уровень кривой, низкая ее вершина и высокий постгликемический коэффициент. При некоторых тяжелых заболеваниях (энцефалит и др.) глюкоза может появляться в моче в результате ренальной глюкозурии. Количественное определение кислотности желудочного сокаЖелудочный сок является секретом желез слизистой оболочки желудка, представляет собой бесцветную жидкость с сильнокислой реакцией (рН=1,5-2,5), объемом 1,5-2 л в сутки. Желудочный сок сложен по составу – состоит из различных органических и неорганических веществ, среди которых особое место занимают соляная кислота и белки-ферменты, а также вода (до 99,2%). Переваривание белков во многом зависит от кислотности желудочного сока. Определение кислотности желудочного сока и наличие молочной кислоты в нем имеет важное диагностическое значение для определения желудочно-кишечных заболеваний. При патологии кислотность желудочного сока может быть нулевой, пониженной или повышенной. Отсутствие соляной кислоты и пепсина (ахилия) часто наблюдается при злокачественных новообразованиях желудка. Пониженная кислотность (гипохлоргидрия) встречается при гипоацидном гастрите, иногда при язвенной болезни желудка. Повышенная кислотность (гиперхлоргидрия) имеет место при гиперацидном гастрите и часто сопровождается язвенной болезнью желудка и двенадцатиперстной кишки. При определении кислотности различают общую кислотность (сумма всех кислореагирующих веществ), общую соляную кислоту: свободную и связанную. Принцип метода. Метод основан на определении кислотных веществ желудочного сока путем титрования их раствором гидроксида натрия с использованием двух различных индикаторов: n-диметиаминоазобензола (зона перехода окраски при рН=2,3-4,2) и фенолфталеина (зона перехода окраски рН=8,2-10,0). По изменению окраски (от красной к оранжевой) индикатора n-диметиаминоазобензола определяется свободная соляная кислота, а по переходу окраски фенолфталеина (от бесцветной к розовой) – общая кислотность желудочного сока. В норме общая кислотность для взрослого человека составляет 40 – 60 ммоль/л, у новорожденных – 2,8 ммоль/л, у детей от 1 месяца до 1 года – 4 – 20 ммоль/л. Содержание свободной соляной кислоты в норме составляет 20 – 40 ммоль/л (у новорожденных – 0,5 ммоль/л). Определение общей кислотности, общей соляной кислоты, свободной соляной кислоты и связанной соляной кислоты проводится в одной порции желудочного сока. Исследуемый материал и реактивы 1. Желудочный сок. 2. Раствор диметиламиноазобензола. 3. Фенолфталеин. 4. Раствор гидроксида натрия (0,1н). Ход работы Отмеривают пипеткой в колбочку 10 мл желудочного сока, добавляют 1 каплю диметиламиноазобензола и 2 капли фенолфталеина. При наличии в желудочном соке свободной соляной кислоты он окрашивается в красный цвет с розовым оттенком, при ее отсутствии сразу появляется оранжевая окраска. Титруют свободную соляную кислоту 0,1н NaOH из микробюретки до появления оранжевого окрашивания и результат записывают (1-ая отметка). Не добавляя щелочи в бюретку, продолжают титрование до появления лимонно-желтого цвета и результат записывают (2-ая отметка от 0). Продолжают титрование до появления розового окрашивания (3-я отметка от 0). 1-ая отметка соответствует количеству свободной соляной кислоты (см. расчет), 2-я – используется для определения связанной соляной кислоты, а последняя отметка соответствует общей кислотности. Расчет. Если на титрование 10 мл желудочного сока израсходовано 3,0 мл 0,1н раствора NaOH, то количество свободной соляной кислоты равно: Х = 3,0*1000 * 0,1 / 10 = 30 ммоль/л. где 3,0 – количество 0,1н раствора NaOH, мл; 10 – количество желудочного сока, взятого для титрования, мл; 0,1 – количество мг–экв. щелочи в 1 мл 0,1н раствора, ммоль; 1000 – пересчет на 1литр. Экспресс-методы обнаружения патологических компонентов мочи с помощью комбинированных тест-полосокКомбинированными тест-полосками можно определить в моче пять важных показателей: рН, белок, глюкозу, кетоновые тела и кровь. Экспресс-методы – это лабораторные методы диагностики, применяемые врачом у постели больного без лабораторного оборудования. Эти методы - простые и быстрые, но не достаточно прочные. Наиболее часто применяются экспресс-методы определения сахара и кетоновых тел в моче, что бывает необходимым для диагностики сахарного диабета, особенно при бессознательном состоянии больных. Xод работы Берут нецентрифугированную мочу, хорошо перемешанную. Тест полоску всю опускают в сосуд с мочой на 1с. Избыток мочи снимают с полоски путем соприкосновения ее со стенкой сосуда. Через 30-60 с. окраску сравнивают со стандартной шкалой. Изменение окраски, которое наступило только на краях индикаторной зоны или только через две мин., не имеет диагностического значения. Моча не должна перед исследованием стоять больше 4 ч при комнатной температуре. Белок. При наличии белка наблюдается изменение цвета тест-полоски от желтого к зеленому (0,3; 1,0, 5,0 г/л) ; патологическая протеинурия при содержании белка более 0,25 г/л. Глюкоза. Положительная реакция от оранжевого до коричневого цвета отмечается через 60с (5,55; 16,65; 55,55 ммоль/л). Окраска появляется даже при небольшой концентрации глюкозы (2,2 ммоль/л). Кетоновые тела. Положительная реакция от розового до фиолетового цвета (+, ++, +++). Чувствительность тест-полоски на ацетоуксусную кислоту выше, чем на ацетон; на бета-гидроксимасляную кислоту тест-полоска не реагирует. Граница обнаружения: 100 мг/л для ацетоуксусной кислоты и от 400 мг/л для ацетона Кровь. Для эритроцитов и гемоглобина дается отдельная шкала. Интактные эритроциты видны в виде отдельных сидящих зеленых точек на желтом фоне (5-10, 50, 250 эрит/мкл). Равномерная зеленая окраска обозначает свободный гемоглобин или гемолизированные эритроциты или миоглобин (50, 250 эрит/мкл). При малых примесях крови в моче или при более длительном смачивании полосок реакция может наступить уже через 1-2 мин. Источники ошибок. Ошибочные результаты получаются после приема больших количеств витамина С и некоторых медикаментов. СПИСОК ЛИТЕРАТУРЫ
|
