Программа блока гетерофункциональные углеводороды
 Скачать 6.9 Mb. Скачать 6.9 Mb.
|
|
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ. Углеводы. Моносахариды. Определение, общая формула. Классификация. Номенклатура, изомерия. Структурные и проекционные формулы, антиподы, диастереомеры. D- и L-ряды. Формулы Хеуорса. Методы получения моносахаридов. Гидролиз. Окисление. Оксинитрильный синтез. Физические и химические свойства. Окисление. Избирательное окисление. Восстановление альдоз и кетоз в многоатомные спирты. Взаимодействие с фенилгидразином. Действие щелочей. Реакции циклических форм. Свойства полуацетального гидроксила. Получение и гидролиз гликозидов. Исчерпывающее алкилирование и ацилирование. Действие кислот на пентозы. Деструкция моносахаридов. Понятие о брожении гексоз. Дисахариды. Общие формулы. Типы дисахаридов. Проекционные и перспективные формулы. Отличие химических свойств восстанавли-вающих и невосстанавливающих дисахаридов. Распространение в природе и биологическое значение дисахаридов. Полисахариды. Природные полимеры. Крахмал, образование в растениях, строение. Амилоза и амилопектин, строение цепей. Гидролиз крахмала. Гликоген и инулин. Целлюлоза. Содержание целлюлозы и лигнина в древесине. Природные источники целлюлозы, отличие от крахмала. Гидролиз целлюлозы. Гидролизный спирт. Применение целлюлозы и ее производных. Искусственные волокна. Понятие о гемицеллюлозах, пектиновых веществах. Хитин. Аминокислоты. Изомерия, номенклатура. Синтез аминокислот. Получение аминокислот из природных веществ. Аминирование. Получение из альдегидов и кетонов. Алкилированние. Присоединение. Способ В.М. Родионова. Получение α-, β-, γ-, ω- аминокислот. Химические свойства аминокислот. Амфотерность и образование биполярных ионов. Соли с кислотами и основаниями. Комплексные соли с ионами меди (II). Реакции по карбоксильной группе. Реакции по аминогруппе. Реакции с одновременным участием карбоксильной и аминогруппы: понятие о полипептидах. Действие окислителей. Основные представители: п-аминобензойная, о-амино-бензойная, аминоуксусная, α-аминокапроновая кислоты. Полиамидные полимеры: капрон, энант. Оксикислоты. Номенклатура и изомерия. Методы получения. Гидролиз. Оксинитрильный синтез. Гидратация непредельных кислот. Реакция Реформатского. Окисление. Физические и химические свойства энантиомеров, рацематов и диастериомеров. Химические свойства. Реакции карбоксильной группы. Реакции гидроксильной группы. Образование рацематов при синтезе соединений с асимметрическим центром. Стереохимия реакций замещения. Нуклеофильное замещение. Стереохимия реакций присоединения. Совместные реакции гидроксильной и карбоксильной групп. Основные представители и применение оксикислот: лимонная, салициловая, галловая кислоты. Гетероциклические соединения. Классификация и номенклатура гетероциклических соединений. Пятичленные гетероциклы с одним гетероатомом. Строение пятичленных гетероциклов; взаимное превращение гетероциклов. Фуран. Тетрагидрофуран. Фурфурол, его применение. Тиофен и пиррол. Пирролидин. Имидазол; биологическое значение производных имидазола; гистидин и гистамин. Тетрапирролы. Строение гемоглобина и его функция в организме; хлорофилл, его физиологическая функция. Индол. Строение. Гетероауксин; ростовые вещества. Триптофан, триптамин, их биологическое значение. Пятичленные гетероциклы с несколькими гетероатомами. Оксазол, пиразол, имидазол. Биологическое и медицинское значение производных тиазола, имидазола. Шестичленные гетероциклы с одним гетероатомом. Пиридин. Строение, получение пиридиновых оснований из каменноугольной смолы. Реакции солеобразования. Реакции гидрирования пиридина; пиперидин. Производные пиридина и пиперидина, их биологическая активность. Никотиновая кислота и ее амид (витамин РР). Хинолин. Обозначения атомов в ядре. Основные свойства. Применение. Шестичленные гетероциклы с несколькими гетероатомами. Пиримидин, его строение. Диазины, пиримидин. Пиримидиновые основания: урацил (2,6-диоксипиримидин), тимин (5-метил-2,6-диоксипиримидин), цитозин (6-амино-2-оксипимиридин). Таутомерные формы пиридиновых оснований. Пурин. Ароматическая система пурина. Пуриновые основания – продукты гидролиза нуклеиновых кислот: аденин (6-аминопурин), гуанин (2-аминопурин). Таутомерные формы мочевой кислоты. Понятие об алкалоидах. Кофеин, теобромин. Шестичленные гетероциклы с атомом кислорода. Производные γ-пирана, хлором, флавон и родственные вещества. Шестичленные гетероциклы с двумя разными гетероатомами. КОНСПЕКТ ЛЕКЦИЙ ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
Углеводы являются важным классом природных органических соединений. Значение углеводов определяется той доминирующей ролью, которая отводится им в живых организмах, и сложностью выполняемых ими функций. Углеводы входят в состав клеток и тканей всех растительных и животных организмов и по массе составляют основную часть органического вещества на Земле (до 80 % сухого вещества растений и около 2 % сухого вещества животных организмов составляют углеводы). В живой природе они имеют большое значение как источники энергии в метаболических процессах (в растениях – крахмал, в животных организмах – гликоген); структурные компоненты клеточных стенок растений (целлюлоза); выполняют роль субстратов и регуляторов специфических биохимических процессов, являются составными элементами жизненно важных веществ: нуклеиновых кислот, коферментов, витаминов и др. Углеводы служат основным компонентом пищи млекопитающих, а человека обеспечивают пищей, одеждой и жилищем. Только растения способны осуществлять полный синтез углеводов путем фотосинтеза, в процессе которого вода и углекислый газ превращаются в углеводы под действием солнечного света как источника энергии. Животные организмы не способны синтезировать углеводы и получают их из растительных источников: солнечная энергия В результате фотосинтеза накапливается огромное количество гомополисахаридов – целлюлозы и крахмала. Некоторые растения накапливают углеводы в виде уникального дисахарида – сахарозы, который выделяют в настоящее время в значительных количествах (8,2×107 т/год). В отличии от невозобновляемых запасов органических веществ (нефть, газ, каменный уголь) запасы углеводов восполняются в живой природе ежегодно. Классификация углеводов. Углеводами (или сахарами) называют группу природных веществ, которые в соответствии с химической классификацией являются полигидроксиальдегидами или полигидроксикетонами либо продуктами их поликонденсации. Впервые термин «углеводы» был предложен профессором Дерптского (Тартуского) университета К. Шмидтом в 1884 г., в связи с тем, что первые из известных их представителей имели состав Сn(Н2О)m, т. е. их рассматривали как соединения углевода с водой. В настоящее время известно множество углеводов, по составу не соответствующих этой формуле. Однако термин «углеводы» сохранился, хотя не отражает ни состава, ни химической природы этого класса соединений. Втрое название углеводов – (сахара) связано с тем, что многие представители этого класса соединений обладают сладким вкусом, обычный сахар С12Н22О11 входит в их состав. Углеводы подразделяются на три основные группы:
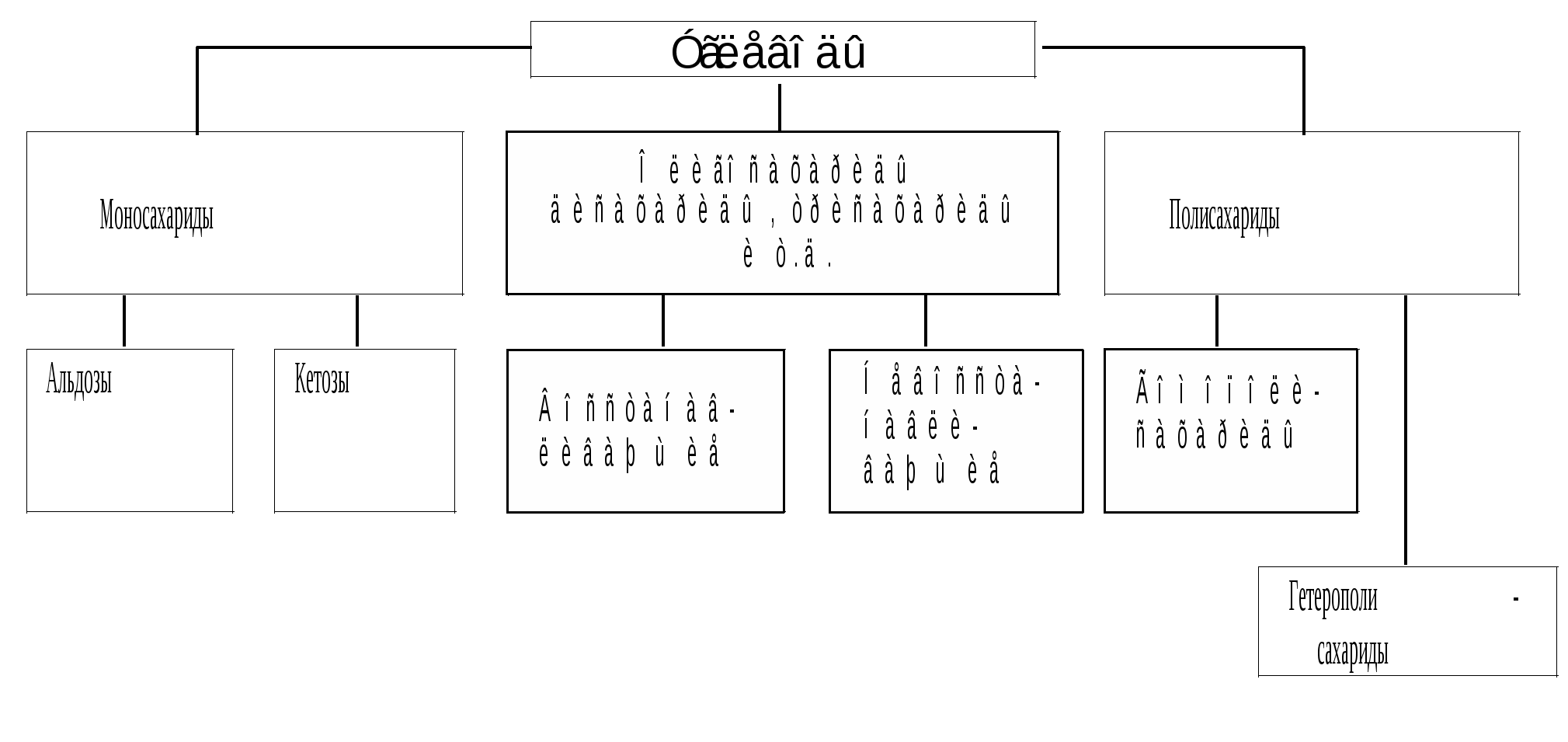 Рисунок 1 – Схема разделения углеводов на группы Рисунок 1 – Схема разделения углеводов на группыМоносахариды (простые сахара) – углеводы, которые не способны гидролизоваться до более простых соединений. Олигосахариды (низкомолекулярные сахара) – углеводы, которые при гидролизе распадаются на 2–8 моносахарида (“oligos” (гр.) – немногий). Полисахариды (сложные сахара) – продукты конденсации моносахаридов. Они способны гидролизоваться с образованием простых углеводов (от десятков до сотен тысяч молекул моносахаридов). По химической природе простые сахара делят на:
Моносахариды, относящиеся к нейтральным сахарам, в большинстве своем имеют состав, соответствующий общей формуле СnН2nОn, т. е. число атомов углерода равно числу атомов кислорода. Однако известны такие моносахариды, у которых число атомов кислорода меньше (например, СnН2nОn-1), чем число атомов углерода в молекуле, т. е. вместо гидроксильной группы в молекуле моносахарида присутствует атом водорода. Такие сахара называют дезоксисахарами. 1.1 МОНОУГЛЕВОДЫ Классификация. Моносахариды (монозы) классифицируют по количеству атомов углерода и по характеру карбонильной группы. По количеству атомов углерода:
Сахара, содержащие семь и более атомов углерода, называют высшими сахарами. По характеру карбонильной группы:
Часто эти названия объединяют, чтобы одновременно показать и число углеродных атомов, и характер карбонильной группы. Например: глюкоза является альдогексозой, а фруктоза – кетогексозой, простейшей альдотриозой является глицериновый альдегид, а простейшей кетотриозой – дигидроксиацетон:  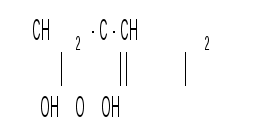 глицериновый альдегид дигидроксиацетон Номенклатура моносахаридов и их производных. Названия моносахаридов строят в соответствии с их классификацией с окончанием “оза” : альдопентоза, кетогексоза и т. д. Наиболее часто встречающиеся в природе моносахариды имеют тривиальные названия, например, альдопентозы – рибоза, ксилоза, арабиноза, дезоксирибоза, ликсоза; альдогексозы - глюкоза, манноза, галактоза, гулоза, иодоза; кетогексоза – фруктоза. По систематической номенклатуре любая альдопентоза имеет название 2,3,4,5-тетрогидроксипентаналь; альдогексоза – 2,3,4,5,6-пентагидрокси-гексаналь; кетопентоза – 1,3,4,5-тетрагидроксипентанон-2; кетогексоза (фруктоза) – 1,3,4,5,6-пентагидроксигексанон-2 и т. д. Однако, заместительная номенклатура в химии углеводов практически не используется и обычно пользуются тривиальными названиями. 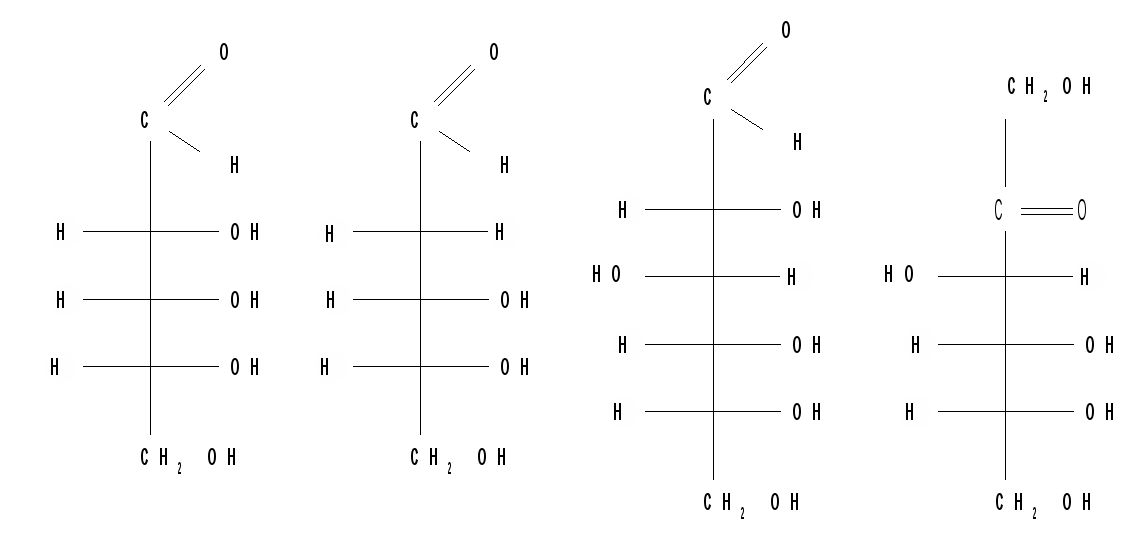
От тривиальных названий производят названия дезоксисахаров, аминосахаров, карбоксилсодержащих сахаров. При образовании названий производных сахаров атомы углерода нумеруют, начиная с того конца, к которому ближе карбонильная группа; цифрами указывают положения заместителей; если заместитель связан не с углеродным атомом, то указывают атом, с которым заместитель связан непосредственно. Например: 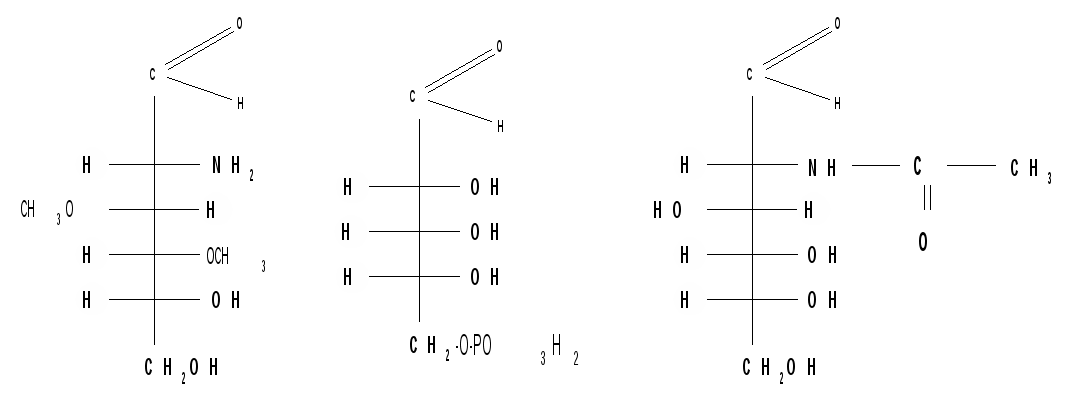
При окислении альдоз в мягких условиях, например, при действии [Аg(NH3)2OH], образуются кислоты, содержащие карбоксильную группу в первом положении. Их называют альдоновые (гликоновые) кислоты. Окончание «оза» в названии монозы меняют на «оновая кислота». Окисление концевой первичноспиртовой – СН2ОН-группы переводит альдозы в уроновые кислоты. Их названия образуют, заменяя окончание «оза» на «уроновая кислота», при нумерации отсчет ведут от альдегидной, а не от карбоксильной группы. Кислоты, образующиеся при энергичном окислении альдоз и содержащие две карбоксильные группы в первом и последнем положениях углеродной цепи, называют альдаровыми (окончание «оза» заменяют на «аровая кислота»). 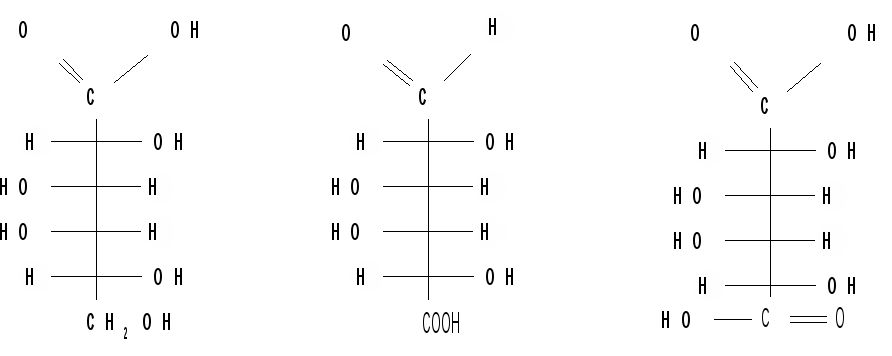
|
