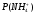Роберт Вильгельм Бунзен
 Скачать 2.24 Mb. Скачать 2.24 Mb.
|
|
Опыт №2. Зависимость от температуры В три пробирки наливают по 5мл 0,1М Na2S2O3, а в три другие. Помещают все пробирки в стакан с водой и через 5 – 7 мин., измерив температуру воды в стакане, сливают вместе содержимое одной пары пробирок с H2SO4 и Na2S2O3 , и отсчитывают время до начала помутнения. Переливают в стакан немного горячей воды так, чтобы температура воды в стакане увеличилась примерно на 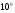 . Слив содержимое второй пары пробирок с H2SO4 и Na2S2O3 , определяют также время до начала появления мути. Опыт с последней парой пробирок проводят при температуре приблизительно на . Слив содержимое второй пары пробирок с H2SO4 и Na2S2O3 , определяют также время до начала появления мути. Опыт с последней парой пробирок проводят при температуре приблизительно на 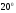 выше первоначальной. выше первоначальной.Результаты записывают в таблицу по форме:
Строят график зависимости логарифма скорости реакции обратной величины абсолютной температуры. Из графика определяют тангенс угла наклона и вычисляют энергию активации: Е=-2,3 tg α Опыт №3. Зависимость от концентрации катализатора. В три пробирки наливают по 2 мл 0,1М Na2S2O3 и добавляют по 1, 2, 3мл 0,05М CuSO4 . Кроме того, в первые две пробирки добавляют 2 и 1 мл воды, чтобы общий объем раствора во всех пробирках составлял 5 мл. В другие три пробирки наливают по 5 мл 1М Na2S2O3. Смешивают попарно растворы тиосульфата натрия и серной кислоты и определяют время до помутнения растворов. Результаты опытов записывают в таблицу по форме:
Строят график зависимости скорости реакции от концентрации ионов катализатора. Работа №2.Исследование скорости гидролиза мочевины. Цель работы. Получить экспериментальную зависимость скорости гидролиза мочевины от времени в присутствии фермента уреазы и научиться определять скорость реакции по графику. Водная суспензия соевой муки или арбузных семечек содержит фермент уреазу. Уреаза катализирует гидролиз мочевины по схеме: H2N-CO-NH2 + H2O 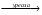 2NH3 + CO2 2NH3 + CO2 Скорость данной химической реакции можно определить по образованию выделяющегося аммиака. Определение аммиака можно осуществлять различными методами: титрометрическим, электрометрическим, колориметрическим. а) Титрометрический метод. В коническую колбу наливают 30 мл мочевины (0,1М) и устанавливают заданную температуру с помощью водяной бани.После установления необходимой температуры по термометру, помещенному в колбу, добавляют 10 капель суспензии, содержащей уреазу, и отмечают время. Через 5 мин. Из колбы обтирают 5 мл. смеси, добавляют 2 – 3 капли фенолфталеина, быстро титруют раствором 0,01HCl до обесцвечивания. Затем через 5 мин. Отбирают следующую пробу и т. д. Результаты заносят в таблицу.
Количество выделившегося аммиака рассчитывают по формуле: P(NH3) = C(1/z HCl) V(HCL) 1000 По полученным данным строится график зависимости P(NH3) от времени (τ). Из полученного графика определяем начальную скорость реакции за пятиминутный интервал: 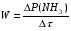 б) Электрометрический метод. Метод основан на использовании специальных электродов, чувствительных к концентрации. Предварительно калибруют прибор по стандартным растворам NH4Cl. Для этого измеряют величину э. д. с. гальванического элемента, состоящего из электрода сравнения и ионоселективного электрода, помещенных в 0,1М, 0,01М, 0,001М раствор. На основе полученных данных строится график, имеющий вид 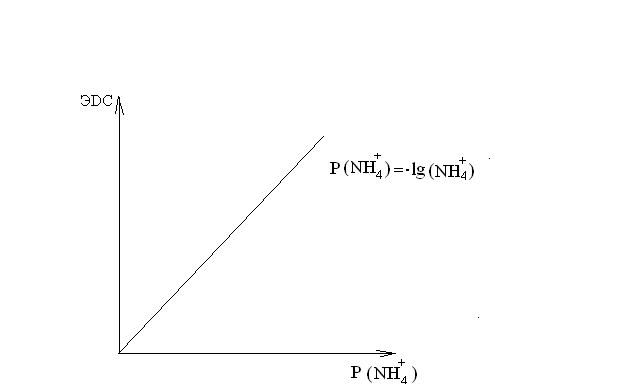 Рис.1 Затем осуществляют изучение скорости гидролиза мочевины этим методом. В стакан помещают 30мл 0,1М раствора мочевины и измеряют температуру раствора. Если температура отличается от заданной, то ее устанавливают с помощью водяной бани. В стакан с раствором мочевины помещают электроды и измеряют э. д. с. Затем вносят суспензии уреазы и отмечают время. Через каждые 3 минуты отмечают величину э. д. с. и заносят в таблицу:
По графику находят 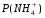 . По формуле . По формуле 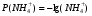 определяют концентрацию. определяют концентрацию.Строится зависимость вида: 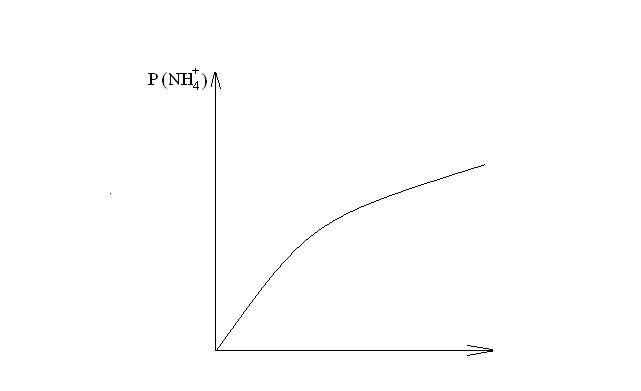 τ τРис.2 Определите скорость реакции за пятиминутный интервал по формуле: 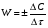 УЧЕБНО-МЕТОДИЧЕСКОЕ И ИНФОРМАЦИОННОЕ ОБЕСПЕЧЕНИЕ ДИСЦИПЛИНЫ а) Основная литература: 1. Беляев А.П. Физическая и коллоидная химия. – М.: ГЭОТАР, 2008.- 243 с. 2. Мушкамбаров Н.Н. Физическая и коллоидная химия. – М.: ГЭОТАР-МЕД, 2001. – 184 с. 3. Евстратова К.И., Купина Н.А., Малахова Е.Е. Физическая и коллоидная химия. – М.: Высшая школа, 1990. – 487 с. б) Дополнительная литература: 3. Фридрихсберг. Курс коллоидной химии. Л.: Химия, 1984. 4. Физическая химия, т.1,2., (под редакцией Краснова К.С.), М.: Высшая школа, 1995. 5. Евстратова К.И. и др. Практикум по физической и коллоидной химии. М.: Высшая школа, 1990. 6. Краткий справочник физико-химических величин (под редакцией Равделя А.А. и Пономаревой А.М.), Л.: Химия, 1993, 1989. 7. Фролов Ю.Г. Курс коллоидной химии. М.: Химия, 1995 8. Зимон А.Д., Лещенко Н.Ф. Коллоидная химия. М.: Химия, 1995. 9. Дулицкая Р.А., Фельдман Р.И. Практикум по физической и коллоидной химии, М.: Высшая школа, 1978. П Р А В И Л А ПО ТЕХНИКЕ БЕЗОПАСНОСТИ И ПРОИЗВОДСТВЕННОЙ САНИТАРИИ ПРИ РАБОТЕ В ХИМИЧЕСКИХ ЛАБОРАТОРИЯХ МЕДИЦИНСКИХ УЧЕБНЫХ ЗАВЕДЕНИЙ
1.1. Студенты до входа в учебное помещение должны надевать халат. 1.2. Каждый студент должен работать на закрепленном за ним рабочем месте. Переход на другое место без разрешения преподавателя не допускается. 1.3. Рабочее место следует содержать в чистоте, не загромождать его посудой и посторонними предметами, по окончании работы убрать все приборы. 1.4. Приборы и установки общего пользования (весы, микроскопы, приборы для определения температуры плавления, кипения и фильтрования при пониженном давлении, установки для перегонки) устанавливают отдельно. 1.5. Рабочие места студентов запрещается загромождать склянками с реактивами, ненужными в данный момент приборами, посудой с посторонними предметами. 1.6. Во время работы в лаборатории следует соблюдать тишину, порядок и чистоту, не допускать торопливости, беспорядочности и неряшливости. 1.7. Запрещается посещение студентов, работающих в лаборатории, посторонними лицами, а также отвлечение студентов посторонними делами или разговорами. 1.8. Студентам запрещается работать в лаборатории в отсутствие преподавателя или лаборанта, а также в неустановленное время без разрешения преподавателя. 1.9. Категорически запрещается выполнять в лаборатории экспериментальные работы, не связанные с выполнением учебного практикума. 1.10. К выполнению каждой работы студенты могут приступать только после получения инструктажа по технике безопасности и разрешения преподавателя. 1.11. Приступая к работе необходимо: – уяснить методику работы; – проверить правильность сборки прибора или установки; – проверить соответствие взятых веществ веществам, указанным в описании работы. 1.12. По окончании работы необходимо: – выключить воду, газ и электричество; – убрать в шкаф реактивы, чистую стеклянную посуду и приборы; – поставить металлические штативы в установленном месте на столе; – унести грязную посуду в моечную; вытереть поверхность стола тряпкой. 1.13. Работы с опасными веществами студенты должны выполнять с использованием соответствующих защитных средств. 1.14. В начале каждого занятия преподаватель проводит краткий инструктаж о мерах безопасности при работе с изучаемым веществом, препаратом, прибором, инструктаж фиксируется в журнале.
2.1. При работе с электрооборудованием и электроприборами возможны случаи поражения людей электрическим током и возникновения пожара. 2.2. Причинами пожара и поражения людей могут быть: работа с неисправным электрооборудованием (рубильники, пускатели, розетки, двигатели и др.); 2.3. Приступая к работе с действующими установками, необходимо: – включать электрическую схему только в присутствии опытного сотрудника (преподавателя, лаборанта.); – при выполнении задачи все необходимые переключения в схемах производить только при выключенном напряжении; – в случае возникновения загорания нужно немедленно отключить напряжение и приступить к тушению пожара порошковым огнетушителем, песком или асбестовым полотном; 2.4. При работе с электрооборудованием и электроприборами строго запрещается: – проверять наличие напряжения пальцами и касаться токоведущих частей электросхемы; – пользоваться неисправным электрооборудованием и розеткой; – вешать на штепсельные розетки, выключатели и электропровода различные вещи; – оставлять без надзора электрическую схему под напряжением.
3.1. В лабораториях используется только специальная (неповрежденная) химическая посуда. 3.2. Посуду, предназначенную для хранения реактивов, нельзя использовать для хранения пищевых продуктов. 3.3. Все сосуды должны иметь четкую и прочную надпись, которую необходимо периодически обновлять. 3.4. При проведении всех видов работ по сборке и созданию приборов из стекломатериалов и посуды (например, вставка стеклянных трубок и стеклянных палочек в пробки, соединение их с резиновыми шлангами), необходимо соблюдать следующие правила: – при соединении стеклянных трубок с просверленной пробкой нужно держать пробку за боковые стороны одной рукой и насаживать ее на трубку, удерживаемую другой рукой; – керну и гильзы шлифов отдельных деталей перед сборкой прибора необходимо смазать вазелином или специальной смазкой; – все приборы нужно собирать так, чтобы они были устойчивы. 3.5 Использование собранного прибора без предварительной проверки его исправности не допускается. 3.6. Оставлять действующий прибор без присмотра не разрешается. 3.7. Нагревая жидкость в пробирке или колбе, сосуд нужно держать специальным держателем и так, чтобы отверстие было направлено в сторону от работающего. 3.8. Перенося сосуды с горячей жидкостью, нужно держать их двумя руками - одной за дно, другой - за горловину, используя при этом полотенце (во избежание ожога кистей и пальцев рук). 3.9. При закрывании тонкостенного сосуда пробкой следует держать его за верхнюю часть горла как можно ближе к пробке. Нагретый сосуд нельзя закрывать притертой пробкой до тех пор, пока он не охладится. 3.10. При переливании жидкостей нужно пользоваться воронкой, поставленной в кольцо штатива нал сосудом-приемником переливаемой жидкости . 3.11. В стеклянные ампулы, как правило, разрешается запаивать сконденсированные газообразные вещества, имеющие температуру кипения не ниже 20 С. Вещества, разлагающиеся при нагревании со взрывом, запаивать в ампулы запрещается. 3.12. Ампулу разрешается заполнять не более, чем на 50% ее объема. 3.13. Ампулы перед запаиванием необходимо охладить ниже температуры кипения помещенного в них вещества. Для охлаждения ампул следует пользоваться негорючими охлаждающими смесями. 3.14. Запаянные ампулы, содержащие сконденсированные газообраз ные вещества, после охлаждения места обогрева до комнатной температуры следует вынуть из охлаждающей смеси и немедленно поместить в цилиндр из металлической сетки. 3.15. Все операции с ампулами до их вскрытия следует проводить в вытяжном шкафу, не вынимая из защитной оболочки. При этом нужно пользоваться защитными очками. 3.16. Для мытья лабораторной посуды выделяется часть помещения, оборудованная моечным устройством, моечными раковинами с подведенной холодной и горячей водой и различными приспособлениями и предметами, нужными для мытья посуды. При большом количестве посуды "моечные" оборудуются в отдельном помещении. 3.17. Химическая посуда должна быть сухой и чистой, так как грязь может резко изменить ход реакции. Грязную посуду следует мыть сразу же после окончания работы. 3.18. Для мытья посуды можно применять мыло, кальцинированную соду, современные моющие средства. 3.19. Для удаления с посуды нерастворимых в воде органических веществ пользуются органическими растворителями. 3.20. Для очистки посуды химическими методами чаще всего применяют хромовую смесь, серную кислоту и растворы щелочей. После тщательной очистки и мытья посуду высушивают в сушильном шкафу. 3.21. В случае получения травм (порезов) при работе со стеклянной посудой необходимо удалить осколки стекла из раны, нейтрализовать или снять попавшее вещество с кожи тампоном, смоченным соответствующим раствором или водой , после этого высушить сухим тампоном, смазать рану настойкой йода и наложить стерильную повязку. |

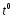 ,С
,С