Системы крови
 Скачать 7.82 Mb. Скачать 7.82 Mb.
|
|
Ренопривная АГ Ренопривная АГ (лат. ren - почка, privo - лишать чего-либо), син.: ренопаренхиматозная. Выявляется в среднем в 3 % от всех АГ. Причиной ренопривной АГ является уменьшение массы паренхимы почек, вырабатывающей биологически активные вещества с гипотензивным действием. К ним относятся простагландины с сосудорасширяющим эффектом (групп Е, I) и кинины (в основном брадикинин и каллидин). Снижение массы почек чаще всего наблюдается при гломерулонефритах, диабетической нефропатии, интерстициальном нефрите, поликистозе, пиелонефритах, опухолях почек, хирургическом удалении части, одной или обеих почек. Патогенез ренопривной АГ представлен на схеме 3. Уменьшение синтеза и выделения в кровь простагландинов и кининов, оказывающих гипотензивное действие обусловливает: 1) снижение кровообращения в ЮГА. Это, в свою очередь, приводит к активации системы «ренин – ангиотензин – альдостерон» и повышению АД; 2) повышение реабсорбции ионов Na+ и жидкости. В результате развивается гипернатриемия, гиперволемия, повышается периферическое сосудистое сопротивление. Это потенцирует степень возрастания уровня АД. Одновременно с этим, недостаток кининов (с гипотензивным эффектом) усугубляет степень нарастания АД. Известно, что простагландиновый и кининовый компоненты почечной «гипотензивной системы» являются физиологическими антагонистами системы «ренин – ангиотензин – альдостерон - АДГ». Снижение «мощности» этих компонентов гипотензивной системы в случае уменьшения массы интерстициальных клеток почечной ткани обусловливает доминирование не только почечной, но и других «гипертензивных» систем и развитие АГ. Именно такой механизм лежит в основе формирования АГ у пациентов, которым по той или иной причине провели одностороннюю или двустороннюю нефректомию. Важно, что «гипотензивная» функция почек не связана с экскрецией прессорных агентов с мочой, поскольку гемодиализ не предупреждает развития АГ. В целом, различные функциональные и органические повреждения почечной ткани, могут активировать «ренопрессорную» систему (ренин – ангиотензин – альдостерон – АДГ) и одновременно (или последовательно) приводить к истощению и/или уменьшению материального субстрата «ренодепрессорных» механизмов. В совокупности это обусловливает развитие стойкой, трудно поддающейся лечению «почечной» АГ. Гипоксические АГ Гипоксические («органно-ишемические», метаболические) АГ наблюдаются при ишемии, венозной гиперемии или гипоксии многих других органов: сердца, печени, селезенки, легких, матки и др. Их общий патогенез заключается в нарушении кровоснабжения органов и тканей (ишемия, венозная гиперемия). Это приводит к гипоксии и расстройству обмена веществ с развитием дисбаланса между образующимися в органах и тканях ФАВ с гипер- и гипотензивным действием. При этом доминируют эффекты метаболитов с гипертензивным влиянием. Это обусловливает увеличение: а) тонуса стенок артериол и сужение их просвета и, как следствие - повышение общего сосудистого сопро- тивления; б) объёма циркулирующей крови; в) сократительной функции сердца и выброса им крови. В результате этих эффектов развивается артериальная гипертензия. В последующем повышенный уровень АД стабилизируется с участием других механизмов развития гипертензии (нейрогенного, эндокринного, гемического). Это, в свою очередь, приводит к нарушению тканевого метаболизма в других органах и сопровождается ослаблением их депрессорной функции – развивается стойкое повышение АД. Гемические АГ Изменение состояния крови (в виде увеличения ее массы и/или вязкости) в 25-30 % случаев обусловливает развитие АГ. Кровопускание, нормализация реологических свойств крови, излечение основного заболевания приводит к нормализации повышенного уровня АД. Причинами гемических АГ являются различные патогенные факторы, вызывающие возрастание либо ОЦК, либо вязкости крови. Увеличение массы циркулирующей крови вызывается полицитемиями различного генеза, которые возникают в результате: 1) опухолевой пролиферации форменных элементов крови при истинной полицитемии (син.: эритремия, болезнь Вакеза, первичная полицитемия) или 2) увеличения числа эритроцитов (вторичный эритроцитоз) при различных типах длительно протекающей гипоксии (например, у пациентов с хронической сердечной или дыхательной недостаточностью. Повышение вязкости крови наблюдается при повышении концентрации в плазме крови белков нормальной структуры, особенно глобулинов, либо появлении в ней аномальных белков, например, амилоида, а также при увеличении числа форменных элементов крови (особенно эритроцитов). В патогенезе гемических АГ важное значение имеет повышение количества эритроцитов и/или уровня фибриногена и других белков в плазме крови, в результате чего вязкость крови увеличивается. Так, если принять за 1 вязкость физиологического раствора NaCl, то относительная вязкость плазмы составит 1,7; цельной крови при гематокрите 40 % - 4; при гематокрите 60 % -8. Увеличение гематокрита значительно снижает скорость кровотока по сосудам и приводит к гипоксии тканей. Так, для сохранения той же скорости протекания по сосудам (что и при нормальном гематокрите) крови с гематокритом 60 %, требуется увеличение градиента давления в два раза. Кроме того, с уменьшением скорости тока крови ее вязкость возрастает в связи с тенденцией к увеличению аггломерации эритроцитов и других форменных элементов. В результате повышается капиллярное давление и возникают условия для еще большего сгущения крови (за счет тока ее жидкой фракции из сосудов в ткани). Адекватной мерой компенсации в такой ситуации является повышение АД. При этом, увеличение кислородной ёмкости крови при гематокрите 60 % и более уже не играет благоприятной роли в отношении транспорта кислорода к ткани. Из-за более высокого изменения ее вязкости снабжение кислородом падает примерно вдвое и ведет к гипоксии. Развивающаяся гипоксия обусловливает выработку метаболитов с гипертензивным действием (простагландинов типа F, биогенных аминов, ангиотензина II, циклических нуклеотидов, особенно цАМФ тромбоксана А2, эндотелина и др.). Увеличение массы циркулирующей крови сопровождается повышением объёма притекающей к сердцу крови. Это обусловливает значительное возрастание величин ударного и сердечного выбросов крови. Как следствие, повышается уровень АД. Развитие АГ потенцируют избыток хлорида натрия в продуктах питания и воде, характер профессии, наличие наследственной предрасположенности. Доказана выраженная конкордантность заболеваемости ГБ у однояйцевых близнецов (около 80-90 %). Наиболее значимым наследственным дефектом является системная мембранопатия, обусловливающая нарушение трансмембранного переноса ионов. Особенно важно накопление в миоцитах стенок сосудов и миокарде избытка ионов Na+ и Са2+. Избыток ионов натрия обусловливает усиление транспорта жидкости в клетки и их набухание. Набухание клеток стенок сосудов ведет к их утолщению, сужению их просвета, повышению ригидности сосудов, снижению способности их к вазодилатации, повышению чувствительности миоцитов стенок сосудов различных органов, в том числе и сердца к вазоконстрикторным факторам. Избыток ионов кальция, в свою очередь, приводик к повышению тонуса стенок сосудов (особенно артериол) и их сенсибилизации к вазопрессорным веществам, а также - увеличению сократимости миокарда и сердечного выброса. Гипертоническая болезнь (эссенциальная гипертензия) Название гипертензии «эссенциальная»,(от лат. essentia - сущность) означает, что стойко повышенное АД при ней составляет сущность (главное содержание) этой разновидности АГ. Каких-либо изменений в других органах, способных привести к АГ при этом не выявляется. Подавляющее большинство пациентов с артериальной гипертензией – (около 95 %) страдает именно гипертонической болезнью (ГБ). Это «самая человеческая из всех болезней человека» (Ф. А. Андреев, 1947). У животных она не встречается, а моделирование у них подобия ГБ, в том числе и путём нервно-психических воздействий, не всегда успешно. Общая этиология ГБ Основная причина гипертонической болезни: повторный, как правило, затяжной психоэмоциональный стресс, имеющий выраженный отрицательный эмоциональный характер. К числу условий, способствующих развитию гипертонической болезни (факторам риска) относятся (схема 12): а) наследственная предрасположенность к ГБ полигенной природы. Аргументами этому являются: - более высокая заболеваемость членов отдельных семей по сравнению с популяцией в целом; - системная мембранопатия, сопровождающаяся накоплением в миоцитах избытка ионов Са2+ и Na+ ; - дисфункции мембранных рецепторов, воспринимающих нейромедиаторы и другие ФАВ, регулирующие уровень АД, что создает условия для доминирования эффектов гипертензивных факторов; - нарушения экспрессии генов клеток эндотелия, контролирующих синтез сосудорасширяющих агентов (оксида азота, простациклина, простагландина E); б) факторы окружающей среды, наибольшее значение среди которых имеют: избыток NaCl в продуктах питания и в воде; профессиональные вредности (например, постоянный шум, необходимость длительного напряжения внимания); неблагоприятные условия проживания (включая коммунальные условия); различные интоксикации (особенно алкоголем, никотином, наркотиками); травмы мозга (ушибы, сотрясения, электротравма и др.); в) индивидуальные характеристики организма, в частности: возраст (по мере взросления перестраивается диэнцефально-гипоталамическая область мозга, структуры которой непосредственно участвуют в регуляции уровня АД. При этом, с увеличением возраста, особенно после 30-40 лет, доминируют гипертензивные реакции на различные экзо- и эндогенные воздействия), мужской пол (мужчины болеют ГБ чаще, чем женщины), повышенная масса тела, гиперхолестеринемия, высокий уровень продукции и содержания ренина в крови, особенности реакции сердечно-сосудистой системы на раздражители. Они заключаются в доминировании гипертензивных реакций на самые различные раздражители. Чаще эти воздействия адресованы второй сигнальной системе. Даже незначительные эмоциональные (особенно негативного характера) влияния, а также факторы внешней среды, приводят к существенному повышению артериального давления. Любой эндо- или экзогенный фактор, который вызывает отклонения в том или ином звене системы регуляции АД, может (при подходящих условиях) одновременно выступать и в качестве предрасполагающего к развитию АГ фактора. В числе этих факторов могут быть и нервные, и перенесенные в прошлом инфекционно-аллергические, эндокринные, почечные и другие заболевания. Однако, значимость каждого фактора различна. Основные звенья патогенеза ГБ Ниже приводится краткая характеристика основных патогенетических звеньев гипертонической болезни Инициальное звено патогенеза ГБ - развитие невротического состояния (невроза). Оно характеризуется нарушением внутрицентральных процессов в нервной системе и «включением» центрогенного нейрогенного звена патогенеза ГБ. Последнее сопровождается формированием устойчивого возбуждения корково-подкоркового комплекса, включающего симпатические ядра заднего отдела гипоталамуса, адренергические структуры ретикулярной формации, а также сосудодвигательный центр. Это сочетается с усилением прессорных (гипертензивных) влияний на сердечно-сосудистую систему, реализующихся по двум взаимозависимым каналам: нервному и гуморальному. Нервный путь заключается в активации симпатических нервных влияний на: 1) стенки артериол (это обусловливает их длительное сужение и повышение общего периферического сосудистого сопротивления. Уровень АД в этих условиях существенно увеличивается. При хронически повышенной симпатической стимуляции гладких мышц артериол наблюдается их гипертрофия, в стенке сосудов развивается фиброзная ткань, они сужаются и деформируются (этот процесс получил название «ремоделирование стенки сосуда»). Это потенцирует степень гипертензии, а также обусловливает сужение просвета артерий; 2) стенки венул и вен (это вызывает сужение ёмкостных сосудов, увеличение притока венозной крови к сердцу, повышение, в связи с этим, ударного и сердечного выбросов); 3) сердце (катехоламины реализуют свои положительные хроно- и инотропные эффекты, что потенцирует увеличение сердечного выброса и степень повышения АД). Гуморальный путь характеризуется активацией образования и высвобождения в кровь комплекса гормонов с гипертензивным действием: АДГ (вазопрессина), адреналина (выделяемого мозговым веществом надпочечников), АКТГ, минерало- и глюкокортикоидов, тироксина и трийодтиронина, эндотелина. Указанные вещества, реализуя своё действие (механизм см. выше) параллельно с активацией симпатической нервной системы, обеспечивают: - повышение общего периферического сосудистого сопротивления; - веноконстрикцию и увеличение, в связи с этим, возврата венозной крови к сердцу; - повышение ОЦК; - увеличение сердечного выброса. Эти эффекты «закрепляют» повышенный уровень АД или увеличивают его дополнительно. Данный этап развития ГБ обозначают как I стадия (стадия становления ГБ или транзиторная). На этой стадии отмечается повторное, преходящее, более или менее длительное, повышение АД выше нормы. Признаки поражения внутренних органов отсутствуют. Выявляется нарастающая гипертрофия мышечных волокон и фиброз стенок артериол и миокарда, дальнейшая деформация просвета сосудов и полостей сердца (ремоделирование стенок артериол и сердца), развитие атеросклероза. Эти изменения обусловливают нарушения в органах и тканях кровообращения (ишемию, венозную гиперемию) и развитие гипоксии (вначале – циркуляторного, а затем – смешанного типа). В последующем, на II стадии (стадии стабильной гипертензии), реализуются механизмы стабилизации уровня АД на повышенном уровне. К этим механизмам представленным на схеме 4 относятся: а) рефлексогенный (син.: барорецепторный; он заключается в нарастающем снижении или даже прекращении афферентной депрессорной импульсации от барорецепторов дуги аорты, синокаротидной и других зон в адрес сосудодвигательного центра); б) эндокринный (характеризуется стимуляцией продукции и инкреции в кровь гормонов с гипертензивным действием); в) метаболический (син.: гипоксический, органно-ишемический; он включает почечные гипертензивные механизмы: вазоренальный, ренопаренхиматозный, а также различные органоишемические. Это сопровождаются синтезом избытка метаболитов с гипертензивным действием и подавлением образования метаболитов с гипотензивным эффектом; г) гемический (заключается в развитии под влиянием хронической гипоксии полицитемии (в основном, за счет значительного эритроцитоза) и повышенной вязкости крови (в связи с полицитемией и диспротеинемией). На II стадии ГБ регистрируются стабильно повышенное (гипертензивное) АД, а также признаки поражения тканей и внутренних органов (гипертрофия сердца, выраженный атеро- и артериосклероз, нефросклероз и другие). В последующем повреждения структурных элементов прогрессируют, развиваются грубые расстройства функций тканей и органов с развитием полиорганной недостаточности. Наиболее часто наблюдаются выраженный атеро- и артериосклероз, приводящие к инфарктам различных органов (наиболее часто – миокарда), инсультам и кардиомиопатиям. Одной из причин этого является нарушение сбалансированности роста структур миокарда (что получило название: «комплекса изнашивания гипертрофи- рованного сердца»). У пациентов выявляются склеротическое поражение почек (обозначается как «первично сморщенная почка», что указывает на первично «гипертензивный» генез патологии почек при ГБ) , а также дистрофические и склеротические изменения в других органах (мозге, эндокринных железах, сетчатке, сердце, глаза. Описанный этап развития ГБ обозначают как III стадия ГБ или стадия органных изменений. Смешанные АГ Помимо указанных выше, могут развиваться АГ в результате одновременного «включения» нескольких описанных выше механизмов, обусловливающих развитие гипертензии. Например, АГ при повреждении мозга или развитии аллергических реакций формируются с участием нейрогенного, эндокринного и почечного патогенетических факторов. Характеристика Местных АГ Регионарные (син. местные, сосудистые) АГ развиваются в отдельных более или менее масштабных сосудистых регионах. Причиной местных АГ является, как правило, сужение просвета крупных артериальных стволов (например, грудного или брюшного отделов аорты, бедренных артерий). Обусловлено это чаще всего: - врожденным или приобретенным сужением (коарктацией) сосудов, например, аорты; - облитерацией сосудов (в результате артериосклероза, гиперплазии и гипертрофии стенок артерий); - воспалением стенок артериол и артерий (панартериитом), с образованием тромбов на них. При этом, АД выше места сужения увеличивается, а ниже его – либо нормальное либо несколько снижено. Основными звеньями патогенеза местных АГ являются: 1) механическое препятствие току крови, приводящее к увеличению АД выше места сужения сосуда 2) кинетическое (син.: сердечно-сосудистое), реализующее путём: а) повышения АД в связи с увеличением сердечного выброса в ответ на препятствие току крови. Благодаря этому достигается нормализация уровня АД ниже места сужения сосуда, препятствующего току крови; б) изменения местной регуляции тонуса артериальных сосудов. Повышение АД создает угрозу избыточного кровотока через данный отрезок кровеносного русла при прежнем просвете сосуда. Для поддержания оптимального притока крови и обеспечения адекватного гемодинамического давления в капиллярах происходит автоматическое (в ответ на повышение АД) сужение артериального сосуда за счет увеличения его мышечного тонуса. Так, например, при повышении перфузионного давления в сонных артериях до 200-250 мм рт.ст. наблюдается резкое сужение артериол бассейна данной артерии, вплоть до полного прекращения проходимости резистивного сосудистого русла (защитное значение этого механизма для капилляров очевидно). Такая автоматическая регуляция местного кровообращения объясняется наклонностью сосудов к локальному повышению тонуса и спазмам при гипертензиях. Однако при этом создается угроза развития реакции по механизму «порочного круга» – чем выше АД, тем выраженнее вазоконстрикция, влекущая за собой дальнейшее повышение АД. При коарктации аорты (а также при других дефектах сосудов, препятствующих нормальному току крови) сосуды выше места сужения находятся в режиме постоянной констрикции, поддерживаемой высоким АД, а ниже сужения – в режиме постоянной дилатации. Высокий локальный тонус сосудов выше места сужения, в свою очередь, поддерживается благодаря действию двух факторов: структурно-миогенного и нейрогенного (регулируемого внутренним и внешним аппаратом управления). Структурно-миогенный фактор определяется автоматической саморегуляцией напряжения мышц стенок сосудов. Он зависит от изменений внутрисосудистого давления: растягивающее усилие давления, являясь адекватным стимулом к сокращению гладких мышц, вызывает сужение просвета резистивных сосудов. Нейрогенный (вазомоторный) фактор обусловлен влиянием различных отделов автономной нервной системы. В различных органах и тканях соотношение миогенного и нейрогенного факторов различно. Для сосудов конечностей, например, оно равно примерно 1:1. Для других зон этот коэффициент иной. Так, в жизненно важных органах (сердце и мозге) тонус сосудов регулируется почти монопольно миогенным компонентом поскольку их кровоснабжение не может «приноситься в жертву», как бы ни складывались условия общего кровообращения. Сосуды других областей (например, многих органов брюшной полости) управляются преимущественно вегетативной (симпатической, парасимпатической, метасимпати- ческой нервной системой, особенно в чрезвычайных ситуациях. Важно, что даже местное нарушение кровообращения при регионарных АГ, как правило, на последующих этапах ведет к включению других механизмов стабилизации высокого АД. Анализ данных об этиологии и патогенезе артериальных гипертензий позволят сделать следующее общее заключение: Несмотря на многообразие причинных факторов и сложность патогенеза АГ, можно выделить несколько общих механизмов их формирования: нейрогенный (центрогенный и рефлекторный), эндокринный, почечный, гемический, смешанный. Отдельные разновидности АГ редко развиваются в «чистом» виде, т.е. на основе включения лишь одного из механизмов повышения АД. Если этиологические факторы вовремя не устранены, то, как правило, в механизм развития данной АГ включаются и другие патогенетические факторы, обусловливающие стабилизацию смешанной гипертензии. В процессе развития АГ, кроме расстройств физиологи- ческих механизмов регуляции кровообращения и уровня АД, наблюдается «включение» и патологических механизмов. Первое наблюдается, как правило, на начальных этапах АГ, второе – на этапах стабилизации, закрепления АД на повышенном, гипертензивном уровне. К последним механизмам относятся: 1) формирование гиперреактивного состояния («доминанты возбуждения») на различных «этажах» cистемы регуляции уровня АД; 2) увеличение образования и выброса в кровь гипертензивных и уменьшение гипотензивных агентов; 3) ослабление, вплоть до истощения, депрессорно-гипотензивных систем регуляции АД; 4) чрезмерное повышение чувствительности рецепторов сердца и стенок сосудов к действию гипертензивных факторов. В механизме формирования АГ существенное значение имеет не только активация прессорных систем и факторов организма, но также и снижение активности депрессорных систем. 30.1.2. Принципы лечения артериальных гипертензий Этиотропный принцип, во-первых, направлен на устранение (снижение) действия причинного фактора АГ. 1. При нейрогенных АГ , обусловленных: - психоэмоциональным стрессом необходимо: 1) устранение («разрешение») стрессовых ситуаций при их возникновении, 2) медикаментозное торможение (снижение степени выраженности) или блокада стресс-реакции (например, с помощью седативных препаратов); - органическим поражением структур мозга, регулирующих уровень АД необходимо: ликвидация или уменьшение степени последствий действия повреждающего фактора (достигаемого, например, лече- нием энцефалитов, удалением новообразований или гематом мозга, устранением ишемии участков мозга); - формированием гипертензивных условных рефлексов необходимо: 1) прекращение применения веществ с гипертензивным действием перед событиями, имеющими личностно важное значение для данного пациента, 2) предотвращение развития стресс-реакции в связи с подготовкой к значимому событию в жизни (например, с помощью психологического тренинга или приема седативных препаратов). - повреждением рецепторов, нервных стволов или нервных центров необходимо: 1) устранение причины боли (например, невритов, неврином, опухолей), 2) лечение энцефалитов и/или менингитов, 3) ликвидация повышенного внутричерепного давления (например, удалением новообразования, избытка ликвора, гематомы мозга); - снижением эффективности афферентной импульсации от «депрессорных» рефлексогенных зон необходимо: 1) устранение факторов, повреждающих рецепторы и/или афферентные нервные проводники, идущие к сосудодвигательному центру (например, устранение из организма нейротропных токсинов и/или микробов; прекращение травмирования нервных стволов; излечение невритов); 2) снижение степени атеро- и артериосклероза (например, применением антиатерогенной диеты и медикаментов или лечением васкулитов). 2) При эндокринных АГ необходимо: 1) лечение эндокринных расстройств, вызывающих АГ; 2) устранение гипертензивных эффектов гормонов, образующихся в избытке (например, применением их «антагонистов» или блокаторов рецепторов к этим гормонам). 3) При гипоксических (метаболических) АГ целесообразно: 1) устранение либо снижение степени общей и/или местной гипоксии; 2) ликвидация или снижение степени нарушений кровообращения в органах (главным образом, в почках); 3) предо- твращение уменьшения массы паренхимы почек (например, лечением гломерулонефритов, пиелонефритов, гидронефроза, нефрозов). 4) При гемических АГ необходимо: ликвидация или снижение степени эритроцитозов и/или гиперпротеинемии, что достигается, как правило, излечением патологии или устранением причины, вызывающей эритроцитоз либо гиперпротеинемию. 5) При местных АГ целесообразно:
Этиотропный принцип, во-вторых, направлен на ликвидацию или снижение действия условий, способствующих реализации причинного фактора (т.е. факторов риска):
Патогенетический принцип имеет целью, во-первых, устранение и/или блокаду гипертензивных механизмов, во-вторых, активацию депрессорных механизмов. Обе эти цели достигаются, главным образом, с помощью следующих основных групп лекарственных средств: снижающих общее периферическое сосудистое сопротивление и уменьшающих величину сердечного выброса. Многие лекарства оказывают оба указанных эффекта, хотя и в разной степени. К последним относятся: а) нейротропные средства центрального действия (например, адреноблокаторы, симпатолитики, стимуляторы имидозалиновых рецепторов), обусловливающих, в основном, снижение выброса крови сердцем; б) регуляторы «медленных» кальциевых каналов (син.: «антагонисты» кальция), блокирующих транспорт Са2+ в клетки и вазоконстрикторный эффект гормона эндотелина; в) блокаторы - и -адренорецепторов, обусловливающих: - снижение сердечного выброса, торможение синтеза ренина в почках; - уменьшение степени вазоконстрикции и периферического сосудистого сопротивления; - торможение высвобождения норадреналина из постганглионарных симпатических волокон; - уменьшение объёма циркулирующей крови; г) ингибиторы ангиотензинпревращающего фактора, обеспечивающие несколько эффектов: - подавле- ние образования ангиотензина II и снижение его содержания в крови; - сохранение высокого уровня в крови гипотензивных кининов, главным образом, брадикинина; д) блокаторы рецепторов ангиотензина II, устраняющие гипертензивный эффект; е) диуретики (в основном сальуретики), приводящие к снижению ОЦК и величины сердечного выброса; ж) «антагонисты» альдостерона, препятствующие реализации почечных и непочечных эффектов альдостерона. Симптоматический принцип направлен на устранение или облегчение симптомов болезни, усугубляющих общее состояние пациента. С этой целью применяют, например, антипсихотические, седативные и анальгетические средства и т.д. 30.2. Артериальные гипотензии Гипотензивные состояния встречаются у человека реже, чем гипертензивные, несмотря на это они встречаются достаточно часто. Различают следующие основные виды артериальных гипотензий: 1) острая (коллапс) и 2) хронические. Коллапс (от лат. collapsus - упавший, ослабевший) является разновидностью острой недостаточности кровообращения. Учитывая, что коллапс нередко сопровождается существенными расстройствами жизнедеятельности организма, его относят к числу экстремальных состояний (см. раздел: «Коллапс»). Хронические артериальные гипотензии характеризуются стойким снижением АД ниже нормы: систолического, как правило, до 90 мм рт.ст. и ниже, диастолического до 60 мм рт.ст. и ниже. У многих практически здоровых людей уровень систоли- ческого АД может колебаться в диапазоне от 90 до 110 мм рт.ст. При этом продолжительность жизни их нередко превышает таковую у людей без нарушения уровня АД. 30.2.1. ХАРАКТЕРИСТИКА ОСНОВНЫХ ВИДОВ ХРОНИЧЕСКИХ АРТЕРИАЛЬНЫХ ГИПОТЕНЗИЙ В настоящее время нет единой классификации артериальных гипотензий. В связи с этим, для упрощения и схематизации представлений о видах артериальных гипотензий используется патогенетический подход к их дифференцировке. По инициальному звену механизма развития артериальных нипотензий различают следующие их виды : 1) Нейрогенные: центрогенные и рефлекторные.
3) Метаболические. Нейрогенные центрогенные артериальные гипотензии Нейрогенные гипотензии центрогенного генеза являются результатом либо функционального расстройства высшей нервной деятельности, либо органического повреждения мозговых структур, участвующих в регуляции уровня АД. Артериальные гипотензии, обусловленные нарушением высшей нервной деятельности Основной причиной является длительный, повторный стресс, обусловленный необходимостью сдерживания его двигательных и эмоциональных проявлений. Это приводит к развитию невротического состояния (невроза). Основной инициальный механизм развития данной гипотензии сводится к перенапряжению и срыву высшей нервной деятельности и развитию невроза. Последний характеризуется формированием корково-подкоркового комплекса возбуждения. Оно распространяется на: парасимпатические ядра переднего гипоталамуса и другие структуры парасимпатической нервной системы (например, на дорзальное двигательное ядро блуждающего нерва). Активация парасимпатических влияний на сердечно-сосудистую систему обусловливает снижение сократительной функции миокарда, сердечного выброса крови, тонуса резистивных сосудов. В итоге развивается артериальная гипотензия. Определенным аргументом приведенным выше представлениям является большой «удельный вес» людей со слабым типом ВНД (с высокой частотой развития у них невротических состояний) среди больных артериальной гипотензией. Считают, что именно такой механизм лежит в основе развития гипотонической болезни. Наряду с этим, «включаются» и другие описанные ниже патогенетические звенья, что способствует стабилизации АД на пониженном уровне или даже усугубляет степень его снижения. Артериальные гипотензии, обусловленные органическими изменениями в центральных (диэнцефально-гипоталамических) и периферических структурах, участвующих в регуляции АД Наиболее частыми причинами их являются травмы головного мозга (при его сотрясенях или ушибах), нарушения мозгового кровообращения (ишемия, венозная гиперемия), дегенеративные изменения в веществе головного мозга. Чаще выявляются у пожилых мужчин. У них наблюдается дегенерация нейронов экстрапирамидной системы, нервных клеток базальных ядер мозга, нейронов заднего ядра блуждающего нерва. Кроме того отмечается снижение выделения в кровь катехоламинов при физической нагрузке и изменении положения тела из горизонтального в вертикальное. В этом случае нередко развиваются ортостатические коллапсы и обмороки. В целом, описанные изменения обозначают как синдром Шая-Дрейджера. ем активности симпатоадреналовой системы и её эффектов на сердечно-сосудистую систему; 2) относительным или абсолютным преобладанием эффектов парасимпатической нервной системы на сердце и сосуды; 3) снижением тонуса стенок артериол и общего периферического сосудистого сопротивления, а также сердечного выброса крови. В совокупности это обусловливает развитие стойкой артериальной гипотензии. Рефлекторные артериальные гипотензии Основной причиной их развития является нарушение проведения эфферентных гипертензивных импульсов от сосудодвигательного центра продолговатого мозга к стенкам сосудов и сердцу. Наиболее часто рефлекторные артериальные гипотензии (син.: рефлексогенные, проводниковые) развиваются при диссеминированном нейросклерозе, нейросифилисе, боковом амиотрофическом склерозе (характеризующимися дегенерацией нейронов спинного мозга, что проявляется гипотензией и атрофией мышц – отсюда название амиотрофия), сирингомиелии (сопровож- дающейся образованием полостей в шейном и грудном отделах спинного мозга, а также в продолговатом мозге), периферических нейропатиях различного генеза (например, диабетического, инфекционного, нейротоксического). Механизм развития рефлекторных артериальных гипотензий заключается в значительном уменьшении или прекращении тонических влияний симпатической нервной системы на стенки сосудов и сердца. Это приводит к снижению периферического сосудистого сопротивления (соответственно – диастолического давления), а также к уменьшению сократительной функции сердца, величины сердечного выброса, систолического давления крови, а в итоге - к развитию артериальной гипотензии. Эндокринные артериальные гипотензии Основными их причинами являются: - снижение синтеза и/или выхода в кровь гормонов с гипертензивным действием (вазопрессина, альдостерона, эндотелина, катехоламинов, тиреоидных); - гипосенситизация рецепторов стенок сосудов и сердца к гормонам с гипертензивным эффектом. При хроническом течении действуют оба фактора. Артериальные гипотензии надпочечникового происхождения Наиболее частыми их причинами являются: гипотрофия коры надпочечников, опухоль коры надпочечников с разрушением их вещества, кровоизлияние в надпочечник (один или оба), туберкулезное поражение надпочечников, деструкция надпочечников в результате иммунной аутоагрессии, травмы, приводящие к повреждению или разрушению надпочечников. Указанные и некоторые другие факторы обусловливают повреждение надпочечников и снижение концентрации в крови гормонов с гипертензивным действием: минерало- и глюкокортикоидов. Меньшее значение имеет разрушение мозгового вещества надпочечников. Катехоламины, помимо надпочечников, вырабатываются в так называемых «дополнительных надпочечниках» (хромаффинной системе органов, расположенной в различных органах, особенно по ходу сосудов). Патогенез гипотензий надпочечникового происхождения заключается в дефиците минерало- и глюкокортикоидов и/или недостаточности их эффектов, что обуславливает снижение тонуса стенок артериол и общего периферического сосудистого сопротивления, объёма циркулирующей крови и сердечного выброса. Артериальные гипотензии при поражении гипофиза Основной их причиной является гипофункция адено- и/или нейрогипофиза, обусловленная его разрушением или гипоплазией. Это приводит снижению продукции гормонов с гипертензивным действием (АКТГ, ТТГ, СТГ, АДГ), а также вторичного дефицита альдостерона, глюкокортикоидов тиреоидных гормонов. В патогенезе развитие артериальной гипотензии при питуи- тарной недостаточности важное значение принадлежит отсутствию или резкому снижению гипертензивных эффектов перечисленных выше гормонов. В конечном итоге это приводит к снижению тонуса артериол и периферического сосудистого сопротивления, ОЦК, сердечного выброса. В совокупности это обусловливает стойкое снижение и систолического и диастолического АД, а значит развитие артериальной гипотензии. Артериальная гипотензия при гипотиреоидных состояниях Главной их причиной является дефицит тироксина и трийодтиронина и/или их эффектов (механизмы возникновения гипотиреоидных состояний и их проявлений см. в разделе «Нарушения функций щитовидной железы»). В патогенезе развития гипотиреоидной артериальной гипотензии важное место занимает брадикардия, возникающая в результате снижения или отсутствия положительного хронотропного эффекта тиреоидных гормонов, а также уменьшения активности симпатоадреналовой системы. Указанные изменения приводят к снижению величины сердечного выброса. Кроме того наблюдается нарушение диастолического расслабления сердца (в связи с его сдавлением избытком жидкости в перикарде), развитие миокардиодистрофии, снижение тонуса стенок сосудов и, как результат – общего периферического сосудистого сопротивления. Артериальные гипотензии, вызванные нарушением метаболизма веществ с гипо- и гипертензивным действием Метаболические артериальные гипотензии встречаются весьма редко. Возможными их причинами являются дистрофические изменения в тканях либо гипогидратация организма. Дистрофические изменения в органах и тканях (например, при хронических интоксикациях, инфекциях, голодании) возникают в результате: а) снижения выработки и/или эффектов метаболитов с гипертензивным действием (например, эндотелина, простагландина F2, тромбоксана А2, ангиотензина II и др.); б) падение тонуса миоцитов стенок артериол; в) снижение сократительной функции миокарда. Два последних изменения являются результатом нарушения синтеза структурных элементов миоцитов и снижения миогенного тонуса стенок сосудов и миокарда (что связано с дефицитом белков, липидов и углеводов в организме) из-за надпочечниковой недостаточности. Это сопровождается дефицитом в организме кортикостероидов и катехоламинов, необходимых для поддержания оптимального тонуса и сократительной функции миоцитов стенок сосудов и сердца. Гипогидратация организма вызвана уменьшением объёма жидкости в организме в связи со снижением интенсивности метаболизма. Последний, как известно, сопровождается образованием воды. Гипогидратация организма может быть потенцирована недостаточным поступлением жидкости в организм и/или избыточной потери её (например, при полиурии, гипертермии, приеме диуретиков). Основными звеньями патогенеза «метаболических артериальных гипотензий» являются: 1) снижение тонуса миоцитов стенок сосудов и, вследствие этого, - общего периферического сосудистого сопротивления; 2) падение сократительной функции сердца, ведущее к уменьшению сердечного выброса крови; 3) уменьшение содержания воды в организме, в том числе – ОЦК. В совокупности, указанные факторы обусловливают развитие стойкой артериальной гипотензии. 30.2.2. Принципы лечения артериальных гипотензий Этиотропный принцип имеет целью устранение или снижение патогенного эффекта причинного фактора гипотензий и условий, способствующих его реализации (факторов риска). При нейрогенных артериальных гипотензиях необходимо устранение или ослабление: - 1) стрессовых ситуаций при их возникновении; 2) последствий органических поражений структур мозга, регулирующих уровень АД, что достигается, например, лечением энцефалитов, менингитов, ишемии участков мозга. 3) факторов, повреждающих рецепторы и/или афферентные нервные проводники к сосудодвигательному центру (что достигается: нейтрализацией в организме нейротропных токсинов и/или ликвидацией микробов; - прекращением травмирования нервных стволов, - излечением невритов). При эндокринных артериальных гипотензиях важно проводить: 1) лечение эндокринных расстройств, вызывающих гипотензии, 2) нейтрализацию гипотензивных эффектов образующихся в избытке ФАВ, (например, применением их «антагонистов» или блокаторов рецепторов к этим веществам). При гипоксических (метаболических) артериальных гипотензиях целесообразно устранение либо снижение степени: 1) общей и/или местной гипоксии; 2) нарушений кровообращения в органах. При гемических артериальных гипотензиях необходимо: ликвидировать или снизить степень гиповолемических состояний, гипопротеинемий и т.п., что достигается излечением основного заболевания, сопровождающегося гипотензией, или устранением причины, вызывающей основную (первичную) патологию. Патогенетический принцип имеет целью: 1) устранение или торможение гипертензивных механизмов; 2) активацию депрес- сорных механизмов. Обе эти цели достигаются, главным образом, с помощью следующих основных групп лекарственных средств: 1) препараты, снижающие общее периферическое сопротивление; 2) средства, уменьшающие величину сердечного выброса. Многие лекарства оказывают оба указанных эффекта, хотя и в разной степени. К ним относятся: а) нейротропные средства центрального действия (например, адреноблокаторы, симпатолитики, стимуля- торы имидозалиновых рецепторов), которые обуславливают, в основном, снижение выброса крови сердцем; б) регуляторы «медленных» кальциевых каналов (син.: «антагонисты» кальция), которые блокируют транспорт Са2+ в клетки и эффекты вазоконстрикторного гормона эндотелина; в) блокаторы -адрено- рецепторов; г) блокаторы -адренорецепторов, которые обуслов- ливают: - снижение сердечного выброса, - торможение синтеза ренина в почках; - уменьшение степени вазоконстрикции и пери- ферического сосудистого сопротивления; - торможение высвобож- дения норадреналина из постганглионарных симпатических волокон; - уменьшение ОЦК; д) ингибиторы ангиотензин- превращающего фактора, обеспечивающие несколько эффектов: - подавляют образование ангиотензина II и снижают его содержание в крови; - способствуют сохранению высокого уровня в крови гипотензивных кининов (главным образом, брадикинина). Это обусловлено тем, что ангиотензин II, являясь кининазой, разрушает кинины и снижает активность симпатоадреналовой системы; е) блокаторы рецепторов ангиотензина II, устраняющие гипер- тензивный эффект ангиотензина; ж) диуретики (в основном сальуретики), которые приводят к снижению ОЦК и величины сердечного выброса; з) «антагонисты» альдостерона, препятствую- щие реализации почечных и непочечных эффектов альдостерона. Симптоматический принцип направлен на устранение или облегчение симптомов болезни, усугубляющих состояние пациента. С этой целью применяют, например, антипсихотические, седативные, болеутоляющие и др. препараты. ГЛАВА 31. ПАТОЛОГИЯ ЛИМФАТИЧЕСКОЙ СИСТЕМЫ 31.1. ВВЕДЕНИЕ Впервые лимфатические сосуды описал швед Олаф Рудбек в 1653 году. В течение нескольких веков существования лимфологии, ее клинический раздел касался заболеваний собственно лимфатической системы. К ним относятся лимфедема, лимфангит, лимфаденит, лимфаденоз, лимфангиома, лимфосаркома, лимфангиоэндотелиома, лимфогранулематоз, метастазы опухоли в лимфатической системе. Роль лимфатической системы в патогенезе неспецифических для нее заболеваний (хирургических, терапевтических, и др.) оставалась вне сферы интересов патологии, патофизиологии и клинических дисциплин. В первой половине прошедшего столетия врачи-клиницисты осуществили такие воздействия на лимфатическую систему, как эндолимфатическое введение лечебных препаратов и наружное дренирование грудного лимфатического протока. Но тогда эти методы, недостаточно подкрепленные экспериментальными данными и клиническим опытом, не нашли широкого распространения. В нашей стране морфологию лимфатической системы изучали В.В. Куприянов, ____________ и др., физиологию - ___________ и др. Научно-технический прогресс, достижения биологии и медицины приблизили реальные возможности изучения роли лимфатической системы при многих заболеваниях, подготовили почву для того, чтобы наметить пути возможных лечебных воздействий.В 60-70 гг. прошедшего столетия в экспериментах с моделированием патологических процессов, Ю.М. Левиным была выявлена и доказана важная, а в ряде случаев, ключевая, роль лимфатической системы в развитии и исходе заболеваний разного патогенеза. Автором были сформулированы следующие положения:
Приведенные положения и стали базой нового раздела общей и частной патологии, вошедшего в медицину под терминами «Общеклиническая (практическая, междисциплинарная) лимфология». В этот раздел входят подразделы, обозначенные в литературе как лечебная, профилактическая, адаптационная и оздоровительная лимфология. Фактически не остается болезней, при которых методы управления функциями лимфатической системы не показали бы положительного эффекта. Кроме того, управление процессами образования тканевой жидкости, лимфатического дренажа тканей, транспорта лимфы, и ее атравматичная детоксикация, повысили эффективность оздоровления организма и вошли в практику под термином «Эндоэкологическая реабилитации на клеточно-организменном уровне», сокращенно – «ЭРЛ». В число основных функций лимфатической системы входят: 1) транспортная, 2) дренажная, 3) таможенная, 4) барьерная, 5) детоксикационная, 6) иммунная, 7) лимфокоагуляционная, 8) резорбционная, 9) концентрационная, 10) лимфопоэтическая. 31.2. ТРАНСПОРТ ГУМОРОВ В ОРГАНИЗМЕ К 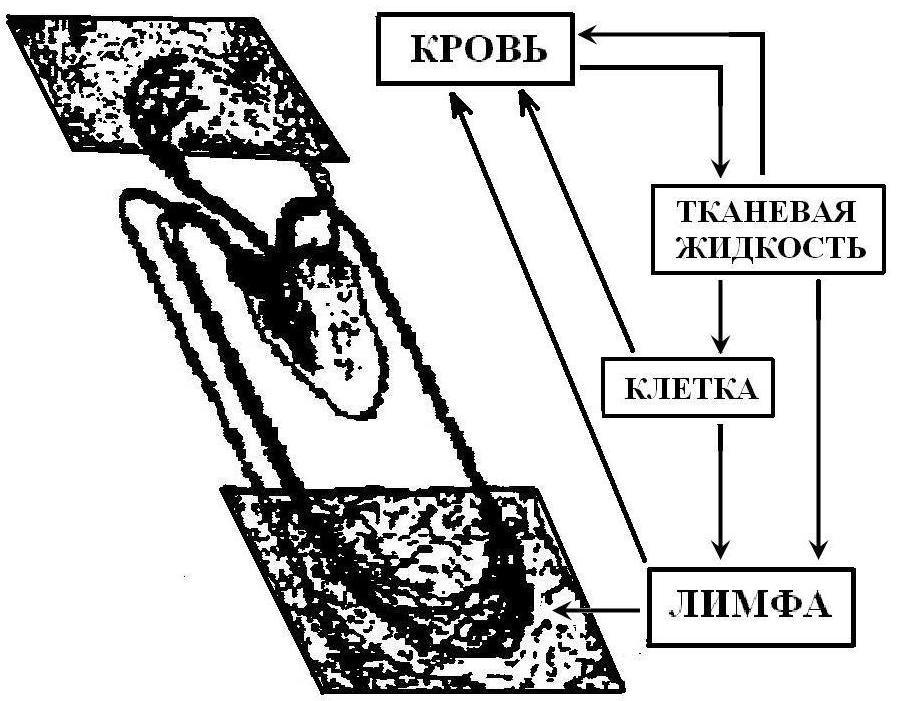 Рис. 31-1. Основные звенья гуморального транспорта и их взаимосвязь ровеносная система, лимфатическая система и внесосудистые ткани представляют неразрывные звенья гуморального транспорта (рис. 31.1). В организме нет процессов, которые протекают без его участия. Известно, что 2/3 массы тела составляет вода. Ее основная часть — 55-70% содержится в клетках и во внеклеточных тканях, соответственно 35±3% и 25±3%. Кровь составляет около 5%; лимфа, в зависимости от условий, — от 0,2% до 2%. В лимфе, в отличие от крови, нет эритроцитов и почти нет тромбоцитов. Ее состав в разных отделах лимфатического русла различен. На него влияют время суток, функциональное состояние органов и систем, интенсивность мышечной деятельности, характер принятой пищи и многие другие факторы. |
