ТЭЛА. Тромбоэмболия легочной артерии (тэла)
 Скачать 4.9 Mb. Скачать 4.9 Mb.
|
|
Синусовая тахикардия. Электрокардиографический признак S I Q III T III . Отмечается также сглаженность T во всех грудных отведениях [73]. Рисунок 9. ЭКГ больного массивной ТЭЛА. Признак перегрузки правого желудочка: симметричная инверсия зубцов T в отведениях V 1 -V 4 [72]. Рисунки 10 и 11. ЭКГ больной 60 лет, страдающей массивной ТЭЛА. С 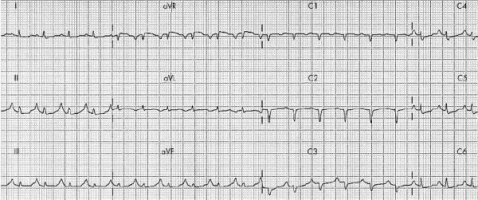 инусовая тахикардия. Гигантские заострённые P-pulmonale (превышающие по амплитуде зубцы R желудочкового комплекса) в отведениях II, III, aVR, низкий вольтаж желудочкового комплекса в стандартных отведениях. Выраженные S С 4 -С 6 (на данной ЭКГ грудные отведения обозначены буковой С вместо V) [74]. инусовая тахикардия. Гигантские заострённые P-pulmonale (превышающие по амплитуде зубцы R желудочкового комплекса) в отведениях II, III, aVR, низкий вольтаж желудочкового комплекса в стандартных отведениях. Выраженные S С 4 -С 6 (на данной ЭКГ грудные отведения обозначены буковой С вместо V) [74].Э 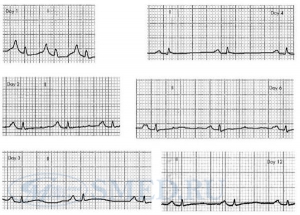 КГ той же больной (см. рисунок 10). Динамика изменений зубца P во втором стандартном отведении на фоне терапии альтеплазой и эноксапарином. На серии ЭКГ (день 1 – день 12) отмечается постепенно уменьшение амплитуды зубца P, нормализация ЧСС [74]. КГ той же больной (см. рисунок 10). Динамика изменений зубца P во втором стандартном отведении на фоне терапии альтеплазой и эноксапарином. На серии ЭКГ (день 1 – день 12) отмечается постепенно уменьшение амплитуды зубца P, нормализация ЧСС [74].Рисунки 12 и 13. ЭКГ больной 42 лет. С 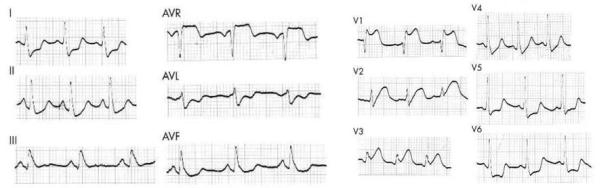 инусовая тахикардия 120 в минуту. Выраженная элевация сегмента ST в отведениях V 1 -V 3 и aVR, формирование глубокого зубца S и депрессия ST в отведения I, aVL, V 4 -V 6 . При обследовании инфаркта миокарда не оказалось, изменения на ЭКГ обусловлены массивной ТЭЛА [75]. инусовая тахикардия 120 в минуту. Выраженная элевация сегмента ST в отведениях V 1 -V 3 и aVR, формирование глубокого зубца S и депрессия ST в отведения I, aVL, V 4 -V 6 . При обследовании инфаркта миокарда не оказалось, изменения на ЭКГ обусловлены массивной ТЭЛА [75].Э 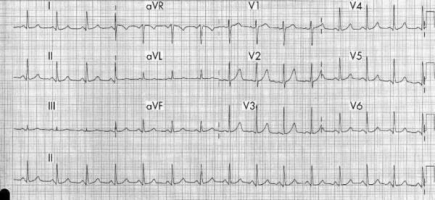 КГ той же больной (см. выше) через 1 час после введения тромболитика. Имевшие место изменения сегмента ST полностью разрешились [75]. КГ той же больной (см. выше) через 1 час после введения тромболитика. Имевшие место изменения сегмента ST полностью разрешились [75].Рисунок 14. ЭКГ больного 69 лет, массивная ТЭЛА. ( 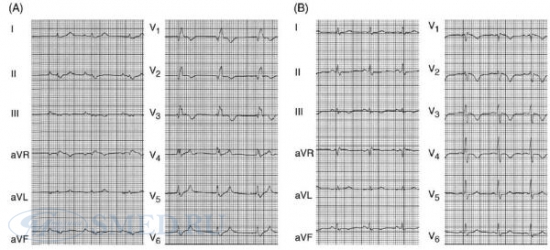 A) Отмечается снижение вольтажа желудочкового комплекса в стандартных отведениях, неопределяемая электрическая ось сердца, блокада правой ножки пучка Гиса с формированием комлпекса rsR׳ в отведениях с V 1 по V 4 , уширенных S в отведениях V 5 , V 6 . Эти признаки свидетельствуют об острой перегрузке и дилатации правого желудочка (что находится в соответствии с данными ЭхоКГ у того же больного). (B) После проведения тромболизиса отмечается явная положительная динамика ЭКГ: комплекс типа rSR׳ сохраняется только в отведении V 1 (что отражает уменьшение размеров правого желудочка согласно ЭхоКГ); инверсия зубцов Т в отведения с V 1 по V 4 (признаки уменьшившейся, но сохраняющейся перегрузки правого желудочка) [76]. A) Отмечается снижение вольтажа желудочкового комплекса в стандартных отведениях, неопределяемая электрическая ось сердца, блокада правой ножки пучка Гиса с формированием комлпекса rsR׳ в отведениях с V 1 по V 4 , уширенных S в отведениях V 5 , V 6 . Эти признаки свидетельствуют об острой перегрузке и дилатации правого желудочка (что находится в соответствии с данными ЭхоКГ у того же больного). (B) После проведения тромболизиса отмечается явная положительная динамика ЭКГ: комплекс типа rSR׳ сохраняется только в отведении V 1 (что отражает уменьшение размеров правого желудочка согласно ЭхоКГ); инверсия зубцов Т в отведения с V 1 по V 4 (признаки уменьшившейся, но сохраняющейся перегрузки правого желудочка) [76].
Рентгенография грудной клетки – метод, обладающий невысокой чувствительностью и специфичностью в отношении диагностики ТЭЛА. По мнению большинства современных авторов, основная ценность бесконтрастной рентгенографии состоит в исключении других состояний, имеющих сходную с легочной эмболией клиническую картину (пневмоний, опухолей, пневмоторакса, отека легких и др.). Рентгенограммы могут оказать помощь в интерпретации перфузионных сцинтиграмм легких (рис. 16,17). В ряде случаев удается поставить диагноз по результатам бесконтрастной рентгенографии, однако отсутствие патологии ни в коей мере не исключает легочной эмболии, в том числе так называемой массивной [64, 77]. В большинстве случаев ТЭЛА сопровождается появлением на рентгенограмме малоспецифичных рентгенологических признаков: высокое стояние купола диафрагмы на стороне поражения; инфильтрация легочной ткани (спустя 12–36 ч от начала заболевания); выбухание конуса легочной артерии; увеличение правых отделов сердца; расширение верхней полой вены и др. Эти признаки лишь с определенной степенью вероятности могут быть ассоциированы с возникновением ТЭЛА, причём только в тех случаях, когда они сочетаются с описанными клиническими симптомами эмболии (внезапно наступающей одышкой, болями в грудной клетке и т.д.). Более специфичным, но относительно редким признаком ТЭЛА является симптом Вестермарка (рис. 16) – обеднение легочного рисунка в области поражения, что свидетельствует о массивной эмболии легочной артерии. Этот рентгенологический признак встречается не более чем у 5% больных ТЭЛА. Довольно редко на рентгенограммах можно обнаружить классические признаки инфаркта легкого – треугольную тень в легочном поле, основанием обращенную к плевре (рис. 18)[51]. Схема рентенографических признаков ТЭЛА представлена на рисунке 15. Р 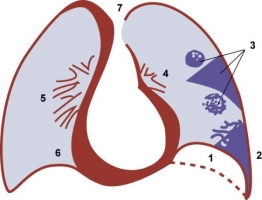 исунок 15. Рентгенологические признаки лёгочной эмболии (схема Heinrich F., 1981 г): 1 – высокое стояние купола диафрагмы; 2 – плевральный выпот; 3 – инфаркт лёгкого; 4 – «обрыв» контуров сосудов у корня лёгкого; 5 – гиперемия контрлатерального лёгкого; 6 – дилатация правого желудочка; 7 – дилатация непарной и верхней полой вен [62]. исунок 15. Рентгенологические признаки лёгочной эмболии (схема Heinrich F., 1981 г): 1 – высокое стояние купола диафрагмы; 2 – плевральный выпот; 3 – инфаркт лёгкого; 4 – «обрыв» контуров сосудов у корня лёгкого; 5 – гиперемия контрлатерального лёгкого; 6 – дилатация правого желудочка; 7 – дилатация непарной и верхней полой вен [62].Подробнее Выделяют следующие группы симптомов легочной эмболии:
Из перечисленных наиболее специфичны симптомы острого легочного сердца, к которым относятся указанные в порядке убывания чувствительности: расширение верхней полой вены, тени сердца, конуса легочной артерии. Верхнюю полую вену считают расширенной при увеличенном более 3 см расстоянии между линией остистых отростков и правым контуром средостения. Расширение конуса легочной артерии проявляется сглаживанием талии сердца или (более отчетливо) проступанием второй дуги за левый контур. Изменения корней легких могут выражаться в виде:
При эмболии в одну из главных ветвей легочного ствола или в смежные долевые или сегментарные ветви в случае отсутствия выраженной фоновой легочной патологии может наблюдаться обеднение легочного рисунка или обрыв окклюдированного сосуда. Эти симптомы лучше выявляются на томограммах. Описаны и другие симптомы эмболии; “включенные” сосуды, очаговоподобные тени, "хаотический" легочный рисунок, однако эти симптомы имеют меньшее значение, так как первый из них наблюдается только при развитии инфаркта легкого, а последние два неспецифичны. Диагностика легочной эмболии по рентгенологическим симптомам инфаркта легкого наиболее достоверна, но несвоевременна. Хотя высокому стоянию купола диафрагмы и дисковидным ателектазам легочной ткани не всегда сопутствует развитие инфаркта легкого, патогенетическая связь этих симптомов с последним осложнением оправдывает их обсуждение в данном разделе. Высокое стояние купола диафрагмы на стороне поражения (чаще справа), наиболее вероятно, обусловлено рефлекторным сморщиванием легкого в ответ на эмболию. Не исключено также участие в развитии этого симптома таких факторов, как поражение диафрагмальной плевры, уменьшенное кровенаполнение пораженного сегмента или доли, увеличение печени вследствие сердечной недостаточности, а также рефлекторное влияние на диафрагмальный и возвратный нервы. Ателектаз легкого, в основном дисковидный, часто предшествует развитию инфаркта в данной зоне. В качестве патогенетического механизма развития этого симптома предполагают увеличение количества бронхиальной слизи, появление геморрагического секрета с обструкцией бронха, ишемическую потерю сурфактанта. Рентгенологическая картина инфаркта легкого может ограничиваться признаками плеврального выпота с высоким стоянием купола диафрагмы на этой же стороне. Объем выпота может варьировать от нескольких миллилитров до 1 — 2 л. Небольшой выпот лучше виден в заднем рёберно-диафрагмальном синусе на боковых рентгенограммах. Эти симптомы хотя и часто наблюдаются при легочной эмболии, но не специфичны. Типичную картину инфаркта легкого удается обнаружить не ранее 2-го дня заболевания и приблизительно лишь у 10% больных, перенесших легочную эмболию. Это осложнение чаще развивается после эмболии в дистальные отделы легочного русла. Типичная картина инфаркта легкого включает достаточно четко очерченное затемнение треугольной формы с основанием, расположенным на плевральной поверхности,и усеченной или выпуклой вершиной, направленной в сторону ворот. Однако из-за инфильтрации окружающей зону инфаркта легочной ткани затемнение может принимать округлую или неправильную форму, что затрудняет дифференциальную диагностику с опухолевыми и воспалительными заболеваниями. Возможны и множественные атипичные инфаркты легких, дифференциальная диагностика которых наиболее затруднена. В большинстве случаев обратное развитие инфарктов легкого начинается с его основания и происходит в течение 2 — 4 недель. Иногда в исходе инфаркта легкого развивается линейный рубец или локальный пневмосклероз. Причинами затруднений при диагностике легочной эмболии методом бесконтрастной рентгенографии являются [64]:
Рисунки 16 и 17. Рентгенограмма грудной клетки пациента 58 лет, обратившегося с жалобами на одышку и повторные потери сознания. Р 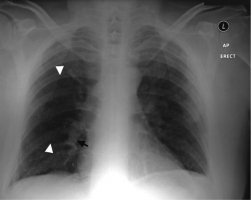 исунок 16. Высокое стояние левого купола диафрагмы. В правом лёгком визуализируется область обеднённого кровотока (между белыми стрелками) - симптом Вестермарка, а также выбухание правой нисходящей лёгочной артерии (чёрная стрелка) - симптом Палла. При перфузионной сцинтиграфии лёгких выявлены множественные двусторонние дефекты наполнения (см. рисунок 17), один из которых соответствует зоне олигемии на рентгенограмме. Таким образом, диагностирована ТЭЛА [78]. исунок 16. Высокое стояние левого купола диафрагмы. В правом лёгком визуализируется область обеднённого кровотока (между белыми стрелками) - симптом Вестермарка, а также выбухание правой нисходящей лёгочной артерии (чёрная стрелка) - симптом Палла. При перфузионной сцинтиграфии лёгких выявлены множественные двусторонние дефекты наполнения (см. рисунок 17), один из которых соответствует зоне олигемии на рентгенограмме. Таким образом, диагностирована ТЭЛА [78].Р 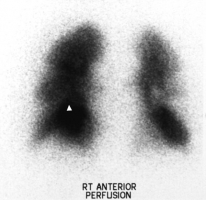 исунок 17. Перфузионная сцинтграмма лёгких в прямой проекции того же больного (см. рисунок 16). Множественные дефекты перфузии. Белой стрелкой показан дефект перфузии, соответствующий области обеднённого кровотока при рентгенографии грудной клетки [78]. исунок 17. Перфузионная сцинтграмма лёгких в прямой проекции того же больного (см. рисунок 16). Множественные дефекты перфузии. Белой стрелкой показан дефект перфузии, соответствующий области обеднённого кровотока при рентгенографии грудной клетки [78].Рисунок 18. Классическая рентгенографическая картина инфаркта лёгкого. К 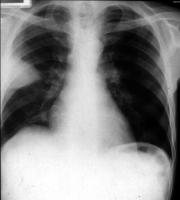 линовидная тень в правом лёгочном поле, основанием обращённая к плевре и верхушкой – к корню лёгкого. линовидная тень в правом лёгочном поле, основанием обращённая к плевре и верхушкой – к корню лёгкого.
Среди лабораторных показателей в диагностике ТЭЛА существенное место занимает уровень D-димера . Интерпретации результатов этого анализа посвящён специальный раздел. Кроме того, для оценки прогноза ТЭЛА имеет значение определение концентрации сердечных тропонинов и мозгового натрийуретического пептида (см. раздел «стратификация риска и прогноз» ). При анализе газового состава крови наиболее частый признак ТЭЛА — падение парциального напряжения кислорода в артериальной крови, что наблюдается уже при окклюзии 13% лёгочного сосудистого русла. Также свойственно развитие гипокапнии и респираторного алкалоза за счёт компенсаторной гипервентиляции [20]. Гиперкапния (повышение PaCO2) возможна в крайне тяжёлых случаях, вследствие отёка лёгких (см. раздел «нарушение газообмена в лёгких» ). Нормальные показатели газового состава крови не исключаеют диагноза ТЭЛА [62]. Все остальные лабораторные показатели при диагностике ТЭЛА являются вспомогательными. При развитии инфаркта лёгких может отмечаться умеренная гипербилирубинемия, лейкоцитоз и повышение СОЭ. Активность аминотрансфераз и креатинфосфокиназы обычно не изменяется, что имеет большое значение при дифференциальной диагностике ТЭЛА с инфарктом миокарда [63]. Возможно повышение уровней ЛДГ, ЩФ. Появление протеинурии и микрогематурии может быть обусловлено гипоксией и нарушенной почечной гемодинамикой [62].
D-димер является продуктом деградации фибрина. Его плазменный уровень повышается при тромбообразовании, так как всегда одновременно активируется фибринолитическая система ( рисунок 2 ). Таким образом, нормальный уровень D-димера делает диагноз ТЭЛА или тромбоза глубоких вен (ТГВ) маловероятным, то есть предсказательная ценность отрицательного результата высока. С другой стороны, фибрин может образоваться при ряде других патологических состояний, таких как злокачественные опухоли, воспаление, некрозы, расслаивающая аневризма аорты и др., то есть повышение уровня D-димера неспецифично для ТЭЛА, и положительный результат обладает низкой предсказательной ценностью в её диагностике. Кроме того, специфичность повышения D-димера для ТЭЛА снижается при беременности и с возрастом, составляя < 10% у больных старше 80 лет. Нормальный уровень D-димера у больных ТЭЛА невысокого риска при клинически высокой вероятности не позволяет надёжно исключить ТЭЛА, поэтому в данной группе больных проведение анализа на D-димер не рекомендуется. ТЭЛА высокого риска (то есть с развитием шока или артериальной гипотонии) – жизнеугрожающее состояние, требующее проведения экстренной дифференциальной диагностики и неотложного лечения; решающее значение при этом имеют спиральная КТ-ангиография грудной клетки и ЭхоКГ, а не измерение уровня D-димера. Таким образом, при подозрении на ТЭЛА определение уровня D-димера показано в группе невысокого риска при клинически низкой или промежуточной вероятностях. В этих категориях больных измерение D-димера выполняет роль «сортировочного» метода обследования: его повышение не дает возможности подтвердить диагноз ТЭЛА, однако нормальный уровень позволяет достоверно исключить её и своевременно направить диагностический поиск в другом направлении (см. раздел алгоритмы диагностики ТЭЛА , рис. 43, таблица 17) [50]. На диагностическую значимость D-димера влияет чувствительность анализа (таблица 17). К высокочувствительным методам относится количественный твёрдофазный ИФА (ELISA). Количественные методы латексной агглютинации и методы, основанные на агглютинации эритроцитов в цельной крови, считаются умеренно чувствительными. Нормальный уровень D-димера, определённый высокочувствительным методом, надёжно исключает ТЭЛА в группе невысокого риска при клинически низкой или промежуточной вероятности, в то время как использование умеренно чувствительных методов позволяет исключить ТЭЛА только у больных с клинически низкой вероятностью. При использовании двухуровневой схемы оценки клинической вероятности по шкале Wells (табл. 8), в категории «ТЭЛА маловероятна» нормальный уровень D-димера надёжно исключает ТЭЛА независимо от чувствительности метода [41, 43].
В 90% случаев лёгочной эмболии источником являются тромбы в глубоких венах нижних конечностей. При венографии ТГВ у больных с подтверждённой ТЭЛА обнаруживался в 70% случаев [41]. Хотя «золотым стандартом» диагностики тромбоза глубоких вен по-прежнему считается венография (контрастная флебография, илеокаваграфия), это инвазивное и технически сложное исследование редко применяется на практике [62, 83]. Сегодня дуплексное УЗИ (с компрессионными пробами) глубоких вен нижних конечностей практически вытеснило венографию. Чувствительность УЗИ в диагностике проксимального ТГВ превышает 90% при специфичности около 95%. Среди больных ТЭЛА ультразвуковые признаки ТГВ выявляются у 30-50%. Обнаружение проксимального тромбоза глубоких вен является достаточным основанием для назначения антикоагулянтов при подозрении на ТЭЛА. Единственным надёжным УЗ-признаком тромбоза является неполная сжимаемость вен (при компрессионных пробах), в то время как воспроизводимость характеристик кровотока (допплеровское сканирование) не высока (рис. 19). Диагностическая значимость УЗИ повышается при полном сканировании (как проксимальных, так и дистальных вен). По данным недавно проведённого исследования, полное сканирование в сравнении с УЗИ только проксимальных вен повышало процент выявления ТГВ у больных ТЭЛА с 22% до 43%. В то же время специфичность снижалась с 96% до 84%. В другом исследовании проксимальный ТГВ по данным УЗИ определялся в 39% случаев (чувствительность) подтверждённой при МСКТ ТЭЛА, специфичность УЗИ при этом составила 99%. При подозрении на ТЭЛА вероятность УЗ-обнаружения тромбов в проксимальных венах выше у больных с яркой клинической картиной ТГВ, чем при бессимптомном его течении [41, 63]. Недавно показано, что после однократной внутривенной инъекции контрастного вещества можно последовательно выполнить КТ грудной клетки и через 3-4 минуты КТ-венографию (непрямую). Чувствительность КТ грудной клетки при этом повышается с 83% до 90%, специфичность же не меняется (95%). Однако соответствующего повышения предсказательной ценности отрицательного результата не наблюдалось. Таким образом, КТ-венография незначительно повышает чувствительность при подозрении на ТЭЛА, однако существенно увеличивает лучевую нагрузку, что нужно учитывать, особенно у молодых женщин [41, 77]. Однако возможности УЗИ для визуализации подвздошных и нижней полой вен ограничены, также затруднения возникают при обследовании больных с ожирением или имеющих нестандартную анатомию венозной системы. При необходимости оценки кровотока по тазовым венам и венам брюшной полости, особенно для решения вопроса о постановке кава-фильтра, непрямая КТ-венография может дать очень ценную информацию (рис. 20 и 21). МР-венография (рис. 22) обладает высокой чувствительностью и специфичностью в диагностике тромбоза глубоких вен, однако это дорогостоящий метод исследования, быстрота его выполнения уступает УЗИ и КТ-венографии. МР-венография является методом выбора при наличии технических сложностей для УЗИ у больных с аллергией на йод-содержащие контрастные препараты или страдающих почечной недостаточностью [31, 77, 81]. Итак, место УЗИ глубоких вен нижних конечностей в диагностике ТЭЛА до сих пор обсуждается. Это исследование должно применяться в качестве «страховочного» метода для уменьшения частоты ложноотрицательных результатов, которые могут быть получены при проведении контрастной ОСКТ грудной клетки (см. алгоритмы диагностики, рис. 42, 43, табл. 17). Применение УЗИ глубоких вен также целесообразно при наличии противопоказаний к проведению КТ (нежелательность облучения, непереносимость контрастных препаратов). Учитывая небольшую дополнительную диагностическую значимость при существенном повышении лучевой нагрузки, выполнение непрямой КТ-венография не рекомендуется в качестве дополнительного обследования к МСКТ грудной клетки [41]. Рисунок 19. Ультразвуковая допплерография вен левой нижней конечности (поперечный срез). С 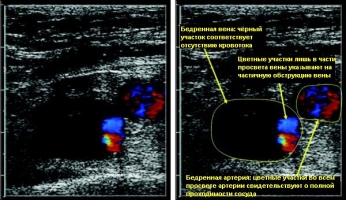 верху вниз – переход от кожи в глубину бедра. На правом рисунке бедренные вена и артерия обведены жёлтыми кружками (диаметр вены больше). Поток, направленный в сторону датчика, изображается красным цветом, от датчика – синим. Наличие красного и синего цвета в одном сосуде говорит о турбулентном кровотоке. В бедренной вене кровоток занимает около 20% просвета сосуда, остальные 80% окрашены в чёрный цвет – отсутствие кровотока. Кроме того, бедренная вена в этой области несжимаема (компрессионная проба). Данные соответствуют тромбозу бедренной вены [83]. верху вниз – переход от кожи в глубину бедра. На правом рисунке бедренные вена и артерия обведены жёлтыми кружками (диаметр вены больше). Поток, направленный в сторону датчика, изображается красным цветом, от датчика – синим. Наличие красного и синего цвета в одном сосуде говорит о турбулентном кровотоке. В бедренной вене кровоток занимает около 20% просвета сосуда, остальные 80% окрашены в чёрный цвет – отсутствие кровотока. Кроме того, бедренная вена в этой области несжимаема (компрессионная проба). Данные соответствуют тромбозу бедренной вены [83].Рисунки 20 и 21. КТ-исследования: женщина 31 года, поступила с жалобами на остро возникший отёк правой ноги и одышку. В анамнезе – приём пероральных контрацептивов. Р 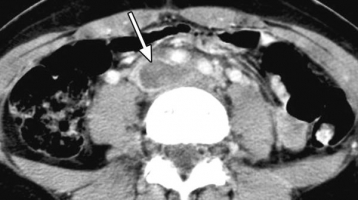 исунок 20. КТ таза с контрастным усилением, венозная фаза исследования; тромбоз дистальной части нижней полой вены (стрелка) [81]. исунок 20. КТ таза с контрастным усилением, венозная фаза исследования; тромбоз дистальной части нижней полой вены (стрелка) [81].Р 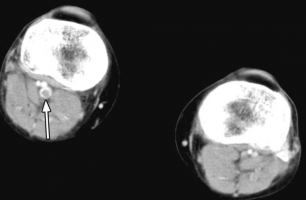 исунок 21. Тот же случай. (см. рис. 20). При КТ-венографии выявляется тромбоз правой подколенной вены (стрелка) [81]. исунок 21. Тот же случай. (см. рис. 20). При КТ-венографии выявляется тромбоз правой подколенной вены (стрелка) [81].Рисунок 22. Магнитно-резонансная ангиография, TOF, фронтальный срез. О 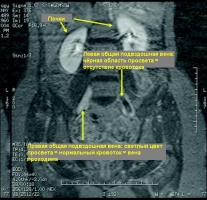 тсутствие кровотока по левой общей подвздошной вене (чёрный цвет – полная обструкция). Правая общая подвздошная вена проходима (белый цвет) [83]. тсутствие кровотока по левой общей подвздошной вене (чёрный цвет – полная обструкция). Правая общая подвздошная вена проходима (белый цвет) [83].
Вентиляционно-перфузионная сцинтиграфия – надёжный и безопасный (описано лишь несколько случаев аллергических реакций) метод диагностики при подозрении на ТЭЛА. Перфузионная сцинтиграфия (пульмоносцинтиграфия) основана на внутривенном введении меченных изотопами 99m Tc макроагрегатов альбумина, которые накапливаются в капиллярном русле лёгких, делая возможной оценку тканевого кровотока. Изображение получают с помощью гамма-камеры в 6 стандартных проекциях (передняя, задняя, левая боковая, левая передняя косая, правая боковая, правая передняя косая). В случае окклюзии лёгочных артерий, в периферическое капиллярное русло частицы не поступают, что создаёт характерную картину дефекта перфузии - «холодную зону». Лучевая нагрузка при проведении исследования с меченными 99m Tc макроагрегатами альбумина составляет в среднем 1.1 мЗв, что значительно меньше, чем при проведении КТ (2-6 мЗв). Для сравнения, лучевая нагрузка при обычной ренгтенографии лёгких составляет 0,05 мЗв. Метод перфузионной сцинтиграфии даёт возможность изучить региональную легочную гемодинамику, что может быть использовано для диагностики ТЭЛА. Он отличается высокой чувствительностью, но недостаточно специфичен, поскольку многие патологические процессы в лёгких сопровождаются региональным снижением перфузии (опухоли лёгкого, пневмонии, обструктивные заболевания лёгких, пневмосклероз, ателектаз, эмфизема и кисты лёгких, гидроторакс, гипоплазия лёгочных сосудов, их артериит и т.д.) [51, 52]. Следовательно, несмотря на высокую чувствительность, диагностика тромбоэмболии лёгочной артерии с помощью перфузионной сцинтиграфии лёгких возможна только в контексте клинической картины и при учёте данных других методов исследования [52]. С целью повышения специфичности перфузионная сцинтиграфия может дополняться вентиляционным сканированием (пневмосцинтиграфией), которое подразумевает ингаляции различных агентов: воздушно-газовой смеси, содержащей 81 Kr с очень коротким периодом полураспада (13 с), ксенона 133 Xe, аэрозоля, меченного 99m Tc, или частиц угля, связанных с 99m Tc (технегаз). Предпочтение следует отдавать не газообразным, а меченным 99m Tc агентам, так как они дольше задерживаются в бронхо-альвеолярном дереве, поэтому позволяют выполнить исследование в нескольких проекциях и более чётко оценить вентиляционно-перфузионные отношения. Однако более продолжительный период их полураспада требует значительного интервала времени между проведением перфузионного и вентиляционного сканирования легких. Вентиляционная сцинтиграфия позволяет выявить зоны гиповентиляции. Гиповентиляция приводит к рефлекторной вазоконстрикции (рефлекс Эйлера-Лильестранда), благодаря чему поддерживается соответствие между вентиляцией и перфузией. Следовательно при локальной бронхиальной обструкции области снижения активности при перфузионной сцинтиграфии будут соответствовать зонам пониженной активности вентиляционной сцинтиграфии. При ТЭЛА в большинстве своём вентиляционная сцинтиграфия патологии выявлять не должна, а на перфузионной имеются дефекты (нарушение вентиляционно-перфузионных отношений – рисунок 23, 24) [52]. При оценке результатов вентиляционно-перфузионного сканирования часто используют четырёхуровневую классификацию из исследования PIOPED: норма, высокая вероятность ТЭЛА и недиагностические сканограммы (низкая и промежуточная вероятности). Под высокой вероятностью подразумевается выраженное несоответствие между значительно сниженной перфузией и нормальной или мало изменённой вентиляцией в двух и более сегментах лёгкого. Нормальные результаты вентиляционно-перфузионной сцинтиграфии лёгких надёжно исключают ТЭЛА; при высокой вероятности ТЭЛА по результатам V/Q сканирования диагноз считается подтверждённым. В то же время некоторые специалисты утверждают, что наличие вентиляционно-перфузионного несоответствия даже в 1 сегменте лёгкого достаточно для постановки диагноза. В некоторых клиниках проводят только перфузионное сканирование, заменяя вентиляционную фазу обычной рентгенографией лёгких (рис. 16, 17). При нарушении перфузии такой подход нежелателен. Он приемлем только при нормальных результатах рентгенографии - в таких случаях любые дефекты перфузии должны рассматриваться как вентиляционно-перфузионное несоответствие. Метод вентиляционно-перфузионной сцинтиграфии для диагностики ТЭЛА подвергается критике в связи с высокой частотой недиагностических результатов (с промежуточной вероятностью ТЭЛА), что требует дальнейшего обследования больного. Диагностическую ценность метода повышает оценка результатов в комплексе с определением клинической вероятности ТЭЛА (см. раздел «алгоритмы диагностики»). Недавно показано, что чувствительность метода повышается при регистрации изображения с помощью однофотонной эмиссионной компьютерной томографии. Итак, отсутствие дефектов перфузии на перфузионной сцинтиграмме лёгких надёжно исключает ТЭЛА. Сочетание клинически низкой вероятности ТЭЛА и недиагностических результатов (низкая и промежуточная вероятность) V/Q сцинтиграфии – приемлемый критерий исключения диагноза (хотя и с меньшей доказательной базой). Высокая вероятность ТЭЛА при V/Q сцинтиграфии позволяет установить диагноз, однако в группе больных с клинически низкой вероятностью тромбоэмболии требуется дальнейшее обследование. При всех других сочетаниях клинической вероятности ТЭЛА и результатов вентиляционно-перфузионной сцинтиграфии необходимо дальнейшее обследование (см. алгоритмы диагностики, таблица 17) [41]. Рисунки 23 и 24. Вентиляционно-перфузионная сцинтиграфия лёгких (вентиляционная – с аэрозолем, меченным 99m Tc, перфузионная – с меченными 99m Tc макроагрегатами альбумина) больной 71 года с жалобами на внезапно возникшую и нарастающую одышку. Р 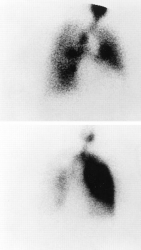 исунок 23. Вентиляционная сцинтиграмма в передней проекции (верхний рисунок) в норме. При перфузионной сцинтиграфии (нижний рисунок) отмечается практически полное отсутствие перфузии правого лёгкого. Массивная ТЭЛА (эмбол в правой лёгочной артерии) [79]. исунок 23. Вентиляционная сцинтиграмма в передней проекции (верхний рисунок) в норме. При перфузионной сцинтиграфии (нижний рисунок) отмечается практически полное отсутствие перфузии правого лёгкого. Массивная ТЭЛА (эмбол в правой лёгочной артерии) [79].Р 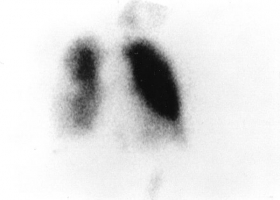 исунок 24. Перфузионная сцинтиграмма лёгких в прямой проекции той же больной (см. рис. 23) через 2 дня после катетерной эмолэктомии. Отмечается восстановление перфузии правого лёгкого. Остающийся небольшой субсегментарный дефект накопления может быть следствием дистальной эмболизации из правой главной лёгочной артерии [79]. исунок 24. Перфузионная сцинтиграмма лёгких в прямой проекции той же больной (см. рис. 23) через 2 дня после катетерной эмолэктомии. Отмечается восстановление перфузии правого лёгкого. Остающийся небольшой субсегментарный дефект накопления может быть следствием дистальной эмболизации из правой главной лёгочной артерии [79].
При подозрении на ТЭЛА компьютерная томография грудной клетки выполняется после введения контрастного препарата в периферическую вену (исследование с контрастным усилением, КТ-ангиография). КТ-ангиография в последнее время стала основным методом визуализации при подозрении на ТЭЛА [41]. По сравнению с ангиопульмонографией, которая считается золотым стандартом диагностики ТЭЛА, выполнение КТ проще, требует меньше времени и персонала, а по информативности КТ-ангиография как минимум не уступает селективной ангиопульмонографии [31, 41]. Для КТ-сканирования грудной клетки достаточно однократной задержки дыхания (рис. 25, 26). При сравнении с вентиляционно-перфузионной сцинтиграфией КТ-ангиография представляется более объективным методом диагностики (меньше расхождений в интерпретации результатов разными врачами лучевой диагностики). Другим преимуществом КТ с контрастным усилением как по отношению к ангиопульмонографии, так и к вентиляционно-перфузионной сцинтиграфии, является визуализация средостения и лёгочной паренхимы и, следовательно, возможность постановки альтернативного диагноза (пневмония, опухоли лёгких, плевральный выпот, пневмоторакс, увеличение внутригрудных лимфоузлов, разрыв пищевода, расслоение аорты, переломы рёбер и костные метастазы) в отсутствие ТЭЛА. Кроме того, КТ-ангиография позволяет выявить дилатацию правого желудочка, что свидетельствует о тяжёлом течении заболевания (рис. 33) [31, 80]. После однократного введения контрастного препарата помимо КТ грудной клетки можно провести КТ-венографию (см. раздел «диагностика ТГВ» , рис. 20, 21). Есть у КТ-ангиографии грудной клетки и свои недостатки. Могут возникать сложности с визуализацией не вертикально расположенных артерий (особенно язычковых сегментов и средней доли). Обструкция верхней полой вены, а также наличие внутрилёгочных и внутрисердечных шунтов могут приводить к ложноотрицательным результатам КТ-ангиографии. Признаки ТЭЛА порой симулируются слизистыми пробками в бронхах, периваскулярным отёком при левожелудочковой недостаточности, локальным повышением сосудистого сопротивления в области ателектазов или инфильтрации лёгких, анатомическими структурами – аксиальными срезами бифуркции сосудов, прикорневыми лимфоузлами; если между введением контраста и началом сканирования лёгких не прошёл некоторый промежуток времени, неполное заполнение сосудов контрастом иногда расценивается как дефект наполнения (ложноположительные результаты) [31, 80]. Прямыми признаками ТЭЛА при КТ-ангиографии являются [80]:
К непрямым признакам относятся [81]:
Значимость для диагностики ТЭЛА односпиральной компьютерной томографии (ОСКТ) и мультиспиральной компьютерной томографии (МСКТ) следует рассматривать отдельно. Чувствительность ОСКТ при ТЭЛА составляет около 70%, специфичность – 90%. Частота получения неинформативных томограмм (артефакты движения, недостаточное контрастирование лёгочных сосудов) составляет 5-8% (аналогична показателю при ангиопульмонографии). Таким образом, отсутствие признаков ТЭЛА при ОСКТ не позволяет исключить этот диагноз. Однако сочетание отрицательных результатов ОСКТ с отсутствием УЗ-признаков проксимального ТГВ надёжно исключает ТЭЛА (см. раздел алгоритмы диагностики, таблица 17). С введением в клиническую практику мультиспиральных компьютерных томографов, МСКТ с контрастным усилением стала методом выбора для визуализации лёгочных сосудов при подозрении на ТЭЛА. При исследовании на четырёхспиральном компьютерном томографе чувствительность составляет 83%, специфичность – 96%. Следует подчеркнуть необходимость анализа результатов КТ в совокупности с оценкой клинической вероятности диагноза. У больных с низкой или промежуточной клинической вероятностью ТЭЛА (по шкале Wells), предсказательная ценность отрицательного результата МСКТ составляет 96% и 89% соответственно, резко снижаясь (до 60%) при высокой клинической вероятности. И наоборот, предсказательная ценность положительного результата МСКТ составила 92%-96% у больных с промежуточной и высокой клинической вероятностью, и лишь 58% - при низкой клинической вероятности ТЭЛА. В редких случаях подобного несоответствия результатов МСКТ и клинической вероятности ТЭЛА врач должен особенно внимательно подойти к диагнозу. Необходимый объём дополнительного обследования (УЗИ глубоких вен и/или вентиляционно-перфузионная сцинтиграфия или ангиопульмонография) при высокой клинической вероятности ТЭЛА, но отрицательных результатах МСКТ до сих пор остаётся предметом споров. Продолжение обследование может обсуждаться для части больных при низкой клинической вероятности, но положительной МСКТ [41]. Точность спиральной КТ при наличии тромбов в субсегментарных артериях явно ниже, чем при их локализации в главных, долевых и сегментарных артериях. Наличие нормальной спиральной КТ не исключает полностью ТЭЛА в субсегментарный сосуд [52]. При подозрении на ТЭЛА изолированное поражение субсегментарного сосуда с помощью МСКТ обнаруживается в 1-5%. В подобных случаях целесообразно выполнить УЗИ глубоких вен нижних конечностей: обнаружение ТГВ делает назначение терапии обоснованным; определённых рекомендаций при отсутствии ТГВ нет за неимением доказательной базы. Таким образом, визуализация тромба в сегментарных и более крупных лёгочных артериях при ОСКТ и МСКТ в большинстве случаев позволяет поставить достоверный диагноз ТЭЛА, в то время как необходимость лечения при выявлении тромба в субсегментарном сосуде при отсутствии УЗ-признаков проксимального ТГВ дискутабельна. У больных с клинически невысокой вероятностью тромбоэмболии для исключения ТЭЛА отрицательный результат ОСКТ следует подкрепить отсутствием УЗ-признаков ТГВ; в тех же условиях негативный результат МСКТ достоверно исключает диагноз без дополнительного обследования. Показано ли продолжение обследования в редких случаях негативных результатов МСКТ при клинически высокой вероятности ТЭЛА, до сих пор не ясно (см. раздел алгоритмы диагностики, рис. 42, 43, таблица 17) [41]. Рисунки 25 и 26. КТ-ангиография грудной клетки больного 44 лет, поступившего в полуобморочном состоянии с жалобами на выраженную одышку. Р 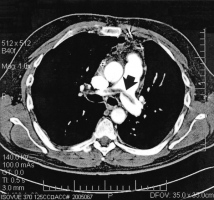 исунок 25. Определяется крупный эмбол в области бифуркации ствола лёгочной артерии («седловидный» эмбол). Массивная ТЭЛА [73]. исунок 25. Определяется крупный эмбол в области бифуркации ствола лёгочной артерии («седловидный» эмбол). Массивная ТЭЛА [73].Р 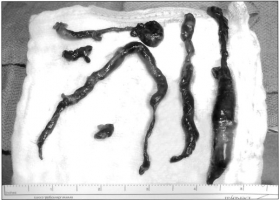 исунок 26. Тот же случай (см. рис. 25). Эмболы, извлечённые при успешной эмболэктомии из лёгочных артерий (больной выжил, ближайший катамнез без существенных проблем). V-образный эмбол извлечён из бифуркации лёгочного ствола (см. рис. 25). Линейка внизу градуирована в дюймах (1 дюйм = 2,54 см) [73]. исунок 26. Тот же случай (см. рис. 25). Эмболы, извлечённые при успешной эмболэктомии из лёгочных артерий (больной выжил, ближайший катамнез без существенных проблем). V-образный эмбол извлечён из бифуркации лёгочного ствола (см. рис. 25). Линейка внизу градуирована в дюймах (1 дюйм = 2,54 см) [73].Рисунок 27. КТ-ангиограмма грудной клетки; женщина 32 лет, поступившая с жалобой на боли в грудной клетки. О 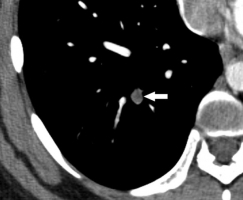 пределяется полностью окклюзирующий эмбол в артерии задне-базального сегмента нижней доли правого лёгкого (стрелка). Обращает на себя внимание расширение поражённой артерии по сравнению с контрастированными соседними [80]. пределяется полностью окклюзирующий эмбол в артерии задне-базального сегмента нижней доли правого лёгкого (стрелка). Обращает на себя внимание расширение поражённой артерии по сравнению с контрастированными соседними [80].Рисунок 28. КТ-ангиограмма грудной клетки, женщина 27 лет. Ц  ентрально расположенный эмбол в артерии задне-базального сегмента нижней доли правого лёгкого (стрелка) с чётким краем, полностью окружённый контрастным веществом (кольцо контрастного препарата, окружающее эмбол - симптом «polo mint»). Тромбы также определяются в субсегментарных артериях латерально-базального сегмента нижней доли правого лёгкого и задне-базального сегмента нижней доли левого лёгкого [82]. ентрально расположенный эмбол в артерии задне-базального сегмента нижней доли правого лёгкого (стрелка) с чётким краем, полностью окружённый контрастным веществом (кольцо контрастного препарата, окружающее эмбол - симптом «polo mint»). Тромбы также определяются в субсегментарных артериях латерально-базального сегмента нижней доли правого лёгкого и задне-базального сегмента нижней доли левого лёгкого [82].Рисунок 29. КТ-ангиограмма грудной клетки, реконструкция артерии задне-базального сегмента нижней доли правого лёгкого по серии срезов (см. рис. 28). С 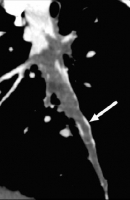 трелка указывает место поперечного, представленного на рисунке 28. Показано, что центральный дефект накопления (симптом «polo mint») возможен, только если тромбоэмбол распространяется с более проксимальных ветвей лёгочной артерии, либо фиксирован в определённых точках к стенке артерии [82]. трелка указывает место поперечного, представленного на рисунке 28. Показано, что центральный дефект накопления (симптом «polo mint») возможен, только если тромбоэмбол распространяется с более проксимальных ветвей лёгочной артерии, либо фиксирован в определённых точках к стенке артерии [82].Рисунок 30. КТ-ангиограмма грудной клетки; мужчина 66 лет, поступивший в стационар с жалобами на одышку и боль в грудной клетке. С 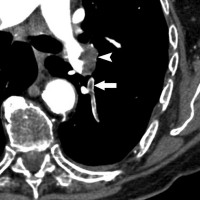 трелка – продольный срез сосуда, частичный дефект наполнения, окружённый контрастным веществом (“railway track” sign - «симптом железнодорожного пути»). Короткая стрелка – эмбол в левой главной лёгочной артерии [80]. трелка – продольный срез сосуда, частичный дефект наполнения, окружённый контрастным веществом (“railway track” sign - «симптом железнодорожного пути»). Короткая стрелка – эмбол в левой главной лёгочной артерии [80].Рисунок 31. КТ-ангиограмма грудной клетки; женщина 58 лет, поступившая с жалобами на боль в грудной клетке и одышку. В 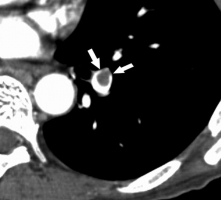 просвете артерии определяется эксцентрично расположенный дефект наполнения, образующий со стенкой сосуда острый угол и окружённый контрастным препаратом. Острая ТЭЛА [80]. просвете артерии определяется эксцентрично расположенный дефект наполнения, образующий со стенкой сосуда острый угол и окружённый контрастным препаратом. Острая ТЭЛА [80].Рисунок 32. Дополнительные КТ-ангиографические признаки ТЭЛА у больной 58 лет. У 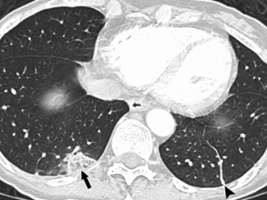 частки повышенной плотности клиновидной (стрелка) и линейной (короткая стрелка) формы, которые могут соответствовать инфаркту лёгкого [80]. частки повышенной плотности клиновидной (стрелка) и линейной (короткая стрелка) формы, которые могут соответствовать инфаркту лёгкого [80].Рисунок 33. ТЭЛА у пациента 42 лет, который поступил в стационар с тяжёлой одышкой и жалобами на боль в грудной клетке. П 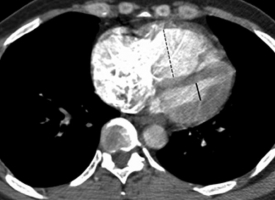 ри КТ-ангиографии грудной клетки выявлены признаки перегрузки правого желудочка: размер правого желудочка по короткой оси (пунктирная линия) превосходит размер левого желудочка (сплошная линия) [80]. ри КТ-ангиографии грудной клетки выявлены признаки перегрузки правого желудочка: размер правого желудочка по короткой оси (пунктирная линия) превосходит размер левого желудочка (сплошная линия) [80].
Селективная ангиопульмонография — это рентгенологический метод исследования сосудов легких и легочного кровотока, при котором контрастный препарат (уротраст, верографин, урографин и др.) вводится с помощью катетеров непосредственно в сосудистое русло лёгких. Для введения рентгеноконтрастного вещества в ствол легочной артерии, левую, правую или концевые (терминальные) ветви легочной артерии производят чрескожную катетеризацию бедренной вены по Сельдингеру и проводят катетер через правое предсердие и правый желудочек в легочную артерию и ее ветви [51]. Прямая ангиография позволяет визуализировать даже мелкие тромбы (1-2 мм в диаметре), хотя при субсегментарных эмболиях отмечаются расхождения в заключениях между врачами лучевой диагностики. Диагностические критерии острой ТЭЛА разработаны более 40 лет назад. К прямым ангиографическим признакам относятся полная обструкция сосуда (его ампутация с вогнутым краем столба контрастного вещества) или дефект наполнения (рис. 34, 35, 36, 37). Косвенные признаки ТЭЛА включают медленное течение контраста, региональную гипоперфузию и замедление или уменьшение венозного кровотока. Однако наличие косвенных ангиографических признаков в отсутствие прямых не позволяет поставить диагноз ТЭЛА [41, 52]. Ангиопульмонография – инвазивный метод диагностики, её выполнение сопряжено с определённым риском. Смертность при ангиографии лёгочной артерии составляет 0,2% и в основном обусловлена проведением исследования у крайне тяжёлых больных с нестабильной гемодинамикой или острой дыхательной недостаточностью. Кроме того, если диагноз ТЭЛА поставлен с помощью ангиопульмонографии, и больному показан тромболизис, возрастает риск кровотечения из места введения катетера. Хотя ангиопульмонография является «золотым стандартом» постановки или исключения диагноза ТЭЛА, в настоящее время её проводят редко в связи с широким внедрением в клиническую практику не уступающей (а то и превосходящей) по информативности неинвазивной компьютерной томографии грудной клетки с контрастным усилением . Интерпретация результатов вентрикулографии правого желудочка сложна, этот метод оценки дисфункции ПЖ устарел и в повседневной клинической практике вытесняется эхокардиографией и определением уровня биомаркеров (см. раздел «стратификация риска и прогноз» ). Таким образом, выполнение ангиопульомнографии, чувствительного и специфичного, но инвазивного метода диагностики, показано, если неинвазивные методы или неинформативны или недоступны. Другим показанием является тяжёлое и/или быстро ухудшающееся состояние больного с сомнительным диагнозом ТЭЛА, когда проведение неинвазивных методик приведёт к ненужной трате времени. Если ангиопульмонография всё же выполняется (см. раздел алгоритмы диагностики, табл. 17), необходимо провести прямое измерение гемодинамических показателей (давление в правых отделах сердца, в лёгочной артерии) [41, 52]. Рисунки 34 и 35. Селективное ангиопульмонографическое и КТ-исследование мужчины 33 лет, который поступил в стационар с жалобами на внезапно появившуюся неделю назад и прогрессивно нарастающую одышку. Р 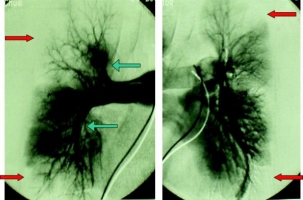 исунок 34. Селективная ангиопульмонография. Множественные двусторонние дефекты перфузии (красные стрелки). Дефекты наполнения в крупных ветвях лёгочной артерии (зелёные стрелки) [85]. исунок 34. Селективная ангиопульмонография. Множественные двусторонние дефекты перфузии (красные стрелки). Дефекты наполнения в крупных ветвях лёгочной артерии (зелёные стрелки) [85].Р 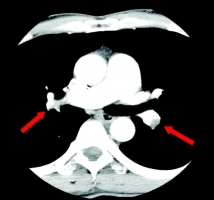 исунок 35. КТ-ангиография грудной клетки, тот же случай (см. рис. 34). Тромбы в главных ветвях лёгочной артерии [85]. исунок 35. КТ-ангиография грудной клетки, тот же случай (см. рис. 34). Тромбы в главных ветвях лёгочной артерии [85].Рисунок 36. Ангиопульмонограмма. К 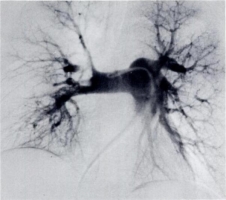 рупные дефект наполнения в правой лёгочной артерии [84]. рупные дефект наполнения в правой лёгочной артерии [84].Рисунок 37. Ангиопульмонограмма. Д 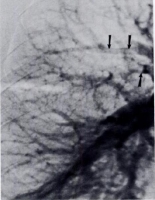 ефекты наполнения в сегментарных и субсегментарных артериях верхней доли правого лёгкого (стрелки) [84]. ефекты наполнения в сегментарных и субсегментарных артериях верхней доли правого лёгкого (стрелки) [84].
У 25% больных ТЭЛА при проведении эхокардиографии (ЭхоКГ) или КТ-ангиографии грудной клетки выявляется дилатация правого желудочка. Наличие изменений на ЭхоКГ используется при стратификации риска . Эхокардиографические критерии диагностики ТЭЛА отличаются в разных исследованиях. В основе их обычно лежит оценка размеров правого желудочка (рис. 38) и скорости регургитационного потока на трёхстворчатом клапане (рис. 39). В виду того, что чувствительность данного метода составляет 60–70%, отрицательный результат не исключает диагноз ТЭЛА. В то же время признаки перегрузки правого желудочка или его дисфункции могут возникать вследствие сопутствующих заболеваний сердца или лёгких при отсутствии ТЭЛА [41]. Если пациент с подозрением на развитие ТЭЛА находится в критическом состоянии, ЭхоКГ у постели больного – метод, позволяющий быстро сориентироваться в ситуации и выработать концепцию дальнейшего обследования и лечения (см. алгоритмы диагностики, рис. 42). У больных в состоянии шока или при выраженной артериальной гипотензии (ТЭЛА высокого риска) отсутствие эхокардиографических признаков перегрузки или дисфункции правого желудочка практически исключает ТЭЛА, как причину нестабильной гемодинамики. В случаях ТЭЛА невысокого риска ЭхоКГ служит главным образом для уточнения категории риска (промежуточный или низкий) [41]. Подробнее Критерии перегрузки ПЖ давлением (1 или более признаков [59, 60]):
При гипертрофии ПЖ (толщина свободной стенки более 7 мм) невозможно с уверенностью судить об остроте появления указанных признаков. Дополнительные признаки перегрузки правого желудочка давлением необходимы для снижения числа ложноположительных (относительно диагностики ТЭЛА) результатов у больных с гипо-акинезом свободной стенки правого желудочка вследствие инфаркта. Данных о специфичных эхокардиографических признаках ТЭЛА немного. В исследование Kurzyna M. с соавт [59] вошли 100 больных с яркой клинической картиной ТЭЛА, из которых 62-м требовалось лечение в отделение интенсивной терапии. Сравнивались три группы эхокардиографических критериев, которые могут использоваться для диагностики ТЭЛА (таблица 16). Критерии диагностики, которые основывались на нарушении выброса из правого желудочка (признак «60/60» - время ускорения кровотока в стволе лёгочной артерии ≤ 60 мс при градиенте давления на трикуспидальном клапане ≤ 60 мм рт. ст., рис. 39), либо на снижении сократительной способности свободной стенки правого желудочка в сравнении с его верхушкой (признак МакКоннелла) [58, 59], несмотря на сопутствующие сердечнососудистые и лёгочные заболевания, обладали более высокой прогностической ценностью, чем признаки перегрузки правого желудочка давлением. Гипо- или акинезия свободной стенки правого желудочка (напоминающая признак МакКоннелла) может развиться вследствие его инфаркта. Во избежание ошибочной диагностики ТЭЛА в этих случаях следует обращать внимание на признаки перегрузки правого желудочка давлением. Сделаны попытки использовать в диагностике ТЭЛА тканевой допплер, однако данные на этот счёт ограничены. Таблица 16. Диагностическая ценность трёх групп эхокардиографических признаков ТЭЛА у больных в зависимости от наличия сопутствующих заболеваний сердца и лёгких [41].
| ||||||||||||||||||||||||||||||||||||||||||||||||
