фарм. Фармакология 3 часть. Учебник Д. А. Харкевич. 12е изд., испр и доп. К кредиту 3
 Скачать 4.44 Mb. Скачать 4.44 Mb.
|
6-10 ч. Выделяется почками.
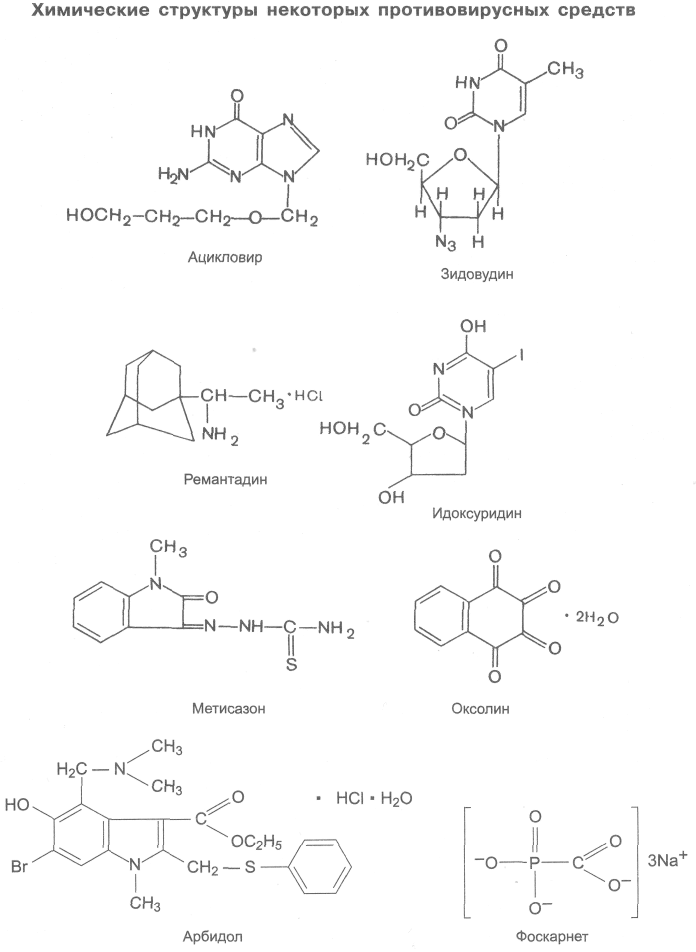
54%, т.е. существенно выше, чем у ацикловира). Это пролекарство; при первом его прохождении через кишечник и печень высвобождается ацикловир, который и обеспечивает противогерпетическое действие.Создание противовирусных средств — одна из наиболее сложных задач химиотерапии инфекций. Связано это с тем, что РНК- и ДНК-содержащие вирусы являются облигатными внутриклеточными паразитами. В процессе размножения вирусы в основном используют аппарат биосинтеза клеток макроорганизма, определенным образом модифицируя его. В связи с этим крайне трудно находить избирательно действующие средства, которые поражали бы вирусы, не повреждая клетки «хозяина». Однако некоторые вирусы (например, вирус простого герпеса, вирус опоясывающего лишая и др.) после проникновения в клетки индуцируют образование своих ферментов, которые могут отличаться от аналогичных ферментов самой клетки. К числу таких ферментов относится, например, ДНК-полимераза. Так, ациклогуанозин (ацикловир), проникая в клетку, фосфорилируется и в виде трифосфата угнетает ДНК-полимеразу вируса простого герпеса (в большей степени, чем ДНК-полимеразу клетки). Кроме того, это соединение встраивается в ДНК вируса. Рибавирин в виде 5-трифосфата специфически угнетает вирусную РНК-полимеразу. Показано, что азидотимидин ингибирует обратную транскриптазу вирионов ВИЧ-инфекции. Препараты пептидной структуры (саквинавир) избирательно ингибируют протеазы ВИЧ. Открыты противогриппозные средства, ингибирующие вирусный фермент нейраминидазу. Полученные данные весьма перспективны для создания новых избирательно действующих противовирусных средств. Направленность действия противовирусных средств может быть различной и касается разных стадий взаимодействия вируса с клеткой. Так, известны вещества, которые угнетают: 1) адсорбцию вируса на клетке и(или) проникновение его в клетку (γ-глобулин); 2) процесс высвобождения («депротеинизации») вирусного генома (мидантан, ремантадин); 3) синтез «ранних» вирусных белков-ферментов (гуанидин); 4) синтез нуклеиновых кислот (зидовудин, ацикловир, видарабин, идоксуридин и другие аналоги нуклеозидов); 5) синтез «поздних» вирусных белков (саквинавир); 6) «сборку» вирионов (метисазон). Кроме того, попадая в организм, вирусы вызывают образование клетками биологически активного гликопротеина интерферона и включение гуморального и клеточного звеньев иммунитета. Вирусные белки, являясь сильными антигенами, вызывают образование антител, нейтрализующих действие вирусов. Создание лекарственных средств, стимулирующих биосинтез интерферона и антителообразование, также перспективно в борьбе с вирусными инфекциями. Противовирусные вещества, которые применяют в качестве лекарственных средств, могут быть представлены следующими группами (подробнее см. в табл. 30.1). Синтетические средства Аналоги нуклеозидов — зидовудин, ацикловир, видарабин, ганцикловир, трифлуридин, идоксуридин Производные пептидов — саквинавир Производные адамантана — мидантан, ремантадин Производное индолкарбоновой кислоты — арбидол Производное фосфономуравьиной кислоты — фоскарнет Производное тиосемикарбазона — метисазон Биологические вещества, продуцируемые клетками макроорганизма Интерфероны Большая группа эффективных противовирусных средств представлена производными пуриновых и пиримидиновых нуклеозидов. Они являются антиметаболитами, ингибирующими синтез нуклеиновых кислот (см. табл. 30.1). В последние годы особенно большое внимание привлекли противоретровирусные препараты, к которым относятся ингибиторы обратной транскриптазы и ингибиторы протеаз. Повышенный интерес к этой группе веществ связан с их применением при лечении синдрома приобретенного иммунодефицита (СПИД). Вызывается он специальным ретровирусом — вирусом иммунодефицита человека (ВИЧ; HIV). Терапия СПИДа требует применения противоретровирусных, а также симптоматических средств.
Противоретровирусные препараты, эффективные при ВИЧ-инфекции, представлены следующими группами. 1. Ингибиторы обратной транскриптазы А. Нуклеозиды Зидовудин Диданозин Зальцитабин Ставудин Б. Ненуклеозидные соединения Невирапин Делавирдин Эфавиренц 2. Ингибиторы ВИЧ-протеазы Индинавир Ритонавир Саквинавир Нельфинавир Одним из противоретровирусных соединений является производное нуклеозидов азидотимидин (3-азидо-3-дезокситимидин), получивший название зидовудин (азидотимидин, ретровир). Принцип действия зидовудина заключается в том, что он, фосфорилируясь в клетках и превращаясь в трифосфат, ингибирует обратную транскриптазу вирионов, препятствуя образованию ДНК из вирусной РНК. Это подавляет синтез иРНК и вирусных белков, что и обеспечивает лечебный эффект. Препарат хорошо всасывается. Биодоступность значительная. Легко проникает через гематоэнцефалический барьер. Около 75% препарата метаболизируется в печени (образуется глюкуронид азидотимидина). Часть зидовудина выделяется в неизмененном виде почками (табл. 30.2). Применение зидовудина следует начинать возможно раньше. Его терапевтический эффект проявляется в основном в первые 6-8 мес от начала лечения. Зидовудин не излечивает больных, а лишь задерживает развитие заболевания. Следует учитывать, что к нему развивается устойчивость ретровируса. Из побочных эффектов на первое место выступают гематологические нарушения: анемия, нейтропения, тромбоцитопения, панцитемия. Возможны головная боль, бессонница, миалгия, угнетение функции почек. В отношении ВИЧ эффективен также ставудин (зерит). Он является синтетическим аналогом тимидина. В организме превращается в трифосфат, который и подавляет репликацию вирусов ВИЧ за счет ингибирования обратной транскриптазы и угнетения синтеза ДНК, иРНК и вирусных белков.
 Хорошо и быстро всасывается при энтеральном введении; биодоступность высокая. Быстро накапливается в плазме крови. С белками плазмы крови связывается в незначительной степени. Основная часть препарата и его метаболитов выделяется почками. Применяется для лечения ВИЧ-инфицированных больных после продолжительного использования зидовудина. Вводится энтерально. Из побочных эффектов отмечаются периферическая нейропатия, головная боль, лихорадка, диспепсические нарушения, анорексия, бессонница, аллергические реакции. Для лечения ВИЧ-инфекций, в том числе СПИДа, предложены также диданозин (видекс) и зальцитабин (хивид). Оба препарата ингибируют обратную транскриптазу вирусов. Из побочных эффектов чаще всего наблюдается периферическая нейропатия. Возможны обострение хронического панкреатита, анемия, лейкопения, тромбоцитопения, диспепсические явления, нарушения со стороны функции печени (для диданозина). Применяют эти препараты последовательно с зидовудином или в случае неэффективности последнего. Вводят внутрь. К этой же группе относятся ламивудин, абакавир (см. табл. 30.2). К ненуклеозидным противоретровирусным препаратам относятся невирапин (вирамун), делавирдин (рескриптор), эфавиренц (сустива). Они оказывают прямое неконкурентное ингибирующее действие на обратную транскриптазу. Связываются с этим ферментом в другом месте по сравнению с нуклеозидными соединениями. Имеются данные о том, что эти вещества оказывают блокирующее влияние на ДНК-полимеразу. Активно метаболизируются в печени цитохромом Р-450. Метаболиты выделяются почками. Применяются только при инфицировании ВИЧ-1. Из побочных эффектов чаще всего возникает кожная сыпь, повышается уровень трансаминазы. Для лечения ВИЧ-инфекции предложена новая группа препаратов — ингибиторы протеаз ВИЧ. Эти ферменты, регулирующие образование структурных белков и ферментов вирионов ВИЧ, необходимы для размножения ретровирусов. При недостаточном их количестве образуются незрелые предшественники вируса, что задерживает развитие инфекции. Аспартатпротеаза ВИЧ по структуре существенно отличается от аналогичных ферментов человека, что позволяет создавать препараты указанного типа с выраженной избирательностью противовирусного действия. К этой группе относятся производные пептидов — саквинавир (инвираза), нельфинавир (вирасепт), индинавир, ритонавир и др. Имеющиеся клинические данные свидетельствуют о выраженной противоретровирусной активности синтезированных ингибиторов ВИЧ-протеаз. Более широко исследован в клинике саквинавир (инвираза). Он является высокоактивным и избирательным ингибитором протеаз ВИЧ-1 и ВИЧ-2. Несмотря на низкую биодоступность препарата ( | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Таблица 30.3 Сравнительная характеристика некоторых ингибиторов ВИЧ-протеаз | ||||||||
| Препарат | Противовирусная активность | Биодоступность, % | Время накопления препарата и максимальных концентраций в плазме крови (Tmax), ч | Время «полужизни» (t1/2), ч. | Связывание с белками плазмы крови, % | Метаболизм в печени, % | Содержание в цереброспинальной жидкости, % | Выведение неизмененного препарата, % |
| Саквинавир | ++ | < 4-12 | 2-4 | 7-12 | 98 | >97 | < 1 | 1 |
| Нельфинавир | +++ | >78 | 2-4 | 3,5-5 | >98 | >78 | < 1 | 1-2 |
| Индинавир | +++ | 60-65 | 0,8 | 1,8 | 60-65 | 88-90 | 12 | 5-12 |
| Ритонавир | +++ | 66-75 | 2-4 | 3-5 | 98-99 | >95 | 1 | 3,5-5 |
К этой же группе относятся фамцикловир и его активный метаболит ганцикловир, сходные по фармакодинамике с ацикловиром.
Эффективным препаратом является также видарабин (аденин арабинозид). Проникнув в клетку, видарабин фосфорилируется. Угнетает вирусную ДНК-полимеразу. При этом подавляется репликация крупных ДНК-содержащих вирусов. В организме частично превращается в менее активный в отношении вирусов гипоксантина арабинозид.
Видарбин с успехом применяется при герпетическом энцефалите (вводят путем внутривенной инфузии), снижая летальность при этом заболевании на 30-75%. Иногда его используют при осложненном опоясывающем лишае. Эффективен при герпетическом кератоконъюнктивите (назначают местно в мазях). В последнем случае он в меньшей степени вызывает раздражение и меньше угнетает заживление роговицы, чем идоксуридин (см. ниже). Легче проникает в более глубокие слои ткани (при лечении герпетического кератита). Возможно применение видарабина при аллергических реакциях на идоксуридин и при неэффективности последнего.
Из побочных эффектов возможны диспепсические явления (тошнота, рвота, диарея), кожная сыпь, нарушения со стороны ЦНС (галлюцинации, психозы, тремор и др.), тромбофлебит на месте введения.
Местно используют трифлуридин и идоксуридин.
Трифлуридин является фторированным пиримидиновым нуклеозидом. Угнетает синтез ДНК. Применяется при первичном кератоконъюнктивите и возвратном эпителиальном кератите, вызванном вирусом простого герпеса (тип 1 и 2). Раствор трифлуридина наносят местно на слизистую оболочку глаза. Возможны преходящее раздражающее действие, отек век.
Идоксуридин (керецид, идуридин, офтан-IDU), являющийся аналогом тимидина, встраивается в молекулу ДНК. В связи с этим он подавляет репликацию отдельных ДНК-содержащих вирусов. Применяют идоксуридин местно при герпетической инфекции глаз (кератите). Может вызывать раздражение, отек век. Для резорбтивного действия малопригоден, так как токсичность у препарата значительная (подавляет лейкопоэз).
При цитомегаловирусной инфекции используют ганцикловир и фоскарнет. Ганцикловир (цимевен) является синтетическим аналогом 2-дезоксигуанозинового нуклеозида. По механизму действия сходен с ацикловиром. Угнетает синтез вирусной ДНК. Препарат применяют при цитомегаловирусном ретините. Вводят внутривенно и в полость конъюнктивы. Побочные эффекты наблюдаются часто; многие из них приводят к тяжелым нарушениям функций различных органов и систем. Так, у 20-40% пациентов отмечаются гранулоцитопения, тромбоцитопения. Нередки неблагоприятные неврологические эффекты: головная боль, острый психоз, судороги и др. Возможны развитие анемии, кожные аллергические реакции, гепатотоксическое действие. В экспериментах на животных установлено его мутагенное и тератогенное влияние.
В связи с тем что ганцикловир плохо всасывается при энтеральном введении, было создано пролекарство валганцикловир (вальцит). Последний хорошо и быстро всасывается из пищеварительного тракта. В кишечнике и печени под влиянием эстераз превращается в ганцикловир, который и оказывает противовирусное действие. При приеме внутрь биодоступность ганцикловира соответствует 5-9%, а при использовании валганцикловира — 60%.
Фоскарнет (фоскарвир) — производное фосфономуравьиной кислоты. Ингибирует ДНК-полимеразу вирусов. Применяется при цитомегаловирусном ретините у больных СПИДом. Используется также в случае неэффективности ацикловира при простом герпесе и опоясывающем лишае. Вводится внутривенно, так как плохо всасывается из пищеварительного тракта. В виде мази применяется также при герпесе, но менее эффективен, чем ацикловир. В целом фоскарнет переносится хуже, чем ганцикловир. Однако лейкопоэз угнетает в меньшей степени. Препарат нефротоксичен. Может вызвать гипокальциемию. При его применении могут возникать лихорадка, тошнота, рвота, диарея, головная боль, судороги.
Исходя из идеи создания так называемых «антисенсовых олигонуклеозидов», предложен первый препарат такого типа — витравен, рекомендованный для лечения ретинита при цитомегаловирусной инфекции.
Ряд препаратов эффективен в качестве противогриппозных средств.
Противовирусные препараты, эффективные при гриппозной инфекции, могут быть представлены следующими группами.
1. Ингибиторы вирусного белка М2
Ремантадин
Мидантан (амантадин)
2. Ингибиторы вирусного фермента нейраминидазы
Занамивир
Осельтамивир
3. Ингибиторы вирусной РНК-полимеразы
Рибавирин
4. Разные препараты
Арбидол
Оксолин
Первая группа относится к ингибиторам М2-белка. Мембранный белок М2, функционирующий в качестве ионного канала, обнаружен только у вируса гриппа типа А. Ингибиторы этого белка нарушают процесс «раздевания» вируса и препятствуют высвобождению в клетке вирусного генома. В итоге подавляется репликация вируса.
К этой группе относится мидантан (адамантанамина гидрохлорид, амантадин, симметрел). Хорошо всасывается из желудочно-кишечного тракта. Выделяется в основном почками.
Иногда препарат примененяется для профилактики гриппа типа А. В качестве лечебного средства малоэффективен. Более широко мидантан используется как противопаркинсоническое средство (см. главу 10). Вводят его внутрь.
Мидантан может оказывать отрицательное влияние на ЦНС (возникают повышенная возбудимость, сонливость, тремор, атаксия). Возможны диспепсические нарушения, кожные поражения.
Аналогичными свойствами, показаниями к применению и побочными эффектами обладает ремантадин (ремантадина гидрохлорид), сходный по химической структуре с мидантаном. У ремантадина t1/2 в 2 раза продолжительнее, чем у мидантана, и соответствует 24-30 ч. В меньшей степени, чем мидантан, препарат влияет на ЦНС. В связи с этим применяется значительно чаще, чем последний.
К обоим препаратам довольно быстро развивается резистентность вирусов.
Вторая группа препаратов ингибирует вирусный фермент нейраминидазу, которая представляет собой гликопротеин, образующийся на поверхности вирусов гриппа типа А и В. Этот фермент способствует попаданию вируса к клеткам-«мишеням» в респираторном тракте. Специфические ингибиторы нейраминидазы (конкурентное, обратимое действие) препятствуют распространению вируса, связанного с инфицированными клетками. Нарушается репликация вируса.
Одним из ингибиторов этого фермента является занамивир (реленца). Его применяют интраназально или ингаляционно (в порошке). При ингаляции препарата биодоступность соответствует примерно 15%. t1/2
| Препараты | ||
| Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
| Мидантан — Midantanum | Внутрь 0,1 г | Таблетки, покрытые оболочкой, по 0,1 г |
| Ремантадин — Remantadinum | Внутрь 0,05-0,1 г | Таблетки по 0,05 г |
| Идоксуридин — Idoxuridine | В полость конъюнктивы 2 капли 0,1% раствора | 0,1% раствор |
| Оксолин — Oxolinum | В полость конъюнктивы 1-2 капли 0,1-0,2% раствора, 0,25% мазь; для смазывания слизистой оболочки носа 0,25—0,5% мазь; наружно 1—3% мазь | Порошок; 0,25%; 0,5%; 1%; 2% и 3% мазь |
| Ацикловир — Acyclovir | Внутрь 0,2 г; внутривенно 5—10 мг/кг; накожно 5% мазь | Таблетки по 0,2 г; 5% мазь в тубах по 5 г; 3% глазная мазь в тубах по 4,5 или 5 г; во флаконах по 0,25 г |
| Валацикловир — Valacyclovir | Внутрь 0,5—1 г | Таблетки по 0,5 г |
| Ганцикловир — Gancyclovir | Внутривенные инфузии 0,005-0,006 г/кг | Лиофилизированный порошок во флаконах по 0,546 г ганцикловира натрия (соответствует 0,5 г ганцикловира основания) |
| Рибавирин — Ribavirin | Внутрь 0,2 г | Таблетки по 0,2 г |
| Зидовудин — Zidovudine | Внутрь 0,1-0, 2 г | Капсулы по 0,1 г |
| Арбидол — Arbidolum | Внутрь 0,1-0, 2 г | Таблетки по 0,025; 0,05 и 0,1 г |
| Амиксин — Amixinum | Внутрь 0,125-0, 25 г | Таблетки по 0,125 г |
