учебник. Учебник ФЛ - Виноградов, Каткова 2016. Учебник для медицинских и фармацевтических учреждений среднего профессионального образования Под
 Скачать 5.41 Mb. Скачать 5.41 Mb.
|
|
Часть рецептора, специфическим образом распознающая ацетилхолин, представляет собой выступающие над поверхностью мембраны участки длин- ной полипептидной цепи, которая пронизывает мембрану, как серпантин, 7 раз. G-белки — это многочисленная группа белков, в которой выделяют Gi (ингибиру- ющие аденилатциклазу), Gs (стимулирующие аденилатциклазу), Gq (активирую- щие фосфолипазу С), G0 (открывающие ионные каналы) и др. В форме, связанной с гуанозинтрифосфатом (ГТФ), G-белок регулирует активность мембранных фер- ментов (стимулирует или ингибирует) или ионного канала, действие прекращает- ся после гидролиза ГТФ. Затем в процесс передачи сигнала включаются так называемые вторичные внутриклеточные посредники (вторичные «мессенджеры»), такие как: продукты, образующиеся при гидролизе фосфолипазой С фосфолипидных компонентов (фосфоинозитидов) клеточной мембраны, — инозитолтрифосфат (ИТФ) и диацилглицерол (ДАГ), ионы кальция, выход которых из внутриклеточ- ных депо усиливает ИТФ; циклический аденозин-3,5-монофосфат (цАМФ), образующийся из АТФ под влиянием аденилатциклазы (активность этого фермента через M2-хо- линорецепторы снижается). Вторичные посредники переводят в активное состояние соответствующие фер- менты-протеинкиназы. Последние регулируют активность ряда внутриклеточных ферментов и белков, при этом возникают определенные сдвиги в метаболических процессах и функциональном состоянии клеток (рис. 11). Таким образом, различ- ные варианты и комбинации вторичных внутриклеточных посредников обеспе- чивают весь спектр реакций клеток в ответ на активацию разных рецепторов. Активация или блокада М-холинорецепторов будет приводить к тем или иным функциональным сдвигам в организме (см. табл. 25), изменениям обмена, которые обозначаются как фармакологические эффекты М-холиномиметиков и М-холиноблокаторов. N-холинорецепторы образованы, как правило, несколькими полипептидными субъединицами (2 альфа-цепи, 1 бета, 1 гамма и 1 дельта, каждая цепь пересекает мембрану 4 раза). Эти субъединицы образуют пентамер, в центре которого имеет- ся натриевый канал (рис. 10, Б). Для понимания механизма сопряжения N-холинорецепторов с функциями клеток необходимо знать, что в состоянии покоя мембрана имеет положительный заряд по наружной поверхности и отрицательный — по внутренней. Заряд обу- словлен различиями в распределении основных катионов по сторонам мембраны: содержание калия внутри клетки значительно больше, чем в окружающей клетку среде, а концентрация натрия — наоборот. Таким образом, цитоплазма весьма обогащена калием, тогда как ионы натрия с помощью специального транспортного механизма («натриевый насос») активно вытеснены из клетки, при этом ионы натрия «тянут» за собой анионы, которые собираются вдоль внутренней поверхности мембраны, обусловливая ее отрица- тельный заряд. Вытесненные же ионы натрия располагаются по наружной по- верхности мембраны, заряжая ее положительно. Молекулы ацетилхолина, связываясь с двумя альфа-субъединицами N-холинорецептора, способствуют открытию натриевого канала. 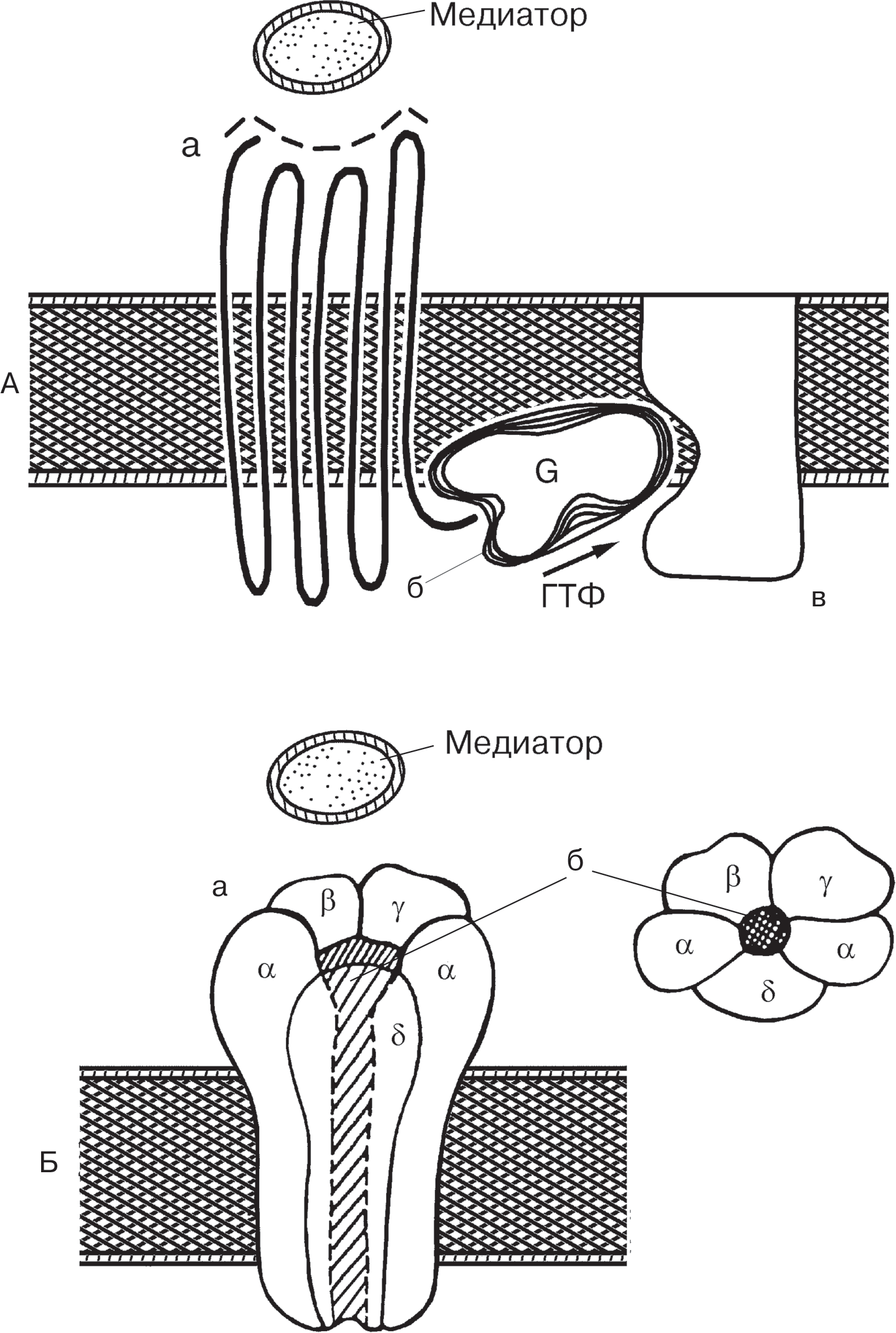 Рис.10.Гипотетическая модель строения холинорецепторов (объяснение в тексте) А — М-холинорецепторы: а — выступающая поверхностная часть рецептора, распознающая медиатор; б — G-белок (связывает и гидролизует ГТФ); в — ферменты (аденилатциклаза или фосфолипаза С) или ионные каналы мембраны (калиевые каналы) (в разных синапсах по-разному). Б — N-холинорецептор: а — поверхностная часть рецептора — пентамер из полипептидных субъединиц, с которыми специфически взаимодействует медиатор; б — ионный (натриевый) канал 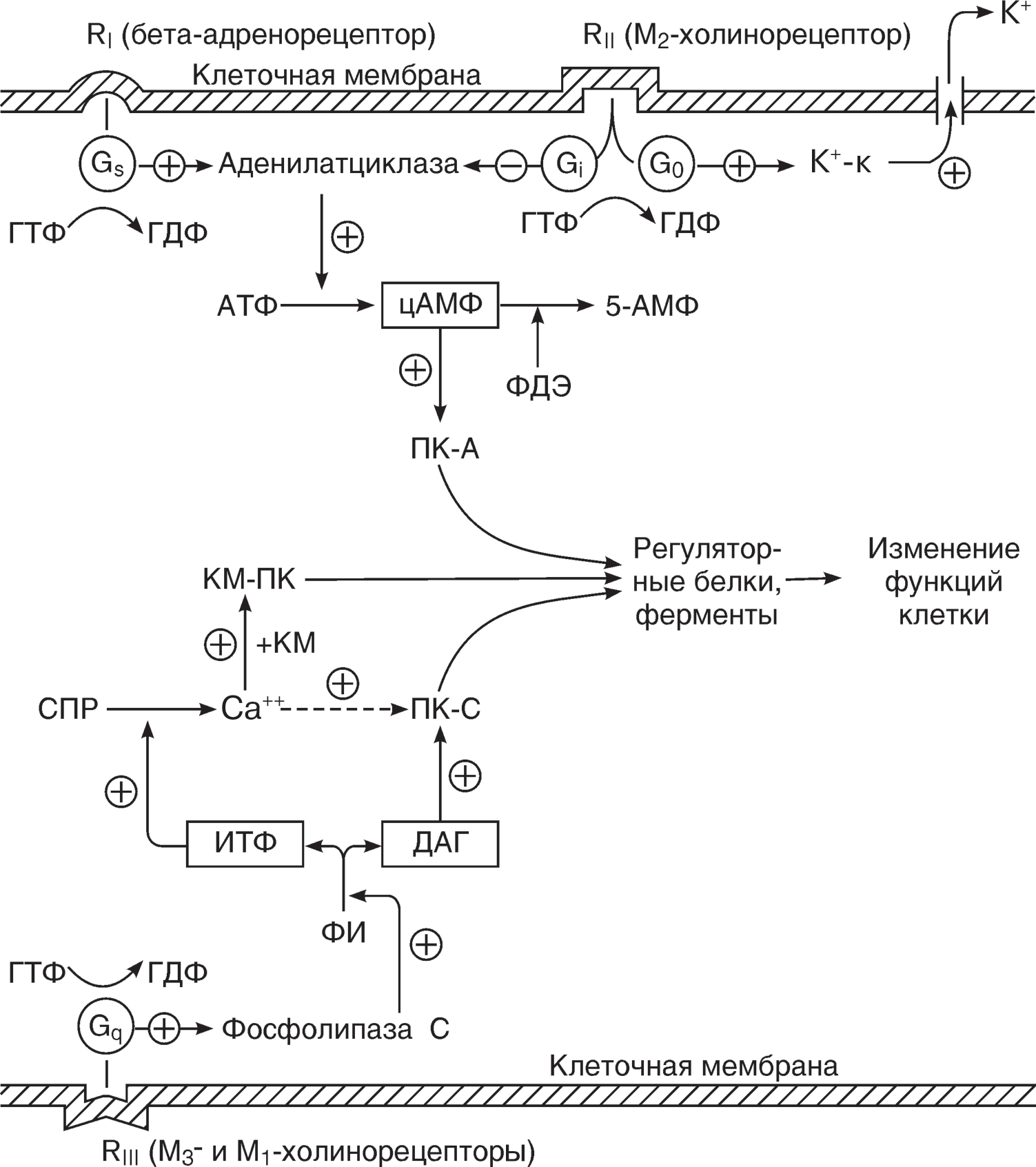 Рис.11.Схема механизмов сопряжения активации рецепторов с функциями клетки (объ- яснение в тексте): RI — рецептор, активирующий аденилатциклазную систему; RII — рецептор, ингибирующий аденилатциклазную систему; RIII — рецептор, активирующий полифосфоинозитидную систему; Gs — белок, стимулирующий аденилат- циклазу; Gi — белок, ингибирующий аденилатциклазу; G0 — белок, активирующий калиевые каналы; Gq — белок, активирующий фосфолипазу С; ПК-А — цАМФ-зависимые протеинкиназы; ПК-С — протеинкиназы С; КМ — каль- модулин; КМ-ПК — кальмодулинзависимые протеинкиназы; СПР — саркоплазматический ретикулум (депо ионов Са); ФИ — фосфоинозитиды; ИТФ — инозитолтрифосфат; ДАГ — диацилглицерол; цАМФ — циклический 3,5-аде- нозинмонофосфат; ФДЭ — фосфодиэстераза, инактивирующая цАМФ; К+-к — калиевый канал Ионы натрия устремляются по градиенту концентрации из внеклеточной жид- кости в клетку, что ведет к деполяризации мембраны и возникновению возбуж- дающего постсинаптического потенциала (ВПСП), ионы калия постепенно на- чинают выходить наружу. При достижении ВПСП определенного (критического) уровня активируются потенциалзависимые натриевые каналы соседних участков мембраны, быстрый входящий ток ионов натрия вызывает потенциал действия (ПД), который распространяется в виде волны возбуждения по нервной клетке (вегетативного ганглия) до следующего синапса или переходит с нерва на мышцу и распространяется по ее мембране. В поперечнополосатых мышцах ПД вызывает активацию кальциевых каналов, в клетку входят ионы кальция, они освобожда- ются также из внутриклеточных структур. Именно ионам кальция здесь придают решающее значение в механизме сопряжения возбуждения и сокращения. Ионы кальция (частично в комплексе с кальмодулином) активируют взаимо- действие актина и миозина, т. е. сокращение мышцы. N-холинорецепторы клеток вегетативных ганглиев и гомологичных им об- разований, обозначаемые как Nn-холинорецепторы, и Nm-холинорецепторы по- перечнополосатых мышц имеют тонкие структурные особенности, которые без- различны для ацетилхолина, но оказываются довольно существенными для их взаимодействия с лекарственными веществами. Инактивация ацетилхолина и восстановление исходного состояния клетки. Взаимодействие ацетилхолина с холинорецепторами чрезвычайно кратковремен- но (порядка 2 мс). Это объясняется очень быстрым освобождением ацетилхоли- на из обратимой связи с рецептором, а также его быстрой инактивацией. В хо- линергических синапсах в пре- или постсинаптической мембране (в разных си- напсах по-разному) имеется фермент ацетилхолинэстераза (АХЭ), или истинная холинэстераза, которая способна ускорить спонтанный гидролиз ацетилхолина в миллионы раз. Фермент имеет активный центр с исключительно высоким срод- ством к ацетилхолину. АХЭ расщепляет ацетилхолин на холин и ацетат, не обла- дающие медиаторным эффектом. Таким образом исчезает фактор, который вызы- вал сдвиги в постсинаптических структурах, и свойства последних возвращаются к исходному уровню. В области N-холинорецепторов происходит реполяризация мембраны. В работу вступает специальный транспортный механизм (натрий-ка- лиевый насос), локализованный в самой мембране и обеспечивающий удаление натрия и поступление в клетку калия. В результате работы этого механизма вос- станавливаются исходный градиент электролитов по сторонам мембраны и заряд покоя. Клетка готова принять следующий нервный импульс. Имеются также данные, что значительная часть медиатора, освободившегося из реакции с рецептором, диффундирует из синаптической щели в интерстициаль- ную среду и кровь и разрушается там ложной холинэстеразой (бутирилхолинэсте- разой), обладающей меньшим сродством к ацетилхолину. Таков в общих чертах механизм передачи импульсов в холинергических си- напсах. Различные звенья этого механизма могут быть объектом воздействия ле- карственных веществ. Лекарственные средства, вмешивающиеся в передачу импульсов в холинер- гических синапсах, в зависимости от направленности своего действия разделя- ются на холиномиметики и холиноблокаторы. В каждой группе препараты под- разделяются по избирательности (селективности) действия на тот или иной тип холинорецепторов. Свойствами холиномиметиков непрямого действия обладают антихолинэстеразные средства, которые, ингибируя фермент, разрушающий аце- тилхолин, усиливают и продлевают все эффекты медиатора. ХОЛИНОМИМЕТИКИ Родоначальники группы М- и N-холиномиметиков — алкалоиды муска- рин и никотин — используются в основном в качестве анализаторов в экспери- ментальной фармакологии, а никотин, как это ни парадоксально, — для борь- бы с никотиновой зависимостью. Очень редко, также в экспериментальных исследованиях, применяют ацетилхолин, возбуждающий одновременно М- и N-холинорецепторы. Напротив, растительные и синтетические заменители му- скарина, никотина и ацетилхолина, особенно антихолинэстеразные препараты (холиномиметики непрямого действия), представляют практический интерес. В табл. 26 представлена классификация холиномиметиков. Таблица26 Классификация холиномиметиков
М-холиномиметики Изучено множество природных алкалоидов, а также синтетических эфиров холина, обладающих М-холиномиметической активностью. В настоящее время в медицинской практике используется один представитель этой группы — пило- карпин — алкалоид листьев южноамериканских растений рода Pilocarpus (сейчас его получают синтетическим путем), который оказывает неселективное прямое активирующее влияние на М-холинорецепторы всех подтипов (М1, М2, М3). Из рассмотренной выше табл. 25 (локализация М-холинорецепторов в ор- ганизме) следует, что действие М-холиномиметиков в первую очередь направ- лено на органы, получающие парасимпатическую иннервацию. Возбуждая М-холинорецепторы этих органов, М-холиномиметики как бы имитируют раз- дражение соответствующих нервов. Поскольку кардиальные ветви вагуса иннервируют в основном синоатри- альный и атриовентрикулярный узлы сердца (мышца желудочков парасимпа- тических волокон не получает), действие М-холиномиметиков направлено на функцию именно этих отделов проводящей системы. Частота разрядов в си- нусном узле, ведущем ритм, уменьшается пропорционально силе активации М2-холинорецепторов. Вследствие брадикардии, которая может быть очень резкой, снижаются АД и минутный объем сердца. При внутривенном введении М-холиномиметиков возможна внезапная остановка сердца. По этой причине на- значение М-холиномиметиков в вену не практикуется. Введение М-холиномиметиков обычно сопровождается гипотонией за счет: а) замедления работы сердца; б) возбуждения M3-холинорецепторов эндотелия сосудов и секреции этими клетками особого релаксирующего фактора (оксида азота), что приводит к рас- ширению сосудов; в) возбуждения M2-холинорецепторов, тормозящих выброс норадреналина из пресинаптических окончаний симпатических нервов, иннервирующих сосуды. Из других сторон фармакодинамики М-холиномиметиков следует отметить влияние на бронхи. Суживая бронхи и повышая секрецию бронхиальных желез, они могут вызывать приступ удушья, особенно у больных, страдающих бронхи- альной астмой. В этом плане действие М-холиномиметиков всегда неблагопри- ятно. М-холиномиметики повышают тонус и возбуждают сокращение кишечника и мочевого пузыря, расслабляя одновременно сфинктеры. Скорость перемещения пищевых масс и газов увеличивается, устраняются атония кишечника, метеоризм, задержка дефекации. Устраняется атония мочевого пузыря. Однако эти эффекты в настоящее время не используются. Наибольший практический интерес представляет действие М-холино- миметиков на глаз. Механизм изменений состоит в активации М3-хо- линорецепторов и сокращении тех внутренних мышц глаза, которые получают парасимпатическую иннервацию. Так, за счет сокращения круговой мышцы ра- дужки суживается зрачок (миоз). Отток жидкости из передней камеры через тра- бекулярную сеть (фонтановы пространства), находящуюся в основании радужки, увеличивается; далее жидкость поступает в шлеммов канал и венозную систему глаза. При повышенном внутриглазном давлении (при глаукоме) это приводит к его понижению. Сокращение цилиарной (круговой) мышцы глаза сопрово- ждается ее утолщением и перемещением брюшка мышцы, к которому крепится циннова связка, ближе к хрусталику (рис. 12). Вследствие расслабления цинновой связки капсула хрусталика перестает растягиваться и хрусталик ввиду своей эла- стичности приобретает более выпуклую форму. Глаз устанавливается на близкое видение (спазм аккомодации). Сокращенная цилиарная мышца натягивает тра- бекулярную сеть, расширяет ее поры и облегчает отток внутриглазной жидкости в шлеммов канал. Действие холиномиметиков на глаз прямо противоположно тому, которое оказывает атропин, блокирующий М-холинорецепторы. Действие М-холиномиметиков на глаз имеет терапевтическое значение при глаукоме — заболевании, характеризующемся стойким повышением внутриглаз- ного давления и распирающими болями в глазах. Глаукома нередко дает обостре- 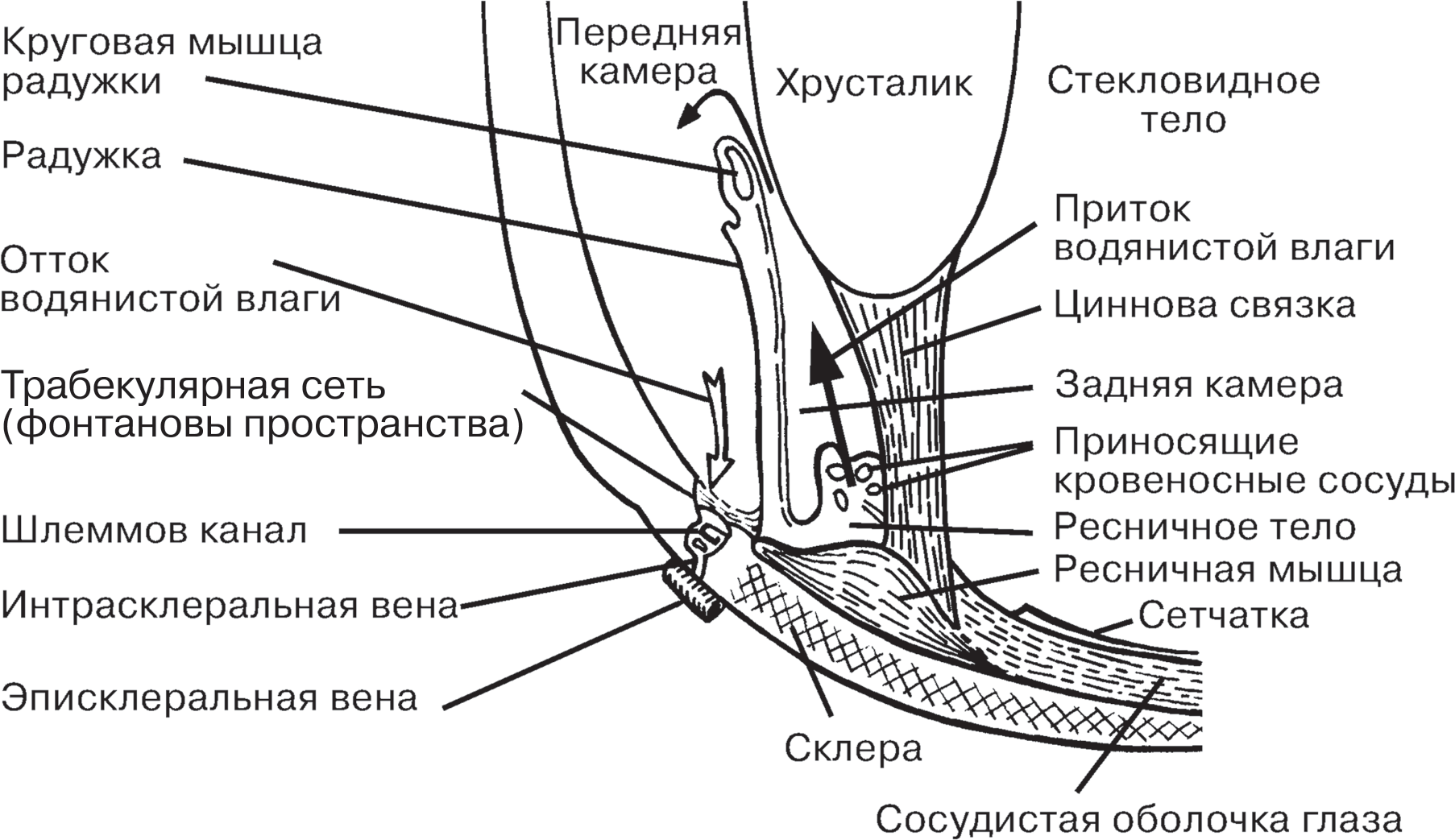 Рис.12.Схема строения глаза (передняя часть в разрезе) ния (глаукоматозные кризы), требующие экстренной симптоматической терапии, и является одной из частых причин слепоты. Закапывание в конъюнктивальный мешок раствора пилокарпина (чтобы раствор не стекал в полость носа, во время закапывания и после него слезный канал прижима- ют пальцем) вызывает снижение внутриглазного давления на несколько часов. Име- ются индивидуальные различия в чувствительности к препарату больных глаукомой. В заключение этого раздела полезно суммировать те изменения, которые воз- никают в организме под влиянием М-холиномиметиков. Это удобнее сделать на примере отравления мухомором (содержащим мускарин) или препаратом данной группы — пилокарпином. Картина очень характерна и ее трудно с чем-либо спу- тать. У отравившегося будут иметь место: брадикардия, гипотония, затрудненное дыхание (вследствие бронхоспазма), усиленная болезненная перистальтика ки- шечника («слышно на расстоянии»), рвота, понос, резкое потоотделение (боль- ной «купается» в собственном поту) и расширение кожных сосудов, интенсивное слюнотечение; сужение зрачков и спазм аккомодации (дальние предметы видны неясно и в увеличенных размерах — макропсия); возможны возбуждение и судо- роги. Из-за сильного увеличения секреции бронхиальных желез отмечается появ- ление вначале вязкой, а затем обильной жидкой мокроты, имитирующей острый отек легких. Смерть обычно наступает вследствие паралича дыхательного центра. Все симптомы отравления легко снимаются М-холиноблокаторами, и первая по- мощь состоит во введении атропина. | ||||||||||||
