Литература
Основная:
Глинка Н.Л. Общая химия. – М.: ВШ, разл. года изд.
Оганесян Э.Т. Неорганическая химия (для фарм. вузов). – М.: ВШ, 1984.
Зеленин К.Н. Химия (для мед. вузов). – С-Пб.: Специальная литература, 1997.
Ахметов Н.С. Общая и неорганическая химия. – М.: ВШ, 1981.
Хомченко Г.П. Химия для поступающих в вузы. – М.: ВШ, 1994.
Цыбукова Т.Н. Лекции по общей и неорганической химии. – Томск: СибГМУ, 2004.
Кузнецова О.Г., Шангина Л.П., Шевцова Т.А., Юсубов М.С. Пособие по химии. Часть II. – Томск, НТЛ, 2001.
Дополнительная:
Ершов Ю.А., Попков В.А. и др. Общая химия. – М.: ВШ, 1993.
Практикум по неорганической химии. Учебное пособие для студентов вузов, обучающихся по специальности «Фармация», под ред. М.А.Остапкевича. – М.: ВШ, 1987.
Глинка Н.Л. Задачи и упражнения по общей химии. – Л.: Химия.
Хомченко Г.П., Хомченко И.Г. Задачи по химии для поступающих в вузы. – М.: ВШ, 1987.
Методические указания и типовые примеры
к контрольному заданию № 1
(по 1 части программы, раздел 1)
1. Атомно-молекулярное учение. Основные понятия и законы химии
Пример 1. Имеется 0,5 кг Al(OH)3. Сколько это составляет: а) моль, б) молекул, в) атомов?
Решение:
Находим количество вещества (n или ) Al(OH)3 по формуле:
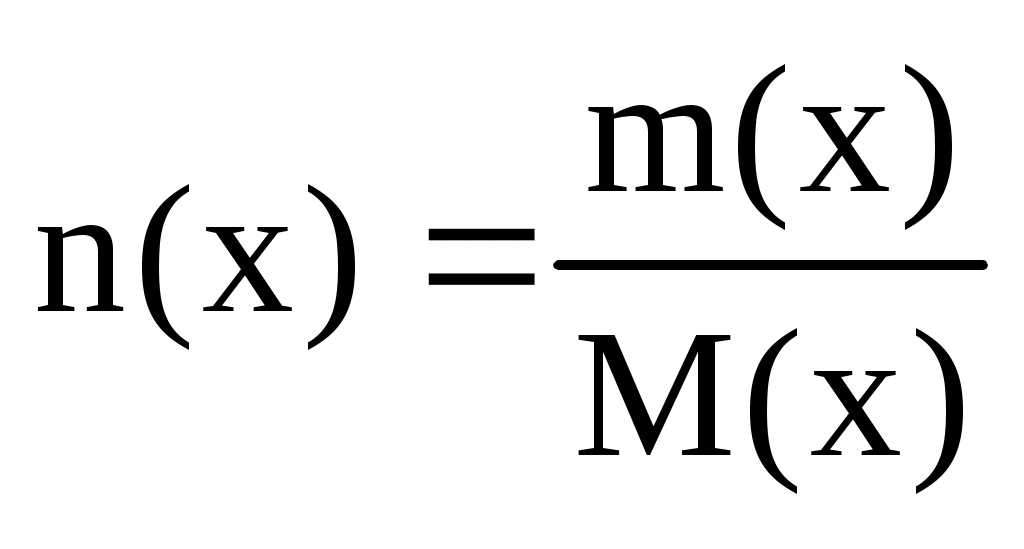 , моль, , моль,
где m(x) – масса вещества, M(x) – молярная масса вещества.
По условию m(Al(OH)3) = 0,5 кг = 500 г;
M(Al(OH)3) = Aг(Al) + 3Aг(O) + 3Aг(H) = 27 + 36 + 31 = 78 г/моль.
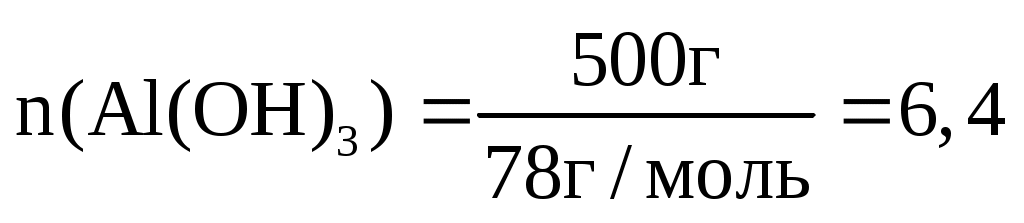 моль моль
Находим количество молекул (N) Al(OH)3 по формуле:
N(x)=n(x)NA, где NA – постоянная Авогадро.
NA =6,021023 моль-1.
N(Al(OH)3) = 6,4 моль 6,021023 моль-1=38,51023 молекул.
Находим число атомов () Al(OH)3 по формуле:
атомов=N(x) число атомов.
Число атомов в молекуле Al(OH)3 равно 7, тогда
атомов=38,510237=269,51023 = 2,71025
Ответ: в 0,5 кг Al(OH)3 содержится 6,4 моль вещества, это составляет 38,51023 молекул и 2,71025 атомов.
Пример 2. Имеется 91025 атомов NO2. Сколько это составляет: а) молекул, б) моль, в) граммов? Какой объем занимает данное количество газа?
Решение:
Находим количество молекул NO2 по формуле:
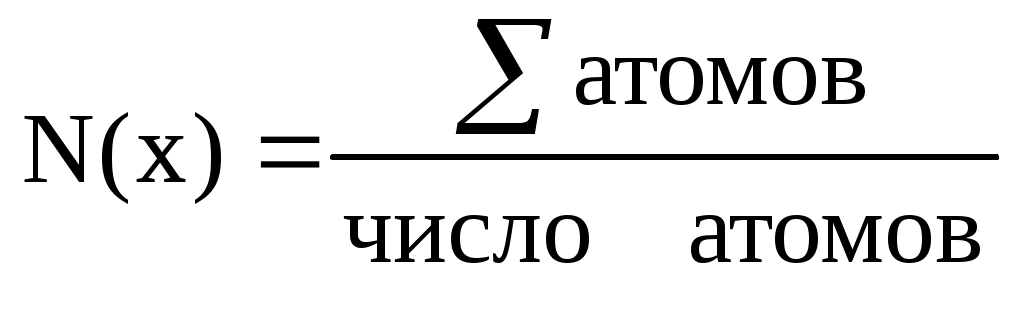 . .
Число атомов в молекуле NO2 равно 3, поэтому
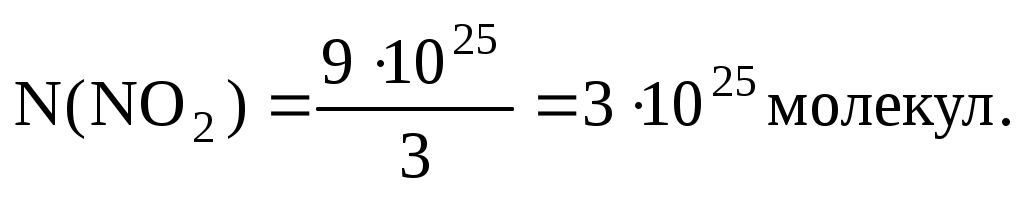
Находим количество вещества NO2 по формуле:
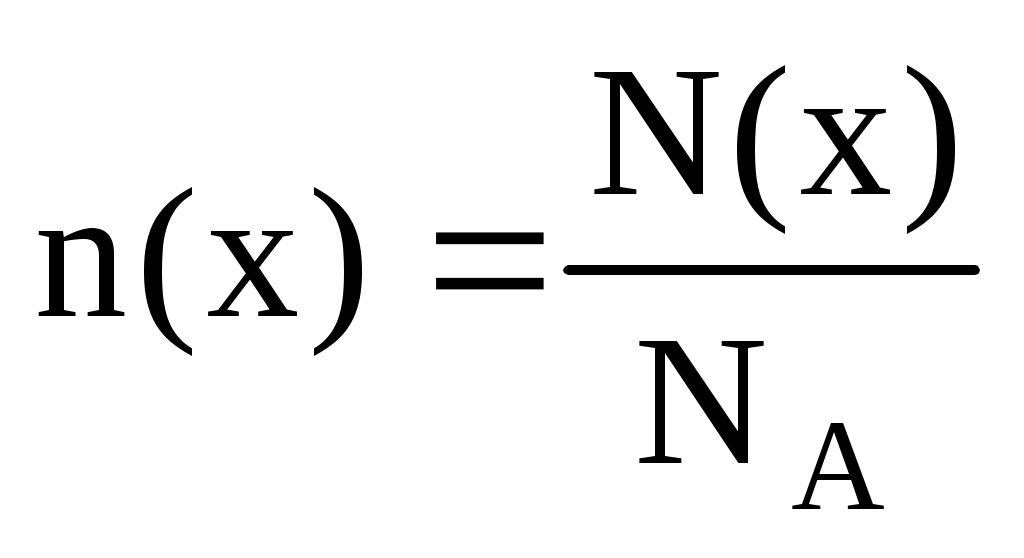 , где NA – постоянная Авогадро, NA =6,021023 моль-1. , где NA – постоянная Авогадро, NA =6,021023 моль-1.
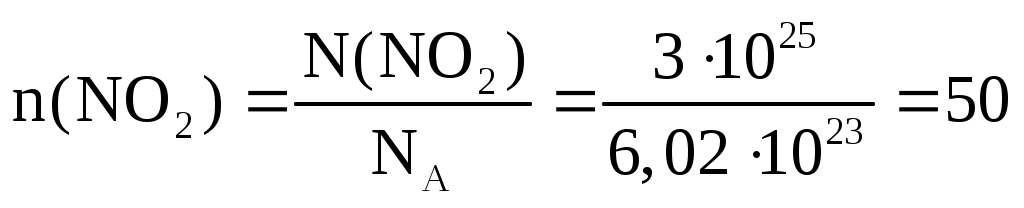 моль моль
Находим массу NO2 по формуле:
m(x) = n(x)M(x), где M(x) – молярная масса. М(NO2) = 46 г/моль.
m(NO2) = n(NO2)M(NO2) = 5046 = 2300 г.
Находим объем газа по формуле:
V(x) = n(x)Vm , где Vm – молярный объем газа. Vm = 22,4 л/моль.
V(NO2) = n(NO2)Vm = 50 22,4 = 1120 л.
Ответ: 91025 атомов NO2 соответствуют: 31025 молекул, 50 моль, 2300 граммов. Объем газа равен 1120 литров.
Пример 3. 100 мл газа, состоящего из азота и кислорода, при нормальных условиях весят 0,206 г. Вычислите молярную массу газа. Приведите его эмпирическую и графическую формулы.
Решение.
Находим молярную массу газа M(x) по формуле
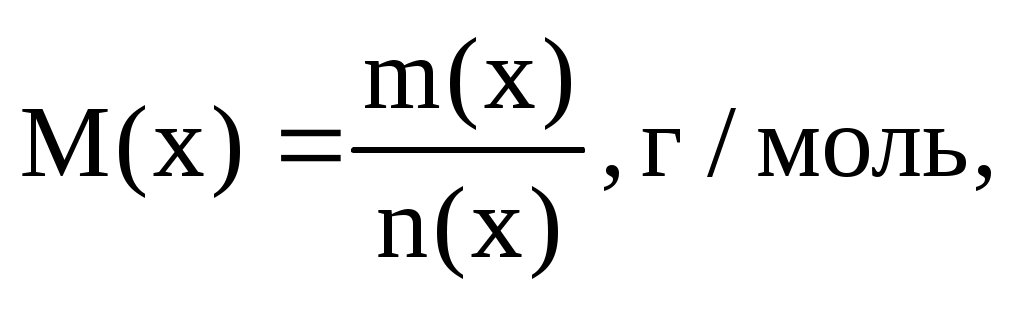
по условию m(x) = 0,206 г.
Количество вещества газа n(x) можно вычислить, используя следствие из закона Авогадро: 1 моль любого газа при нормальных условиях занимает один и тот же объем (молярный объем Vm)
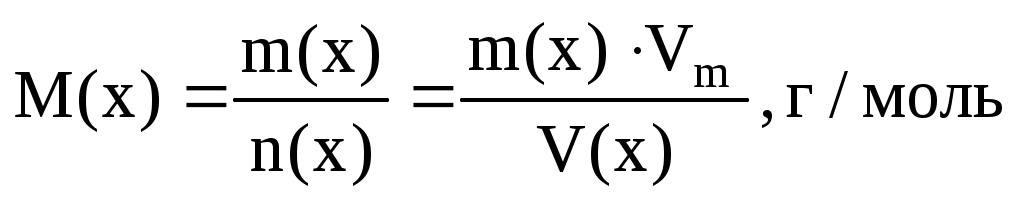
Подставляем данные в формулу и вычисляем M(x)
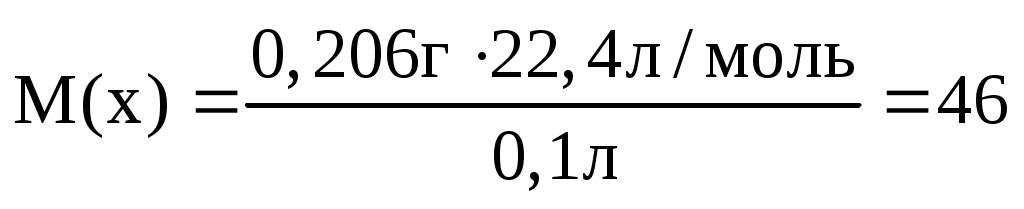 г/моль г/моль
Можно вычислить M(x), используя пропорцию:
0,1 л газа весит 0,206 г
22,4 л газа весят x г, отсюда
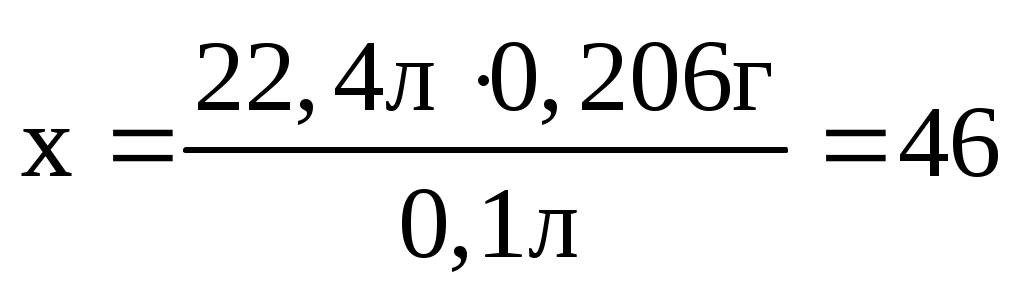 г г
Т.к. x – это масса 1 моль газа, то M(x) = 46 г/моль.
Выводим эмпирическую формулу газа.
Зная атомные массы элементов N (Aг = 14) и O (Аг = 16), методом подбора устанавливаем, что массу 46 г будет иметь 1 моль оксида азота NO2.
Составляем графическую формулу.
Для этого учитываем валентность кислорода, она равна II, т.е. каждый атом О должен образовывать с атомом N по две связи. При этом получается, что на атом N приходится в сумме 4 связи, т.е. он четырехвалентен. Тогда графическая формула имеет следующий вид: O=N=O.
Ответ: молярная масса газа NO2 составляет 46 г/моль. Графически формула изображается так: O=N=O.
Пример 4. В состав вещества входят 31,8% калия, 29,0% хлора и 39,2% кислорода. Установите его эмпирическую формулу, изобразите ее графически. Вычислите молярную массу вещества.
Решение:
Так как массовые доли всех компонентов вещества составляют в сумме 100%, можно принять массу всего вещества за 100 граммов.
Учитывая это, находим массы отдельных элементов по формуле:
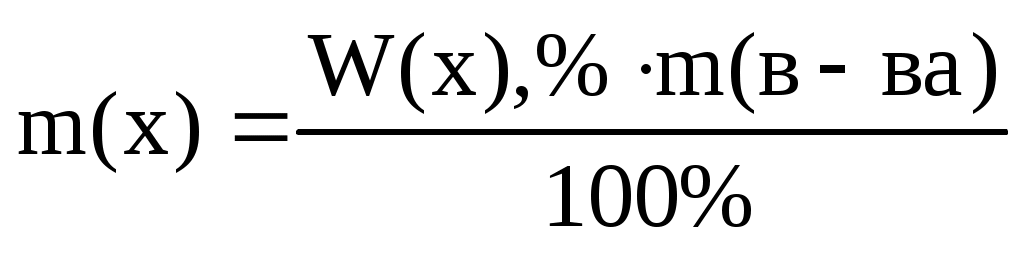 . .
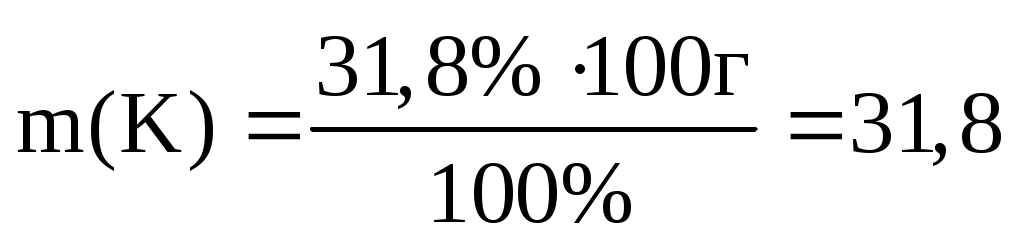 г г
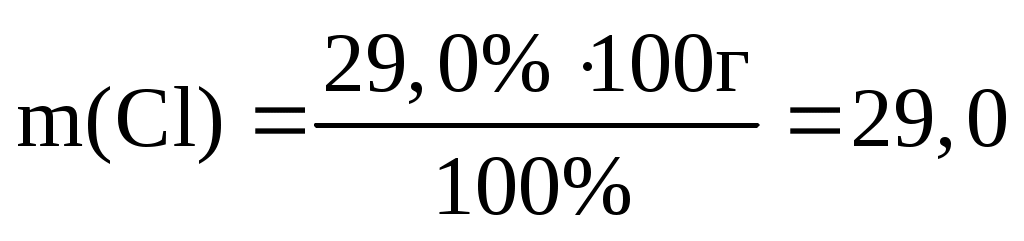 г г
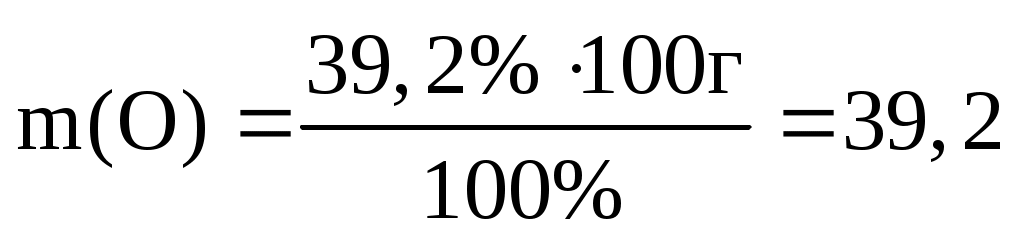 г. г.
Обозначим формулу вещества KxClyOz, где x, y, z – количество вещества каждого элемента соответственно. Так как количество вещества можно вычислить по формуле 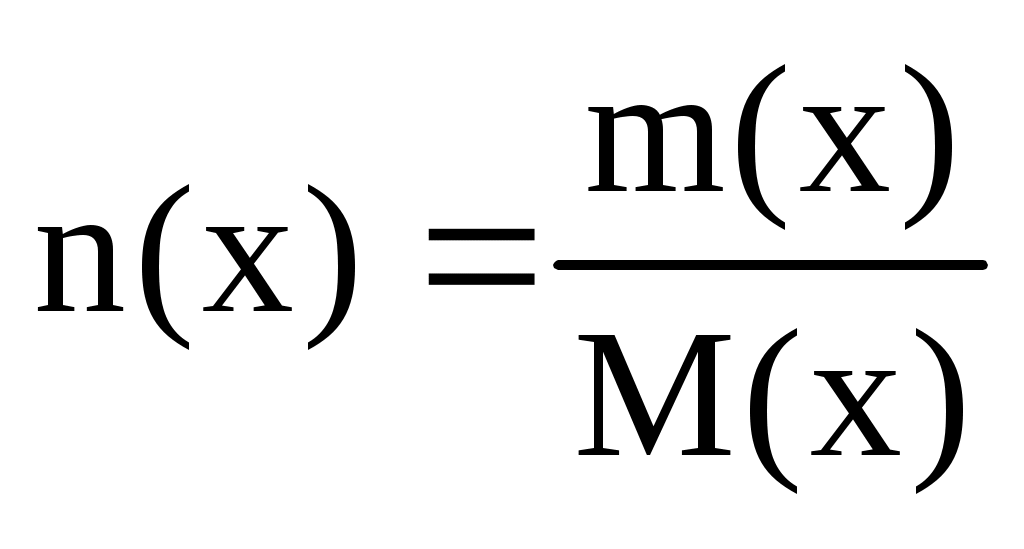 , найдем мольное соотношение x:y:z. , найдем мольное соотношение x:y:z.
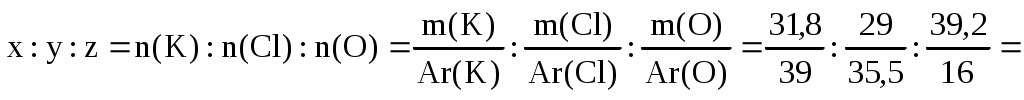 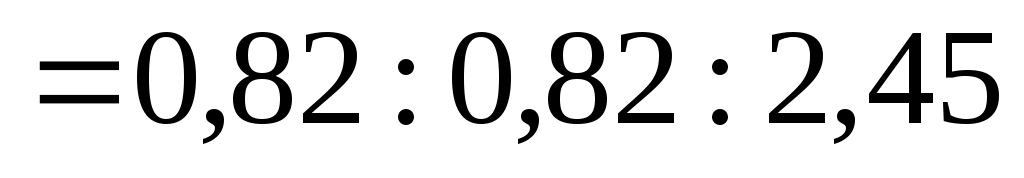 . .
Для приведения этого соотношения к целым числам разделим каждое на меньшее из них, т.е. на 0,82, при этом получаем 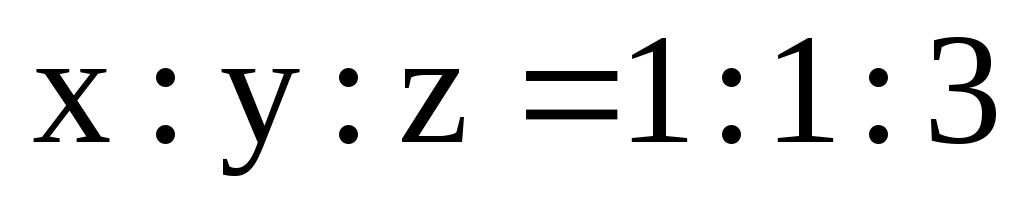 . Следовательно, эмпирическая (простейшая) формула вещества KClO3. . Следовательно, эмпирическая (простейшая) формула вещества KClO3.
Для графического изображения молекулы определим степени окисления элементов, которые в данном случае будут соответствовать их валентности: 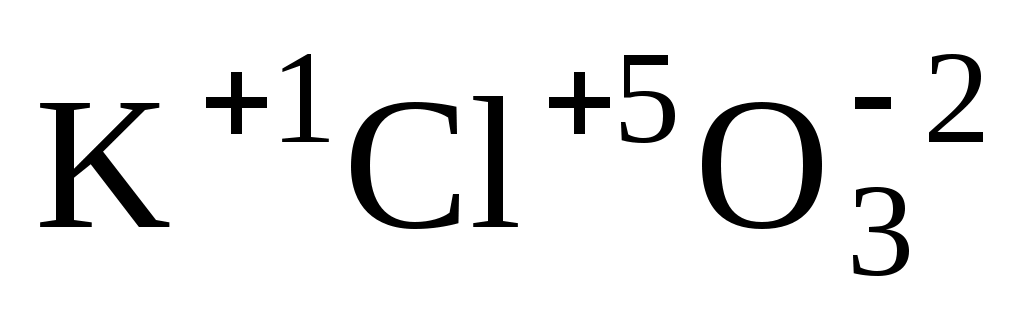 , значит , значит 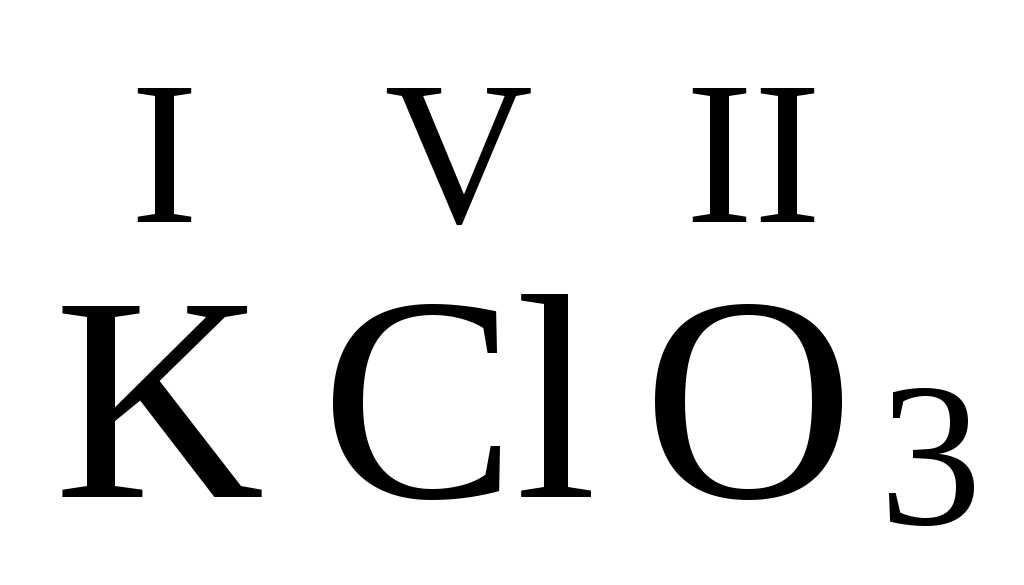 . Тогда графическая формула имеет следующий вид: . Тогда графическая формула имеет следующий вид: 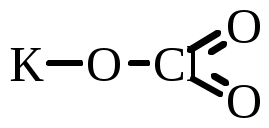 . .
Находим молярную массу вещества:
M(KClO3)=Ar(K) + Ar(Cl) + 3Ar(O) = 39 + 35,5 + 316 = 122,5 г/моль.
Ответ: молярная масса вещества KClO3 составляет 122,5 г/моль. Графически формула вещества изображается так: 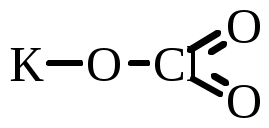
Пример 5. К раствору, содержащему 4 моль FeCl3, прибавили 0,5 кг KOH. Определите массу полученного осадка.
Решение:
В основе решения лежит реакция:
FeCl3 + 3KOH Fe(OH)3 + 3KCl
Находим вещество, по которому следует вести расчет продуктов реакции, т.е. выясняем избыток и недостаток реагирующих веществ. По уравнению соотношение количества веществ FeCl3 к KOH равно 1 : 3. По условию дано 4 моль FeCl3, значит надо вычислить количество вещества n(x) KOH по формуле:
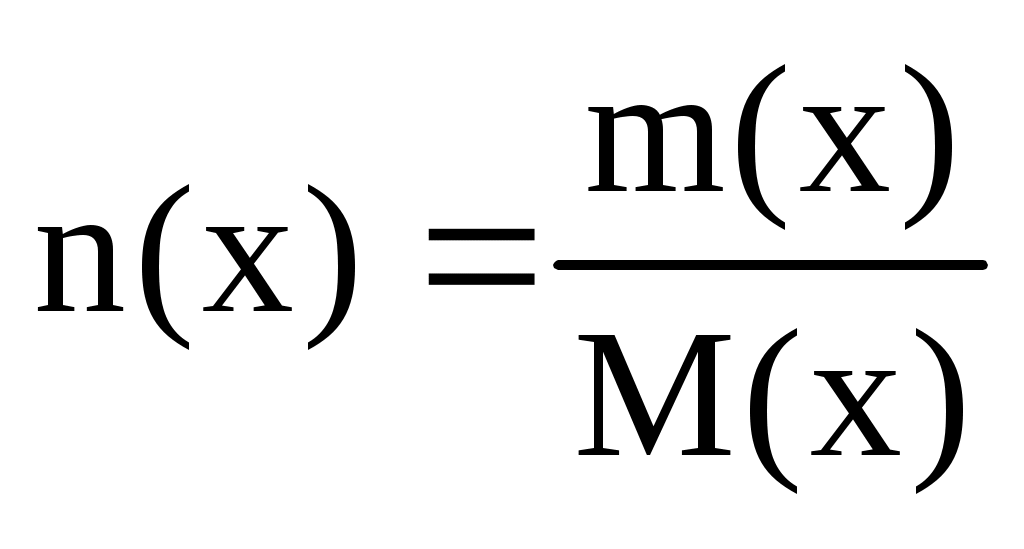
По условию m(KOH) = 0,5 кг = 500 г.
M(KOH) = Ar(K) + Ar(O) + Ar(H) = 39 + 16 + 1 = 56 г/моль.
На 4 моль FeCl3 должно приходиться 12 моль KOH по уравнению реакции. Имеется 8,9 моль, значит KOH находится в недостатке и расчет продукта следует вести по KOH.
Находим массу осадка.
Для этого составляем пропорцию:
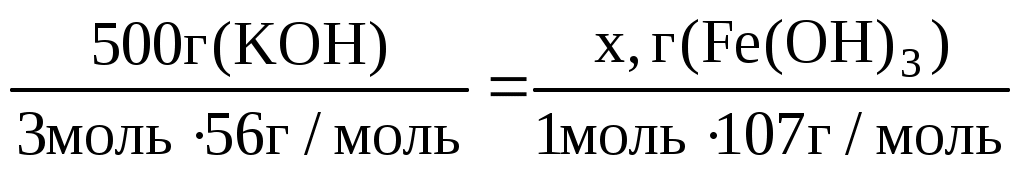 , где 107 г/моль = M(Fe(OH)3) , где 107 г/моль = M(Fe(OH)3)
решая которую, находим массу осадка.
m(Fe(OH)3) = x = 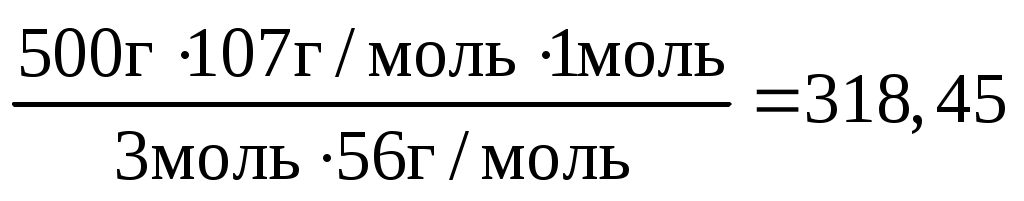 г г
Ответ: масса осадка Fe(OH)3 составляет 318,45 грамма.
Пример 6. Сколько литров водорода выделится при действии разбавленной серной кислоты на 0,6 моль алюминия? Сколько соли при этом образуется?
Решение:
В основе решения лежит реакция:
2Al + 3H2SO4 Al2(SO4)3 + 3H2
Находим объем водорода по пропорции:
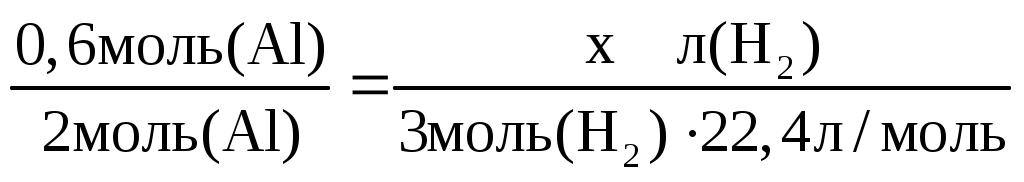 , где 22,4 л/моль – молярный объем газа. , где 22,4 л/моль – молярный объем газа.
V(H2) = x = 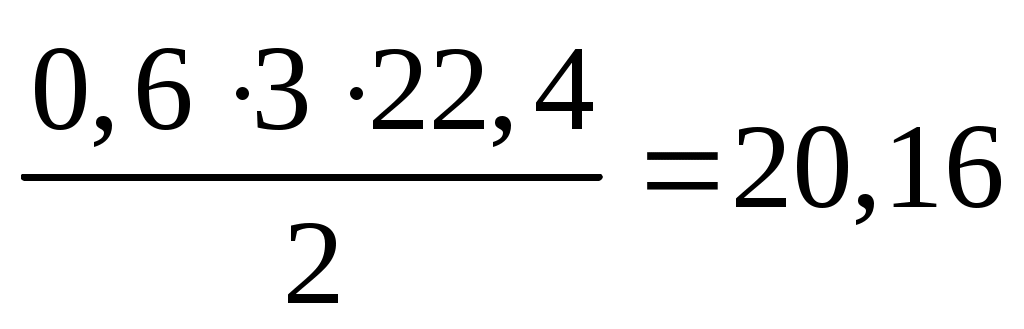 (л) (л)
Находим массу соли Al2(SO4)3.
Исходя из условия: m(Al) = n(Al)Ar(Al) = 0,6 моль27 г/моль = 16,2 г.
Составим пропорцию:
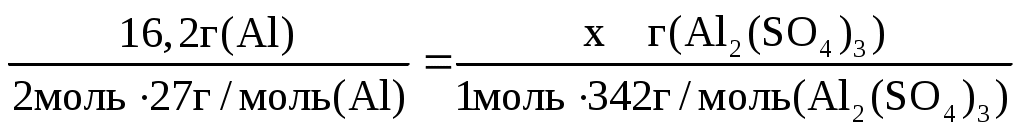 , ,
исходя из которой найдем массу соли
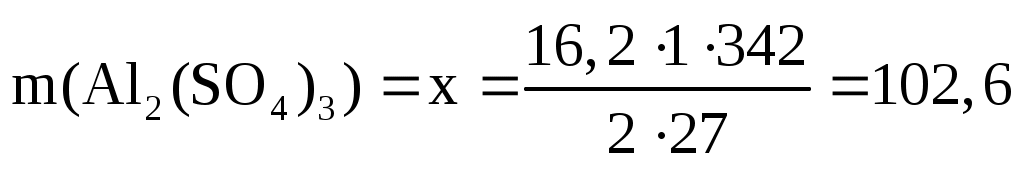 г. г.
Ответ: выделится 20,16 л H2 и образуется 102,6 г соли.
|
 Скачать 1.14 Mb.
Скачать 1.14 Mb.