|
|
Учебнометодическое пособие для студентов i курса медицинского вуза Рекомендовано Учебнометодическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов медицинских вузов
G = Н Т S, = Н Т S,
г де Н – характеризует полное изменение энергии системы в изобарно-изотермическом процессе и отражает стремление системы к минимуму энергии; де Н – характеризует полное изменение энергии системы в изобарно-изотермическом процессе и отражает стремление системы к минимуму энергии;
Т · S – характеризует ту часть энергии, которую нельзя превратить в работу (связанная энергия), и отражает стремление системы к максимуму беспорядка; · S – характеризует ту часть энергии, которую нельзя превратить в работу (связанная энергия), и отражает стремление системы к максимуму беспорядка;
G – характеризует ту часть энергии системы, которую можно превратить в работу (свободная энергия). – характеризует ту часть энергии системы, которую можно превратить в работу (свободная энергия).
Изменение энергии Гиббса позволяет судить о возможности самопроизвольного протекания процессов.

В системе при постоянных температуре и давлении могут самопроизвольно совершаться только такие процессы, в результате которых энергия Гиббса уменьшается  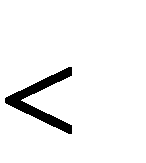 G 0, т.е.Gкон. Gнач.. G 0, т.е.Gкон. Gнач..
И з уравнения G = Н – Т S можно определить направление протекания реакций различных типов. з уравнения G = Н – Т S можно определить направление протекания реакций различных типов.
П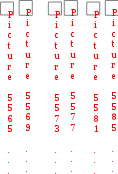 ри Н 0 и S 0, G 0, процесс протекает самопроизвольно слева направо. ри Н 0 и S 0, G 0, процесс протекает самопроизвольно слева направо.
П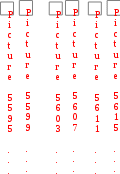 ри Н 0 и S 0, G 0, процесс не может самопроизвольно протекать слева направо. ри Н 0 и S 0, G 0, процесс не может самопроизвольно протекать слева направо.
П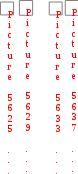 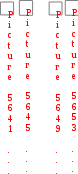  ри Н 0 и S 0, а также при Н 0 и S 0 знак G зависит от соотношения энтальпийного и энтропийного факторов. ри Н 0 и S 0, а также при Н 0 и S 0 знак G зависит от соотношения энтальпийного и энтропийного факторов.
И  зменение знака G при изменении знаков Н и S зменение знака G при изменении знаков Н и S
|
Знак
|
Вывод
|
Примеры
|
H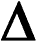
|
S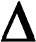
|
G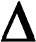
|
–
|
+
|
–
|
Процесс самопроизвольный при любой температуре
|
Горение сложных органических веществ
|
+
|
–
|
+
|
Процесс несамопроизвольный
|
Фотосинтез
|
–
|
–
|
–
|
Процесс самопроизвольный при низкой температуре
|
Конденсация пар–жидкость; жидкость–кристалл
|
–
|
–
|
+
|
Процесс несамопроизвольный при высокой температуре
|
2 Н Н2
|
+
|
+
|
–
|
Процесс самопроизвольный при высокой температуре
|
Н 2 2Н
|
+
|
+
|
+
|
Процесс несамопроизвольный при низкой температуре
|
Плавление (т–ж)
Испарение (ж–г)
|
|
|
|
 Скачать 5.49 Mb.
Скачать 5.49 Mb.
 = Н Т S,
= Н Т S, 
 з уравнения G = Н – Т S можно определить направление протекания реакций различных типов.
з уравнения G = Н – Т S можно определить направление протекания реакций различных типов.  ри Н 0 и S 0, G 0, процесс протекает самопроизвольно слева направо.
ри Н 0 и S 0, G 0, процесс протекает самопроизвольно слева направо.  ри Н 0 и S 0, G 0, процесс не может самопроизвольно протекать слева направо.
ри Н 0 и S 0, G 0, процесс не может самопроизвольно протекать слева направо. 
 зменение знака G при изменении знаков Н и S
зменение знака G при изменении знаков Н и S