Учебное пособие по химии для учащихся 10 классов, обучающихся в лицеях фдп рниму под редакцией проф. Теплова В. В
 Скачать 3.52 Mb. Скачать 3.52 Mb.
|
Пример 18.При хлорировании 70 г циклоалкана, в молекуле которого содержится 40 е, было получено монохлорпроизводное массой 83,6 г. Определить выход реакции галогенирования и массовые доли веществ, в полученной жидкой органической смеси. Решение:1) Общая формула циклоалканов СnH2n В одном атоме углерода содержится 6 е, в атоме водорода 1е, в молекуле СnH2n n(е)= 6n+2n=8n Составляем уравнение: 8n= 40; n=5, следовательно, циклоалкан С5Н10 - циклопентан 2) Монохлорпроизводное образуется в реакции хлорирования без разрыва цикла 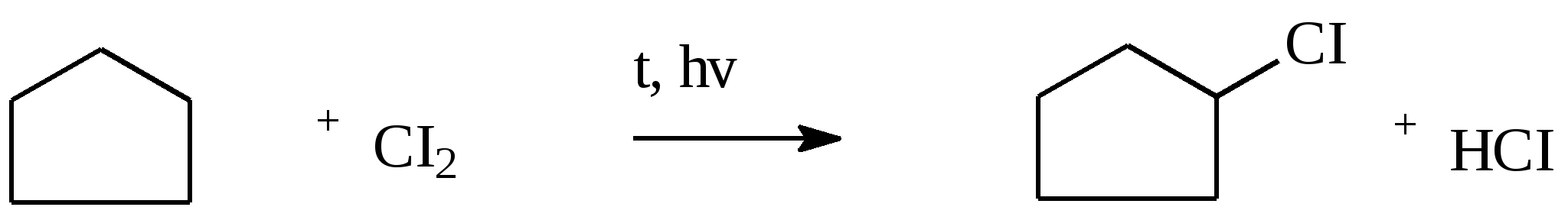 3) Определяем количество вещества циклоалкана: M (C5H10) = 70г/моль М (С5Н9Сl) = 104,5 г/моль n(С5Н10) = m (C5H10)/M(C5H10) = 70/70= 1моль 4) Определяем количество вещества монохлорпроизводного, полученного практически n( С5Н9Сl) = 83,6/104,5 = 0,8 моль 5) Выход в реакции (η ) определяется как отношение количества вещества, полученного практически n(пр) к количеству вещества рассчитанному по уравнению химической реакции (теоретически) n( теор) η = n(пр) / n(теор) = 0,8: 1 = 0,8 (80%) 6) Таким образом, в жидкой органической смеси после реакции будут находиться хлорциклопентан и непрореагировавший циклопентан: m ( C5H9Cl) = 83,6 г(по условию) и n( С5Н10) ост = 1,0-0,8 = 0,2 моль m ( C5H10) ост = 0,2 ∙ 70 =14 г m (смеси) = 83,6 +14 = 97,6 г 7) Массовая доля циклохлорпентана ω(С5Н9Сl) = m(C5H9Cl) /m (cм) = 83,6:97,6 = 0,857 (85,7%) массовая доля оставшегося циклопентана ω (С5Н10) = m( C5H10) / m (см) = 14 : 97,6 = 0,147 ( 14,7%) Ответ: ω(С5Н9Сl) = 85,7% ; ω (С5Н10) = 14,7% Пример 19.Газовая смесь состоит из пропана, СО2, циклопропана. Выделить каждый компонент газовой смеси в чистом виде. Решение:1) В газовой смеси находится углекислый газ, который, в отличие от углеводородов, вступает в реакции со щелочами. Пропустим смесь через избыток раствора гидроксида кальция СО2 + Са(ОН)2 Оставшаяся газовая смесь содержит С3Н6 и С3Н8. Для того чтобы выделить СО2 в чистом виде, отфильтруем осадок и прокалим: t СаСО3 Соберем в пробирку выделившийся газ, получим CO2 в чистом виде 2) Оставшуюся газовую смесь пропустим через избыток раствора бромной воды C3H6 + Br2(aq) | | Br Br Непрореагировавший газ соберём в пробирку. Получим С3Н8 в чистом виде 3) .На оставшуюся жидкость действуем избытком Zn, при нагревании CH2−CH−CH3 + Zn | | Br Br Выделившийся газ соберём в пробирку, получим циклопропан в чистом виде. Пример 20.Среди перечисленных веществ выберете гомологи и изомеры: метилциклобутан, циклобутан, пентен-1, бутен-2, метилбутан, метилпропан. Решение: Поскольку, гомологами называтся вещества, отличающиеся друг от друга на одну или несколько гомологических единиц (-СН2-) и имеющие сходное строение и свойства, выберем среди перечисленных веществ гомологи: 1)  метилциклобутан циклобутан 2) CH3−CH2−CH − CH3 ; CH3 −CH −CH3 ; | | CH3 СН3 метилбутан метилпропан 3) СH3−CH2−CH2−CH=CH2 ; СH3−CH=CH−CH3 пентен-1 бутен-2 Изомеры – это вещества, имеющие одинаковый состав, но различное строение. Изомерами являются: 1) циклобутан бутен-2 2) 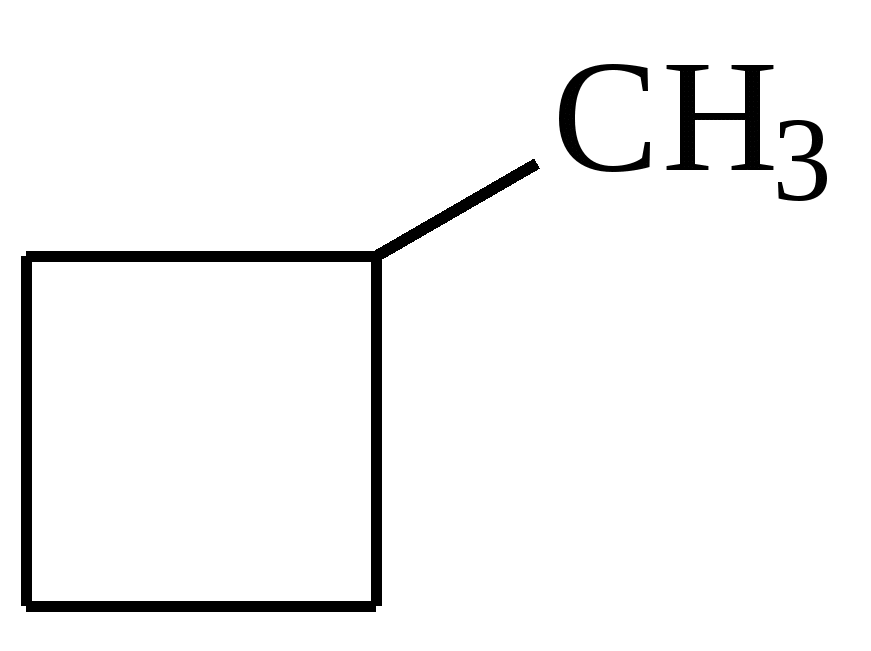 ; и СH3−CH2 −CH2−CH=CH2 ; и СH3−CH2 −CH2−CH=CH2 метилциклобутан пентен-1 6.4. Задачи и упражнения для самостоятельного решения 171. С какими перечисленными реагентами будет вступать в реакцию метилциклобутан: бром, гидроксид натрия, натрий, вода, водород, кислород, бромоводород. Напишите уравнения, укажите условия протекания реакций. 172. Напишите структурные формулы всех дибромпроизводных алканов, из которых при нагревании с натрием может быть получен 1,2-диметил-3-этилциклопропан. Один из них назовите по систематической номенклатуре. Приведите уравнения соответствующих реакций. 173. Напишите структурные формулы и назовите по систематической номенклатуре все дихлорпроизводные алканов, из которых при нагревании с цинком может быть получен 1-изопропил-2,5- диметил-3-этилциклопентан. Приведите уравнения соответствующих реакций. 174. В продуктах реакции гидрирования циклоалкана был обнаружен 2-метилбутан. Напишите структурные формулы и назовите по систематической номенклатуре все циклоалканы, которые могли бы дать подобный результат. 175. Приведите структурные формулы всех циклоалкенов, в молекуле которых находится 46 электронов. Приведите формулы двух других углеводородов, в молекуле которых будет на 2 е больше. 176. Газовая смесь состоит из пропана, пропина и циклопропана. Выделите каждый компонент газовой смеси в чистом виде. 177. Смесь состоит из 1,6-дибромгексана, циклогексана, циклогексена. Получите максимальное количество чистого циклобромгексана. Приведите уравнения реакций, укажите условия протекания реакций. 178. Идентифицируйте вещества, находящиеся в пробирках без этикеток: а) циклогексан, циклогексен и пентин-1; б) этан, циклопропан, пропин; в) углекислый газ, ацетилен, метан, циклопропан. 179. Смесь метана, этена и циклопропана имеет плотность по гелию 7,125. К 4 л этой смеси добавили 4 л водорода и пропустили над нагретым платиновым катализатором. При этом объем смеси уменьшился до 5 л. Определите объемные доли газов в исходной смеси. 180. Через бромную воду с массовой долей брома 20 % пропустили 3 л смеси этана и циклопропана с плотностью по водороду 19. Определите, какая масса раствора брома была обесцвечена этой смесью. 181. При гидрировании некоторого циклоалкана массой 11,2 г требуется 4,48 л водорода (н.у.). Напишите структурную формулу исходного циклоалкана. 182. При горении предельного циклического углеводорода образовалось 3,60 г воды. Вычислите массу углекислого газа, которая образуется при этом. 183.15 г смеси гексана, циклогексана и циклогексена обесцветили 76,8 г раствора брома в тетрахлорметане с массовой долей брома 10%. Определите массовую долю циклогексена в смеси. 184. При пропускании 2,24 л ( н.у.) смеси этена, циклобутана и бутана через бромную воду прореагировало 40 г раствора с массовой долей брома 20%. Плотность газовой смеси по водороду равна 24,3. Определите состав смеси углеводородов ( в %% по объёму). 185. Рассчитайте массу раствора бромной воды с массовой долей брома 4%, которая может прореагировать с 10 л ( н.у.) смеси углеводородов, содержащей ( в %% по объёму): 16,4% этана, 33,6% этина и 50% метилциклопропана. 186. Рассчитайте, как изменится масса склянки с бромной водой после пропускания через неё 22,4 л газовой смеси, состоящей из пропана, циклопропана и углекислого газа. Плотность газовой смеси равна 1,607 г/л (н.у.) 187. Для сгорания циклоалкана требуется в 4,5 раза больший объем кислорода, чем объем исходного углеводорода (при одинаковых условиях). Какая масса этого углеводорода сгорела, если масса осадка, образовавшегося при пропускании продуктов реакции через избыток раствора гидроксида бария, составила 1,97 г? 188. При бромировании 92 г метилциклогексана образовалось 108 г монобромпроизводного. Определите выход реакции галогенирования и массовые доли веществ в полученной жидкой органической смеси Глава 7. АРЕНЫ Аренами называются циклические непредельные углеводороды с системой сопряженных π -связей. Общая формула аренов СхН2х-6, где х≥6. Простейшим ареном является бензол С6Н6. Структурная формула бензола ранее описывалась шестичленным циклом с 3-мя двойными связями (т.н. формула Кекуле).  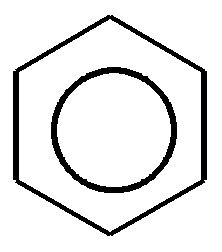 Сейчас принято изображать структуру бензола шестиугольником с внутренним кольцом, отражающим существование единой циклической сопряженной системы из 6 р-электронов, хотя допускается и использование формулы Кекуле, помня, однако, что она не вполне соответствует реальному строению бензола. Если изобразить молекулу бензола как бы «в профиль», то получится что-то вроде сэндвича, где вытянутые овалы соответствуют верхней и нижней областям кольцевой π- электронной системы («вид на бублик сбоку»). Отрезок прямой отвечает проекции плоскости из 6 атомов углерода, связанных σ-связями. Цикл является плоским, так как все атомы углерода в бензоле имеют гибридизацию sp2. Проекция плоского цикла Отрицательно заряженные облака из 6 σ- связей С-С сопряженных π-электронов 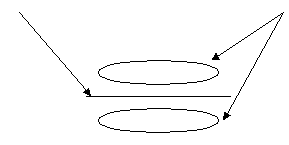 Так как «овалы» заряжены отрицательно (ведь заряд электронов отрицателен), то отрицательные частицы или отрицательно заряженные фрагменты молекул не могут приблизиться к бензольному кольцу из-за электростатического отталкивания одноименных зарядов. Подойти к молекуле бензола могут т.н. электрофильные частицы - положительные ионы (NO2+) или электроположительные фрагменты молекул. Поэтому для бензола и аренов в большей степени характерны реакции электрофильного замещения. Кроме этого типа реакций можно назвать реакции радикального замещения, окисления(у гомологов бензола), У бензола – реакции радикального присоединения. Гомологи. Изомерия. Ближайшим гомологом бензола является толуол (метилбензол) С6Н5СН3 , у которого изомеров нет. Для следующего гомолога С8Н10 насчитывается уже 4 изомера. Один из них –этилбензол С6Н5С2Н5, 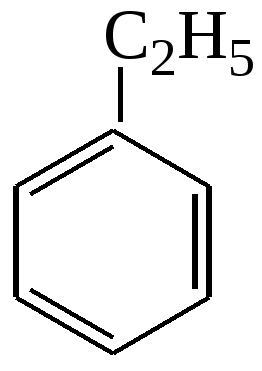 а три других - изомеры диметилбензола С6Н4(СН 3)2, так называемые ксилолы. 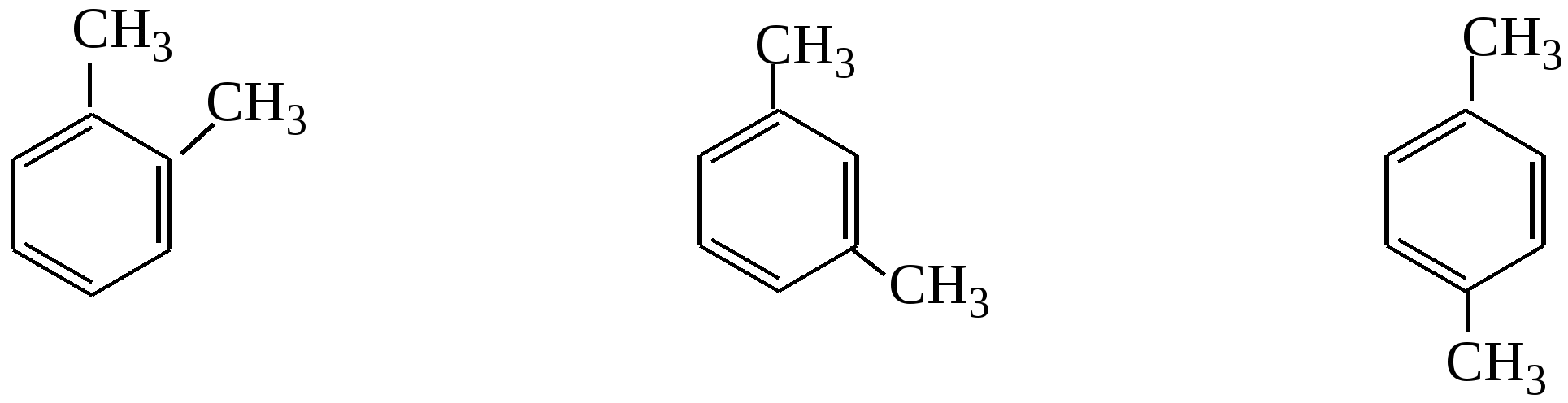 орто-ксилол мета-ксилол пара-ксилол 1,2-диметилбензол 1,3- диметилбензол 1,4-диметилбензол Изомеров пропилбензола –пять:(н-пропилбензол С6Н5С3Н7, изопропилбензол (кумол) С6Н5СН(СН3)2 и др.) Существуют 3 изомера триметилбензола С6Н3(СН3)3, формулы которых предлагается изобразить самостоятельно. Важным производным бензола является стирол, который, вообще говоря, не относится к аренам, так как имеет в боковой цепи двойную связь. 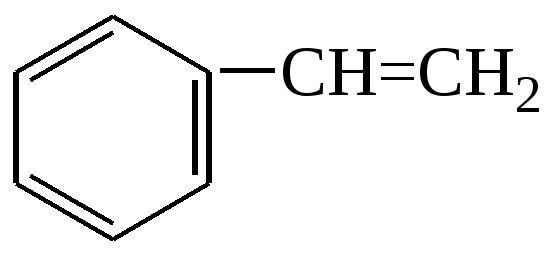 винилбензол(стирол) Физические свойства аренов Арены плохо растворимы в воде, хорошо -- в органических растворителях, Сами являются хорошими растворителями органических и некоторых неорганических веществ. Плотность их меньше, чем у воды, следовательно, в смесях с водой слой арена будет сверху, а водный – снизу. Температуры кипения относительно невысокие: у бензола 80оС, а у толуола 110оС. Арены имеют характерный, достаточно неприятный запах. Легко воспламеняются, горят ярким, но сильно коптящим пламенем. 7.1. Получение аренов 1. Дегидроциклизация(ароматизация) природных неразветвленных алканов с цепью, содержащей от 6 и выше атомов углерода - основной промышленный способ. При нагревании над катализатором (Cr2O3 или Pt) происходит замыкание цикла и одновременное отщепление водорода. Если исходным алканом является н-гептан, то получится толуол:  2. Дегидрирование циклогексана и его производных над платиновым катализатором - другой промышленный способ:  3. Циклотримеризация ацетилена над раскалённым активированным углём - самая старая реакция получения бензола: 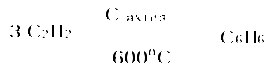 4. Гомологи бензола получают каталитическим алкилированием бензола алкенами или галогеналканами. Более подробно этот тип реакций будет разобран при изложении химических свойств аренов. 5. Лабораторный способ получения бензола, очень похожий на способ получения легких алканов, при котором соли органических кислот сплавляются с твердыми щелочами. Так, при сплавлении натриевой соли бензойной кислоты с гидроксидом натрия образуется бензол. 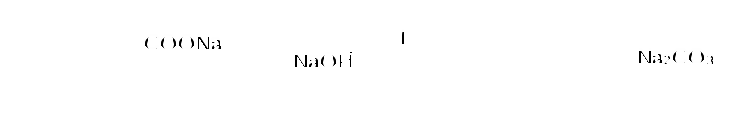 6. Еще одна реакция получения аренов в лаборатории весьма сходна с реакцией Вюрца. Она носит название реакция Вюрца-Фиттига и описывает образование гомологов бензола при обработке натрием галогенпроизводных бензола и галогеналканов 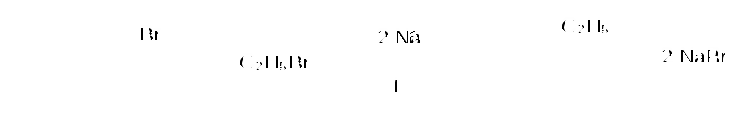 Правила ориентации в бензольном кольце Данный эффект относится к многочисленным производным бензола. Заместители, в зависимости от вида содержащихся в них атомов, способны влиять на распределение электронной плотности в бензольном кольце. Несколько упрощая ситуацию, влияние заместителей можно свести к 2-м основным случаям. Существуют заместители, увеличивающие электронную плотность в бензольном кольце (ориентанты I рода, электронодонорные заместители). К ним относятся: алкильные радикалы - СН3,- С2Н5,- ОН, -NН2. Ориентанты 1 рода облегчают дальнейшее замещение в бензольном кольце Замещение идет в орто- и пара- положения. К ориентантам 1 рода относятся также галогенные группы - Cl и -Br , но они затрудняют дальнейшее замещение. Так, толуол алкилируется в присутствии катализатора AlCl3 с образованием смеси о- и п- ксилолов:  Наибольшей активностью обладают гидроксильная и аминная группы. Например, при обработке фенола (гидроксибензола) бромной водой происходит замещение водорода бромом и по орто- и по пара- положениям: 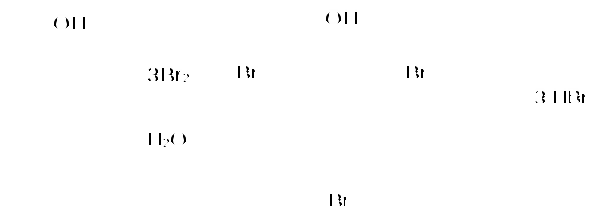 Другой вид заместителей – электроноакцепторных, уменьшающих электронную плотность в бензольном кольце – относят к ориентантам II рода(нитрогруппа -NO2, карбоксильная -COOH, альдегидная -HCO и некоторые другие). Уменьшение электронной плотности происходит во всем бензольном кольце. В меньшей степени это относится к мета-положению, куда и направляется электрофильная частица. При наличии ориентанта II рода дальнейшее замещение затрудняется. В качестве примера приведем реакцию галогенирования нитробензола: 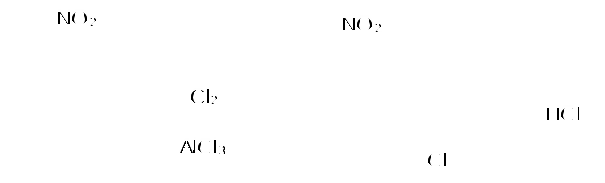 7.2. Химические свойства аренов Шесть р-электронов бензольного кольца образуют единую устойчивую замкнутую π-систему, что делает ароматические соединения более стабильными и химически менее активными. Поэтому для аренов более характерны реакции электрофильного замещения при которых сохраняется ароматичность. Необходимо отметить, что химические свойства гомологов бензола несколько отличаются от свойств самого бензола. Так, несмотря на явную непредельность структуры, бензол не реагирует с водой, галогеноводородами, бромной водой, водным раствором перманганата калия. 1. Электрофильное замещение в бензольном кольце а) Галогенирование. Реакции электрофильного замещения проходят в присутствии катализаторов – хлоридов или бромидов алюминия или железа. 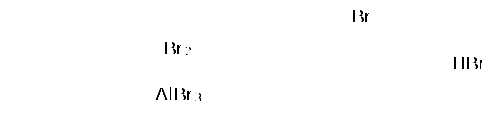 При галогенировании гомологов бензола обычно получается смесь изомеров, т.к. алкильные заместители – ориентанты I рода. В общем случае процесс показан на схеме: б) Нитрование. Бензол и его гомологи достаточно легко образуют нитропроизводные, если используется не чистая азотная кислота, а так называемая нитрующая смесь - концентрированные HNO3 и H2SO4: 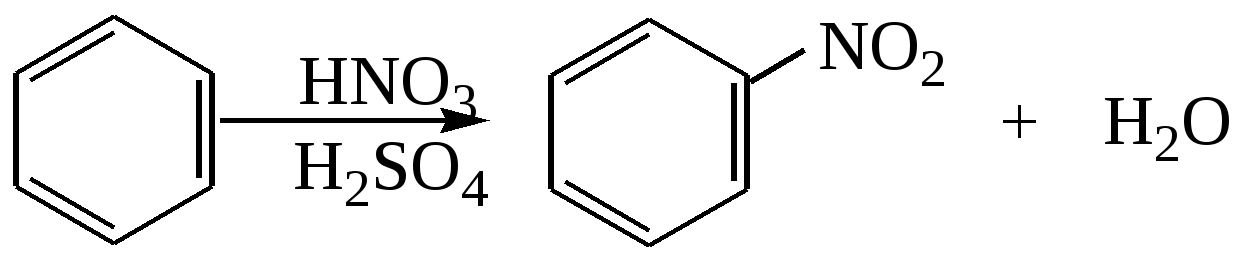 нитробензол 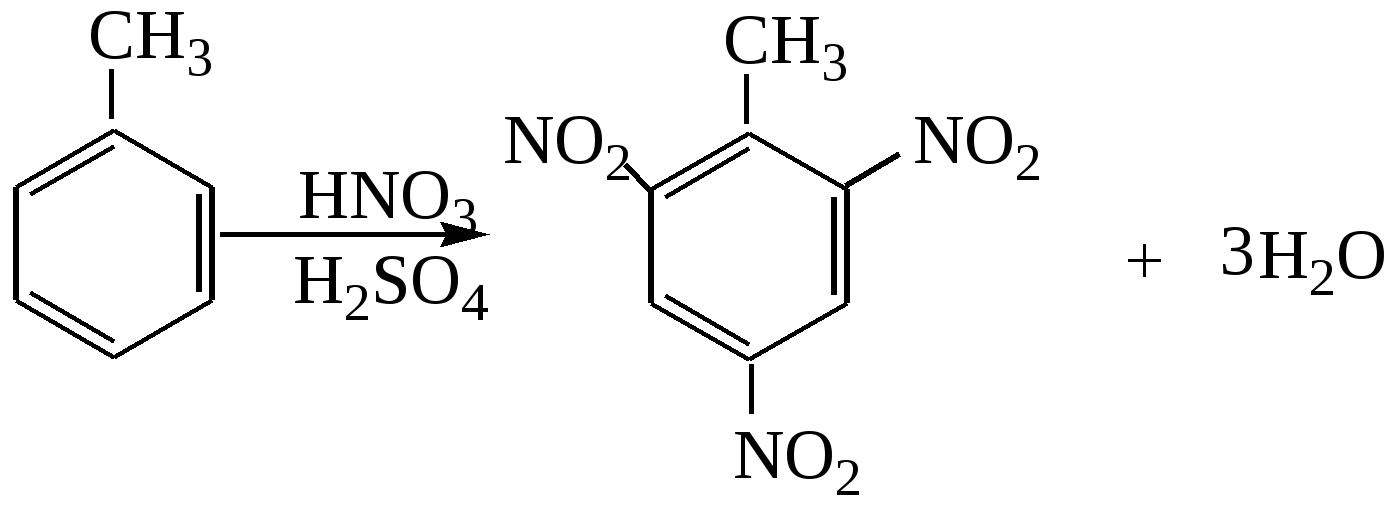 тринитротолуол в) Алкилирование. Как уже упоминалось выше, алкилирование по Фриделю-Крафтсу является одним из основных лабораторных способов получения гомологов бензола: 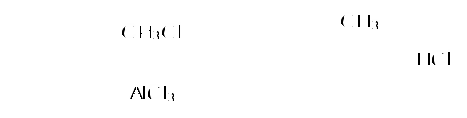 В промышленности широко используется алкилирование алкенами. Роль катализатора в этом случае играет ион водорода Н+. Других продуктов, кроме гомологов бензола, не образуется. При алкилировании этеном (этиленом) получается этилбензол, а в случае пропена (пропилена) образуется изопропилбензол (кумол)  2. Каталитическое гидрирование бензола и его гомологов происходит при повышенном давлении с использованием катализаторов (Ni, Pt). При этом бензол гидрируется до циклогексана, а, например, метилбензол (толуол) – до метилциклогексана. C6H5CH3 + 3H2 Ni 3. Радикальные реакции протекают при взаимодействии паров аренов в жестких условиях (УФ-излучение или температуры порядка 500оС). Надо отметить, что бензол иего гомологи реагируют по разному. В случае бензола реализуется радикальное присоединение 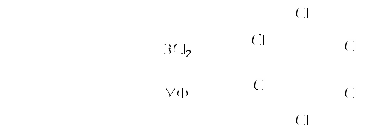 При радикальном хлорировании толуола будут последовательно замещаться атомы водорода по механизму радикального замещения. 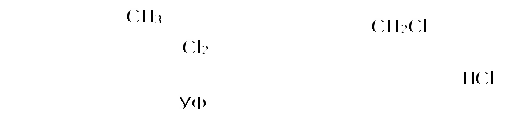 4. Окисление. Окисление более характерно для гомологов бензола. Если гомолог имел только одну боковую цепь, то органическим продуктом окисления будет бензойная кислота. При этом длина и строение цепи значения не имеют. При окислении перманганатом калия в кислой среде гомологов, следующих за толуолом, кроме бензойной кислоты образуется угольная кислота. 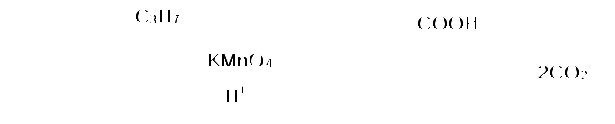 Некоторые свойства стирола. Как уже было сказано выше, стирол не относится к аренам, так как имеет двойную связь, и основным типом химических реакции для него будут реакции присоединения, окисления и полимеризации. Так стирол легко реагирует с бромной водой, обесцвечивая ее, что является качественной реакцией на двойную связь: 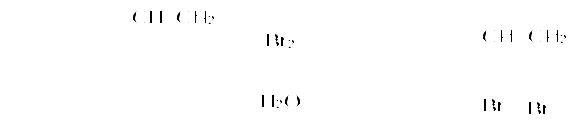 По той же схеме происходит гидрирование стирола на никелевом катализаторе: 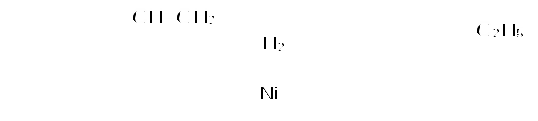 Окисление стирола осуществляется холодным водным раствором перманганата калия, продуктом окисления будет ароматический двухатомный спирт: 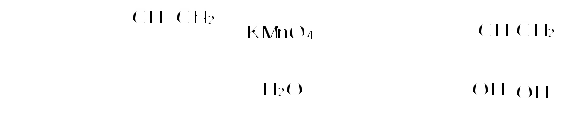 При окислении горячим раствором перманганата калия в присутствии серной кислоты будет образовываться бензойная кислота и углекислый газ. Важной реакцией, имеющей большое практическое значение, является реакция полимеризации стирола: 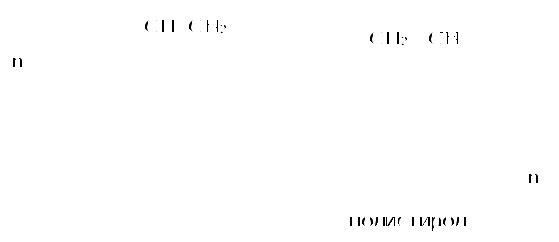 Винильная группа представляет собой ориентант I рода, поэтому дальнейшее каталитическое замещение (например, галогеналканами) пойдет в орто- и пара- положения. 7.3. Примеры решения задач Пример 21. Плотность по озону газовой смеси, состоящей из паров бензола и водорода, равна 0,2. После пропускания через контактный аппарат для синтеза циклогексана величина этой относительной плотности составила 0,25. Определить объемную долю паров циклогексана в конечной смеси и практический выход циклогексана. Решение: 1)Найдем молярную массу исходной смеси: Мсм = D(O3)∙M (O3) = 0.2∙ 48=9.6 г/моль. 2) Молярная масса конечной смеси равна 0,25 ∙ 48=12 г/моль. 3) Найдем молярное соотношение компонентов в исходной смеси Мсм= φ∙М(бенз.) + М(водор.) ∙(1-φ ), где φ-молярная (объемная) доля бензола 9,6 = 78φ + 2(1 –φ); 7,6 = 76φ; φ =0,1. Значит, объемная доля водорода равна 0,9. Следовательно, водород – в избытке, расчет ведем по бензолу. 4) Пусть количество исходной смеси равно 1 моль. Тогда n(C6H6) = 0.1 моль, n(H2) = 0,9 моль, а масса исходной смеси mсм =1∙9,6= 9,6г. Обозначим количество прореагировавшего бензола – z(моль) и составим количественный баланс этой реакции. С6Н6 + 3Н2 = С6Н12 Было 0,1 0,9 0 Прореагировало z 3 z z Запишем эти данные для удобства в виде таблицы:
5) Найдем общее количество веществ в конечной реакционной смеси: n(кон) = 0,1 – z + 0,9 – 3z + z = 1 - 3 z . Так как общая масса веществ в контактном аппарате не изменилась, то n(кон)= mсм/ М(конечн) = 9,6/12 = 0,8моль. 6) Тогда 1 – 3 z = 0,8; 3 z = 0,2; z = 0,067. В таком случае объемная доля циклогексана равна 0,067/0,8 = 0, 084. 7) Теоретическое количество циклогексана составляет 0,1 моль; количество образовавшегося циклогексана 0,067 моль. Практический выход η =0,067/0,1= 0,67 (67,0%). Ответ: φ(циклогексана) = 0,084. η =0,067/0,1= 0,67 (67,0%). Пример 22. На нейтрализацию смеси ароматических кислот, полученных окислением смеси этилбензола и его изомеров, требуется объем раствора гидроксида натрия в пять раз меньший, чем минимальный объем такого же раствора, необходимого для поглощения всего углекислого газа, полученного при сжигании той же порции смеси изомеров. Определить массовую долю этилбензола в исходной смеси. Решение: 1) Этилбензол - С6Н5С2Н5. М = 106 г/моль; его изомерами являются диметилбензолы, имеющие одинаковую молекулярную формулу С6Н4(СН3)2 и ту же молярную массу, что и этилбензол. Пусть количество этилбензола равно х(моль), а количество смеси диметилбензолов – y(моль). 2) Напишем уравнения реакций окисления этилбензола и его изомеров: 5C6H5C2H5 + 12KMnO4 + 18H2SO4 x x + 12MnSO4 + 6K2SO4 + 28H2O 5C6H4(CH3)2 + 12KMnO4 + 18H2SO4 y y + 12MnSO4 + 6K2SO4 + 28H2O Очевидно, что количества бензойной кислоты и смеси фталевых кислот тоже равны x и y соответственно. 3) Уравнения нейтрализации полученных органических кислот: С6Н5СООН + NaOH = С6Н5СООNa + H2O x x С6Н4(СООН)2 + 2NaOH = С6Н4(СООNa)2 + 2 H2O y 2 y Из этих уравнений следует, что общее количество щелочи, пошедшее на нейтрализацию смеси кислот n(общ) = x + 2 y 4) Рассмотрим уравнения сжигания углеводородов, учитывая, что все они имеют молекулярную формулу С8Н10. С6Н5С2Н5 + 10,5 О2 x 8x С6Н4(СН3)2 + 10,5 О2 y 8y 5) Из этих уравнений следует, что общее количество углекислого газа после сжигания исходной смеси аренов равно n(СО2) = 8x + 8y 6) Так как требуется затратить минимальное количество щелочи, то нейтрализация протекает с образованием кислой соли: NaOH + СО2 = NaHCO3 8x + 8y 8x + 8y Таким образом, количество щелочи на нейтрализацию СО2 тоже равно 8x + 8y. В таком случае 8x + 8y = 5(x + 2y ); y =1,5x. x =2/3y 7) Расчет массовой доли этилбензола ω(этилбензола) = m(этилбензола)/m(общ) = 106x/(106x +106y) = 1/ ( 1 +1,5) = 0,4 . Ответ: ω (этилбензола) = 0,4 =40% . Пример 23. Смесь толуола и стирола сожгли в избытке воздуха. При пропускании продуктов сгорания через избыток известковой воды образовалось 220 г осадка. Найдите массовые доли компонентов в исходной смеси, если известно, что она может присоединить 2,24 л HBr (н. у.). Решение: 1) С бромоводородом реагирует только стирол в соотношении 1:1. C8H8 + HBr = C8H9Br 2) Количество вещества бромоводорода n( HBr) = n (C8H8) = 2,24/22,4 = 0,1моль. 3) Запишем уравнение реакции сгорания стирола: C8H8 + 10 О2 В соответствии с уравнением реакции при сгорании 0,1моль стирола образуется 0,8 моль углекислого газа. 4) Углекислый газ реагирует с избытком гидроксида кальция тоже в мольном соотношении 1:1 с образованием осадка карбоната кальция: Ca(OH)2 + СО2 = CaCO3 5) Общее количество карбоната кальция равно n(CaCO3) = m(CaCO3)/ M(CaCO3) = 220/100 = 2,2моль. Значит, при сгорании углеводородов образовалось тоже 2,2моль СО2, из которых 0,8моль дает при сгорании стирол. Тогда на долю толуола приходится 2,2 - 0,8 = 1,4 моль СО2. 6) Уравнение сгорания толуола: C7H8 + 9 О2 Количество толуола в 7 раз меньше, чем количество углекислого газа: n(толуол) = 1,4/7 = 0,2 моль. 7) Масса стирола m(стир.) = n(стир)∙M(стир) = 0,1∙104 =10,4(г); масса толуола m(тол) = n(тол)∙M(тол) =0,2∙92 = 18,4(г). 8) Общая масса смеси углеводородов 10,4 + 18,4= 28,8(г). массовая доля стирола: ω =10,4/ 28,8 = 0,361; массовая доля толуола ω=0,639. Ответ: ω(стирол) = 0,361 = 36,1%; ω(толуол)=0,639=63,9%. 7.4. Задачи и упражнения для самостоятельного решения189. Изобразите графические формулы всех изомеров аренов с общей формулой С9Н12.Назовите эти соединения. 190. Получите а) из метана мета-нитротолуол, б) из этана стирол, в) из н-гептана бензиловый спирт, используя любые неорганические вещества и катализаторы 191. Идентифицируйте следующие соединения: а) бензол, стирол, толуол; б) гексен, циклогексан, толуол; в) этилбензол, стирол, фенол. 192. Осуществите цепочку превращений: кокс HCl Cакт CH3Cl Cl2. а) CaCO3 1000o 500o FeCl3 УФ NaOH C2H4 Br2 KOH KMnO4 б) бензоат натрия сплавл. Н+ УФ спирт H2O t KMnO4 C2H5Cl Cl2 KOH в) н-гептан Cr2O3 Н+ AlCl3 УФ H2O 193. Углеводород С9Н12 прореагировал с бромом при нагревании. В результате было получено соединение состава С9Н5Br7. Напишите структурные формулы всех углеводородов, которые могли бы дать такой результат. Ответ обоснуйте. 194. Изобразите структурную формулу ближайшего гомолога стирола, имеющего цис- и транс-изомеры. Укажите типы гибридизации атомов углерода в этом соединении. 195. В каких из перечисленных веществ все атомы углерода имеют sp2 – гибридизацию: толуол, бутадиен 1,3, циклогексан, этилбензол, стирол, бензол? 196. Из этанола получите этилбензол, не используя другие органические реагенты. Можно использовать любые неорганические вещества и катализаторы. 197. Приведите последовательность реакций, с помощью которых можно из кумола получить изофталевую кислоту (1,3 бензолдикарбоновую кислоту ). 198. а)Сколько изомеров имеет арен, молекула которого содержит 58 протонов. Изобразите и назовите эти изомеры. б)Имеет ли изомеры арен, в молекуле которого содержится 50 электронов? Ответ обоснуйте 199. При циклотримеризации ацетилена при 500оС образовалась газовая смесь с плотностью по воздуху 2,24. Рассчитайте практический выход бензола. 200. В результате циклотримеризации ацетилена при 500оС и давлении 1013 кПа, после охлаждения было получено 177,27мл жидкости с плотностью 0,88г/мл. Определите объем затраченного ацетилена при условиях синтеза, если практический выход составил 60%. 201. При каталитической дегидроциклизации 80 г н-гептана выделилось 67,2 л водорода (н.у.). Рассчитайте практический выход полученного продукта. 202. Углеводород обесцвечивает бромную воду, при действии подкисленного раствора KMnO4 образует бензойную кислоту с выделением диоксида углерода, При обработке избытком аммиачного раствора оксида серебра наблюдается выделение белого осадка. При комнатной температуре исходный углеводород – жидкий, а массовая доля водорода в нем - 6,9%. Определите углеводород. 203. Смесь бензола и циклогексена с молярной долей бензола 80% обесцвечивает 200 г 16%-го раствора брома в тетрахлорметане. Какая масса воды образуется при сгорании в кислороде той же массы смеси? 204. При реакции нитрования бензола избытком нитрующей смеси было получено 24,6г нитробензола. Какой объём бензола(плотность 0,88г/мл) вступил в реакцию? 205. При нитровании одного из аренов массой 31,8 г образовалось только одно нитропроизводное массой 45,3 г. Определите формулу арена и продукта нитрования. 206. Смесь бензола и циклогексана массой 5 г прореагировала с бромом (в темноте и без нагревания) в присутствии бромида железа (III). Объем выделившегося бромоводорода составил 1,12л (н. у.). Определите состав смеси в массовых долях. 207. Рассчитайте массу бромбензола, которая получится при взаимодействии 62,4г бензола с 51,61мл брома с плотностью 3,1г/мл в присутствии бромида железа(III), если выход составляет 90% от теоретического. 208. При каталитическом бромировании 50 мл толуола (плотность 0,867 г/мл) с выходом 75% была получена смесь двух монобромпроизводных и газ, который пропустили через 70 г 40%-го раствора бутена-1 в бензоле.найдите массовые доли веществ в полученном растворе. 209. В результате бромирования 46 г толуола на свету была получена смесь моно- и дибромпроизводных. Объем выделившегося газа составил 17,92 л (н.у.) Какой объем 10%-го раствора карбоната натрия (плотность 1,1г/мл) прореагировал с выделившимся газом, если в полученном растворе молярные концентрации кислой соли и бромоводорода равны. 210. Газ, выделившийся при получении бромбензола из 44,34мл бензола(плотность 0,88г/мл) прореагировал с 8,96л(н.у.) изобутилена. Выход бромбензола составлял 80% от теоретического, а реакция с изобутиленом прошла со 100% выходом. Какие соединения образовались при этом? Рассчитайте их массы. 211. Какой объём 10% раствора гидроксида натрия с плотностью 1,1г/мл потребуется для нейтрализации газа, выделившегося при получении бромбензола из 31,2г бензола? 212. При сжигании 5,2г некоторого углеводорода в избытке кислорода образуется 8,96л углекислого газа (н.у.). Определите истинную формулу вещества, если относительная плотность его паров по гелию равна 26. 213. Смесь стирола и этилциклогексана, способную прореагировать с 4,48л хлороводорода (н.у.) сожгли. При этом образовалось 134,4 г смеси воды и углекислого газа. Найдите объем кислорода, необходимый для сжигания этой же порции смеси. 214. Масса смеси толуола и стирола в 29, 23 раза больше, чем масса водорода, необходимого для полного каталитического гидрирования исходной смеси. Найдите количественное соотношение компонентов смеси. 215. Смесь бензола, толуола и этилбензола массой 13,45 г окислили перманганатом калия в кислотной среде. При этом образовалось 12.2 г бензойной кислоты и 1,12 л (н.у.) углекислого газа. Найдите массовые доли углеводородов в исходной смеси. 216. При сжигании 23,7 г смеси бензола и этилбензола объем затраченного кислорода оказался в 1,2917 раз больше суммарного объема углекислого газа. Определите массовые доли веществ в исходной смеси, а также массу осадка, который образуется при пропускании продуктов горения через избыток раствора известковой воды. 217. При окислении 26,5 г 1,4-диметилбензола горячим нейтральным раствором перманганата калия выпало 66,55 г осадка. Определите, какая часть исходного вещества окислилась. 218. Этилбензол, массой 42,4 г, обработали сначала избытком подкисленного раствора перманганата калия, а затем еще большим избытком раствора КОН. Затем воду выпарили, а сухой остаток прокалили. После конденсации паров получили 26,59 мл бесцветной жидкости с плотностью 0,88 г/мл. Определите практический выход продукта. 219. Смесь стирола и диметилциклогексана, способную обесцветить 320 г 5-ной% бромной воды сожгли на воздухе. При этом образовалось 67,2 г смеси воды и диоксида углерода. Рассчитайте объем воздуха, затраченного на сжигание, если объемная доля кислорода 20%. 220. В одном из аренов массовая доля нейтронов составляет 54,717%. Определите арен, изобразите и назовите его изомеры. 221. Определите истинную формулу углеводорода, если масса одной его молекулы составляет 17,276 .10-23 г, а массовая доля водорода равна 7,69%. 222. Относительная плотность паров углеводорода по неону равна 6. Известно, что углеводород не реагирует с бромной водой, окисляется подкисленным раствором перманганата калия до терефталевой(1,4-бензолдикарбоновой) кислоты, а число атомов углерода составляет 75% от числа атомов водорода. Определите углеводород. 223. Какая масса толуола потребуется для получения 113,5г тринитротолуола, если выход продукта составляет 82% от теоретического? 224. Какой объём бензола (плотность 0,88г/мл) можно получить из 33,6л(н.у.) ацетилена? 225. Для получения изопропилбензола взяли 70,0мл 2-бромпропана с плотностью 1,314г/мл и 39г бензола. Объём полученного изопропилбензола оказался равным 55,5мл(плотность 0,862г/мл). Вычислите выход изопропилбензола. |
