Учебное пособие по химии для учащихся 10 классов, обучающихся в лицеях фдп рниму под редакцией проф. Теплова В. В
 Скачать 3.52 Mb. Скачать 3.52 Mb.
|
Глава 10. КАРБОНИЛЬНЫЕ СОЕДИНЕНИЯК карбонильным соединениям относятся соединения, содержащие карбонильную группу( альдегиды, кетоны) 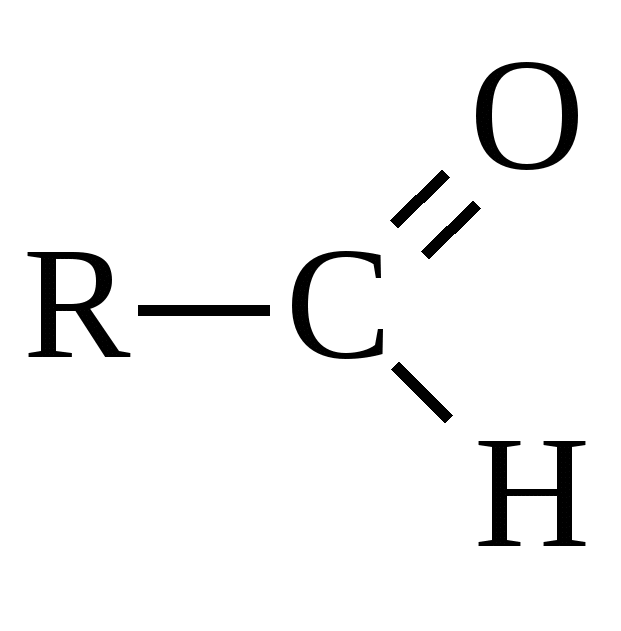 -альдегиды -альдегиды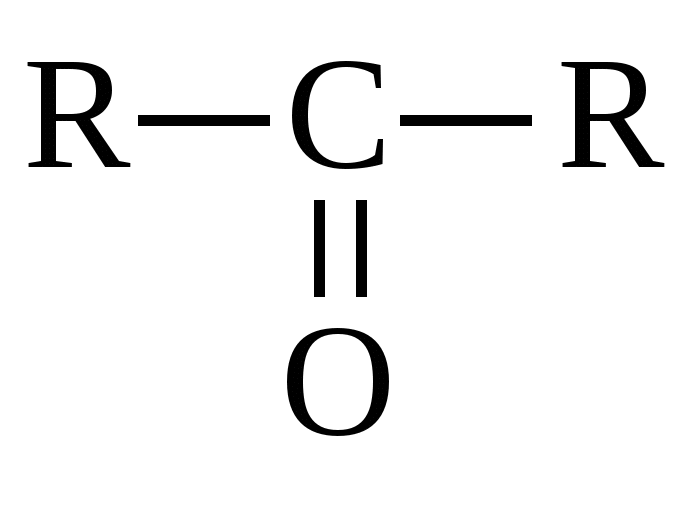 -кетоны. -кетоны. Номенклатура Для альдегидов к названию главной цепи добавляется окончание «аль» или «ал». Для кетонов «он» 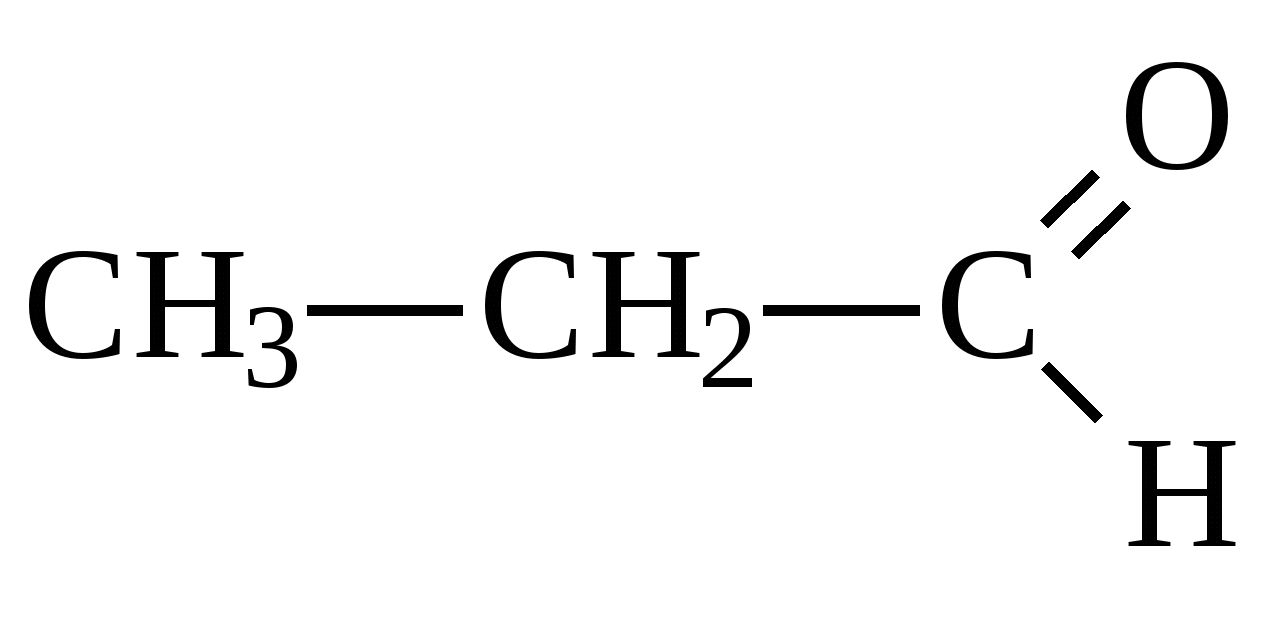 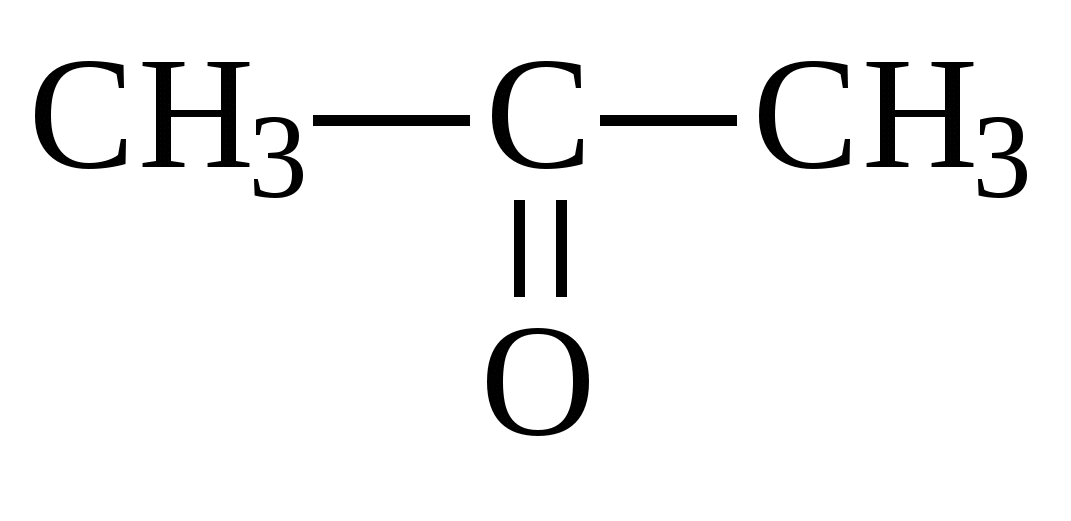 пропаналь пропанон Т 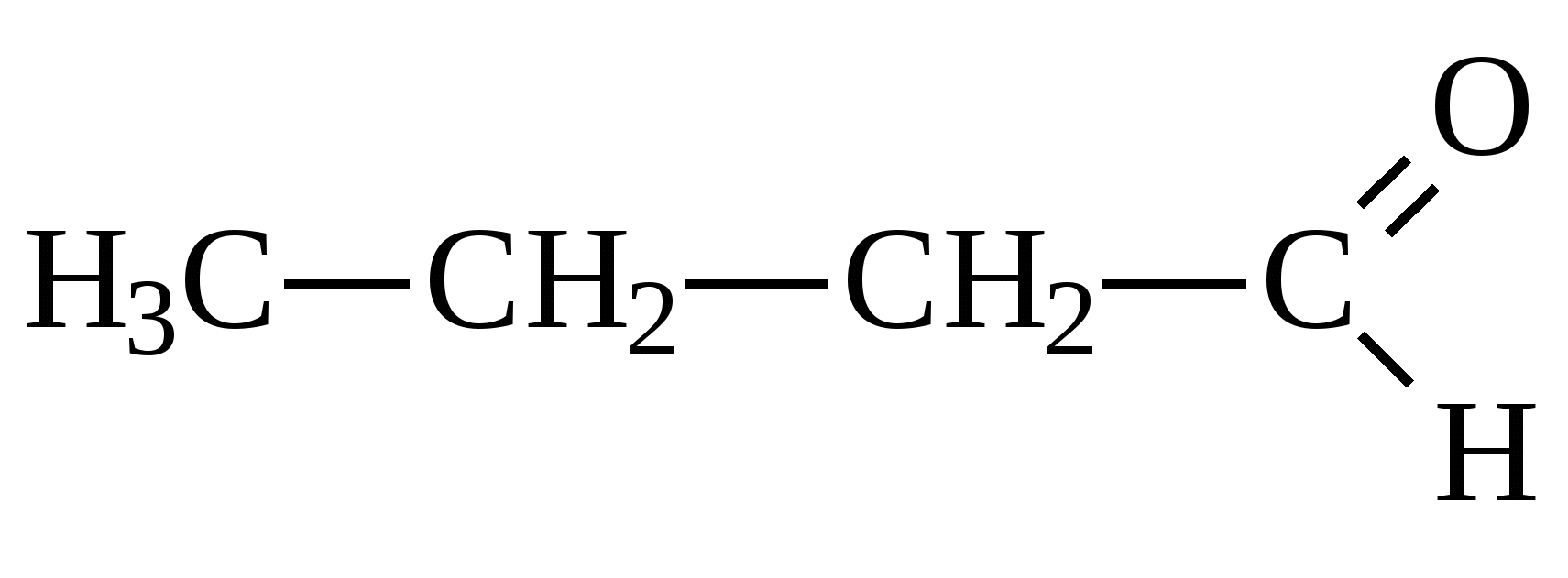 акже альдегиды называются по названию тех кислот, в которые они переходят при окислении. акже альдегиды называются по названию тех кислот, в которые они переходят при окислении.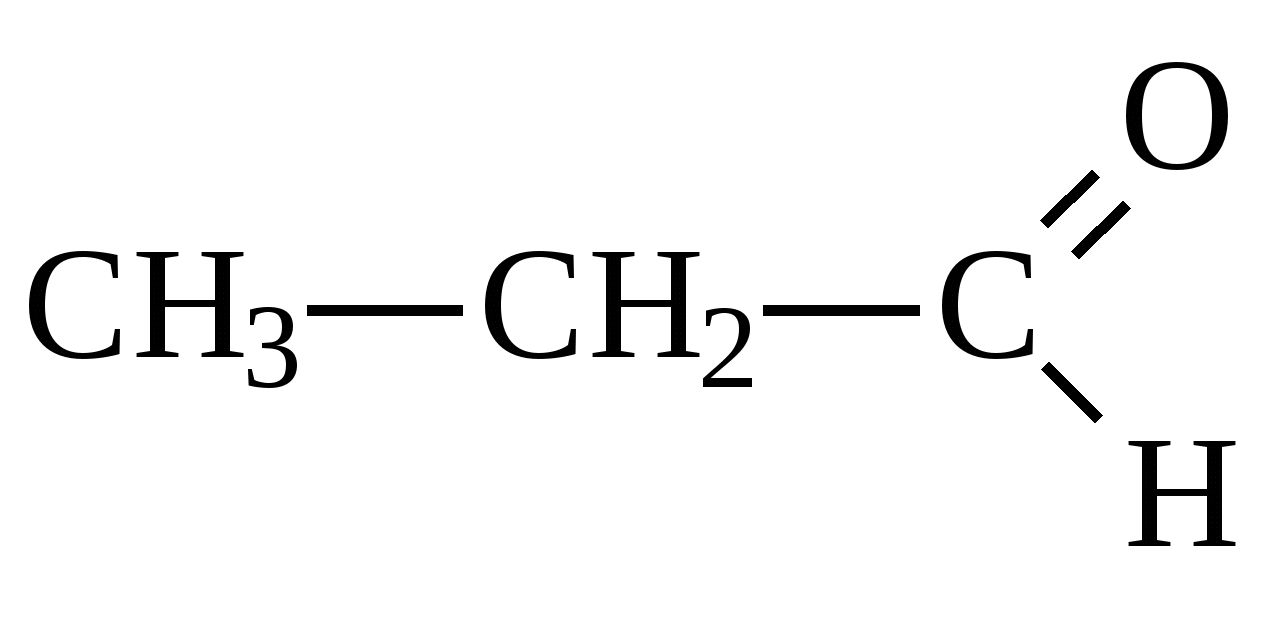 пропионовый альдегид масляный альдегид Изомерия Изомерия альдегидов зависит от изомерии радикалов, соединений с карбонильной группой. 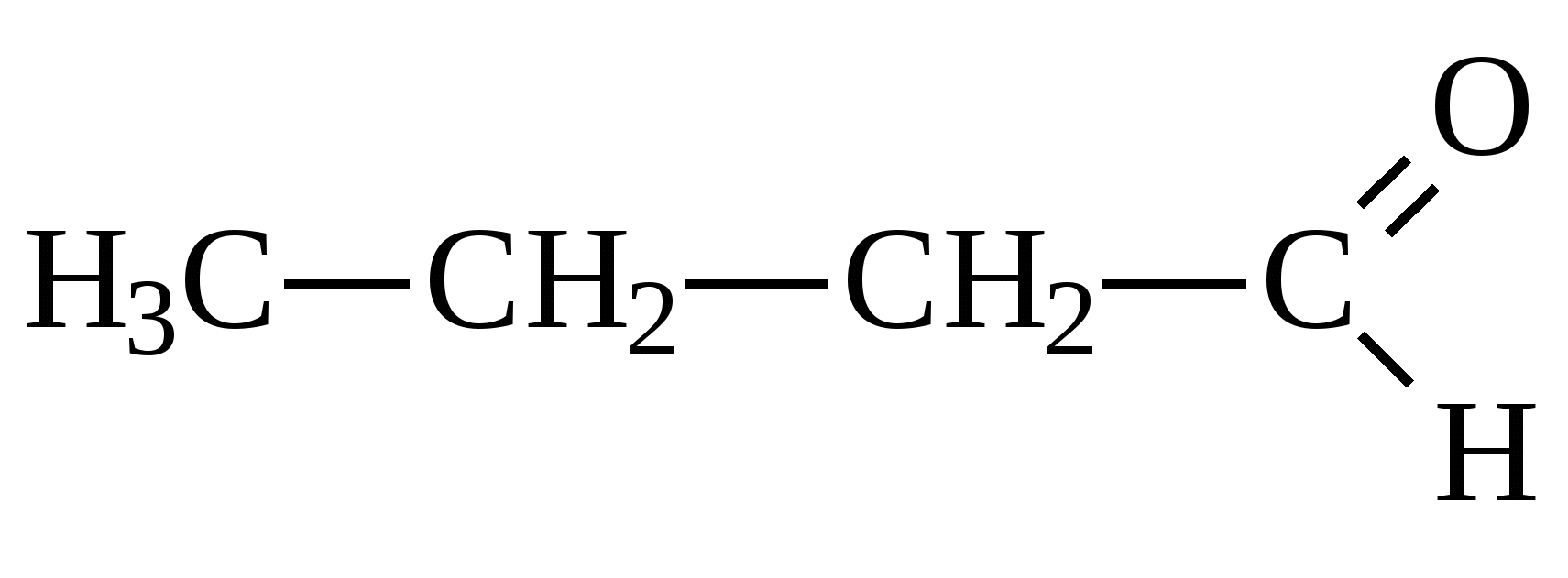 бутаналь( масляный альдегид)  2-метилпропаналь(изомасляный альдегид) Строение карбонильной группы 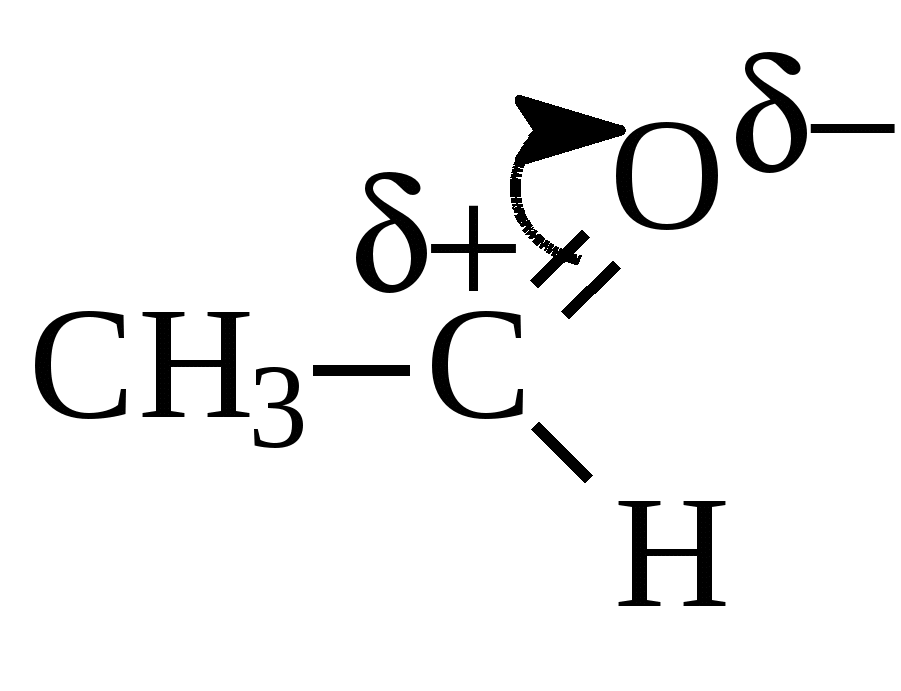 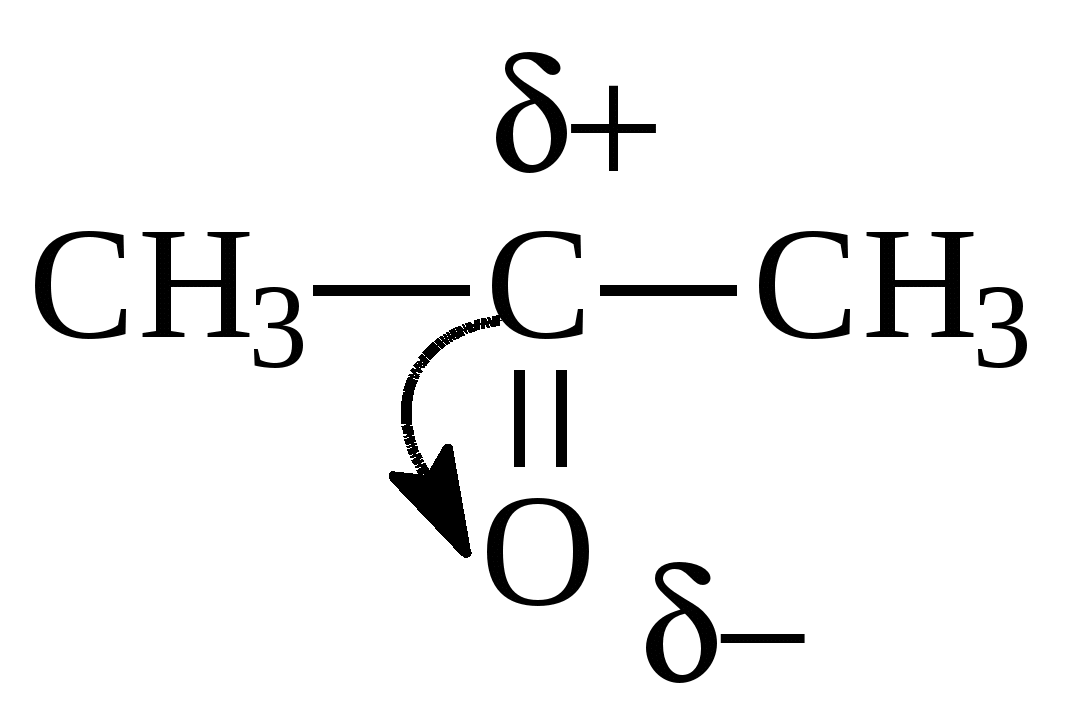 В альдегидах и кетонах карбонильный атом углерода находится в sp2 – гибридном состоянии и образует 3 σ-связи, которые располагаются в плоскости под углом 120о друг к другу. Вследствие большей электроотрицательности атома кислорода электронная плотность π–связи смещена в его направлении. В результате этого у атома кислорода карбонильной группы создаётся повышенная электронная плотность и он приобретает частичный отрицательный заряд δ- а на атоме углерода возникает частичный положительный заряд δ+. Атом углерода приобретает электрофильные свойства и активно взаимодействует с нуклеофильными реагентами (реакции присоединения), а атом кислорода становится нуклеофильным и поэтому способен взаимодействовать с электрофильными реагентами. Большая реакционная способность карбонильной группы объясняется сильной поляризацией этой группы. С одной стороны, атом кислорода оказывает влияние на атом водорода, соединенный с карбонильной группой и он легко окисляется, а с другой стороны, так как есть двойная связь, то для карбонильной группы характерны реакции присоединения по карбонильному углеродному атому, на котором частичный положительный заряд ( Физические свойства. Карбонильные соединения бывают газообразные (формальдегиды); жидкие(уксусный альдегид); твердые(параформ). Также у них нет водородных связей, то температура кипения ниже, чем у спиртов. Имеют характерный запах. 10.1. Получение карбонильных соединений1. Окисление спиртов В качестве окислителей обычно используется CuO(1 стадия окисления), кислород воздуха в присутствии катализаторов(Cu и др.), подкисленный раствор KMnO4 или K2Cr2O7 . При окислении первичных спиртов на первой стадии образуются альдегиды которые далее могут окисляться до карбоновых кислот. Вторичные спирты в этих условиях окисляются до кетонов. Например: 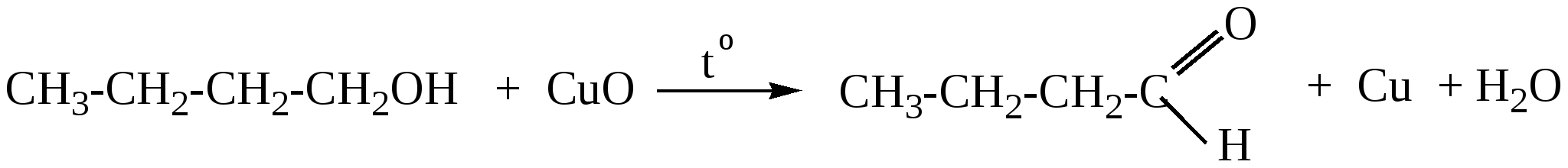 бутаналь 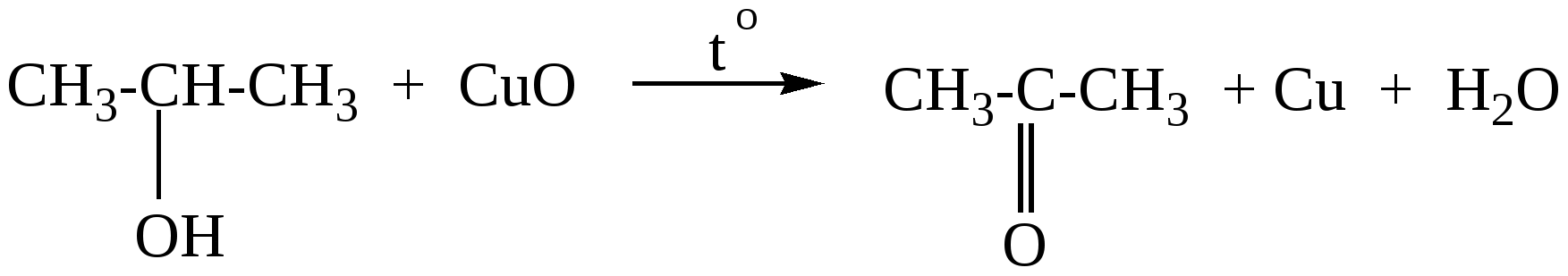 пропанон
 пропаналь 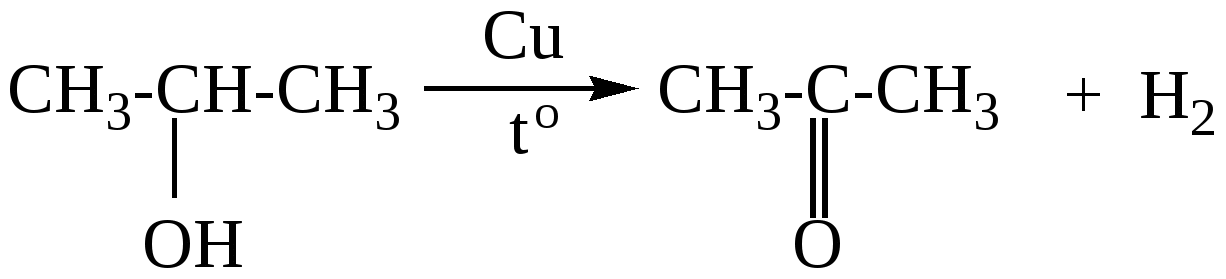 пропанон 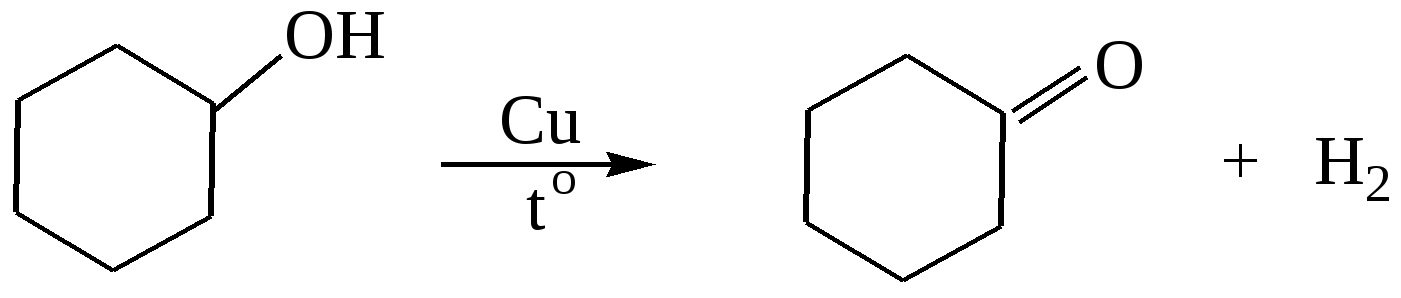 циклогексанол циклогексанон
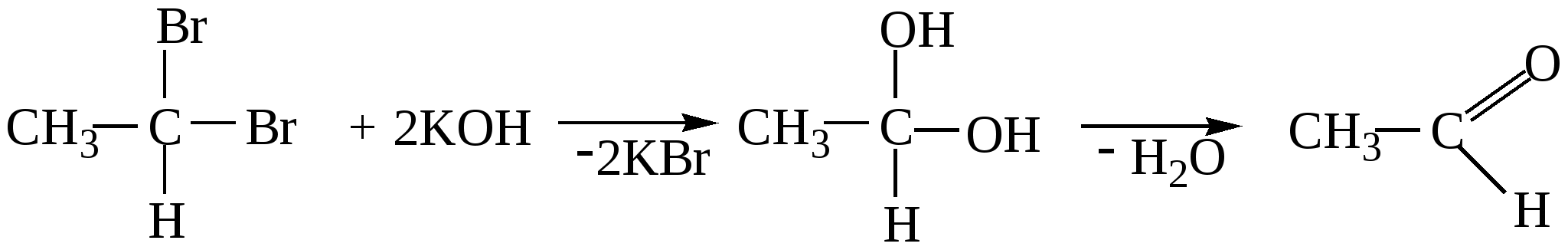 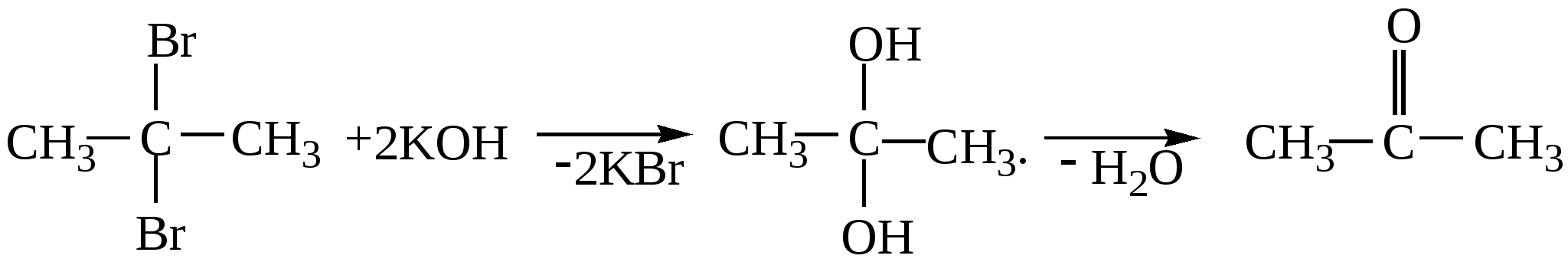 4. Гидратация алкинов (реакция Кучерова). Реакции присоединения воды в присутствии солей Hg2+ . Из ацетилена образуется ацетальдегид, из гомологов ацетилена образуются кетоны. 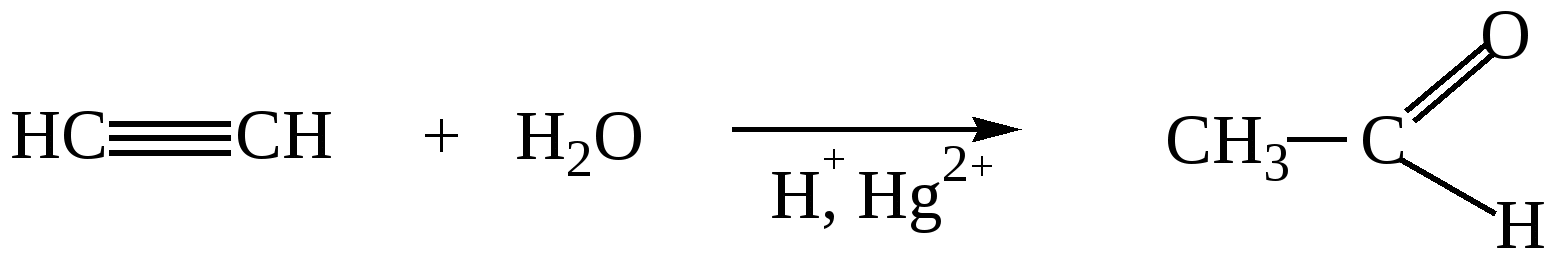 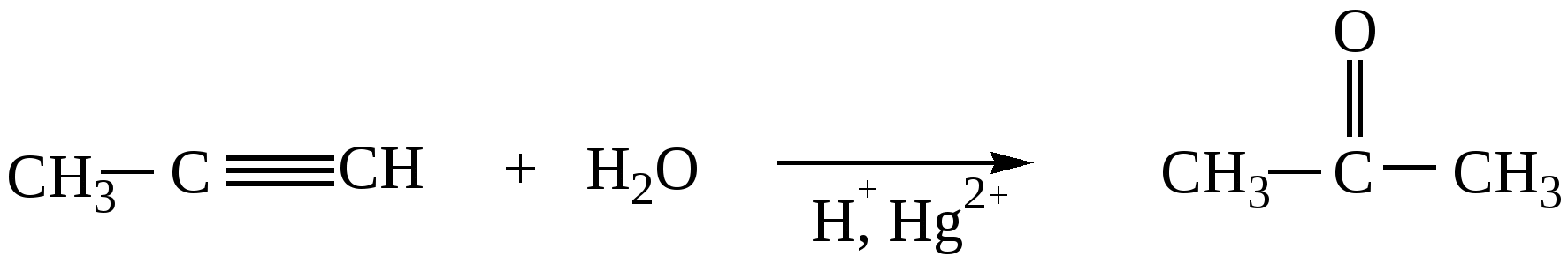 5. Получение ацетона в промышленности - при кумольном методе получения фенола 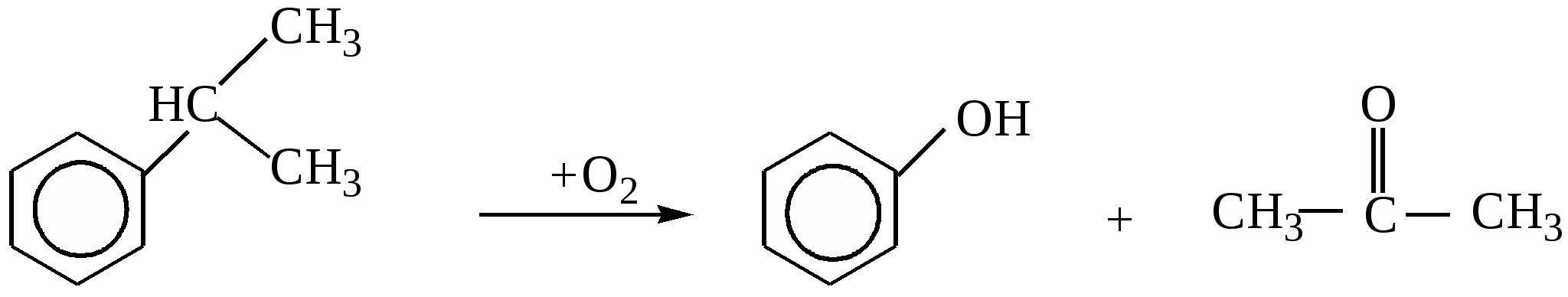 изопропилбензол(кумол) ацетон 6. Ацилирование ароматических соединений по Фриделю-Крафтсу 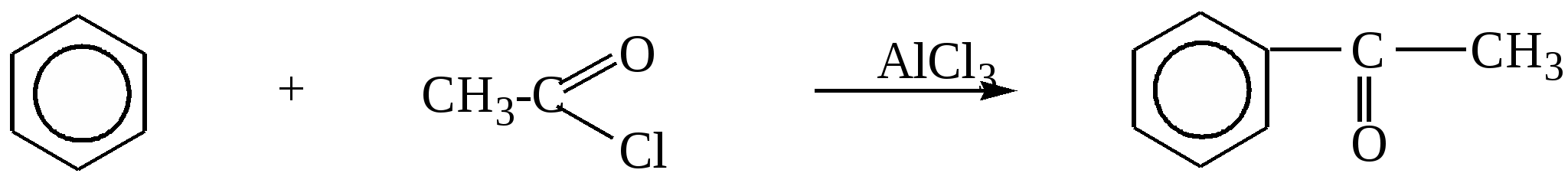 |
