7.6. АНАЛИЗ АЭРОЗОЛЕЙ
Аэрозоли - лекарственная форма, в которой лекарственные и вспомогательные вещества находятся под давлением газа-вытеснителя в аэрозольном баллоне, герметически закрытом клапаном.
ПРОПИСЬ 63 «Каметон» (аэрозоль) Состав на один баллон: Хлорбутанолгидрата 0,1 г или 0,15 г Камфоры 0,1 г или 0,15 г Ментола 0,1 г или 0,15 г Масла эвкалиптового 0,1 гили 0,15 г Масла вазелинового 9,6 г или 14,4 г Дифтордихлорметана (Хладона-12) 20 г или 30 г
Отбор средней пробы для испытания подлинности и количественного определения. С 6 аэрозольных баллонов снимают насадки с предохранительными колпачками. Металлическую капсулу клапана прокалывают металлическим бойком на расстоянии примерно 5 мм от центра. В полученное отверстие для лучшего выхода хладона-12 вставляют иглу для инъекций (игла не должна касаться поверхности раствора) и оставляют баллон в вертикальном положении доля выхода хладона-12. После прекращения шипения выходящего газа осторожно встряхивают баллон и дают ему около 3 минут постоять; принтом происходит удаление дополнительного количества хладона-12. Эту операцию повторяют несколько раз до полного прекращения шипения выходящего газа.
Затем баллон вскрывают, отгибая края металлической капсулы в месте завальцовки. Содержимое баллонов после взбалтывания сливают в колбу вместимостью 100 мл, откуда после тщательного перемешивания отбирают пробы для испытания подлинности и количественного определения. Подлинность. Ментол. К 2 мл препарата прибавляют 1 мл кислоты серной концентрированной и 1 мл свежеприготовленного 1% раствора ванилина в кислоте серной концентрированной; появляется желтое окрашивание, переходящее в фиолетовое при добавлении 1 мл воды. Цинеол, камфора, хлорбутанолгидрат, ментол. Определяют время удерживания указанных веществ на хроматограмме анализируемого раствора при количественном определении. Количественное определение. Содержание камфоры, хлорбутанолгидрата и ментола в препарате определяют методом газовой хроматографии с использованием нафталина в качестве внутреннего стандарта. Условия разделения:хроматограф газовый с пламенно-ионизационным детектором; колонка стеклянная или из нержавеющей стали размером 300 х 0,3 см, заполненная сорбентом - 15% полиэтиленгликолем (М.м. - 20000, карбовакс 20 М) на хроматоне N-AW-DMCS зернения 0,16 - 0,20 мм или 0,315 - 0,430 мм; температура термостата колонки 150° С, испарителя - 200° С; скорость газа-носителя (азота), гелия и водорода - 25 мл/мин, воздуха - 300 мл/мин; скорость диаграммной ленты - 240 мм/час. Методика. Около 5,0 г препарата, охлажденного от хладона-12 (точная навеска средней пробы из шести баллонов), помещают в мерную колбу вместимостью 25 мл прибавляют около 0,05 г (точная навеска) нафталина для хроматографии, 10 мл хлороформа, перемешивают до полного растворения нафталина и доводят объем раствора хлороформом до метки. Около 1 мкл приготовленного ораствора вводят микрошприцем в испаритель хроматографа. Содержание камфоры, хлорбутанолгидрата и ментола в одном баллоне в граммах (X) вычисляют по формуле: где Si - площадь пика определяемого вещества на хроматограмме испытуемого раствора; Soi - площадь пика нафталина;к - поправочный коэффициент для определяемого вещества; а0, - навеска нафталина, г; а - навеска препарата, г;m - масса содержимого, указанная на баллоне, без учета хладона-12, г.Определение поправочного коэффициента. Готовят три модельные смеси, состоящие из масла эвкалиптового, камфоры, хлорбутанолгидрата, ментола и нафталина, взятых в массе около 0,05 г (точная навеска) каждого вещества, помещают в мерную колбу вместимостью 25 мл, прибавляют 5 г масла вазелинового, 10 мл хлороформа, перемешивают до полного растворения компонентов и доводят объем раствора хлороформом до метки.Каждую смесь вводят в испаритель хроматографа не менее двух раз в объеме около 1 мкл и вычисляют поправочные коэффициенты по формуле:к = —- (80) Si а0|I 01где к - поправочный коэффициент для определяемого вещества; Si - площадь пика определяемого вещества; Soi - площадь пика нафталина; aoi- навеска нафталина, г;а - навеска камфоры, хлорбутанолгидрата или ментола, г.В препарате «Ингалипт» (пропись 64) два лекарственных вещества, принадлежащих к одной химической группе, количественно определяют в одной навеске с помощью дифференциальной спектрофотомет-рии.Ингалипт (аэрозоль) Состав на один баллон: Стрептоцида растворимого 0,75 г Норсульфазола-натрия 0,75 г Тимола 0,015 г Масла эвкалиптового 0,015 г Масла мяты перечной 0,015 г Спирта этилового 95% 1,8 г Сахара-рафинада 1,5 г Глицерина 2,1 г Твина-80 0,9 г Воды очищенной до 30 мл Азота от 0,3 до 0,4 г Подлинность. Стрептоцид растворимый. К 0,5 мл препарата прибавляют 10 мл воды, затем последовательно прибавляют 1 мл 3% раствора пероксида водорода и 1 мл раствора железа (III) хлорида; появляется бурое окрашивание, переходящее в темно-красное. Норсульфазол-натрий. 1 мл препарата взбалтывают с 3 мл 0,1 н. раствора натрия гидроксида в течение 2 минут, затем прибавляют 1 мл раствора меди сульфата; образуется осадок грязно-фиолетового цвета. Тимол. 20 мл препарата помещают в делительную воронку, прибавляют 50 мл эфира и взбалтывают в течение 5 минут. Эфир отгоняют. Остаток переносят в фарфоровую чашку, растворяют в 1 мл кислоты уксусной ледяной, прибавляют 0,2 мл кислоты серной концентрированной; появляется красное окрашивание (тимол). Количественное определение. Стрептоцид-растворимый и нор-с ульфазол-натрий. 2 мл раствора препарата и 2 мл раствора стандартных образцов норсульфазола и стрептоцида растворимого помещают в мерные колбы вместимостью соответственно 200 и 100 мл, доводят объем растворов водой до метки и перемешивают. 11о 2 мл каждого из полученных растворов переносят в мерные колбы вместимостью 100 мл, прибавляют по 1 мл 0,1 н. раствора кислоты хлороводородной, доводят объемы растворов водой до метки и перемешивают. Измеряют оптическую плотность полученных растворов на спек-фофотометре при длинах волн 268 и 291 нм в кювете с толщиной слоя 1 см.
Содержание норсульфазола-натрия и стрептоцида растворимого в баллоне в граммах вычисляют по формулам:
. 291А, А 2Г (si:
(- 1,1270 )
1,8770
X
«291
А,
(82)
+ (-0,9435 )
1,6935
норсульфазол натрий (г/1 баллон) X стрептоцид растворимый (г/1 баллон) где Ai - оптическая плотность испытуемого раствора при соответствующих длинах волн; Ао - оптическая плотность раствора стандартного образца при соответствующих длинах волн; (- 1,1270 ), 1,8770, 1,6935, (- 0,9435 ) - расчетные коэффициенты. Приготовление раствора стандартных образцов. 0,4140 г норсульфазола (точная навеска), высушенного до постоянной массы при температуре 100° С, количественно переносят 20 мл 0,1 М раствора натрия гидроксида в мерную колбу вместимостью 50 мл и взбалтывают до растворения. 0,6250 г (точная навеска) стрептоцида растворимого, высушенного до постоянной массы при температуре 100° С, количественно переносят 20 мл воды в ту же мерную колбу вместимостью 50 мл взбалтывают до растворения, доводят объем водой до метки и перемешивают. 8. ИСПОЛЬЗОВАНИЕ РЕФРАКТОМЕТРИИ В ФАРМАЦЕВТИЧЕСКОМ АНАЛИЗЕ8 .1. ОБЩИЕ ПОЛОЖЕНИЯ Если луч света пересекает границу раздела двух прозрачных однородных сред, то направление луча изменяется - происходит его преломление или рефракция.Согласно закону преломления света, отношение синусов углов падения (а) и преломления (Р) - величина постоянная: 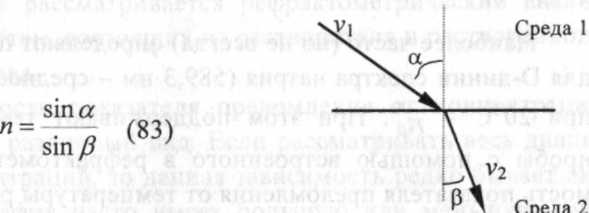 Коэффициент п называется показателемпреломления.Это безразмерная величина, которая указывает, во сколько раз скорость света в «среде 1» больше скорости света в «среде 2»: в'=й (84) Если «среда 1» является вакуумом, то V|- скорость света в вакууме («3x10 8 м/с), а коэффициент п - абсолютныйпоказательпреломления (обычно его определяют для газов). Для жидкостей и твердых тел наиболее часто определяют показатель преломления относительно воздуха. В этом случае п - относительныйпоказательпреломлениявещества. Связь между абсолютным п а6с и относительным п отн показателями преломления имеет вид: ^абс Пв03д X Потн , (85) интерферометры, принцип действия которых основан на интерференции света. Эти приборы позволяют измерять разности показателей преломления с точностью до 10 7 - 1(Г 8, что используется, например, для определения содержания метана в рудничном воздухе (переносные «шахтные» интерферометры) и для исследования обмена веществ при дыхании. • 8 .2. АНАЛИЗ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ, СОДЕРЖАЩИХ ОДНО РАСТВОРЕННОЕ ВЕЩЕСТВОВ данном разделе рассматривается рефрактометрический анализ двухкомпонентных систем, состоящих из растворителя и растворенного лекарственного вещества. График зависимости показателя преломления от концентрации раствора может иметь различный вид. Если рассматривать весь диапазон возможных концентраций, то данная зависимость редко бывает линейной. Напротив, график часто имеет большую или меньшую кривизну, а иногда - максимумы или минимумы. Последнее означает, что одномузначениюпоказателяпреломлениямогутсоответствоватьдве различныеконцентрациираствора.Вместе с тем, научасткахсбольшойкривизнойпризначительныхизмененияхконцентрациираствора показательпреломленияможетменятьсянестольсущественно,что снижаетточностьрефрактометрическихопределений.Вышесказанное можно продемонстрировать на примере водных растворов этилового спирта (рис. 2). Из рисунка видно, что при концентрациях спирта от 0% до примерно 35% зависимость близка к линейной. При концентрациях более 60% показатель преломления изменяется очень незначительно, а при содержании этанола около 80% наблюдается точка максимума, и при дальнейшем увеличении концентрации показатель преломления уменьшается. Важно отметить, что при содержании спирта 58% и выше (кроме точки максимума) одному показателю преломления соответствуют две различные концентрации спирта. Поэтому рефрактометрический анализ водно-спиртовых растворов с целью определения концентрации спирта проводят при содержании этанола до 50%, а более концентрированные растворы перед измерением показателя преломления разбавляют или анализируют по плотности (см. раздел 4 «Рефрактометрический анализ спиртовых растворов»). как в рефрактометрических таблицах для жидких и твердых веществ (и для растворов лекарственных веществ) также приводят значения п охн. Показатель преломления зависит от следующих факторов:
природы вещества;
плотности вещества;
концентрации вещества в растворе;
температуры и давления, при которых проводится измерение (так как они влияют на плотность вещества);
длины волны света.
Наиболее часто (но не всегда) определяют показатель преломления для D-линии спектра натрия (589,3 нм - среднее значение для дублета) при 20°С - nD.При этом поддерживают температуру исследуемой пробы с помощью встроенного в рефрактометр термостата (зависимость показателя преломления от температуры рассмотрена ниже). Из вышесказанного следует, что при прочих равных условиях показатель преломления раствора зависит от концентрации растворенного вещества (или веществ). Прибором для измерения показателя преломления является рефрактометр.Мы не будем останавливаться на его устройстве и принципе работы, поскольку данная тема подробно рассматривается в курсе физики, и больше внимания уделим использованию рефрактометрии в фармацевтическом анализе. Измеряют показатель преломления для различных целей:
идентификация и оценка чистоты веществ;
изучение взаимодействия и превращений компонентов химических систем (комплексообразование, диссоциация, фазовые превращения и др.);
количественное определение.
В фармацевтическом анализе наибольшее значение приобрел количественный анализ растворов лекарственных веществ. С этой целью применяются рефрактометры, позволяющие определять показатель преломления с относительно высокой точностью: n ± 0,0001. {Примечание.Рефрактометр - не единственный прибор, используемый для измерения показателя преломления. В некоторых случаях •%>ебуется более высокая точность и чувствительность анализа. Например, показатели преломления газов при обычных условиях близки к единице, отличаясь на несколько десятитысячных долей. Поэтому в газовом анализе используют 1 m интерферометры, принцип действия которых основан на интерференции света. Эти приборы позволяют измерять разности показателей преломления с точностью до 1(Г 7 - 10" , что используется, например, для определения содержания метана в рудничном воздухе (переносные «шахтные» интерферометры) и для исследования обмена веществ при дыхании. 8 .2. АНАЛИЗ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ, СОДЕРЖАЩИХ ОДНО РАСТВОРЕННОЕ ВЕЩЕСТВО В данном разделе рассматривается рефрактометрический анализ двухкомпонентных систем, состоящих из растворителя и растворенного лекарственного вещества. График зависимости показателя преломления от концентрации раствора может иметь различный вид. Если рассматривать весь диапазон возможных концентраций, то данная зависимость редко бывает линейной. Напротив, график часто имеет большую или меньшую кривизну, а иногда - максимумы или минимумы. Последнее означает, что одномузначениюпоказателяпреломлениямогутсоответствоватьдве различныеконцентрациираствора.Вместе с тем, научасткахсбольшойкривизнойпризначительныхизмененияхконцентрациираствора показательпреломленияможетменятьсянестольсущественно,что снижаетточностьрефрактометрическихопределений.Вышесказанное можно продемонстрировать на примере водных растворов этилового спирта (рис. 2). Из рисунка видно, что при концентрациях спирта от 0% до примерно 35% зависимость близка к линейной. При концентрациях более 60% показатель преломления изменяется очень незначительно, а при содержании этанола около 80% наблюдается точка максимума, и при дальнейшем увеличении концентрации показатель преломления уменьшается. Важно отметить, что при содержании спирта 58% и выше (кроме точки максимума) одному показателю преломления соответствуют две различные концентрации спирта. Поэтому рефрактометрический анализ водно-спиртовых растворов с целью определения концентрации спирта проводят при содержании этанола до 50%, а более концентрированные растворы перед измерением показателя преломления разбавляют или анализируют по плотности (см. раздел 4 «Рефрактометрический анализ спиртовых растворов»). 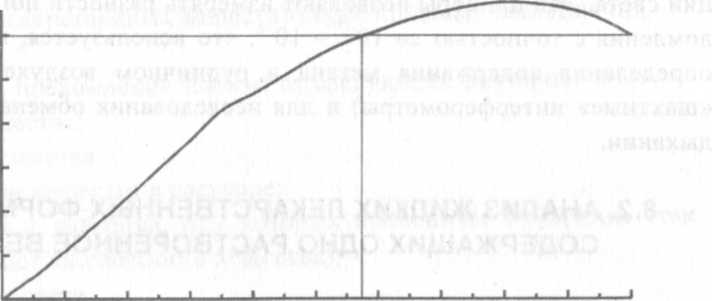 1.3660 г 1.3613 1.3566 1.3519 1.3471 1.3424 1.3377 1.3330 0 10 20 30 40 50 60 70 80 90 100 К'онц. этанола, об.% Рис. 2. График зависимости показателя преломления водных растворов этанола от концентрации (об. %). На примере водно-спиртовых смесей видно, что наиболее точный рефрактометрический анализ возможен только в определенном диапазоне концентраций. Для большинства лекарственных веществ верхний предел этого диапазона находится в области 20-30%.При этом важно отметить, что регламентируется и нижний предел концентрации: вобщемслучаеон составляет 3%.Это связано с тем, что при низком содержании вещества в растворе недопустимо возрастает относительная погрешность рефрактометрического анализа. Продемонстрируем это на примере растворов натрия хлорида с концентрациями 10% и 0,9% в герметически укупоренных флаконах по 400 мл. В обоих случаях колебаниям показателя преломления +0,0001 (максимальная точность измерения) соответствуют колебания концентрации примерно ±0,06%. Но совершенно очевидно, что такие колебания имеют разное значение для 10% и 0,9%. В первом случае относительная погрешность определения концентрации (или массы, что то же самое) е%составляет 0,6%, во втором - 6,7%. Допустимое отклонение от прописанной массы для 400 мл 0,9% раствора (3,6 г) составляет 4%. Следовательно, относительная погрешность количественного определения 6,7% в данном случае неприемлема. Для 400 мл 10% раствора натрия хлорида относительная погрешность определения (0,6%) намного меньше допустимого отклонения от прописанной массы (± 3%). Конечно, можно было бы возразить, что для 0,9% раствора натрия хлорида в ампулах по 5 мл и 10 мл допустимое отклонение от пропи- санной массы (0,045 г и 0,09 г) составляет 15%, а поэтому кажется, что относительная погрешность количественного определения 6,7% вполне приемлема. Но ведь и точность определения показателя преломления в реальных условиях ниже, чем ±0,0001 (согласно ГФ она должна быть не ниже ±0,0Q02). Следовательно, относительная погрешность определения концентрации (массы) может оказаться в два раза выше - примерно 13,4%, что близко к допустимому отклонению 15% и чего при количественном анализе следует избегать. Из вышесказанного следует один частный, но очень важный вывод: изотоническийрастворнатрияхлориданеанализируютметодом рефрактометрии.
|
 Скачать 2.86 Mb.
Скачать 2.86 Mb.