Учебное пособие рекомендовано Управлением учебных заведений Министерства здравоохранения РФ в качестве учебного пособия для студентов фармацевтических институтов и фармацевтических факультетов медицинских вузов
 Скачать 2.86 Mb. Скачать 2.86 Mb.
|
Мазь «Эфкамон» Состав: Камфоры 10 г Масла гвоздичного Масла эфирного горчичного по 3 г Масла эвкалиптового 7 г Ментола 14 г Метилсалицилата 8 г Настойки перца стручкового 4 г Тимола Хлоралгидрата по 3 г Спирта коричного 1 г Парафина нефтяного твердого, Моноглицеридов дистиллированных, Вазелина до 100 г Подлинность. Идентификацию хлоралгидрата, масла горчичного, масла эвкалиптового, ментола, метилсалицилата, масла гвоздичного и тимола проводят с помощью метода ГЖХ одновременно с количественным определением. Содержащийся в настойке перца стручкового капсаицин идентифицируют по реакции с ванадатом аммония. Методика. 2 г препарата помещают в колбу с пришлифованной пробкой вместимостью 25 мл, прибавляют 10 мл 95% спирта, нагревают на водяной бане до расплавления, взбалтывают 3 мин, охлаждают на льду и фильтруют. 5 мл фильтрата помещают в фарфоровую чашку и нагревают на водяной бане до удаления растворителя. К остатку прибавляют 2 мл ацетона, 5 мл кислоты хлороводородной и 0,1 г аммония ваналата; появляется зеленое окрашивание. Количественное определение. Около 1 г (точная навеска) препарата растворяют в 8 мл эфира в мерной колбе вместимостью 10 мл и доводят объем раствора в колбе тем же растворителем до метки. 1 мкл полученною раствора вводят микрошприцем в испаритель газожидко-сгного хроматографа с пламенно-ионизационным детектором. Анализ проводят на двух колонках: I - стеклянная колонка размером 200 х 0,3 см^заполненная сорбенты 5" о S| -30 на хроматоне N-AW-DMCS, зернение 0,16 - 0,20 мм, рс-иользуется для определения масла эвкалиптового; II - стеклянная колонка размером 200 х 0,3 см, заполненная сорбентом - 3% НПГС (неопентилгликольсукцинат) на хроматоне N-AW-DMCS, зернение 0,16 - 0,20 мм, используется для определения камфоры, ментола, метилсалицилата, масла гвоздичного и тимола. Приготовление модельной смеси 1. Около 0,175 г (точная навеска) масла эвкалиптового, 0,075 г (точная навеска) хлоралгидрата, 0,075 г (точная навеска) масла горчичного эфирного растворяют в мерной колбе вместимостью 25 мл и доводят объем до метки тем же растворителем. В модельной смеси 1 масло эвкалиптовое используется для количественного и качественного определений, хлоралгидрат и масло горчичное используются только для определения подлинности. Приготовление модельной смеси 2.Около 0,25 г (точная навеска) камфоры, 0.35 I (точная навеска) ментола, 0,20 г (точная навеска) метилсалицилата. 0,075 г (точная навеска) масла гвоздичного, 0,075 г (точная навеска) тимола синтетического растворяют в эфире в мерной колбе вместимостью 25 мл и доводят объем тем же растворителем до метки. В модельной смеси 2 камфора, ментол, метилсалицилат, масло гвоздичное, тимол используются для количественного и качественного определений. Условия разделения: программированный режим термостата колонок от 60 до 130' С со скоростью 2° С/мин, после завершения программы режим изотермический (130° С) в течение 10 минут; о температура испарителей 180 С; скорость газа-носителя: гелия и водорода 30 см3/мин, воздуха - 300 см /миП' скорость диаграммной ленты 240 мм/час. Параллельно проводят анализ модельной смеси 1 при определении масла эвкалиптового и модельной смеси 2 при определении камфоры, ментола, метилсалицилата, масла гвоздичного и тимола. Количественное определение анализируемых компонентов мази проводят методом абсолютной градуировки. Содержание определяемого компонента (масло эвкалиптовое, камфора, ментол, метилсалицилат, масло гвоздичное, тимол) в процентах в препарате вычисляют по формуле: II - стеклянная колонка размером 200 х 0,3 см, заполненная сорбентом - 3% НПГС (неопентилгликольсукцинат) на хроматоне N-AW-DMCS, зернение 0,16 - 0,20 мм, используется для определения камфоры, ментола, метилсалицилата, масла гвоздичного и тимола. Приготовление модельной смеси 1. Около 0,175 г (точная навеска) масла эвкалиптового, 0,075 г (точная навеска) хлоралгидрата, 0,075 г (точная навеска) масла горчичного эфирного растворяют в мерной колбе вместимостью 25 мл и доводят объем до метки тем же растворителем. В модельной смеси 1 масло эвкалиптовое используется для количественного и качественного определений, хлоралгидрат и масло горчичное используются только для определения подлинности. Приготовление модельной смеси 2. Около 0,25 г (точная навеска) камфоры, 0.35 I (точная навеска) ментола, 0,20 г (точная навеска) метилсалицилата. 0,075 г (точная навеска) масла гвоздичного, 0,075 г (точная навеска) тимола синтетического растворяют в эфире в мерной колбе вместимостью 25 мл и доводят объем тем же растворителем до метки. В модельной смеси 2 камфора, ментол, метилсалицилат, масло гвоздичное, тимол используются для количественного и качественного определений. Условия разделения: программированный режим термостата колонок от 60 до 1301 С со скоростью 2° С/мин, после завершения программы режим изотермический (130° С) в течение 10 минут; температура испарителей 180° С; скорость газа-носителя: гелия и водорода 30 см3/мин, воздуха - 300 см /мин; скорость диаграммной ленты 240 мм/час. Параллельно проводят анализ модельной смеси 1 при определении масла эвкалиптового и модельной смеси 2 при определении камфоры, ментола, метилсалицилата, масла гвоздичного и тимола. Количественное определение анализируемых компонентов мази проводят методом абсолютной градуировки. Содержание определяемого компонента (масло эвкалиптовое, камфора, ментол, метилсалицилат, масло гвоздичное, тимол) в процентах в препарате вычисляют по формуле: S; acmi 10 100 X % = —!—Ш (74) Semi ' 25 • anp где Si - площадь пика определяемого компонента; Semi - площадь пика стандартного образца; acmi - навеска определяемого компонента в модельной смеси, г; апр - навеска препарата, г. В суппозиториях «Релиф» с помощью метода ВЭЖХ проводят идентификацию лекарственных веществ, биологически активного вещества (витамина А) масла печени акулы, консервантов. Количественное определение также проводят указанным методом. ПРОПИСЬ 61 Релиф (суппозитории) Состав на один суппозиторий: Масла печени акулы 3% (75 мг) Масла какао 85,5% (2137 мг) Фенилэфрина гидрохлорида 0,25% (6,25 мг) Метилпарабена 2,5 мг Пропилпарабена 5,0 мг Крахмала 273,5 мг Подлинность. Идентификацию ретинола пальмитата и фенилэфрина гидрохлорида проводят при количественном определении. Метилпарабен и пропилпарабен. Условия разделения: колонка типа Nucleosil С 185 мк размером 150 х 4,6 мм; подвижная фаза - вода-муравьиная кислота-ацетонитрил- метанол (470 : 2,3 : 265 : 265); скорость потока 1,2 мл/мин; УФ-детектор с рабочей длиной волны 254 нм; объем вводимой пробы 10 мкл; растворитель - 96% этанол. Приготовление испытуемого раствора. 1 суппозиторий измельчают, помещают в колбу вместимостью 100 мл, добавляют раствори- тель, гомогенизируют, фильтруют в мерную колбу вместимостью 100 мл и доводят объем растворителем до метки. 1 мл полученного раствора переносят в мерную колбу вместимостью 10 мл, добавляют 1,0 мл основного раствора внутреннего стандарта и доводят объем растворителем до метки. Приготовление основного раствора внутреннего стандарта. 70 мг стандартного образца п-гидроксиэтилбензоата помещают в мерную колбу вместимостью 100 мл, растворяют в растворителе и доводят объем раствора до метки. Приготовление растворов сравнительных стандартных образцов.
Измеряют времена удерживания анализируемых веществ и внутреннего стандарта. Количественное определение. Масло печени акулы. Количественно определяют содержащийся в масле печени акулы ретинол в виде пальмитата с помощью метода ВЭЖХ. Условия разделения колонка из нержавеющей стали с внутренним диаметром 4,6 мм и длиной 15 см; сорбент типа Zorbax с диаметром сферических частиц 5 мкм; скорость потока 0,6 мл/мин; УФ-детектор с переменной длиной волны, рабочая длина волны 235 нм; фильтры вакуумные для подвижной фазы с размером пор 0,45 мкм, устойчивые к тетрагидрофурану и фильтры для очистки образца с размером пор 0,45 мкм типа Найлон 66; объем вводимой пробы 5 мкл; S аы Р 5 100 50 100 Х% = —! °- (76) фенилэфрина Soi а 50 50 • 1000 гидрохлорид где Si - площадь пика фенилэфрина гидрохлорида на хроматограмме испытуемого раствора; Soi - площадь пика фенилэфрина гидрохлорида на хроматограмме раствора стандартного образца; a0j - навеска стандартного образца фенилэфрина гидрохлорида, мг; Р - содержание стандартного образца фенилэфрина гидрохлорида в 1 мл раствора стандартного образца. Суппозитории «Бетиол» (пропись 62) не содержат индивидуальных лекарственных веществ. Содержащиеся в экстракте красавки алкалоиды и сумма солей аммония сланцевых кислот в ихтиоле анализируют с помощью химических и физико-химических методов. ПРОПИСЬ 62 Бетиол (суппозитории) Состав: Экстракта красавки густого 0,015 г Ихтиола 0,2 г Основы для суппозитриев достаточное количество до получения суппозитория массой от 1,05 до 1,35 г Подлинность. Ихтиол идентифицируют по содержащемуся в препарате иону аммония и органолептически. Методика. Один суппозиторий помещают в колбу вместимостью 25 мл, прибавляют 5 мл воды, нагревают на водяной бане до расплав- ления, сильно взбалтывают, охлаждают до застывания основы и фильт- руют через вату. " ^ . Фильтрат должен быть темно-бурого цвета с запахом ихтиола. При нагревании его с 3 мл раствора натрия гидроксида выделяется аммиак, который обнаруживают по посинению влажней красной лакмусовой бумаги. Алкалоиды группы тропана. содержащиеся в экстракте красавки густом открывают характерной для этой группы алкалоидов реакцией Витали-Морена. Суть испытания заключается в том, что при нитровании в жестких условиях с последующим добавлением спиртового раствора калия гидроксида и ацетона образуется мезомерно стабилизированный краситель азаоксонолового типа. 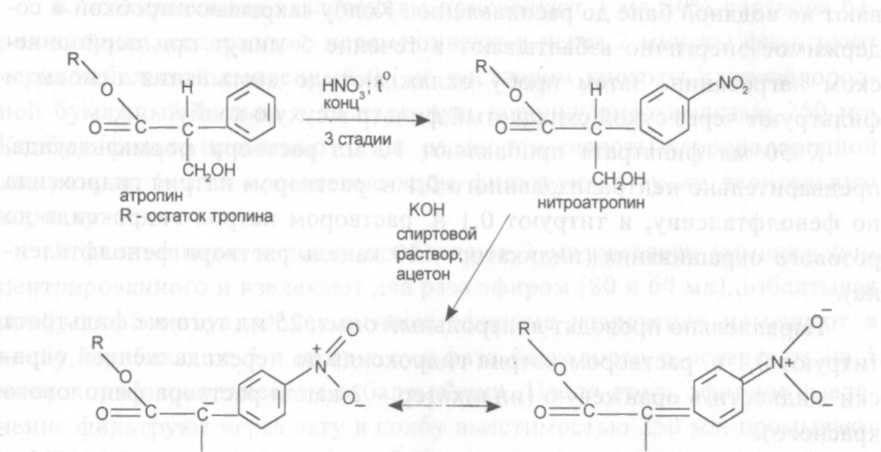 снрн СН2ОН Методика. 5 суппозиториев помещают в коническую колбу вместимостью 100 мл, прибавляют 30 мл 0,1 н. раствора кислоты хлороводородной в насыщенном растворе натрия хлорида, нагревают на водяной бане до расплавления, взбалтывают в течение 10 минут при периодическом нагревании, охлаждают до застывания основы и фильтруют через фильтр, смоченный водой, в делительную воронку. К фильтрату прибавляют около 1 мл раствора аммиака (до щелочной реакции по фенолфталеину), 30 мл хлороформа и взбалтывают в течение 3 минут. Хлороформный слой промывают 50 мл воды и фильтруют в фарфоровую чашку через фильтр с 2 г алюминия оксида «для хроматографии» II степени активности. Хлороформ отгоняют на водяной бане. К остатку прибавляют 0,5 мл кислоты азотной концентрированной и выпаривают на водяной бане досуха. Остаток охлаждают и смачивают 4 каплями 0,5 М спиртового раствора калия гидроксида и 8 каплями ацетона; появляется фиолетовое быстро исчезающее окрашивание. фенилэфрина Soi а 50 50 1000 гидрохлорид где Sj - площадь пика фенилэфрина гидрохлорида на хроматограмме испытуемого раствора; Soi - площадь пика фенилэфрина гидрохлорида на хроматограмме раствора стандартного образца; a0i - навеска стандартного образца фенилэфрина гидрохлорида, мг; Р - содержание стандартного образца фенилэфрина гидрохлорида в 1 мл раствора стандартного образца. Суппозитории «Бетиол» (пропись 62) не содержат индивидуальных лекарственных веществ. Содержащиеся в экстракте красавки алкалоиды и сумма солей аммония сланцевых кислот в ихтиоле анализируют с помощью химических и физико-химических методов. ПРОПИСЬ 62 Бетиол (суппозитории) Состав: Экстракта красавки густого 0,015 г Ихтиола 0,2 г Основы для суппозитриев достаточное количество до получения суппозитория массой от 1,05 до 1,35 г Подлинность. Ихтиол идентифицируют по содержащемуся в препарате иону аммония и органолептически. Методика. Один суппозиторий помещают в колбу вместимостью 25 мл, прибавляют 5 мл воды, нагревают на водяной бане до расплав- ления, сильно взбалтывают, охлаждают до застывания основы и фильт- руют через вату. *«., Фильтрат должен быть темно-бурого цвета с запахом ихтиола. При нагревании его с 3 мл раствора натрия гидроксида выделяется аммиак, который обнаруживают по посинению влажней красной лакмусовой бумаги. Алкалоиды группы тропана, содержащиеся в экстракте красавки густом открывают характерной для этой группы алкалоидов реакцией Витали-Морена. Суть испытания заключается в том, что при нитровании в жестких условиях с последующим добавлением спиртового раствора калия гидроксида и ацетона образуется мезомерно стабилизированный краситель азаоксонолового типа. R \ о R\ HN03;t° \ н ^/N°2 о=с— с—, *" о=с—с—1- 3 стадии . |тр°™? кон нитроатропин СНРНснрн IH R- остаток тропина спиртовой раствор, ацетон О R у0 снрн снрн Методика. 5 суппозиториев помещают в коническую колбу вместимостью 100 мл, прибавляют 30 мл 0,1 н. раствора кислоты хлороводородной в насыщенном растворе натрия хлорида, нагревают на водяной бане до расплавления, взбалтывают в течение 10 минут при периодическом нагревании, охлаждают до застывания основы и фильтруют через фильтр, смоченный водой, в делительную воронку. К фильтрату прибавляют около 1 мл раствора аммиака (до щелочной реакции по фенолфталеину), 30 мл хлороформа и взбалтывают в течение 3 минут. Хлороформный слой промывают 50 мл воды и фильтруют в фарфоровую чашку через фильтр с 2 г алюминия оксида «для хроматографии» II степени активности. Хлороформ отгоняют на водяной бане. К остатку прибавляют 0,5 мл кислоты азотной концентрированной и выпаривают на водяной бане досуха. Остаток охлаждают и смачивают 4 каплями 0,5 М спиртового раствора калия гидроксида и 8 каплями ацетона; появляется фиолетовое быстро исчезающее окраши- Количественное определение. Ихтиол, являющийся суммой аммониевых солей сланцевых кислот, количественно определяют по аммиаку. В основном опыте ион аммония связывают формальдегидом, а сланцевые кислоты титруют стандартным раствором натрия гидроксида. В контрольном опыте формальдегид не используют. 5 суппозиториев помещают в колбу вместимостью 250 мл, прибавляют пипеткой 100 мл насыщенного раствора натрия хлорида и нагревают на водяной бане до расплавления. Колбу закрывают пробкой и содержимое энергично взбалтывают в течение 5 минут при периодическом нагревании. Затем пробу охлаждают до застывания основы и фильтруют через сухой складчатый фильтр в сухую колбу. К 50 мл фильтрата прибавляют 10 мл раствора формальдегида, предварительно нейтрализованного 0,1 н. раствором натрия гидроксида по фенолфталеину, и титруют 0,1 н. раствором натрия гидроксида до розового окрашивания (индикатор - 10 капель раствора фенолфталеина). Параллельно проводят контрольный опыт. 25 мл того же фильтрата титруют 0,1 н. раствором натрия гидроксида до перехода желтой окраски жидкости в оранжевую (индикатор - 2 капли раствора фенолового красного). 1 мл 0,1 н. раствора натрия гидроксида соответствует 0,001703 г NH3 (аммиака). Содержание ихтиола в одном суппозитории (в г) вычисляют по формуле: 0,001703 • (а - 2Ь) • 2 42,37 X = (77) ихтиол 5 (г/1 суппозиторий) где а -- объем 0,1 н. раствора натрия гидроксида, израсходованно- го на титрование испытуемого раствора, мл; b - объем 0,1 н. раствора натрия гидроксида, израсходованно- го на титрование контрольного опыта, мл; 42,37 - коэффициент пересчета аммиака на ихтиол (при содер- жании влаги в ихтиоле 46%); 2 -- разведение; ^ 5 - количество суппозиториев, взятых для определения. Алкалоиды красавки. Один суппозиторий помещают в колбу вместимостью 100 мл, прибавляют 15 мл 0,1 н. раствора кислоты хлороводородной, нагревают на водяной бане до расплавления, взбалтывают в течение 5 минут при периодическом нагревании, затем охлаждают на льду и фильтруют через вату, стараясь не переносить основу на фильтр. Извлечение таким же образом повторяют еще раз 10 мл 0,1 н раствора кислоты хлороводородной, взбалтывая пробу 3 минуты. К объединенным извлечениям прибавляют 4 мл 30% раствора бария хлорида, содержимое перемешивают и через 2 минуты фильтруют через небольшой смоченный 0,1 н. раствором кислоты хлороводородной бумажный фильтр в делительную воронку вместимостью 250 мл. Колбу и фильтр промывают 0,1 н. раствором кислоты хлороводородной два раза по 5 мл и промывные воды фильтруют в ту же делительную воронку. В делительную воронку прибавляют 3 мл раствора аммиака концентрированного и извлекают два раза эфиром (80 и 60 мл), взбалтывая пробу по 5 минут. Объединенные эфирные извлечения помещают в колбу, прибавляют 5 г натрия сульфата безводного и оставляют на 5 минут при периодическом взбалтывании. После этого эфирное извлечение фильтруют через вату в колбу вместимостью 250 мл, промывают колбу и натрия сульфат эфиром (2 раза по 5 мл), который присоединяют к основному раствору. Эфир выпаривают на водяной бане досуха, удаляя остатки продуванием воздуха. Остаток растворяют в 20 мл хлороформа. Раствор переносят в делительную воронку, прибавляют 5 мл гидрофталатного буферного раствора с рН 4,5, 1 мл 1% раствора кислоты пикриновой и встряхивают 2 минуты. Хлороформный слой фильтруют через небольшой смоченный хлороформом бумажный фильтр в мерную колбу вместимостью 25 мл. Колбу с остатком промывают 5 мл хлороформа, который переносят в ту же делительную воронку, и содержимое встряхивают в течение одной минуты. Раствор в мерной колбе доводят хлороформом до метки. Оптическую плотность полученного раствора измеряют на фотоэлек-троколориметре при длине волны около 364 нм в кювете с толщиной поглощающего слоя 1 см. Параллельно измеряют оптическую плотность раствора стандартного образца атропина сульфата. В качестве раствора сравнения используют хлороформ. Содержание суммы алкалоидов красавки в одном суппозитории в пересчете на гиосциамин в граммах вычисляют по формуле: сумма алкалоидов красавки (г/1 суппозиторий) где А - оптическая плотность испытуемого раствора; А0 - оптическая плотность раствора стандартного образца; b - содержание атропина сульфата в 1 мл раствора стандартного образца в пересчете на гиосциамин, г. ■ |
