Учебное пособие рекомендовано Управлением учебных заведений Министерства здравоохранения РФ в качестве учебного пособия для студентов фармацевтических институтов и фармацевтических факультетов медицинских вузов
 Скачать 2.86 Mb. Скачать 2.86 Mb.
|
|
Выделение газообразных продуктов происходит при сочетании веществ с выраженными кислотными свойствами с солями слабых летучих кислот (цианидами, сульфидами, карбонатами, нитритами, на- Между ингредиентами, входящими в состав смесей, могут происходить химические реакции, обусловленные взаимодействием ионов, реже - молекул, что приводит к явлению несовместимости. Взаимодействие между ингредиентами может стать причиной несовместимости только тогда, когда реакция протекает до конца, т.е. становится практически необратимой. Таким образом, ингредиенты будут несовместимы, если при их химическом взаимодействии происходит выпадение осадков, выделение газов, протекают окислительно-восстановительные процессы или гидролиз. Химические несовместимости легче всего распознать при наличии внешних проявлений взаимодействия (выделение газа, образование осадка, изменение цвета, запаха, агрегатного состояния). Рассмотрим некоторые типичные случаи химической несовместимости. Так, несовместимости, сопровождающиеся выпадением осадков, могут привести к завышенной дозировке, что особенно опасно для осадков ядовитых и сильнодействующих веществ. Осадки органических оснований (алкалоидов и органических синтетических оснований) образуются при сочетании лекарственных веществ, являющихся солями алкалоидов или синтетических органических оснований с растворимыми карбонатами, иатрия тетраборатом, солевыми формами барбитуратов и сульфаниламидов, гидрофосфатами и другими веществами, обуславливающими в водных растворах щелочную реакцию среды. Например, в прописи 43 30% раствор сульфацил-натрия создает рН = 9,5, при котором в осадок выпадает основание ди-каина. ПРОПИСЬ 43 Дикаина 0,1 Раствора сульфацил-натрия 30% - 10,0 мл Выделение основания дикаина можно предотвратить, если использовать в качестве растворителя 2% раствор кислоты борной, создающей рН п6,9. Прописанный в рецепте (пропись 44) кофеин-бензоат натрия создает щелочную среду, в результате чего выпадает в осадок основание папаверина. ПРОПИСЬ 44 Папаверина гидрохлорида Новокаина по 0,2 Кофеина-бензоата натрия 0,8 Воды для инъекций 20,0 мл трия тиосульфатом и др.), а также при взаимодействии веществ с выраженными основными свойствами с солями летучих оснований (соли аммония, гексаметилентетрамин, различные амины). Например, в процессе приготовления прописи 45 наблюдается выделение пузырьков оксида углерода (1У)^вследствие взаимодействия кислоты хлороводородной и натрия гидрокарбонатом. ПРОПИСЬ 45 Натрия хлорида 6,2 Натрия гидрокарбоната 2,5 Кислоты хлороводородной разведенной 4,4 мл Воды для инъекций до 1,0 л Чтобы избежать выделения оксида углерода (IV), необходимо приготовить данную пропись без натрия гидрокарбоната. Более сложными примерами несовместимых сочетаний ингредиентов являются случаи, сопровождающиеся реакциями, проходящими без видимых изменений: гидролиз сложных эфиров, инактивация гли-козидов, антибиотиков, ферментов и других лекарственных веществ. Реакция гидролиза органических лекарственных веществ, как правило, обусловлены взаимодействием воды со сложными эфирами, а также амидами и гликозидами. Гидролиз лекарственных веществ по указанным функциональным группам приводит к образованию малоактивных, неактивных или токсичных продуктов. Лекарственные вещества - гликозиды легко подвергаются гидролизу в кислой среде или в присутствии ферментов. Важнейшими лекарственными веществами этой группы являются сердечные гликозиды, распадающиеся при кислотном гидролизе на простые сахара и агликоны группы циклопетанпергидрофенантрена. А в щелочной среде происходит изомеризация агликона с образованием фармакологически неактивного продукта. Например, в прописи 46 происходит изомеризация сердечных гликозидов горицвета (главным образом цимарина и адонитоксина) вследствие щелочной среды, создаваемой эуфиллином:  он о О изоагликон (фармакологически неактивный) ПРОПИСЬ 46 Настоя травы горицвета 6,0 - 200,0 мл Папаверина гидрохлорида 0,6 Натрия бромида 4,0 Эуфиллина 2,0 Чтобы сделать пропись рациональной, необходимо выписать эу-филлин отдельно в виде таблеток или дозированных порошков. К лекарственным веществам, представляющим собой амиды кислот, относятся пенициллин, левомицетин, тетрациклины и др. Пенициллин содержит очень лабильное лактамное кольцо, легко подвергающееся гидролизу под действием кислот, щелочей, а также некоторых спиртов, солей тяжелых металлов и ферментов. Даже органические кислоты, как аскорбиновая или салициловая, превращают пенициллин в неактивную кислоту пенилловую (минеральные кислоты приводят к более глубокому гидролитическому расщеплению антибиотика). Вещества щелочного характера раскрывают лактамное кольцо пенициллина и приводят к образованию фармакологически неактивных солей кислоты пенилловой. Соли тяжелых металлов (Pb2+, Hg2+ и др.) инактивируют пенициллин вследствие расщепления тиазолидинового кольца и, кроме того, образуют с антибиотиком плохо растворимые соединения. Поэтому не рекомендуется смешидать пенициллиновые мази с цинковой, ртутной и свинцовыми мазями< 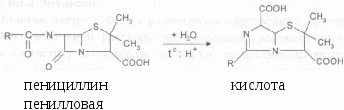 Нагревание антибиотика приводит к его инактивации. Особенно быстро инактивируются водные растворы, срок хранения которых в прохладном месте составляет 1 - 2 дня: 7. АНАЛИЗ ПРЕПАРАТОВ ЗАВОДСКОГО ИЗГОТОВЛЕНИЯ Лекарственные формы заводского изготовления содержат смеси различных веществ (лекарственных веществ, вспомогательных веществ, стабилизаторов, антиоксидантов и др.). Поэтому методический подход к анализу лекарств заводского изготовления, базирующийся на физико-химических свойствах ингредиентов, аналогичен подходу при экспресс-анализе препаратов аптечного производства. Вместе с тем, анализ лекарственных средств заводского изготовления имеет и ряд существенных отличий. Так, на каждое лекарство заводского изготовления имеется нормативная документация (НД) - фармакопейная статья (ФС), фармакопейная статья предприятия. Лекарства заводского изготовления подлежат масштабному лабораторному анализу с использованием физико-химических методов (ИК- и УФ- спектрофотометрия, ГЖХ, ВЭЖХ, полярография и др.) и с применением Государственных стандартных образцов лекарственных веществ. При этом каждое лекарство должно соответствовать требованиям общей фармакопейной статьи на собственную лекарственную форму:
Определенным требованиям по общим статьям должны отвечать также аэрозоли, капли глазные, гранулы, порошки, мази, настои и отвары, настойки, пластыри, порошки, сиропы, суппозитории, суспензии, экстракты, эмульсии. Многие частные ФС на различные лекарственные препараты (например, таблетки и растворы для инъекций) регламентируют испытание на чистоту для содержащихся в них лекарственных веществ. При проведении экспресс-анализа провизор-аналитик, как правило, руководствуется методическими указаниями, учебными пособиями, специальной научной и периодической литературой, где приводятся методики анализа сложившихся лекарственных смесей. Но может предложить и использовать собственную методику или выбрать одну из опубликованных. Соответствие лекарственной смеси действующим венные формы с пенициллином должны изготовляться в асептических условиях. Фармакологические несовместимости представляют собой различные комбинации лекарственных веществ, вызывающие изменение жизненно важных функций организма, что является предметом подробного изучения фармакологии. 7.1. АНАЛИЗ ТАБЛЕТОК Как и в экстемпоральной рецептуре, состав таблеток, имеющих несколько лекарственных веществ, весьма разнообразен. Здесь также встречаются лекарственные вещества из разных химических групп и, кроме того, содержатся вспомогательные вещества. Таким образом, таблетки, содержащие только одно лекарственное вещество, в сочетании со вспомогательными веществами можно рассматривать как лекарственную смесь. В разделе, посвященном анализу экстемпоральной рецептуры, представлена пропись 15, содержащая 0,1 г кислоты аскорбиновой и 0,5 г глюкозы. Поскольку смесь аналогичного состава выпускается и в виде таблеток, представляется целесообразным сравнить методики их анализа. ПРОПИСЬ 47 Таблетки кислоты аскорбиновой 0,1 г с глюкозой Состав на одну таблетку: Кислоты аскорбиновой 0,1 г Глюкозы 0,877 г Вспомогательных веществ до получения таблетки массой 1,0 г Глюкозу в присутствии кислоты аскорбиновой рационально определять общей' для моносахаридов реакцией Селиванова. Здесь при 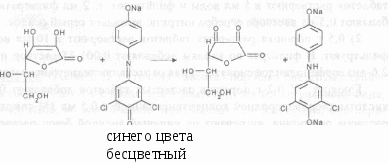 Подлинность кислоты аскорбиновой подтверждают реакциями с раствором серебра нитрата (химизм - см. пропись 15 стр. 29,54) и с 2,6-дихлорфенолиндофенолятом натрия (по исчезновению синей окраски реактива): приказам о качестве экстемпоральных лекарств провизор-аналитик проверяет по результатам анализа с помощью норм допустимых отклонений (см. приложение). Фармацевтический анализ лекарств заводского изготовления требует неукоснительного соблюдения методик, приведенных в НД, то есть является фармакопейным. Способы расчета содержания лекарственных веществ в дозированных лекарственных формах заводского изготовления принципиально не отличаются от таковых в экстемпоральной рецептуре. Так, например, в таблетках, капсулах и других дозированных лекарственных формах определяют массу каждого из входящих в лекарственную форму лекарственных веществ в граммах на одну таблетку (капсулу). При прямом титровании без контрольного опыта применяют формулу: X = (г/1 таблетку или капсулу) где V - объем титрованного раствора, в мл; к - коэффициент поправки на титрованный раствор; Т - титр по определяемому веществу (титриметрический фактор пересчета); а - навеска препарата , в г; b - средняя масса одной таблетки или другой дозированной лекарственной формы, в г. Данная формула идентична формуле 4, применяемой для расчетов экстемпоральных лекарственных смесей. Также аналогичны с приведенными ранее для экстемпоральной рецептуры и способы расчета с применением разведений, контрольного опыта и обратного титрования. Сказанное относится и к растворам для инъекций, мазям, аэрозолям и другим лекарствам промышленного изготовления. Поэтому при приведении способов расчета будут даны ссылки на приведенные ранее формулы. Вместе с тем, при количественном определении ингредиентов в лекарственных средствах заводского изготовления, применяются и другие способы расчета, особенно при сочетании химических и физико-химических методов анализа. взаимодействии глюкозы с раствором кислоты хлороводородной концентрированной происходит дегидратация молекулы глюкозы с образованием 5-гидроксиметилфурфурола, который при дальнейшем нагревании со спиртовым раствором резорцина дает окрашенный в красный цвет продукт конденсации: 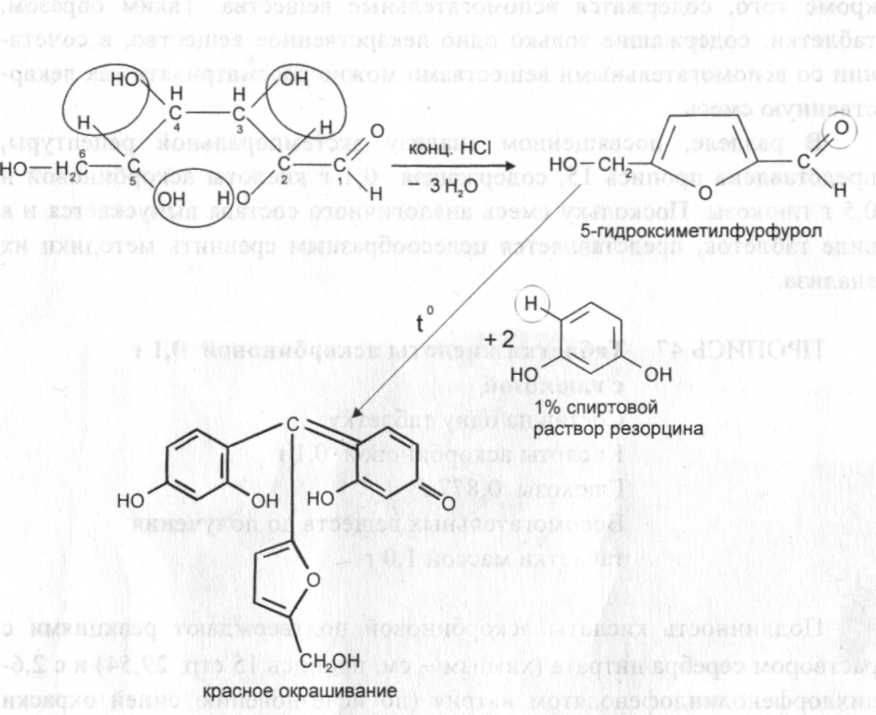 Подлинность. Кислота аскорбиновая. 1) 0,5 г порошка растертых таблеток растворяют в 5 мл воды и фильтруют. К 2 мл фильтрата прибавляют 0,5 мл раствора серебра нитрата; выпадает серый осадок. 2) 0,5 г порошка растертых таблеток растворяют в 10 мл воды и фильтруют. В фильтрат по каплям добавляют 0,001 М раствор натрия 2,6-дихлорфенолиндофенолята; синяя окраска последнего исчезает. Глюкоза. К 0,2 г порошка растертых таблеток добавляют 0,5 мл кислоты хлороводородной концентрированной и 0,5 мл 1% спиртового раствора резорцина, нагревают на кипящей водяной бане; раствор окрашивается в красный цвет. Количественное определение. Как указывалось ранее (стр. 54), количественное определение кислоты аскорбиновой и глюкозы прово- дят в одной навеске методом йодометрического титрования в нейтральной и щелочной средах. В лекарственной форме заводского изготовления для повышения точности анализа целесообразно применение раздельного определения лекарственных веществ. Глюкозу определяют йодометрически в щелочной среде (химизм - см. стр. 60). В другой навеске проводят количественное определение кислоты аскорбиновой методом йодатометрии: ОН ОН 0 0 н н 3 = 0 + KI + ЗН,0 > = 0 + К10, --♦ 3 -о-^ н + но—сн но—сн СНГЭН CHfJH КГОз + 5 KI + 6 НС1 = 3 12 + 6 КС1 + 3 Н20 Методика. Кислота аскорбиновая. Около 0,5 г (точная навеска) порошка растертых таблеток растворяют в 20 мл воды, прибавляют 0,5 мл 1% раствора калия йодида, 2 мл раствора крахмала и 1 мл 2% раствора кислоты хлороводородной и титруют 0,1 н. раствором калия йодата до появления стойкого светло-синего окрашивания. 1 мл 0,1 н. раствора калия йодата соответствует 0,008806 г СбН80б (кислоты аскорбиновой). • V vT h vkio3' ккюз 1 кю,/к-та аскорб. ' X = • кислоты а И1Ртабл, СМ. формулу (33) Глюкоза. Около 0,12 г (точная навеска) порошка растертых таблеток растворяют в 10 мл воды, прибавляют 25 мл 0,1 н. раствора йода, затем медленно, по одной капле через каждые 2-3 секунды, при перемешивании прибавляют 10 мл 1% раствора натрия гидроксида и оставляют на 5 минут в темном месте. Через 5 минут прибавляют 5 мл кислоты серной разведенной и избыток йода оттитровывают 0,1 н. раствором натрия.тиосульфата (индикатор - крахмал). Подлинность эфедрина гидрохлорида подтверждают образованием комплексного соединения с меди (II) сульфатом, экстрагируемого из щелочного раствора эфиром, а димедрола -получением окрашенной оксониевой соли (см. пропись 12). Методика. Эфедрина гидрохлорид. 0,5 г порошка растертых таблеток взбалтывают с 5 мл воды в течение двух минут и фильтруют. К фильтрату прибавлЛот 0,1 мл раствора меди (II) сульфата и 1 мл раствора натрия гидроксида; появляется синее окрашивание, быстро переходящее в фиолетовое. При взбалтывании полученного раствора с 1 мл эфира эфирный слой окрашивается в фиолетово-красный цвет, а водный слой сохраняет синее окрашивание. Димедрол. 0,1 г порошка растертых таблеток взбалтывают с 10 мл хлороформа в течение двух минут, хлороформное извлечение фильтруют в фарфоровую чашку и хлороформ выпаривают досуха. К остатку прибавляют 2 мл смеси, состоящей из 1 мл кислоты азотной концентрированной и 9 мл кислоты серной концентрированной; появляется красное окрашивание. Затем прибавляют по каплям при постоянном перемешивании и охлаждении 5 мл воды; окраска переходит в коричневую, а затем в оранжевую. При взбалтывании полученного раствора с 3 мл хлороформа слой органического растворителя окрашивается в фиолетовый цвет, переходящий в коричнево-красный. Количественное определение. Оба вещества в своих молекулах имеют одинаковые хромофорные группы и, следовательно, поглощают УФ-излучение в одной области спектра. Вследствие этого их нельзя анализировать с помощью УФ-спектрофотометрии при совместном присутствии, а разделение этих лекарственных веществ крайне затруднительно из-за сходных физико-химических свойств. Однако димедрол не влияет на образование комплексного соединения эфедрина с ионом Си2+ с последующей экстракцией в органический растворитель. Это позволяет провести экстракционно-фотометрическое определение эфедрина гидрохлорида в присутствии димедрола. При этом в качестве органического экстрагента, в отличие от методики определения подлинности лекарственного вещества, используют не быстро улетучивающийся эфир, а н-бутанол. Методика. Около 0,25 г (точная навеска) порошка растертых таблеток помещают в делительную воронку вместимостью 100 мл, прибавляют 10 мл воды и перемешивают в течение 2 минут. К полученному раствору прибавляют 4 мл раствора натрия гидроксида, 2 мл рас- хроматография (ВЭЖХ). Времена удерживания пиков основных компонентов на хроматограмме препарата должны соответствовать временам удерживания на хроматограмме раствора их рабочих стандартных образцов (см. количественное определение). Количественное определение. Метод 1. По этой методике анальгин определяют йодометрически, парацетамол - методом УФ-спектрофотометрии, а кофеин, кодеина фосфат и фенобарбитал - с по-" мощью метода ВЭЖХ. сн / 3 CH-N СН, Нл сн, / 3 n + СН, SO,Na + l,+ 2Н.0 N СН3 гГ СН. + NaHS04 + HI + CH20 |
