ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ
|
ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ
|
на нахождение массы вещества
|
метод пропорций
|
1.Прочитайте текст задачи.
|
Какая масса гидроксида натрия необходима для реакции с 68,6 г ортофосфорной кислоты с образованием средней соли?
|
2.Запишите условие и требование задачи с помощью общепринятых обозначений.
|
 2.Дано: 2.Дано:
m (H3PO4) = 68,6 г
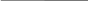 
m (NaOH) = ?
|
3. Запишите уравнение реакции
|
3.Решение:
3NaOH + H3PO4 = Na3PO4 + 3H2O
|
4. Над формулами записать, что известно по условию задачи
|
Х г 68,6 г
3NaOH + H3PO4 = Na3PO4 + 3H2O
|
5. Под уравнением записываем то, что следует из уравнения реакции с учётом условий задачи (находим массы гидроксида натрия и ортофосфорной кислоты). (ν – коэффициенты перед соответствующими веществами)
|
Mr (NaOH) = Ar(Na) + Ar(O) + Ar(H) = 23 + 16 + 1 = 40
M (NaOH) = 40 г/моль
m (NaOH) = ν · M = 3 моль · 40 г/моль = 120 г
Mr (H3PO4) = 3Ar(H) + Ar(P) + 4Ar(O) = 3 · 1 + 31 + 4 · 16 = 98
M (H3PO4) = 98 г/моль
m (H3PO4) = ν · M = 1 моль · 98 г/моль = 98 г
Х г 68,6 г
3NaOH + H3PO4 = Na3PO4 + 3H2O
120 г 98 г
|
6. Составляем пропорцию и производим расчёт
|
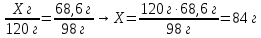
|
количественный метод
|
выполнить пункты 1 - 3
|
|
4. Рассчитать молярные массы гидроксида натрия и ортофосфорной кислоты
|
Mr (NaOH) = Ar(Na) + Ar(O) + Ar(H) = 23 + 16 + 1 = 40
M (NaOH) = 40 г/моль
Mr (H3PO4) = 3Ar(H) + Ar(P) + 4Ar(O) = 3 · 1 + 31 + 4 · 16 = 98
M (H3PO4) = 98 г/моль
|
5. Рассчитать количество ортофосфорной кислоты по формуле
|
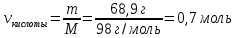
|
6. Записать в уравнении данные по условию уравнения и полученные величины над формулами, под формулам - количество данных веществ (ν – коэффициенты перед соответствующими веществами)
|
Х моль 0,7 моль
3NaOH + H3PO4 = Na3PO4 + 3H2O
3 моль 1 моль
|
7. Составить и решить пропорцию
|
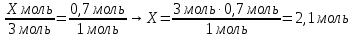
|
8. По формуле найти массу гидроксида натрия
|
m (NaOH) = ν · M = 2,1 моль · 40 г/моль = 84 г
|
Записать ответ
|
Ответ: m (NaOH) = 84 г
|
на нахождение объёма вещества
|
1.Прочитайте текст задачи.
|
Какой объём газа выделится при взаимодействии 6,5 г цинка с избытком раствора серной кислоты?
|
2.Запишите условие и требование задачи с помощью общепринятых обозначений.
|
 2.Дано: 2.Дано:
m (Zn) = 6,5 г
V(Н2) = ?
|
3. Запишите уравнение реакции
|
3.Решение:
Zn + H2SO4 = ZnSO4 + H2↑
|
4. Над формулами записать, что известно по условию задачи
|
6,5 г Х л
Zn + H2SO4 = ZnSO4 + H2↑
|
5. Вычислить массу цинка и объём водорода по уравнению реакции
|
Mr (Zn) = Ar(Zn) = 65
M (Zn) = 65 г/моль
m (Zn) = ν · M = 1 моль · 65 г/моль = 65 г
V = ν · Vm = 1 моль · 22,4 л/моль = 22,4 л
|
6. Полученные величины записать под соответствующими формулами
|
6,5 г Х л
Zn + H2SO4 = ZnSO4 + H2↑
65 г 22,4 л
|
7. Составить и решить пропорцию
|
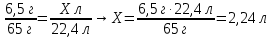
|
количественный метод
|
выполнить 1 – 3
|
|
4. Рассчитать количество цинка
|
Mr (Zn) = Ar(Zn) = 65
M (Zn) = 65 г/моль
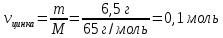
|
5. Полученную величину записать в уравнение над формулой цинка, под формулами количество вещества по уравнению реакции (коэффициенты перед формулами)
|
0,1 моль Х моль
Zn + H2SO4 = ZnSO4 + H2↑
1 моль 1 моль
|
6. Составить пропорцию и решить
|
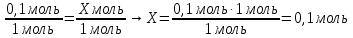
|
7. По формуле найти объём выделившегося газа
|
Vm = 22,4 л/моль
V = ν · Vm
V(H2) = 0,1 моль · 22,4 л/моль = 2,24 л
|
Записать ответ
|
Отсвет: V(H2) = 2,24 л
|
на нахождение количества вещества
|
1.Прочитайте текст задачи.
|
Какое количество вещества алюминия реагировало с избытком соляной кислоты, если в ходе реакции выделилось 13,44 л (н.у.) водорода?
|
2.Запишите условие и требование задачи с помощью общепринятых обозначений.
|
 2.Дано: 2.Дано:
V (Н2) = 13,44 л
н.у.
ν (Al) = ?
|
3. Запишите уравнение реакции
|
3 Решение:
Al + HCl = AlCl3 + H2↑
|
4. Над формулами записать, что известно по условию задачи
|
Х моль 13,44 л
2Al + 6HCl = 2AlCl3 + 3H2↑
|
5. По формуле вычислите объём водорода (по уравнению реакции)
|
V = ν · Vm
V(H2) = 3 моль · 22,4 л/моль = 67,2 л
|
6. Под формулами записать рассчитанный объём водорода и количество алюминия по уравнению реакции (коэффициент перед формулой)
|
Х моль 13,44 л
2Al + 6HCl = 2AlCl3 + 3H2↑
2 моль 67,2 л
|
7. Составить пропорцию и решить
|
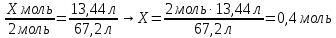
|
количественный метод
|
выполнить пункты 1 - 3
|
|
4. Рассчитать количество водорода
|
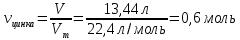
|
5. Над формулами записать, что известно и что надо найти
|
Х моль 0,6 моль
2Al + 6HCl = 2AlCl3 + 3H2↑
|
6. Под формулами записать количество водорода и количество алюминия по уравнению реакции (коэффициент перед формулой)
|
Х моль 0,6 моль
2Al + 6HCl = 2AlCl3 + 3H2↑
2 моль 3 моль
|
7. Составить пропорцию и решить
|
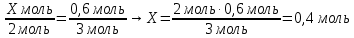
|
Записать ответ
|
Ответ: ν (Al) = 0,4 моль
|
 Скачать 267.71 Kb.
Скачать 267.71 Kb.