Окисление. Федеральное агентство по образованию
 Скачать 1.34 Mb. Скачать 1.34 Mb.
|
|
7. ОКИСЛЕНИЕ ОДНОАТОМНЫХ СПИРТОВ Под действием концентрированной HNO3, щелочного раствора KMnO4 и многих других окислителей первичные спирты окисляются в карбоновые кислоты:  При окислении первичных спиртов до альдегидов дихроматом натрия и серной кислотой образующийся альдегид, кипящий, как правило, при температуре значительно ниже, чем исходный спирт, немедленно удаляют отгонкой и тем предотвращают его дальнейшее окисление. Таким путем могут быть получены только низкокипящие альдегиды.  Для получения высококипящих альдегидов в качестве окислителя применяют трет-бутиловый эфир хромовой кислоты (получается из CrO3 и трет-бутанола):  Для селективного окисления первичных спиртов до альдегидов в настоящее время лучшими реагентами являются комплекс CrO3 с двумя молями пиридина: CrO3·2С5Н5N (реагент Саррета - Коллинза) и хлорхромат пиридиния CrO3·С5Н5N·HCl (реагент Кори) в хлористом метилене. Оба реагента обеспечивают очень высокие выходы альдегидов, однако хлорхромат пиридиния имеет важное преимущество в том отношении, что этот реагент не затрагивает двойную или тройную связь и поэтому особенно эффективен для получения ненасыщенных альдегидов: 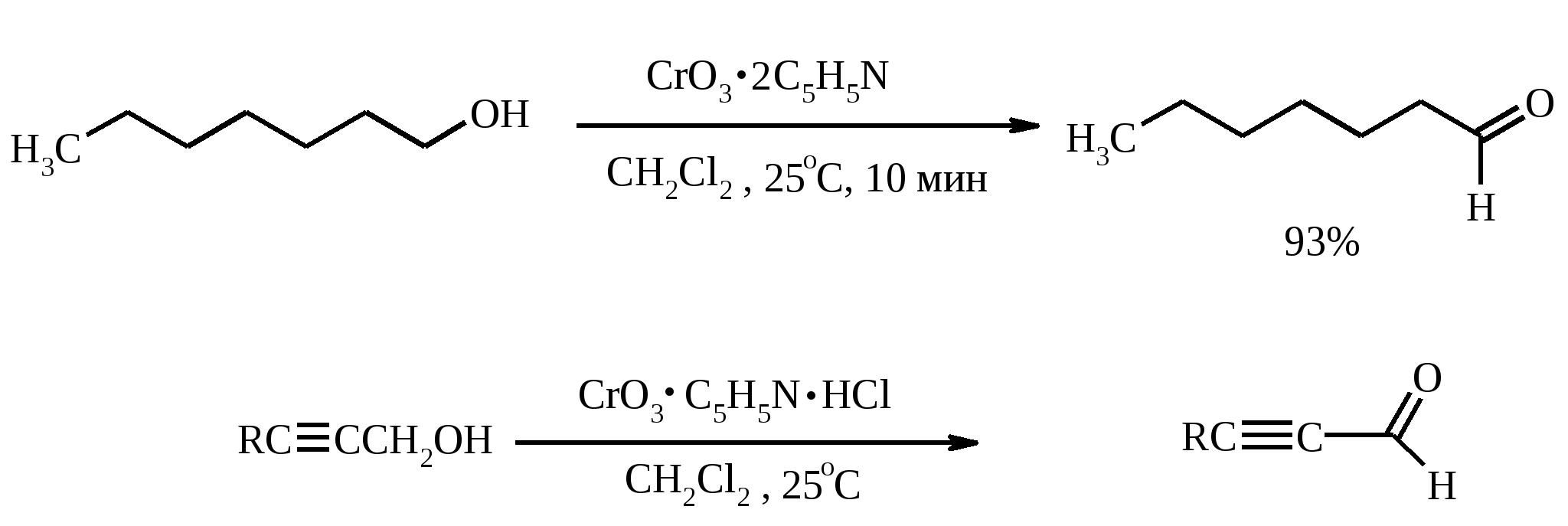 Один из промышленных способов получения формальдегида заключается в окислении метанола кислородом воздуха на серебряном катализаторе: Аллиловые, бензиловые и пропаргиловые спирты можно окислять до альдегидов диоксидом марганца:  Этот реагент окисляет в петролейном эфире или хлористом метилене ненасыщенные спирты с одной или несколькими двойными или тройными связями без изомеризации и перегруппировки. Однако, если окисление диоксидом марганца проводить в присутствии цианид-иона, то аллиловые спирты окисляются до карбоновых кислот или их сложных эфиров (в последнем случае спирты используются в качестве растворителей). В этом варианте окисления первоначально также образуется альдегид, но в присутствии цианид-иона он дает циангидрин, который содержит группировку аллилового спирта и поэтому способен окисляться далее под действием того же окислителя. 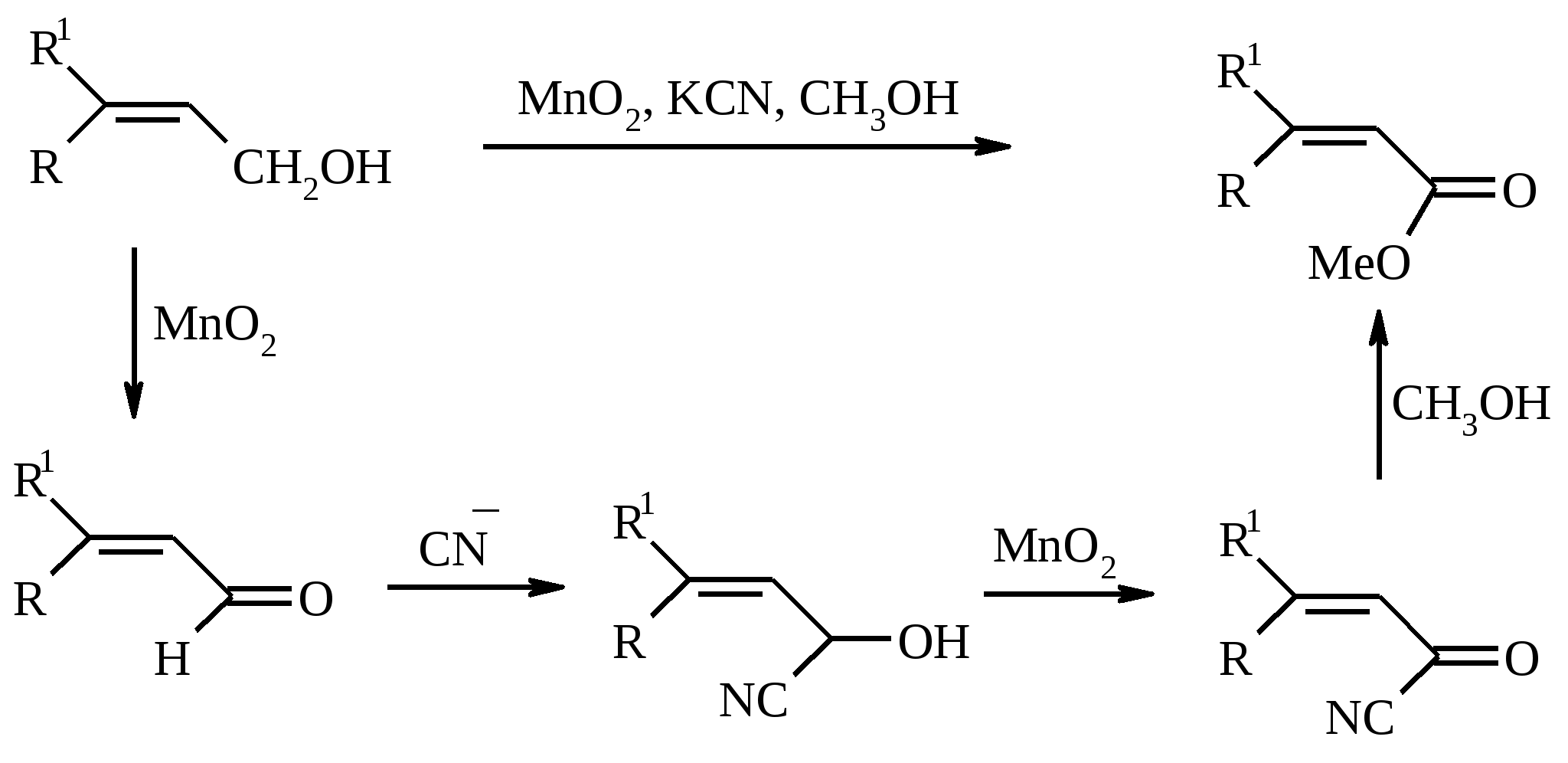 С высоким выходом бензиловый спирт может быть превращен в бензальдегид под действием 1-хлор- или 1-бромбензотриазола. Для превращения вторичных спиртов в кетоны используют смесь дихромата натрия и серной кислоты.  Если в молекуле спирта содержится кратная углерод-углеродная связь, то окисление ведут при комнатной или пониженной температурах в инертных неполярных растворителях строго рассчитанным количеством CrO3 в водной серной кислоте (реагент Джонса). Первичные спирты окисляются реагентом Джонса до карбоновых кислот: 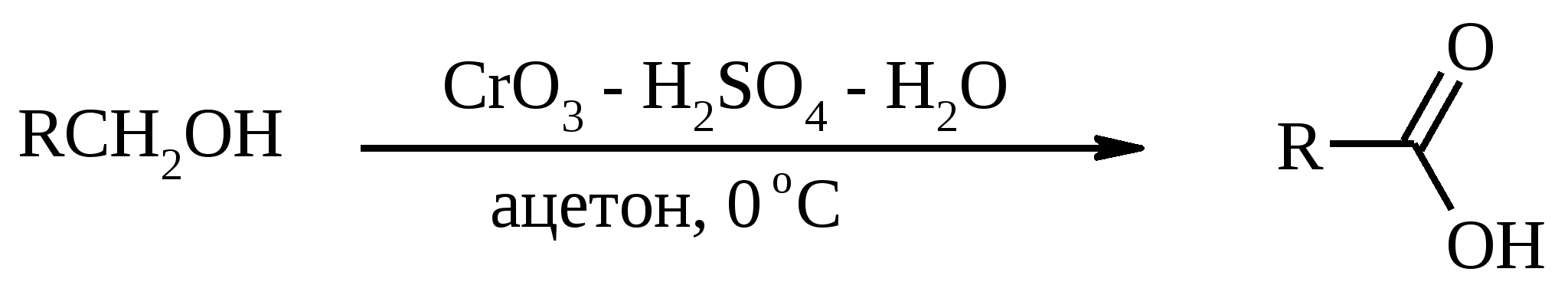 В последнее время разработан целый ряд новых эффективных методов окисления первичных и вторичных спиртов с помощью ДМСО или комплексов ДМСО с различными электрофильными агентами. Тозилаты первичных спиртов, также как и бензилтозилаты, окисляются в альдегиды при нагревании в ДМСО в течение 10-30 мин при 120-150С в присутствии гидрокарбоната натрия как слабого основания: 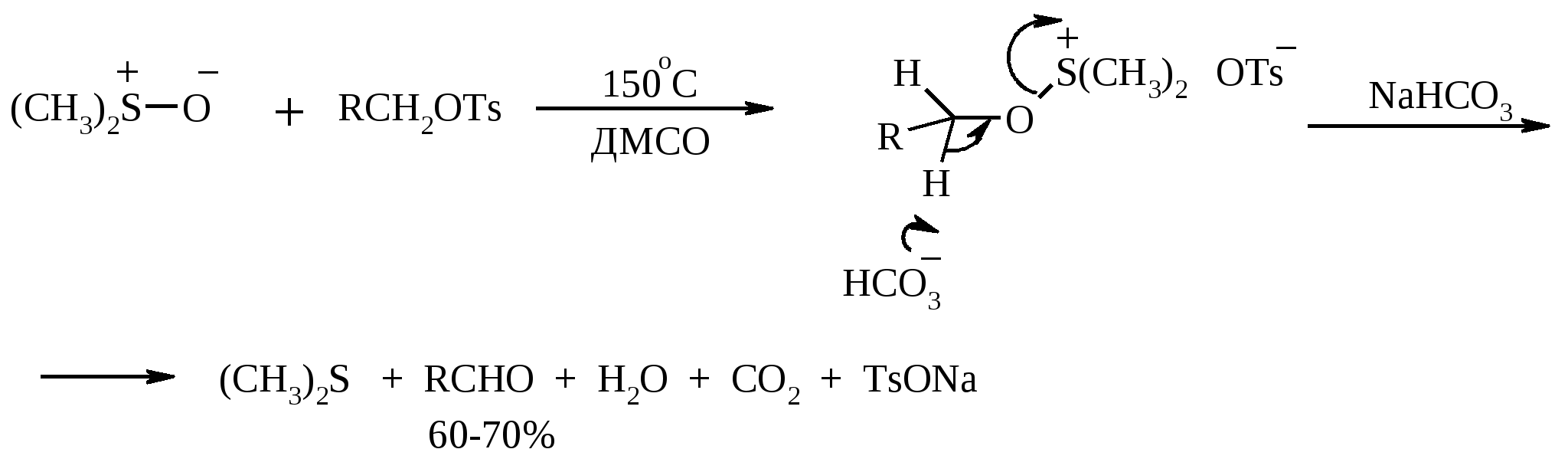 ДМСО в этой реакции выполняет роль нуклеофильного агента, который замещает тозилоксигруппу по SN2 механизму с образованием алкоксисульфониевых солей. Катион алкоксисульфония далее подвергается окислительно-восстановительному элиминированию, при этом гидрокарбонат или карбонат-ион является основанием в этой Е2-реакции элиминирования, приводящей к альдегиду и диметилсульфиду. 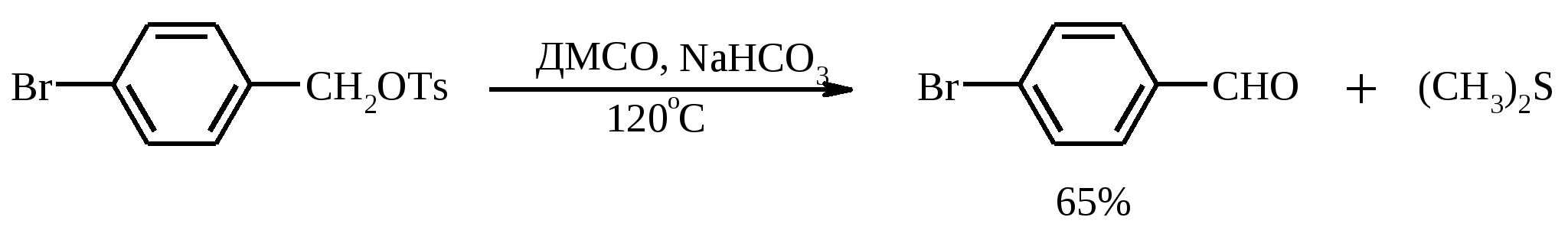 Однако данный метод окисления первичных спиртов в альдегиды требует проведения дополнительной стадии превращения спирта в тозилат. Одностадийное селективное окисление достигается путем превращения слабого нуклеофильного агента ДМСО в сильный электрофильный агент, который непосредственно реагирует с первичными и вторичными спиртами в очень мягких условиях при 0С и ниже. Необходимую активацию ДМСО проводят с помощью триоксида серы, трифторуксусного ангидрида, уксусного ангидрида, N-хлорсукцинимида, N,N-дициклогексилкарбодиимида С6Н11N=C=NC6H11, бромоводорода, оксалилхлорида (COCl)2, хлористого тионила SOCl2 и др. Во всех случаях в качестве реакционноспособного интермедиата образуется активированная алкоксисульфониевая соль, которая далее подвергается внутримолекулярной окислительно-восстановительной фрагментации. Комплекс ДМСО с SО3 образуется при взаимодействии пиридинсульфотриоксида с ДМСО: 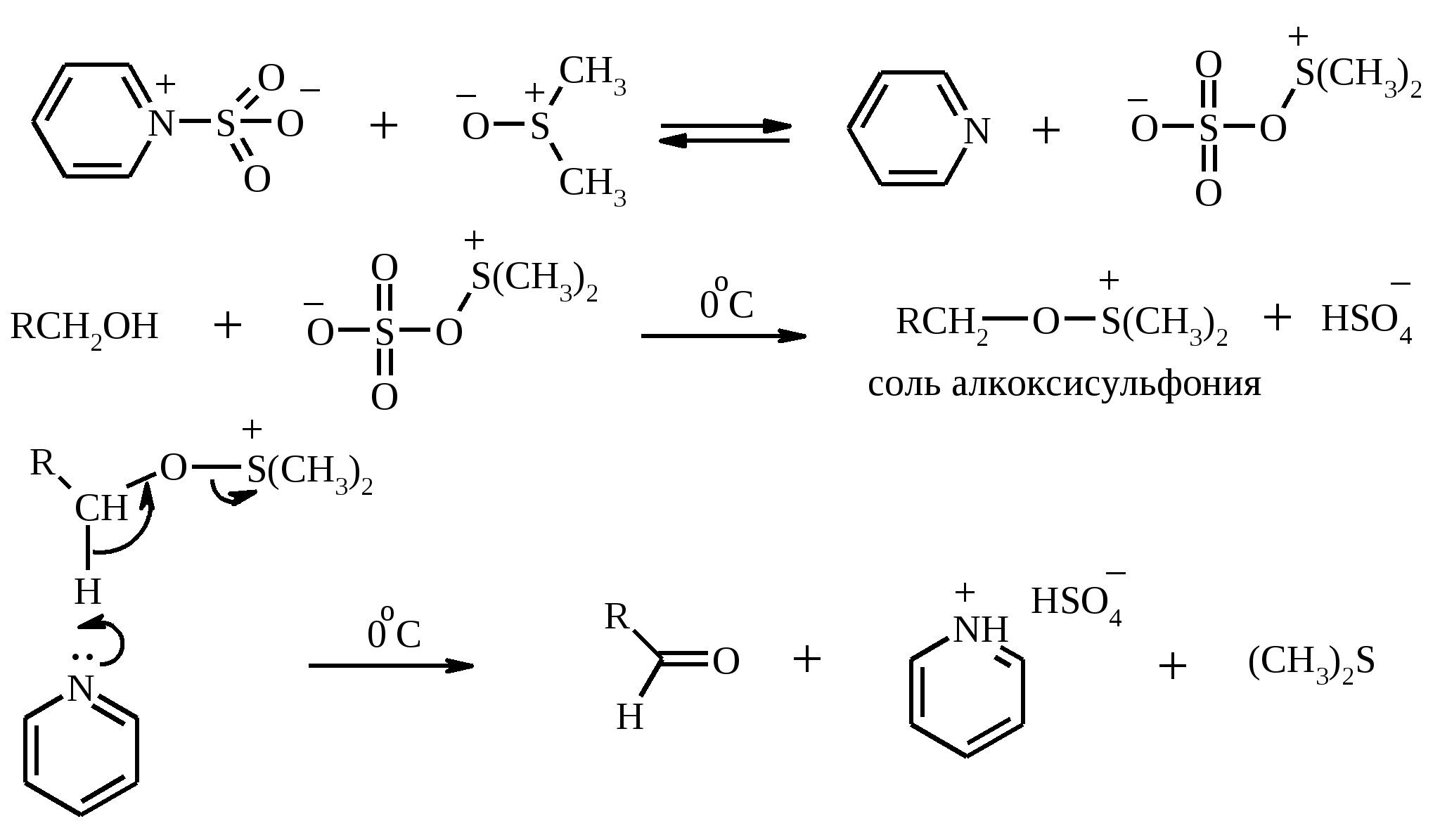 Наиболее часто используется комбинация ДМСО с N,N-дициклогексилкарбодиимидом (метод Пфитцера - Моффата): 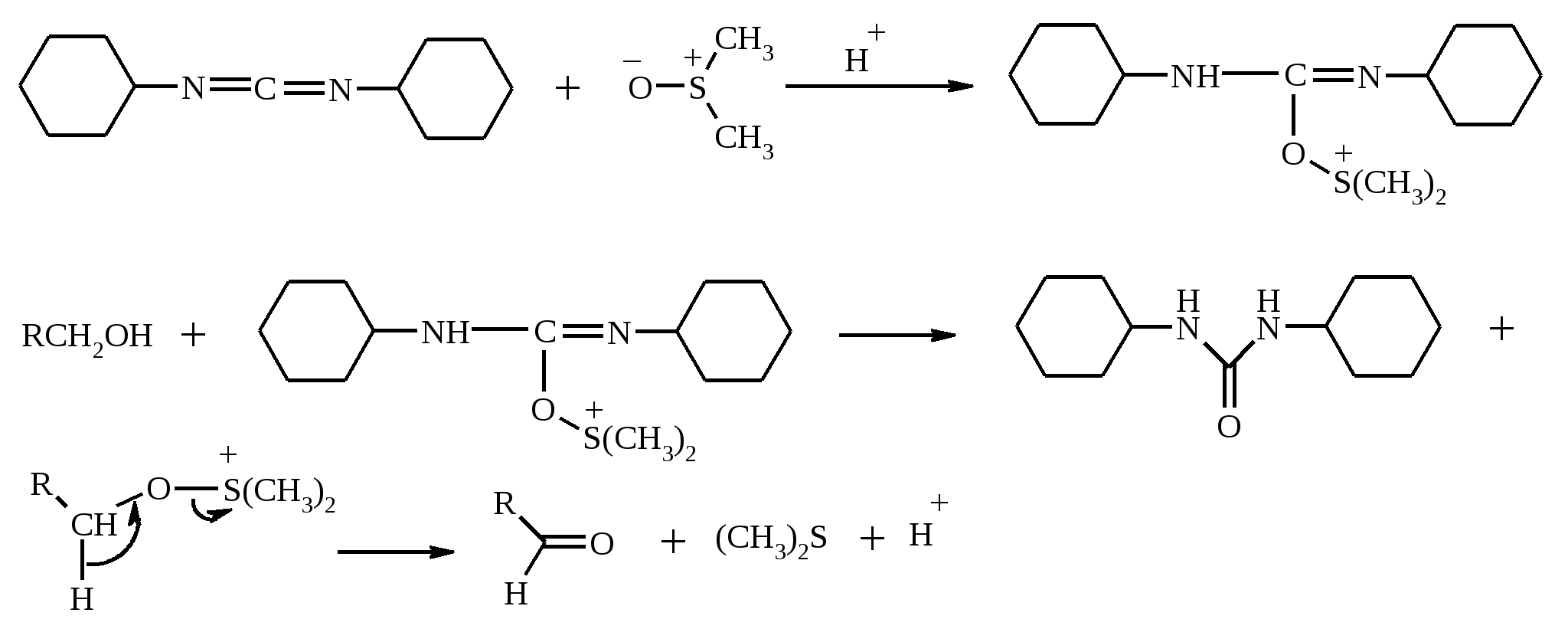 Диметилсульфид при взаимодействии с N-хлорсукцинимидом дает хлорсульфониевую соль, которая реагирует со спиртами уже при -30С с образованием карбонильного соединения: 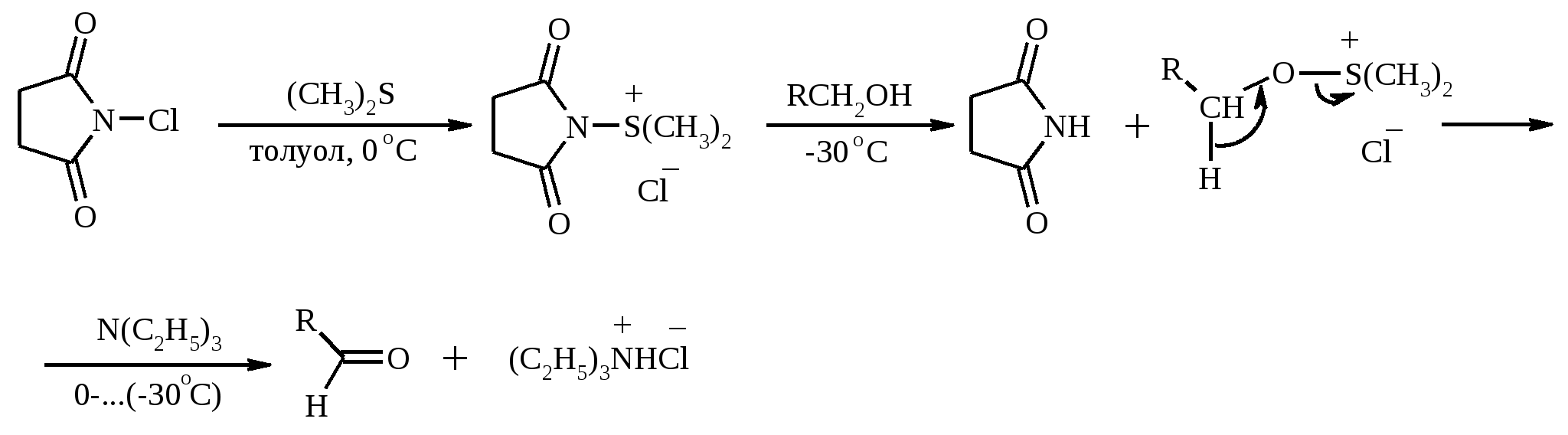 Вторичные спирты можно превратить в кетоны под действием кетонов (обычно ацетона) и алкоголятов алюминия (реакция Оппенауэра). Если в систему вводить большой избыток ацетона (50-200 молей), то равновесие сдвигается в сторону образования кетона из вторичного спирта. После установления равновесия реакционную смесь обрабатывают 30%-ной серной кислотой, отгоняют избыток ацетона и образовавшийся изопропанол и выделяют продукт окисления – кетон. В качестве акцептора водорода вместо ацетона иногда берут циклогексанон (избыток до 20 молей). Катализаторами служат трет-бутилат алюминия или изопропилат алюминия (не менее 0.25 моля на 1 моль окисляемого соединения; лучше 1-3 моля на 1 моль). Реакцию проводят в кипящем бензоле или толуоле.  Роль алкоголята алюминия сводится к тому, что он образует комплекс с ацетоном и, действуя как кислота Льюиса, увеличивает избыточный положительный заряд на карбонильном атоме углерода. Благодаря этому в реакционном комплексе, включающем окисляемый спирт, облегчается гидридный переход от атома углерода, связанного с гидроксильной группой, что в конечном счете и приводит к превращению исходного спирта в кетон.  Окисление -гидроксикетонов (ацилоинов) в соответствующие дикарбонильные соединения легко осуществляется при действии солей меди (II):  Третичные спирты весьма устойчивы к окислению и в жестких условиях происходит окисление с разрывом углерод-углеродных связей и образование кислот и (или) кетонов, содержащих меньше углеродных атомов, чем исходный спирт. Обычно окисление проводят в кислой среде. При этом спирт сначала дегидратируется до алкена, который далее легко расщепляется:  Дегидрирование спиртов. Окисление первичных и вторичных спиртов в карбонильные соединения сводится по существу к отщеплению водорода от молекулы исходного спирта. Такое отщепление можно осуществить не только с помощью окислителей, но и используя каталитическое дегидрирование. В качестве катализаторов обычно применяют тонкодисперсные медь и серебро, а также оксид цинка, которые для придания им структурной устойчивости наносят в тонкодисперсном состоянии на пемзу, асбест или другие инертные носители.  При дегидрировании изопропанола над медно-цинковым катализатором при 450ºС или оксидом цинка при 380ºС образуется ацетон:  В случае высококипящих спиртов реакцию проводят при пониженном давлении. Непредельные спирты в обычных условиях дегидрирования превращаются в соответствующие предельные карбонильные соединения. Гидрирование кратной связи осуществляется выделяющимся в процессе дегидрирования водородом.  Простейшие двухатомные спирты при каталитическом дегидрировании образуют дикарбонильные соединения:  8. РАСЩЕПЛЕНИЕ α-ГЛИКОЛЕЙ И РОДСТВЕННЫХ СОЕДИНЕНИЙ Под действием иодной кислоты HIO4 и ее солей, а также тетраацетата свинца Pb(OAc)4 1,2-диолы и полиолы подвергаются окислительному расщеплению с образованием альдегидов и кетонов:  Если в исходном полиоле три или более гидроксильных групп связаны с соседними атомами углерода, то из средних атомов углерода образуются карбоновые кислоты. 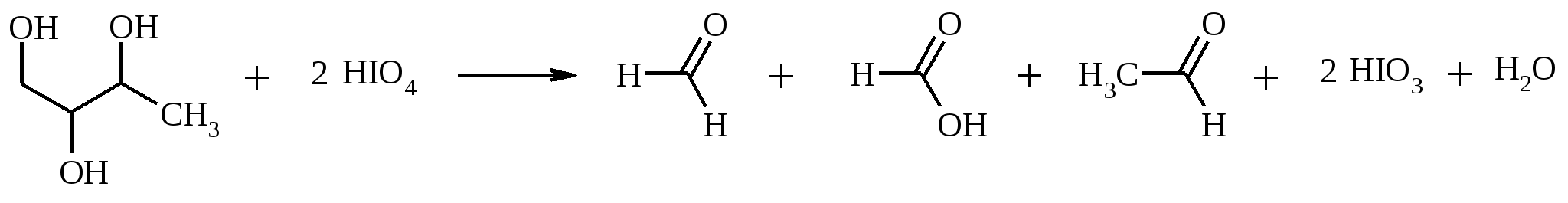 При использовании тетраацетата свинца вторичные спиртовые группы в полиолах окисляются до диоксида углерода. Для окисления 1,2-диолов, растворимых в воде или в бинарной смеси вода – ТГФ, вода – диоксан, используют HIO4 и ее соли, для окисления нерастворимых в воде диолов – тетраацетат свинца в бензоле или в уксусной кислоте. В обоих вариантах окислительной деструкции 1,2-диолов в качестве интермедиата образуются циклические эфиры иодной или свинцовой кислоты. Циклические эфиры затем подвергаются окислительно-восстановительному элиминированию с образованием карбонильных соединений и иодат-иона или ацетата свинца (II) соответственно:   Для окислительного расщепления 1,2-диолов используются и другие реагенты: соли церия (IV), ванадия (V), фенилиодозодиацетат С6H5I(OCOCH3)2, хлорохромат пиридиния и др. В некоторых случаях для окисления диолов в нейтральной среде применяют пероксид никеля NiO2 и MnO2: 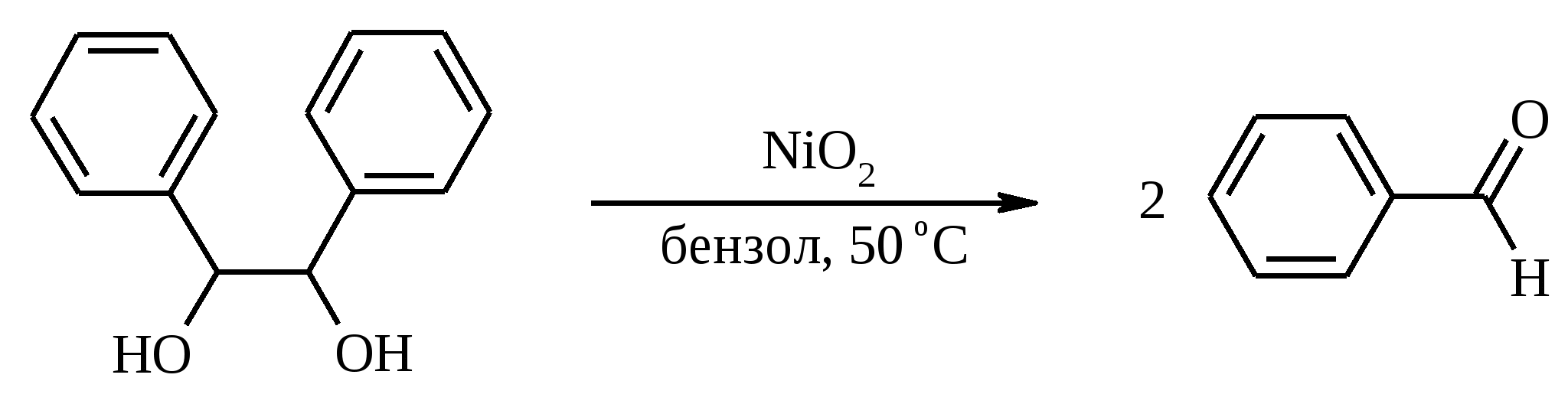 Такие окислители как KMnO4, Na2Cr2O7, N-иодсукцинимид также расщепляют 1,2-гликоли, но при этом вместо альдегидов образуются карбоновые кислоты. Аналогичное расщепление наблюдается и для других соединений, содержащих атомы кислорода или азота у соседних атомов углерода: -аминоспирты, -гидроксиальдегиды и -гидроксикетоны, -дикетоны, -кетоальдегиды, глиоксаль.  -Дикетоны и -гидроксикетоны расщепляются также под действием H2O2 в щелочной среде. 9. ОКИСЛЕНИЕ АЛЬДЕГИДОВ Окисление альдегидов протекает значительно легче, чем окисление спиртов. Превращение альдегидов в карбоновые кислоты можно осуществить действием многих окислителей: HNO3, H2O2, KMnO4, NaClO2, Ag2O, щелочным раствором иода, соединениями хрома (VI). Наилучшие результаты дает обычно реагент Джонса. В этом случае окисление проводится при 0-20С в течение короткого промежутка времени с выходами больше 80%. 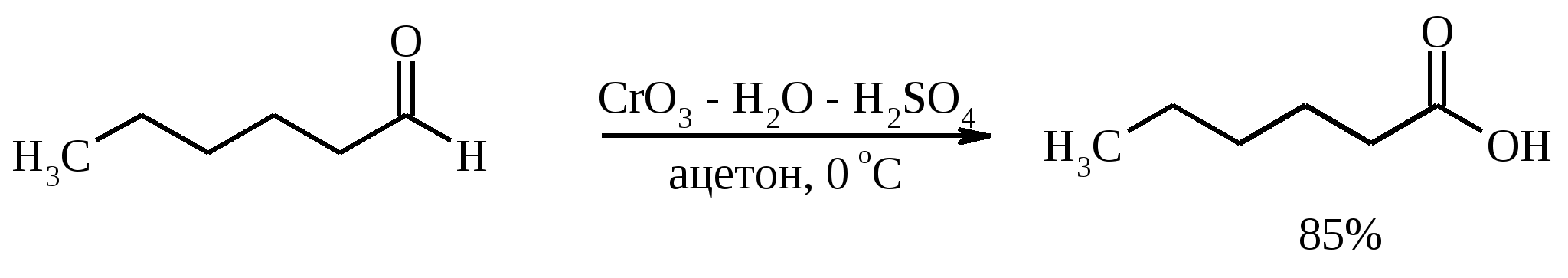 Однако реагент Джонса не обладает высокой избирательностью по отношению к другим функциональным группам, а кислая среда иногда приводит к изомеризации или деструкции. В таких случаях идеальным селективным окислителем является водно-спиртовой раствор оксида серебра или раствор AgNO3 в водном аммиаке (реагент Толленса). Этот реагент не затрагивает кратные углерод-углеродные связи, гидроксильную группу спиртов и ряд других функциональных групп:  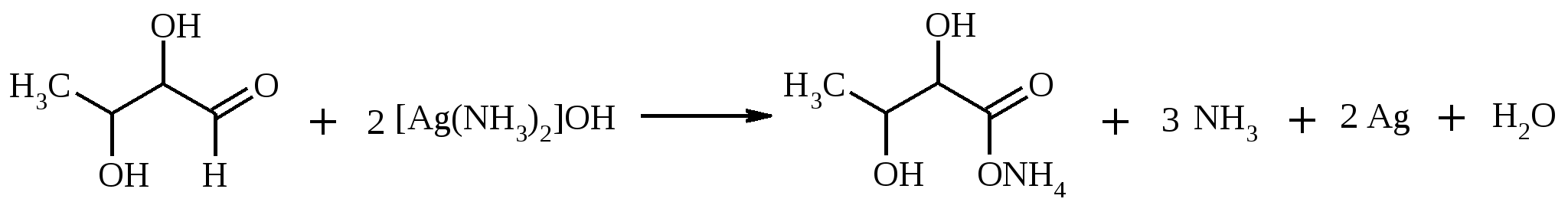 Окисление уксусного альдегида в промышленности осуществляют действием кислорода в присутствии солей кобальта или марганца в качестве катализатора: 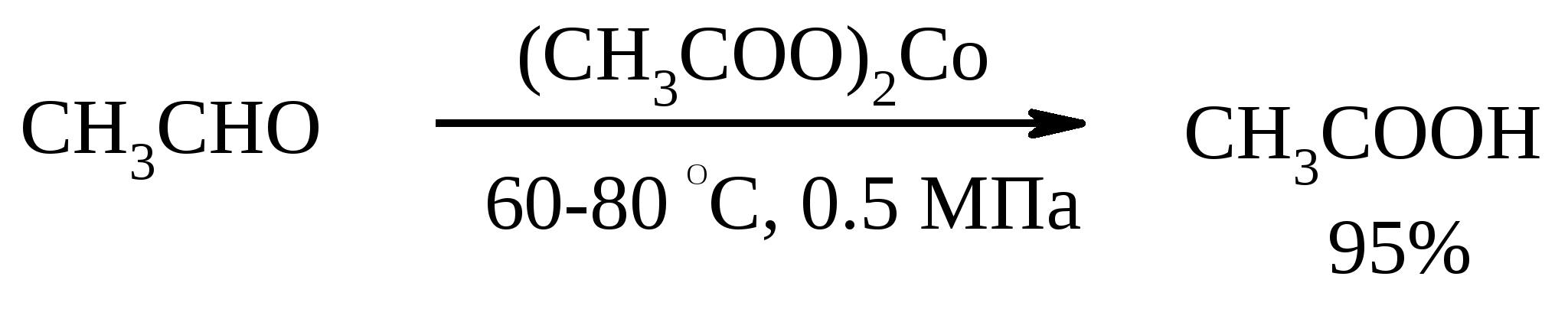 В химии углеводов для селективного окисления альдегидных групп применяется щелочной раствор иода. Так из D-глюкозы образуется D-глюконовая кислота:  Применяя разбавленную азотную кислоту, осуществляют окисление альдегидной группы, не затрагивая присутствующей в молекуле вторичной спиртовой группы, однако первичная спиртовая группа при этом окисляется в карбоксильную:  При обработке щелочным раствором пероксида водорода ароматических альдегидов (а также кетонов), содержащих в орто- или пара-положении NH2- или OH-группу, образуются соответственно аминофенолы или двухатомные фенолы (реакция Дакина): 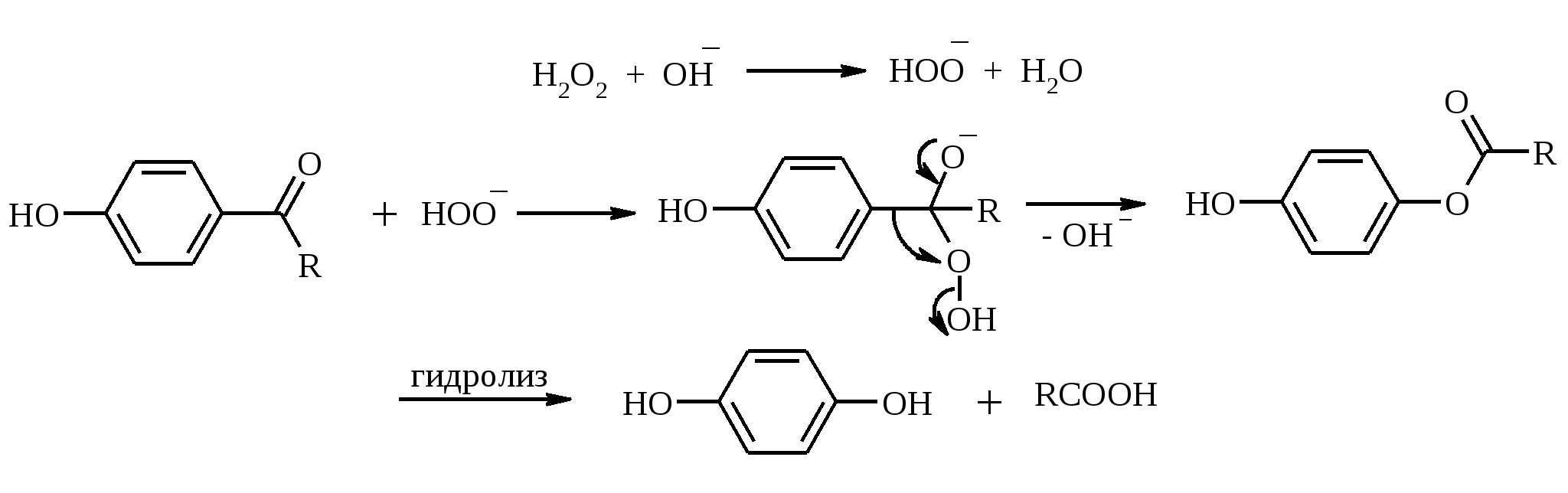 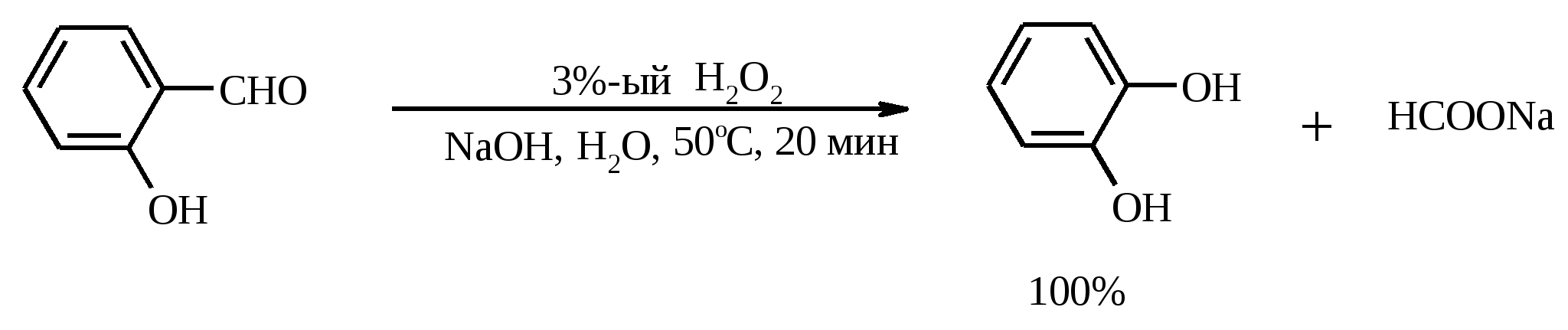 Под действием SeO2 альдегиды окисляются в -дикарбонильные соединения:  Интересно отметить, что при окислении диоксидом селена формальдегида образуется глиоксаль:  Альдегиды медленно окисляются кислородом воздуха при комнатной температуре до карбоновых кислот (аутоокисление альдегидов). 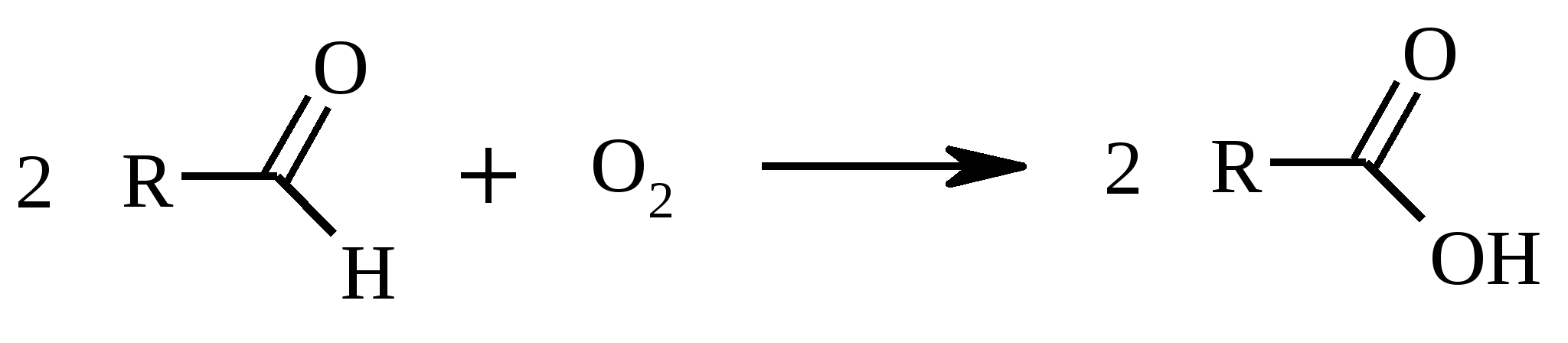 Эта реакция ускоряется при облучении или ионами Fe(II) и представляет собой цепной радикальный процесс:  10. ОКИСЛЕНИЕ КЕТОНОВ Окисление кетонов протекает в более жестких условиях, чем окисление альдегидов и сопровождается расщеплением углеродного скелета молекулы. Из несимметрично построенного кетона при окислении могут образоваться все четыре возможные карбоновые кислоты (правило Попова):  Если кетон в -положении содержит третичный атом углерода, то в результате окисления образуется три карбоновые кислоты и новый кетон, который в зависимости от условий может или подвергнуться дальнейшему окислению, или остаться неизменным:  Кетоны, как правило, устойчивы к окислению в нейтральной среде и подвергаются расщеплению только в кислой и щелочной средах: щелочным раствором KMnO4, горячей HNO3, соединениями Cr(VI) в серной кислоте. В связи с этим считают, что окислению кетона предшествует его енолизация; образовавшийся енол подобно другим алкенам окисляется по кратной связи с расщеплением углеродного скелета. Поскольку несимметричные кетоны могут енолизоваться в обоих возможных направлениях, их окислительное расщепление также осуществляется по двум направлениям. Промышленное значение имеет окисление циклогексанона, поскольку он легко доступен и при расщеплении дает только одну адипиновую кислоту. Реакцию проводят при повышенной температуре, применяя в качестве окислителя конц. HNO3, CrO3+H2SO4, щелочной раствор KMnO4:  При окислении азотной кислотой алициклических кетонов температура реакции может быть снижена, а выход продукта повышен, если применять более разбавленную азотную кислоту и добавлять в реакционную смесь каталитические количества V2O5. Циклические 1,3-дикетоны, которые существуют в основном в моноенольной форме, расщепляются периодатом натрия NaIO4 с потерей одного атома углерода:  Метилкетоны легко превращаются в соответствующие карбоновые кислоты при обработке их щелочными растворами гипобромита или гипохлорита натрия, т. е. смесью галогена и щелочи (галоформная реакция). Таким образом из окиси мезитила можно, например, получить ,-диметилакриловую кислоту:  Метиларилкетоны окисляются с еще более высокими выходами. Реакция обычно проводится в водно-диоксановом растворе:  Механизм процесса можно представить следующим образом:  Далее под действием щелочи тригалогенметилкетон расщепляется по следующей схеме:  Под действием перкислот, а также кислоты Каро H2SO5 и H2S2O8 кетоны окисляются в сложные эфиры (реакция Байера-Виллигера). Реакция обычно проводится при комнатной температуре в полярных органических растворителях, устойчивых к действию надкислот (хлороформ, уксусная кислота, уксусный ангидрид):  Наилучшие результаты достигаются при расщеплении алифатических и циклических кетонов комплексом 90%-ного пероксида водорода и эфирата трехфтористого бора:  В начале под действием надкислоты, если она достаточно сильная, или каталитических количеств серной кислоты происходит протонизация карбонильного атома кислорода кетона. При этом карбонильный атом углерода приобретает избыточный положительный заряд. Затем к нему нуклеофильно присоединяется анион надкислоты. Последующий гетеролитический разрыв связи кислород-кислород, миграция одного из радикалов в виде аниона к положительно заряженному атому кислорода и отрыв протона приводят к образованию сложного эфира:  Несимметричные кетоны в общем случае образуют два изомерных сложных эфира, соотношение которых зависит от относительной способности групп к миграции к атому кислорода. По способности к миграции группы располагаются в следующем ряду H > C6H5 > (CH3)3C >> (CH3)2CH > RCH2 >> CH3. Если две группы сильно различаются по способности к миграции, реакция характеризуется высокой региоселективностью. Особое значение имеет реакция Байера-Виллигера для циклических кетонов, которые при окислении дают циклические сложные эфиры – лактоны:  Метиленовая (метильная) группа в -положении к карбонильной группе кетонов легко окисляется диоксидом селена:  Для реакции окисления кетонов, а также альдегидов диоксидом селена был предложен следующий механизм:  Вместо прямого окисления можно воспользоваться двухстадийным методом, приведенным ниже:  Алкоксисульфониевая соль, образующаяся при замещении галогена или тозилата, подвергается внутримолекулярному окислению-восстановлению с образованием кетоальдегида:  В то же время окисление α-бромкетонов диоксидом селена в спиртовой среде приводит к α-кетоэфирам: 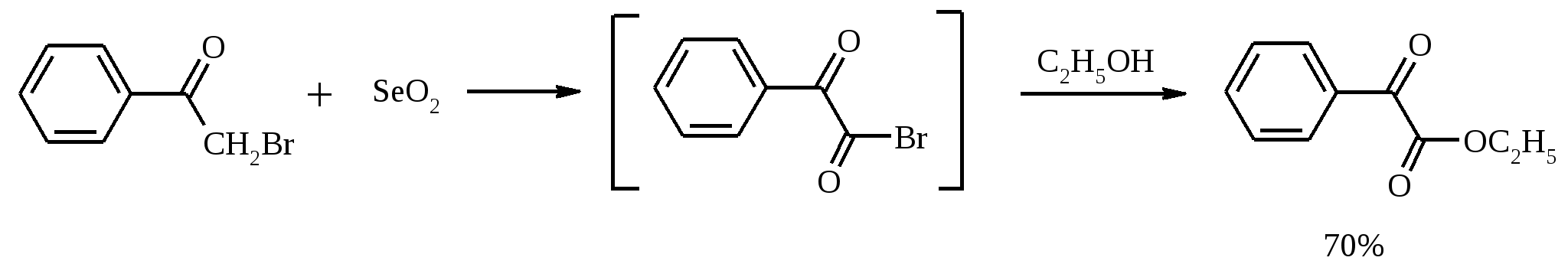 Под действием раствора полисульфида аммония (как правило, под давлением) арилалкилкетоны превращаются в ω-арилкарбоновые кислоты с сохранением общего числа атомов углерода (реакция Вильгеродта): 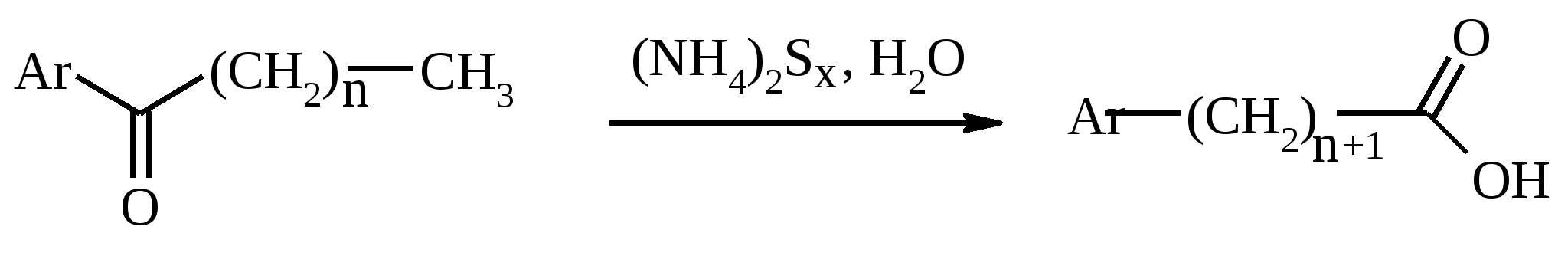 В результате карбонильная группа кетона восстанавливается до метиленовой, а метильная окисляется до карбоксильной. Фактически сначала получают тиоамид (или амид) кислоты, который затем омыляют. С ростом числа атомов углерода в цепи (n) выходы карбоновых кислот падают. Улучшенный вариант реакции, не требующий применения давления, заключается в применении вместо полисульфида серы и вторичного амина (обычно морфолина) (модификация Киндлера): 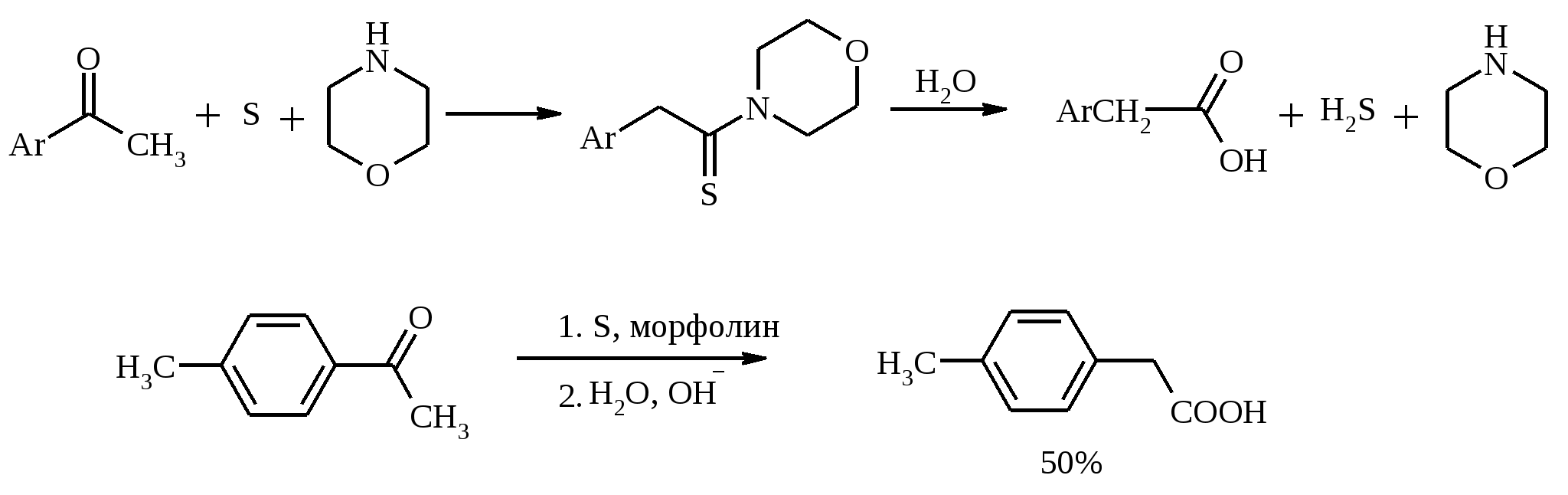 При обработке циклогексанонов серой или селеном протекает дегидрирование и образуются фенолы. По-видимому, реакция протекает через стадию предварительной енолизации исходных кетонов: 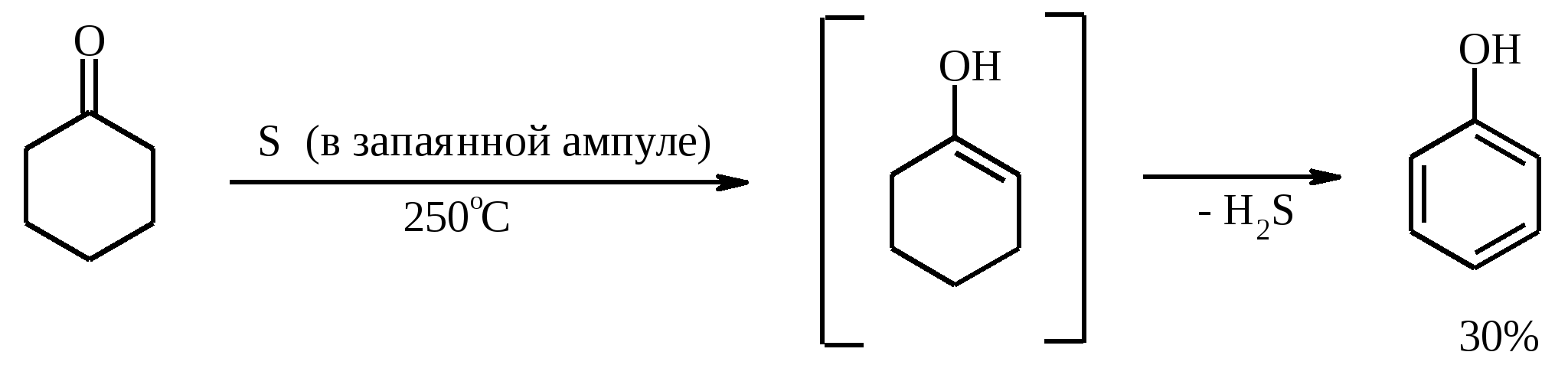 |
