|
|
МОНОГРАФИЯ Гепатит и последствия гепатита. Майер К.-П (в word). Гепатит и последствия гепатита Практич рук. Пер с нем. Под ред. А. А. Шепулина. М. Гэотар медицина, 1999. 432 с
12.7.4. ПРАКТИЧЕСКИЕ ВЫВОДЫ
Болезнь Вильсона представляет собой наследственно обусловленное нарушение обмена меди, которое приводит к развитию хронического заболевания печени уже в молодом возрасте и без лечения всегда заканчивается смертью. Диагностика заболевания может быть достаточно трудной.
О возможности данного заболевания следует думать у всех больных моложе 30 лет с этиологически не ясным поражением печени при неврологических симптомах и особенностях поведения, часто оказывающихся ведущими в клинической картине, треморе и ригидности, а также характерном роговичном кольце Кайзера—Флейшера.
Диагноз заболевания основывается на обнаружении сниженной концентрации церулоплазмина в сыворотке (менее 20 мг/дл). Лишь у 4 из 475 пациентов с болезнью Крона концентрация церулоплазмина в сыворотке превышала 20 мг/дл! Правда, само по себе выявление сниженной концентрации церулоплазмина еще не доказывает болезнь Вильсона, Однако обнаружение роговичного кольца Кайзера—Флейшера с помощью щелевой лампы в сочетании с низкой концентрацией церулоплазмина в сыворотке почти всегда указывает на это заболевание. В сомнительных случаях диагноз может быть окончательно подтвержден результатами определения содержания меди в печени (резко повышенного) при одновременном выявлении гистологических изменений, соответствующих болезни Вильсона. Выделение меди с мочой в течение суток значительно возрастает. Однако этот метод может иногда давать ошибочные результаты, связанные с неправильным сбором мочи, загрязнением посуды и т.д.
Этиотропного лечения этого заболевания пока не существует.
Симптоматическое лечение с применением хелатобразующих препаратов, таких как DPA [торговые названия препаратов троловол (trolovol), ме-талкаптазе (metalcaptase)], проводимое в течение всей жизни, компенсирует, однако, этот дефект обмена веществ за счет повышенного выделения меди с мочой.
Контролируя эффективность лечения, можно отметить уменьшение выраженности клинических симптомов, нормализацию функциональных печеночных тестов, обратное развитие роговичного кольца Кайзера—Флейшера, а также улучшение гистологической структуры печени при проведении контрольной биопсии. Правда, цирроз печени (неактивный) может сохраняться в течение всей жизни. Регулярное определение содержания свободной меди в сыворотке, концентрация которой в случаях эффективного лечения сохраняется заметно ниже 20 мкг/дл, легко осуществимо.
Последовательно проводимая у пациентов с болезнью Вильсона (а также у бессимптомных носителей, выявленных в процессе обследования окружающих больного лиц) пожизненная терапия с применением DPA способствует тому, что ожидаемая продолжительность жизни не уменьшается. В диагностике этого редкого заболевания ни в коем случае нельзя допускать ошибок!
Прекращение медикаментозного лечения при «нормальных печеночных пробах» и хорошем самочувствии пациентов с болезнью Вильсона следует считать серьезной ошибкой, поскольку оно чревато фульминантным течением заболевания со смертельным исходом.
Во время беременности также следует продолжать лечение. Серьезные побочные эффекты терапии DPA встречаются редко, но могут обусловить у некоторых пациентов необходимость отмены препарата. Альтернативным лечением в таких случаях становится применение триэтилентетрамина и препаратов цинка.
Хирургическое лечение (трансплантация печени) проводится при фульминантном течении болезни Вильсона, а также у больных, резистентных к консервативному лечению, т.е. тогда, когда, несмотря на проводимое по всем правилам лечение DPA, прогрессивно ухудшаются функции печени с повышением уровня билирубина, падением содержания альбуминов, усилением изменений свертывающей системы крови. Фульминантное течение болезни Вильсона нельзя распознать по концентрации церулоплазмина. Вместе с тем в указанных случаях (обычно у больных в возрасте от 17 до 19 лет) обнаруживаются резкое снижение активности щелочной фосфатазы (в сравнении с умеренным повышением уровня трансаминаз) и другие признаки фульминантного некроза гепатоцитов.
Таким образом, перед практическим врачом стоит чрезвычайно ответственная задача, связанная с необходимостью активного исключения у каждого больного молодого возраста (до 30 лет) с хроническим гепатитом невыясненной этиологии болезни Вильсона. При выявлении этого заболевания врач должен наблюдать такого пациента в течение всей его жизни, постоянно побуждая больного к регулярному приему лекарственных препаратов.
12.8. ИДИОПАТИЧЕСКИЙ ГЕМОХРОМАТОЭ 12.8.1. ЧАСТОТА, ГЕНЕТИКА И ЭПИДЕМИОЛОГИЯ
Поданным американских исследований, частота гена идиопатического гемохроматоза (ИГХ) среди всего населения составляет 6,7%. Частота монозиготного носительства равна приблизительно 0,45%. Это позволяет утверждать, что, в отличие от прежних представлений, гемохроматоэ относится к числу наиболее частых наследственно обусловленных нарушений обмена веществ. Манифестные формы поражения печени, связанного с гемохроматозом, встречаются среди всего населения с частотой 2 случая на 1000 жителей!
Если и отец, и мать являются гетерозиготными (носителями дефектного гена), то вероятность появления гомозигнотных детей (имеющих дефектный ген и клинически больных) составляет 1 : 4, гетерозиготных —1:2.
Примерно у трети гетерозиготных носителей обнаруживается умеренное повышение параметров обмена железа. В отличие от гомозиготных пациентов, которые в итоге все заболевают, у гетерозиготных лиц не развиваются манифестные формы ИГХ. Заболевание наследуется по аутосомно-рецес-сивному типу. Отмечена его достоверная связь с типами HLA A3, В7 и В14.
Заболевание сопровождается отложением железа во многих органах (печень, поджелудочная железа, гипофиз, суставы, половые железы).
У гомозиготных лиц начиная с рождения в организме начинает постепенно накапливаться железо, пока, наконец, спустя многие годы, не манифестируют симптомы заболевания, обусловленные поражением органов вследствие задержки железа (рис. 65).
Ежегодное накопление железа заметно различается у гетерозиготных и гомозиготных мужчин и женщин (табл. 84). Если предположить, что такое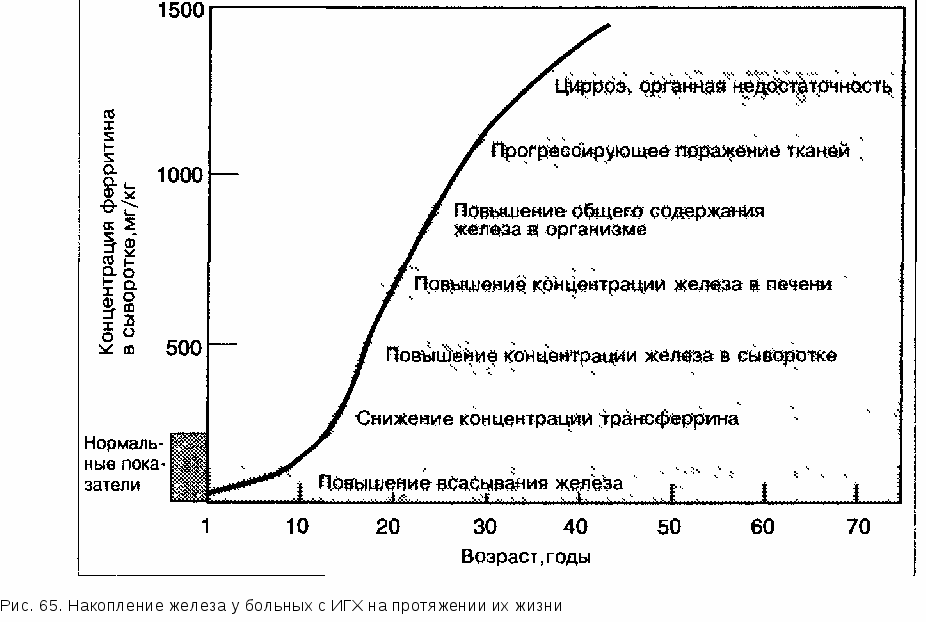

накопление железа, начиная с рождения, происходит постоянно, то у мужчин к 50-летнему возрасту в организме может накопиться 20 г железа — количество, достаточное для того, чтобы повреждения тканей стали заметными. Как раз в этот период при обследовании мужчин возникает подозрение на гемохроматоэ.
12.8.2. КЛИНИКА
Классическое описание клинической картины ИГК рисует обычно мужчину среднего возраста, которого беспокоит утомляемость. Сексуальная активность снижена, частые жалобы на боли в суставах. При клиническом обследовании выявляется гепатомегалия.
Типичные изменения кожи в сочетании с диабетом обозначаются как «бронзовый диабет».
Какие симптомы приводят больного ИГХ к врачу?
На рис. 66 показано, что примерно у трети больных ИГХ заболевание не проявляется специфическими симптомами, а обнаруживается случайно.
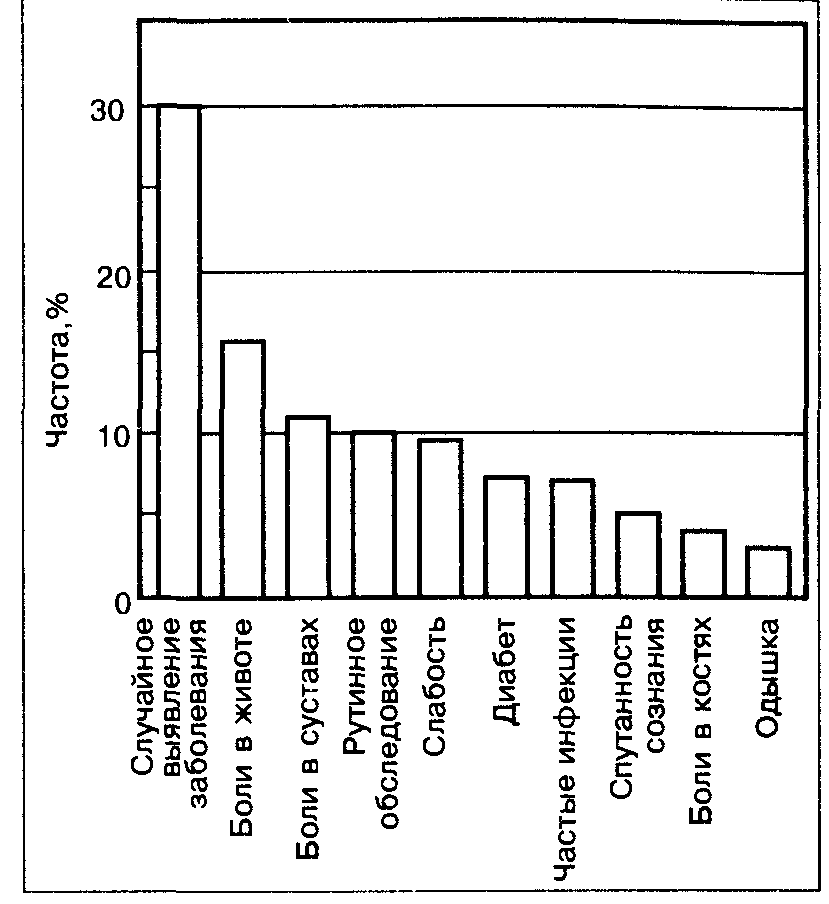
Рис. 66. Клинические симптомы у больных с ИГХ (по P.C.Adams: Amer. J. Med., 1991)
Какие симптомы заставляют врача думать о возможности ИГХ?
Данные, представленные на рис. 67, свидетельствуют, что гепатомега-лия и патологически измененные печеночные функциональные пробы являются главными симптомами, на которых основывается диагностика заболевания.
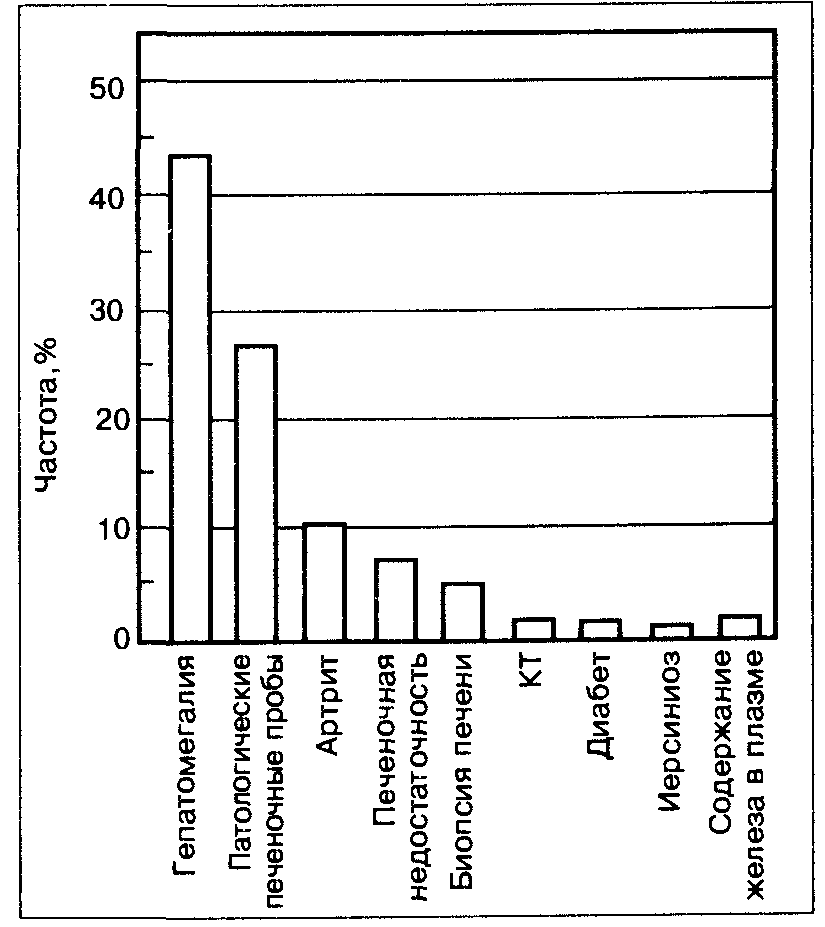 Рис. 67. Данные обследования у больных с ИГХ (по P.CAdams: AmerJ.Med., 1991)
(кровопускания) может значительно улучшить прогноз заболевания и у «клинически здоровых» членов семьи с латентно протекающим ИГХ. Продолжительность жизни этих лиц в результате не снижается!
Какие лабораторные методы исследования целесообразно применять в качестве скрининговых тестов?
У родственников больного нужно определить концентрацию ферритина в сыворотке, поскольку это высоко чувствительный (85%) и специфичный (95%) метод. Кроме того, при концентрации ферритина в сыворотке более 700 мг/л возрастает вероятность развития фиброза или цирроза. Напротив, нормальная концентрация ферритина в сыворотке, особенно в сочетании с нормальным насыщением сывороточного трансферрина, имеет высокую отрицательную предсказывающую ценность (97%). Свободную железосвязывающую способность как отдельный параметр можно считать надежным признаком ИГХ. При увеличении насыщения трансферрина выше 62% подозрение на ИГХ становится очень серьезным. Подобное уменьшение железосвязывающей способности при алкогольных поражениях печени обнаруживается лишь в очень редких (исключительных) случаях.
Практически это означает, что если у «здорового» члена семьи концентрация ферритина более 700 мкг/л и одновременно есть высокое насыщение трансферрина, целесообразно перейти на следующую ступень диагностического поиска и провести биопсию печени с количественным определением железа. Если у таких пациентов (чаще всего не имеющих клинических симптомов) предположительный диагноз ИГХ находит гистологическое подтверждение, то назначают кровопускания, которые позволяют предотвратить кумуляцию железа и последующие повреждения органов.
Ни улиц с подозрением на гемохроматоэ, ни у родственников пациентов (при обследовании) применение неинвазивных методов не имеет существенного значения. Это относится как к КТ, так и к ЯМР. Если концентрация железа в печени становится очень высокой, то можно обнаружить определенную корреляцию между интенсивностью печеночных сигналов при ЯМР и концентрацией ферритина в сыворотке. Однако расхождения, обусловленные приборами и интерпретацией результатов исследования, могут быть очень значительными.
12.8.4.ЛЕЧЕНИЕ
Лечение гомозиготных больных проводится до развития осложнений, связанных с хроническим перенасыщением железом различных органов и систем. Воздействовать на избыточное всасывание железа у больных ИГХ с помощью лекарственных препаратов невозможно.
Цели терапии реализуются с помощью чрезвычайно эффективных (правда, лишь симптоматических) методов лечения.
Каким образом можно осуществить цели лечения?
Кровопускания остаются самым эффективным методом лечения больных ИГХ. При изъятии 500 мл крови из организма удаляются примерно 250 мг железа. Если вспомнить, что положительный баланс железа у больных гемохроматозом составляет в среднем 25 г (!), то становится очевидным, что нужно проводить кровопускания еженедельно в течение 2 лет, прежде чем запасы железа в какой-то мере иссякнут. Поскольку фактор времени играет существенную роль в плане предупреждения осложнений ИГХ (см. ниже), то при лечении таких больных, особенно в первые полгода после установления диагноза, необходимо стремиться к возможно более частым кровопусканиям. При отсутствии у больного с гемохроматозом анемии (уровень гемоглобина выше 12 г/дл) конкретная тактика лечения может быть следующей.
Кровопускания проводят еженедельно объемом около 500 мл до нормализации содержания ферритина в сыворотке. После этого поддерживающие кровопускания проводятся с различной частотой.
Поскольку ИГХ — наследственно обусловленное заболевание, связанное с повышенным всасыванием железа, полностью прекращать кровопускания нельзя. У некоторых больных удается длительно поддерживать гоме-остаз железа с помощью 4—6 кровопусканий в год объемом 500 мл каждое. Содержание железа в сыворотке начинает снижаться только тогда, когда концентрация ферритина падает ниже 30 нг/мл. Это означает, что после нормализации концентрации ферритина уровень железа еще долго может оставаться повышенным. Таким образом, определение содержания железа в сыворотке нельзя считать методом контроля эффективности кровопусканий при ИГХ.
Какие лабораторные параметры целесообразно контролировать при проведении кровопусканий у больных ИГХ?
Для контроля общего содержания железа в организме можно определять концентрацию ферритина в сыворотке. Если концентрация сывороточного ферритина падает ниже 50 мкг/мл, а насыщение трансферрина снижается до нормы, то правомерно делать вывод о существенной элиминации железа. В подобной ситуации можно увеличить интервалы между кровопусканиями (обычно до 1—2 кровопусканий объемом по 500 мл каждые 3 мес). Содержание железа в сыворотке в таких случаях падает ниже 100 мкг/дл. Если, однако, интервал между кровопусканиями оказывается слишком значительным, то уровень сывороточного железа, концентрация ферритина и насыщение трансферрина вновь быстро возрастают и становятся выше нормальных показателей. У таких больных нужно заново обдумывать и устанавливать интервалы между кровопусканиями. Если при контрольных исследованиях указанные параметры сохраняются стабильными, то для поддержания достигнутого баланса железа достаточно 48 кровопусканий в год.
У некоторых пациентов такая схема поддерживающей терапии применяется в течение всей жизни.
К умеренной анемии (уровень гемоглобина около 12 г/дл) можно относиться спокойно, если содержание общего белка в сыворотке не падает ниже 6 г/дл (что иногда встречается на далеко зашедшей стадии цирроза печени со сниженной синтетической функцией печени). В такой ситуации может уменьшаться и концентрация факторов свертывания крови. При лечении этих немногочисленных больных необходимо решать вопрос о ретрансфузии плазмы, взятой при кровопускании.
Возможно ли медикаментозное лечение ИГХ?
Врачу постоянно приходится сталкиваться с вопросом о том, какая эффективная длительная лекарственная терапия ИГХ могла бы заменить кровопускания. Здесь необходимо сказать, что медикаментозное воздействие в указанных ситуациях недостаточно. С помощью хелатобразующих препаратов, например десферриоксамина (desferrioxamin), даже при его парентеральном введении, удается элиминировать не более 20 мг железа в сутки, тогда как при однократном кровопускании выводится количество железа в 10 раз большее. Комбинация кровопусканий с применением хелатобразующих препаратов также не рекомендуется. Мы полагаем, что применение данных препаратов показано лишь тогда, когда вторичная тяжелая анемия или гипопротеинемия (чаще на далеко зашедших стадиях цирроза печени) делают невозможными кровопускания и ретрансфузии плазмы. В этих очень редких случаях применяют портативные приспособления, обеспечивающие постоянное парентеральное введение десферриоксамина.
Существует ли при ИГХ специальная диета?
Назначение строгой диеты с низким содержанием железа с целью влияния на течение болезни вряд ли возможно. Все же мы рекомендуем больным избегать употребления продуктов, богатых железом, таких, например, как потроха, перебродившие фруктовые соки, красное вино.
Какое место влечении больных ИГХ занимает трансплантация печени?
Число больных ИГХ, у которых была проведена трасплантация печени, еще невелико. Общее плохое состояние и тяжелые сопутствующие заболевания служат противопоказанием к применению активной хирургической тактики лечения. Сказанное относится и к первичной гепатоцеллюлярной карциноме, которая к моменту ее выявления уже часто дает метастазы, в связи с чем трансплантация печени уже не приносит больному никакой пользы.
В отличие от результатов трансплантации печени при болезни Вильсона, приводящей к излечению, патогенетический дефект при ИГХ с помощью этой операции не ликвидируется. Это означает, что даже в случае успешного исхода трансплантации печени у больного гемохроматозом в послеоперационном периоде должен проводиться контроль содержания железа в пересаженной печени.
12.8.5. ТЕЧЕНИЕ, ОСЛОЖНЕНИЯ И ПРОГНОЗ
Течение ИГХ зависит от многих факторов.
Возможно более ранняя нормализация обмена железа в организме (хотя бы в течение 18 мес) имеет решающее значение для течения и прогноза (рис. 68).
Общие показатели выживаемости больных, полученные при динамическом наблюдении 85 пациентов с ИГХ, представлены на рис. 69. При
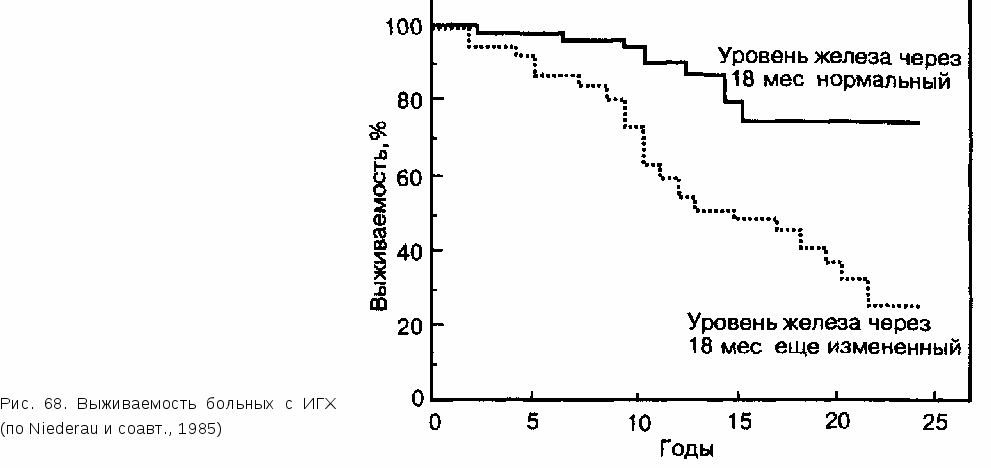
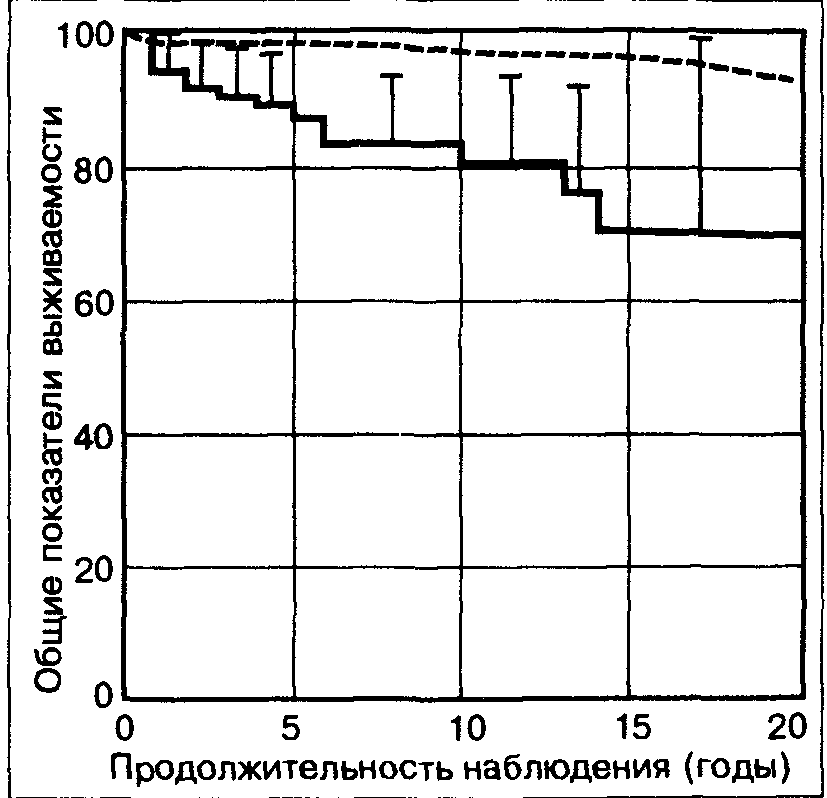
Рис. 69. Общие показатели выживаемости больных с ИГХ и лиц контрольной группы (по P.C.Adams: Gastroenterology, 1991, 101, 368)
сравнении с ожидаемой продолжительностью жизни в популяции лиц аналогичного пола и возраста выживаемость больных с ИГХ достоверно снижается с 14-го года наблюдения. Развитие цирроза печени заметно ухудшает прогноз. Если у больных без признаков цирроза общая 10-летняя выживаемость составляет 93%, то у пациентов с манифестными формами цирроза печени она снижается до 62%. Какие параметры можно использовать для прогностической оценки у больных ИГХ?Многовариантный анализ, проведенный в итальянских исследованиях у 212 больных ИГХ, показал, что употребление алкоголя, повышенное содержание гамма-глобулинов и цирроз печени в стадии В или С по Чайльду являются отрицательными прогностическими факторами. Напротив, у этих пациентов, не имевших цирроза печени, не наблюдалось ни одного летального исхода. Высокая летальность у больных, одновременно употреблявших большое количество алкоголя, подтверждает, что алкоголь может утяжелять клинические проявления ИГХ (факт, получивший и экспериментальное обоснование в исследованиях на животных). Эти данные еще раз показывают, как важно диагностировать и последовательно лечить в течение всей жизни ИГХ у гомозиготных больных еще на доцирротической стадии заболевания. От чего умирают больные ИГХ?В уже упоминавшемся исследовании, проведенном у 212 итальянских больных ИГХ, первичная гепатоцеллюлярная карцинома оказалась самой частой причиной смерти (45%). Эти данные заметно превышают частоту гепатоцеллюлярной карциномы, которая приводится в других многочисленных работах и колеблется в пределах от 25 до 35%. Таким образом, перенасыщение железом значительно повышает риск развития злокачественной опухоли, но лишь тогда, когда уже имеется цирроз печени. В целом риск развития гепатоцеллюлярной карциномы у больных ИГХ превышает таковой в популяции более чем в 200 раз. Гепатоцеллюлярная карцинома, развившаяся на фоне цирроза печени, вызванного ИГХ, не имеет каких-либо клинических отличий от гепатоцеллюлярной карциномы другого происхождения. В патогенетическом плане многолетнее перенасыщение организма железом действует как кокарцино-ген. Гепатоцеллюлярная карцинома может возникать как у леченых, так и у нелеченых пациентов. Однако у всех больных с гепатоцеллюлярной карциномой, развившейся на фоне многолетнего ИГХ, выявляется значительное увеличение содержания железа в печени, как правило, более чем в 10 раз превышающее нормальные показатели. Остается противоречивой точка зрения о более частом возникновении у больных ИГХ злокачественных опухолей внепеченочной локализации. Данные о частоте таких опухолей значительно различаются. Согласно итальянской работе, частота таких опухолей у больных ИГХ составляет 3,7%; в 14% случаев они служат причиной смерти пациентов. Обсуждается также вопрос о дополнительной роли других факторов (алкоголь, вирусы). Известно, что при ИГХ часто встречаются вирусные инфекции. Кроме того, у больных ИГХ и гепатоцеллюлярной карциномы алкоголизм и пристрастие к никотину выявляются значительно чаще, чем улиц, которые страдают циррозом печени и гепатоцеллюлярной карципомой другого генза. ИГХивирусныйгепатит(ВГВ,ВГС)Недавно отмечено, что у некоторых больных ИГХ при гистологическом исследовании определяется типичная картина хронического вирусного гепатита. Эти наблюдения имеют значение в первую очередь в тех странах, (например, в Италии), где часто встречаются инфекции ВГВ и ВГС. Последние данные, полученные в этой стране, показывают, что частота обнаружения HBsAg у больных ИГХ более чем в 2 раза превышает таковую у здоровых лиц контрольной группы, проживающих в той же области. В равной мере частота выявления анти-ВГС у больных ИГХ более чем в 3 раза превышала таковую у здоровых доноров крови. Существует спекулятивное утверждение, что перенасыщение железом способствует развитию хронической вирусной инфекции, возможно, вследствие блокады иммунной реактивности организма на фоне перегрузки железом. Интересны в этой связи последние пилотные исследования, которые свидетельствуют, что, наоборот, при исходном вирусном гепатите без ИГХ кровопускания способствуют улучшению функции печени. Предполагают, что в случае предшествующего ИГХ возникает синергич-ное токсическое действие железа и вирусной инфекции на гепатоцит. Поскольку и железо, и хроническая вирусная инфекция неблагоприятно влияют в плане развития гепатоцеллюлярной карциномы, при нарушении метаболизма железа и инфекции ВГВ или ВГС необходимо обращать особое внимание на риск по гепатоцеллюлярной карциноме. Целесообразность противовирусной терапии в комбинации с кровопусканиями пока не установлена. ИГХ и алкогольКлинические наблюдения показывают, что больные ИГХ почему-то употребляют больше алкоголя, чем здоровые лица. Известно, что алкоголь стимулирует всасывание железа из кишечника. Правда, концентрация железа в печени улиц, злоупотребляющих алкоголем, никогда не бывает столь высокой, как у пациентов с ИГХ. В то же время алкоголь и ИГХ потенцируют развитие цирроза печени, возможно, в связи с тем, что алкоголь ведет к «дополнительному» поступлению железа. Больному ИГХ лучше отказаться от такого дополнительного поступления железа (к сожалению, это касается в первую очередь любителей красного вина сорта бордо, которое содержит немалое количество железа), а также воздерживаться от продуктов, богатых железом, например, не есть потроха. 12.8.6. ПРАКТИЧЕСКИЕ ВЫВОДЫ ИГХ является одним из наиболее частых наследственно обусловленных заболеваний. Диагностика ИГХ оказывается несложной, если помнить о возможности этого заболевания, когда у больного с умеренным повышением трансаминаз выявляются отчетливое увеличение концентрации ферритина в сыворотке и значительное повышение насыщения трансферрина. Тем не менее и в настоящее время, как правило, проходит до 5 лет, пока, наконец, не проводятся исследования, ведущие к диагностика ИГХ. В эпоху лучевой диагностики ИГХ по-прежнему подтверждается с помощью биопсии печени с определением концентрации железа в биоптате. В сомнительных случаях и при необходимости дифференциальной диагностики с гемосидерозом, часто встречающимся при хроническом алкоголизме, можно определять индекс железа печени (Ни), позволяющий хорошо дифференцировать эти заболевания на дофибротической стадии. Часто забывают о том, что диагностика наследственно обусловленного заболевания должна сопровождаться обследованием родственников больного, которое дает возможность своевременно (т.е. при отсутствии клинических симптомов и на доцирротической стадии) выявить это нарушение метаболизма и назначить соответствующее лечение. Обследование клинически здоровых членов семьи включает в себя определение концентрации сывороточного ферритина и насыщения трансферрина. Концентрация ферритина выше 1000 нг/мл и насыщение трансферрина выше 60% должны вызывать серьезные подозрения на нераспознанный ИГХ у «здоровых в остальном» членов семьи. Следующим шагом диагностического поиска в таких случаях должна быть биопсия печени с определением содержания железа в биоптате. Кровопускания начинают у больных ИГХ сразу после установления диагноза и проводят в течение всей жизни. Это правило относится и к пациентам на доцирротической стадии ИГХ без клинических симптомов заболевания. Цель лечения заключается в предупреждении изменений паренхиматозных органов, обусловленных перенасыщением железом, и снижении риска осложнений, связанных с поражением органов. Важную роль играет фактор времени. Первые 18 мес лечения должны привести к нормализации баланса железа. В связи с этим кровопускания (объемом 500 мл) необходимо проводить еженедельно (!) до тех пор, пока не нормализуется уровень ферритина в сыворотке. Медикаментозная терапия не может заменить кровопусканий. Целесообразность ее проведения можно обсуждать только в крайне редких случаях (обычно у больных на далеко зашедшей стадии цирроза печени). Для того чтобы устранить у больных ИГХ в течение заданных 18 месяцев положительный баланс железа, требуется в среднем от 50 до 150 кровопусканий. Если эта цель в указанные сроки не достигается, то продолжительность жизни больных значительно уменьшается. Кровопускания у пациентов с ИГХ никогда нельзя полностью прекращать. Однако их частота может быть сокращена (как правило, до 1—2 кровопусканий в 3 мес), если удается достичь стабилизации обмена железа, подтверждаемой нормальной концентрацией ферритина в сыворотке. Кровопускания улучшают у больных ИГХ функцию печени, иногда — сократительную функцию сердца, но не уменьшает выраженности эндокринных нарушений и артропатии. О предотвращении развития гепатоцеллюлярной карциномы можно говорить только тогда, когда пациент последовательно лечится кровопусканиями уже на доцирротической стадии, и когда стадия цирроза печени еще не наступила. Стадия цирроза означает уже стадию предраковых изменений. При прогрессирующем ухудшении функции печени следует ставить вопрос о трансплантации печени. Хотя патогенетический дефект при этой операции не устраняется, больные получают драгоценные годы жизни. Ошибки в диагностике и лечении ИГХ встречаются часто. К наиболее серьезным из них относятся: 1. Затягивание диагностического процесса (особенно промедление с проведением биопсии печени и количественным определением железа в биоптате).
Недостаточные кровопускания и слишком большие интервалы между ними.
Недостаточное обследование родственников больного.
Простое «наблюдение» за членами семьи больного, не имеющими клинических симптомов заболевания, вместо их активного лечения.
|
|
|
 Скачать 6.25 Mb.
Скачать 6.25 Mb.