МОНОГРАФИЯ Гепатит и последствия гепатита. Майер К.-П (в word). Гепатит и последствия гепатита Практич рук. Пер с нем. Под ред. А. А. Шепулина. М. Гэотар медицина, 1999. 432 с
 Скачать 6.25 Mb. Скачать 6.25 Mb.
|
|
12.9. ПЕРВИЧНЫЙ БИЛИАРНЫЙ ЦИРРОЗ ПЕЧЕНИ 12.9.1. ЧАСТОТА И ЭПИДЕМИОЛОГИЯ Если прежде первичный биллиарный цирроз печени (ПБЦ) рассматривался как редкое заболевание, то в настоящее время его распространенность стала весьма значительной (табл. 87). Учащение диагностики ПБЦ, причем уже на ранней стадии, объясняется, кроме всего прочего, типичными лабораторными изменениями. ПБЦ встречается у представителей всех рас. По неясным причинам этим заболеванием страдают преимущественно женщины, причем 90% в возрасте старше 40 лет. Имеются отдельные сообщения о семейных случаях ПБЦ, а также о возможности более высокой заболеваемости в отдельных регионах. Так, в одной английской работе было показано, что 88% больных ПБЦ проживали в одном районе города с общим водоснабжением. Отсюда был сделан вывод, что определенные компоненты питьевой воды могут способствовать развитию заболевания. В отдельных сообщениях приводятся очень редкие случаи ПБЦ у близнецов, братьев и сестер и даже у контактировавших лиц. Правда, до сих пор не выявлено связи между аллелями системы HLA и частотой развития ПБЦ. 12.9.2. КЛИНИКА Жалобы больных могут быть многообразными. У большой части пациентов клинические симптомы заболевания могут вообще отсутствовать. Частыми жалобами больных являются утомляемость и зуд (табл. 88). Симптомы, указывающие на поражение печени, включают в себя гепа-томегалию и спленомегалию, а также гиперпигментацию и ксантелазмы. Резко выраженная желтуха встречается редко. Уровень билирубина к моменту первого выявления заболевания остается, как правило, в пределах от Таблица 87 Эпидемиология ПБЦ Заболеваемость (Частота новых случаев заболевания в течение года) 1,4/100 ООО (Швеция) Распространенность (Частота на 100 000 населения) 0,7 Германия
  1 до 2 мг/дл. В табл. 89 приводится ожидаемая частота данных клинического обследования у большого числа больных с ПБЦ в сравнении с таковыми у пациентов с первичным склерозирующим холангитом. Важное место в клинической картине занимают внепеченочные проявления, которые могут вызвать подозрения на коллагеноз. К ним относятся поражения суставов, синдром Шегрена, изменения кожи. В редких случаях наблюдаются альвеолиты, имеющие, по-видимому, иммунокомплексную природу. В отличие от больных первичным склерозирующим холангитом, у пациентов с ПБЦ сопутствующие хронические воспалительные заболевания кишечника встречаются очень редко (табл. 90). Важно отметить, что ПБЦ может протекать одновременно с другими заболеваниями печени, а также непеченочными заболеваниями (синдром «перекрывания»). Примерно у 10—15% анти-М2/анти-М9-положительных больных обнаруживаются лабораторные и гистологические признаки второго заболевания. Это означает, что у некоторых пациентов могут одновременно существовать два аутоиммунных заболевания печени. Хронический аутоиммунный гепатит, алкогольные токсические поражения печени или классическая системная красная волчанка представляют собой примеры такого «перекрывания». Наличие или отсутствие внепеченочных проявлений может облегчить дифференциальную диагностику.  В практическом плане важно, что примерно у трети всех больных с ПБЦ могут обнаруживаться бессимптомные поражения мочевых путей, а у 40% пациентов — камни в желчном пузыре, часто также без клинических проявлений. Причина более частого (в 3—4 раза) развития опухолей (особенно рака молочной железы) у больных ПБЦ по сравнению с представителями общей популяции пока остается невыясненной. 12.9.3. ЛАБОРАТОРНАЯ ДИАГНОСТИКА, ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА И БИОПСИЯ ПЕЧЕНИ Лабораторные исследования вносят существенный вклад в установление диагноза при подозрении на ПБЦ. Часто встречаются постоянное повышение активности ферментов холестаза (щелочной фосфатазы, гамма-ГТ), увеличение содержания холестерина, повышение уровня IgM и гамма-глобулинов, хотя они неспецифичны. Отмечается повышение СОЭ, а также увеличение концентрации IgG в сыворотке. Пограничные или умеренно повышенные показатели активности трансаминаз хорошо укладываются в предположительный диагноз ПБЦ. Напротив, высокая концентрация билирубина (более 2 мг/дл), отмечаемая при впервые выявленном заболевании (особенно при отсутствии клинических симптомов), служит необычной находкой и заставляет думать о том, что в основе этих изменений лежит заболевание другой этиологии. Специфичным для ПБЦ считается М2-антиген, состоящий из 5 антигенных детерминант. Детерминанта с мол. массой 70—75 кД была идентифицирована как комплекс ферментов на внутренней мембране митохондрий. Эти М2-антигены имеют диагностическое значение. Был разработан тест ELISA против компонентов М2-комплекса. Чувствительность теста в диагностике ПБЦ составляет 98%, специфичность — 96%. Это означает, что менее 5% больных с ПБЦ не имеют антимитохондриальных антител (АМА). В настоящее время можно выделить 4 подтипа АМА. Наряду с антителами анти-М2 встречаются, в большинстве случаев вместе, антитела анти-М9, анти-М4 и анти-М8, которые реагируют с различными эпитопами мембраны митохондрий. Какое значение для клинической практики имеет выделение подтипа АМА? По-видимому, существует связь между профилем АМА и прогнозом заболевания. По результатам наблюдения за течением заболевания (более 16 лет), с терапевтических позиций (см. ниже) можно утверждать, что изолированное обнаружение анти-М9 и/или анти-М2 коррелирует с хорошим прогнозом. Прогрессирующее течение заболевания отмечается у больных с анти-М2, анти-М4 и анти-М8, а также у пациентов, у которых выявляются анти-М2, анти-М4 и/или анти-М8. Это означает, что с помощью профиля АМА в будущем можно будет идентифицировать неактивные (ранние) и активные (прогрессирующие) формы ПБЦ и соответственно выделять группы больных с низким и высоким риском. Необходимо помнить о возможных лабораторных диагностических «ловушках». Очень небольшая часть больных ПБЦ оказывается АМА-отрица-тельной. Примерно у 3% всех пациентов с ПБЦ имеется синдром «перекрывания» с другими аутоиммунными заболеваниями, который идентифицируется с помощью диагностически значимых антител. Так, при обнаружении АМА-отрицательного, IgM-положительного холестатич ее кого заболевания печени необходимо проводить дифференциальную диагностику с иммунной холангиопатией («перихолангитом»), при которой в большинстве случаев обнаруживаются и антинуклеарные антитела (AHA). Более чем у половины больных с активным течением ПБЦ и более чем у половины пациентов с хроническим активным гепатитом также выявляются AHA. Таким образом, с помощью только лабораторных исследований иногда трудно различить эти заболевания. Все же следует иметь в виду, что при аутоиммунном хроническом гепатите уровень IgG в 3/4 случаев повышен более чем вдвое, а уровень IgM остается нормальным. В свою очередь почти у 90% больных ПБЦ активность щелочной фосфатазы превышает 200 ЕД/л, составляя в среднем 453 ЕД/л. Это означает, что при обследовании больных большое дифференциально-диагностическое значение имеет количественное определение иммуноглобулинов. Дифференциальная диагностика при ПБЦ предусматривает также исключение: а) саркоидоза, б) первичного склерозирующего холангита, холестаза, обусловленного приемом лекарственных препаратов. Саркоидоз можно распознать на основании многообразных внепеченоч-ных клинических проявлений заболевания (поражения легких, лимфатических узлов, костной и нервной системы, глаз) и результатов соответствующих лабораторных исследований (определение уровня кальция, конвертирующего фермента, тромбоцитов). Первичный склерозирующий хо-лангит диагностируется по характерной картине ЭРХПГ. Холестаз, обусловленный приемом лекарственных препаратов, распознается на основании соответствующих анамнестических данных. В эпоху лучевых методов исследования диагноз ПБЦ все равно подтверждается гистологически. Выделяют 4гистологические стадии заболевания, причем на ранних стадиях заболевания правильный морфологический диагноз часто не может поставить даже опытный патолог. Точный патологоанатомический диагноз предполагает взятие биоптата печени возможно большего объема. Биопсии тонкой иглой редко удовлетворяют этому требованию Гистологические стадии могут в значительной мере перекрывать друг друга, поэтому при взятии нескольких биоптатов из одной печени можно одновременно диа» ностировать различные гистологические стадии заболевания. У небольшого числа AMА-отридательных больных с атипичным течением заболевания может возникнуть необходимость в проведении (в первую очередь с целью дифференциальной диагностики) ЭРХПГ в дополнение к лапароскопии и биопсии 12.9.4. ЛЕЧЕНИЕ И ПРОГНОЗ Естественное течение заболевания необходимо принимать во внимание при определении показаний к тому или иному методу лечения. Течение ПБЦ очень различно, спонтанные ремиссии неизвестны. Отдаленный прогноз считается серьезным, хотя ближайший прогноз может быть чрезвычайно вариабельным. У больных с бессимптомным течением за-болевания (по крайней мере, в первые 5 лет) он не отличается от такового у здоровых лиц в популяции (рис. 70), но в дальнейшем ухудшается. Правда, нельзя утверждать, что у всех больных без клинических проявлений заболевания показатели выживаемости действительно уменьшаются. Необходимо иметь в виду, что первично бессимптомные пациенты представляют собой неоднородную группу. У одних больных (пока их нельзя идентифицировать) бессимптомное течение заболевания сохраняется, так что продолжительность жизни у них, по-видимому, не уменьшается. У других пациентов заболевание прогрессирует. В связи с этим можно выделить различные доклинические и клинические фазы ПБЦ (табл. 91) и приблизительно оценить продолжительность каждой фазы. В швейцарском иссле- 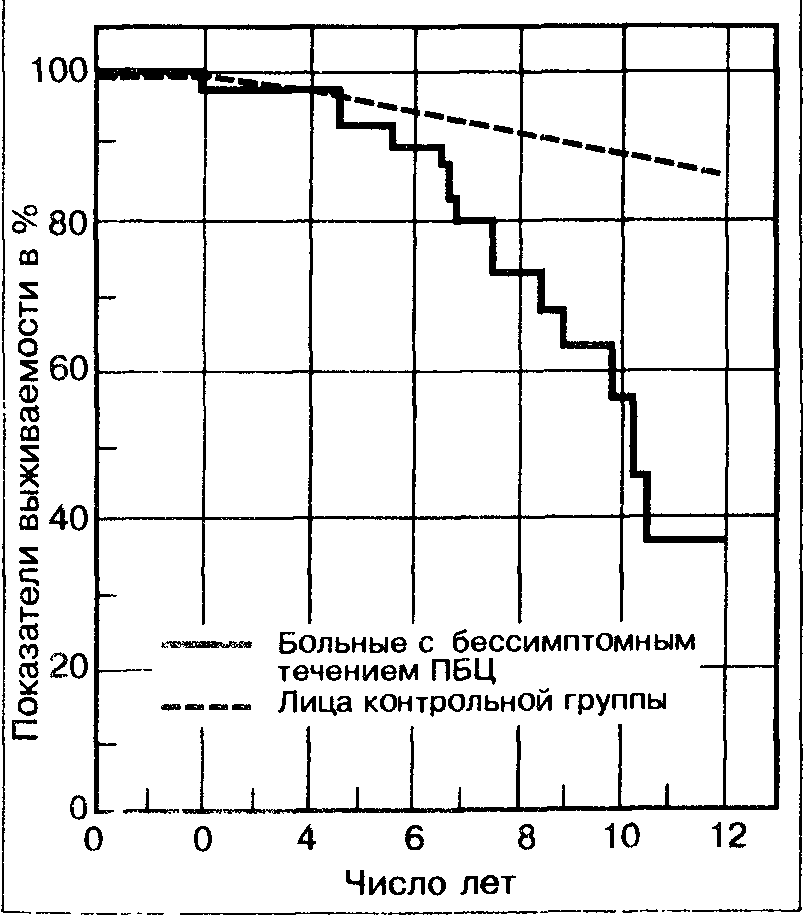 Рис. 70. Показатели выживаемости больных с бессимптомным течением ПБЦ (по К Balasubramaniam и соавт Gastroenterology, 1990) Таблица 91 Стадии ПБЦ при естественном течении заболевания Стадия Ориентировочная иродолжительиость
неопределенная у некоторых больных у других — от 2 до 20 лет от 3 до 11 лет 0-2 года довании на материале 61 больного было показано, что средняя продолжительность жизни больных ПБЦ, у которых имеются клинические симптомы заболевания, составляет 12,1 ± 1,0 год. Модель, позволяющая оценить прогноз в отдельном случае заболевания, представлена в табл. 92. У пациентов, имеющих клинические симптомы заболевания, прогноз ухудшается (рис. 71). Определить прогноз в каждом отдельном случае непросто. По-видимому, вопреки распространенному мнению, степень повышения маркеров холестаза или показателей ферментов цитолиза не влияет на прогноз! Напротив, в оценке прогноза имеют значение следующие дискриминирующие факторы: 1) показатели пробы Квика, 2) концентрация альбуминов, 3) концентрация билирубина, 4) возраст больных, 5) гепатоспленомегалия.  Практическому врачу, наблюдающему больного ПБЦ, наряду с контролем клинических симптомов достаточно определить концентрацию билирубина. Это простое исследование билирубина в сыворотке необходимо проводить 2 раза в год с интервалом 6 мес. Нарастание уровня билирубина свидетельствует о прогрессировании заболевания! Зависимость выживаемости больных ПБЦ от концентрации билирубина представлена в табл. 93. Неблагоприятные факторы, выявление которых у больных ПБЦ, имеющих клинические симптомы, может стать показанием для назначения лечения, приведены в табл. 94. Ясно, что в каждом конкретном случае заболевания 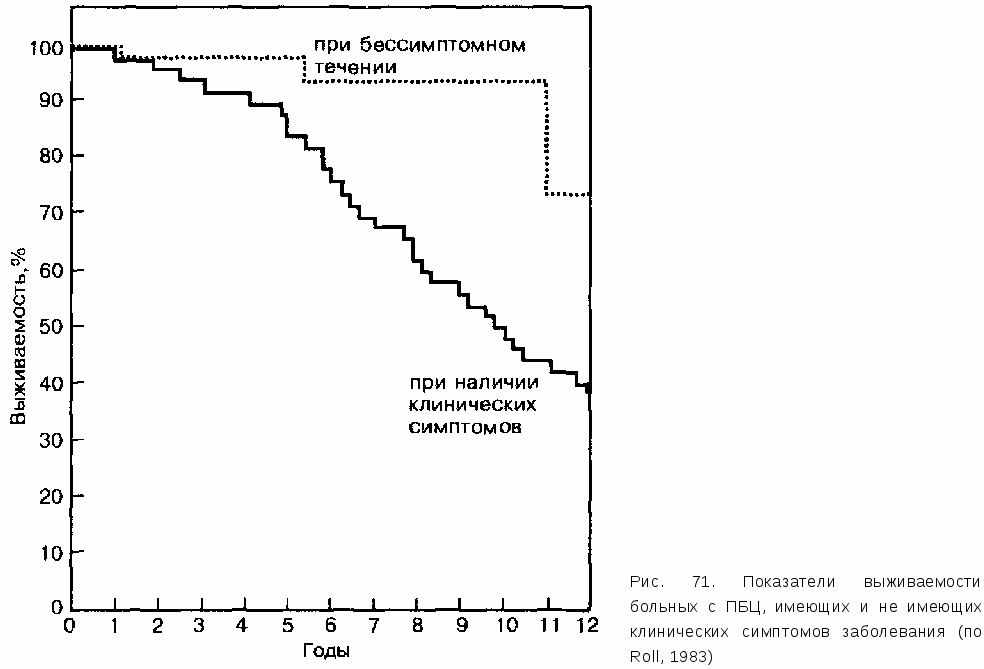 Таблица 93 Прогноз ПБЦ (по S. Sherlock 1985) Концентрация билирубина (мг/дл) до 3 2,1-6,0 свыше 6 Ожидаемая продолжительность жизни 8-13 лет 2—7 лет менее 2 лет Таблица 94 Плохой прогноз при ПБЦ если: имеются клинические симптомы старший возраст ге патоспле номегал ия обнаружение положительных АМА М2 + М4 повышение билирубина гистологически: отсутствуют гранулемы (?) цирроз (?) по-прежнему очень трудно решить вопрос, проводить лечение у больного с подтвержденным диагнозом ПБЦ или нет. Эта неопределенность привела к тому, что врачи крупного английского гепатологического центра, основываясь на простой классификации, учитывающей выраженность симптомов,  концентрацию билирубина и прогноз, либо ограничиваются наблюдением больных, либо включают их в контролируемые исследования с проведением лекарственной терапии, либо направляют пациентов в центры трансплантации печени (табл. 95). Какими возможностями лечения ПБЦ мы располагаем? Целесообразно различать общие мероприятия, способствующие симптоматическому улучшению, и различные методы лекарственной терапии, направленные против вероятного патогенетического фактора (или факторов?) заболевания и последствий его воздействия на печень. Поскольку в насющее время наши знания о патогенезе и этиологии ПБЦ недостаточны, эти методы лечения находятся еще на стадии контролируемых клинических исследований. Напротив, активная хирургическая тактика, предусматривающая проведение трансплантации печени на поздних стадиях заболевания, представляет собой общепризнанный метод лечения ПБЦ. а) Общие мероприятия (табл. 96) Общие мероприятия направлены на лечение зуда, печеночной остеоди-строфии и синдрома недостаточного пищеварения, обусловленного поражением печени. Препаратом выбора для борьбы с зудом по-прежнему является холести-рамин. Этот нерастворимый анионообменный препарат связывает желчные кислоты в тонкой кишке, в результате чего образуются нерастворимые комплексы, которые выделяются с калом. Наиболее выраженный эффект препарата наблюдается когда концентрация желчных кислот в тонкой кишке становится максимальной. Обычно это бывает во время завтрака. Отсюда следует, что первую дозу препарата (как правило, 4 г) нужно принимать непосредственно перед завтраком, а вторую — сразу после него. Если такой дозы препарата достаточно для купирования зуда, то этой схемы лечения придерживаются и в дальнейшем. Если все-таки зуд сохраняется, то Таблица 96 Симптоматическая терапия при ПБЦ и ПСХ Зуд Стеаторея Холестирамин Ограничение жира, прием СЦТ [церес (ceres)] 8—24 г/сут 40-50 г/сут Гиповитаминозы А Витамин А 100 ООО ЕД внутримышечно в месяц D Холекал ьциферол 100 000 ЕД внутримышечно в месяц К Витамин К 10 мг внутримышечно в месяц может оказаться целесообразным дополнительный прием препарата перед обедом, а в ряде случаев — и перед ужином. Побочный эффект высоких доз холестирамина — диарея — вполне объясним, если принимать во внимание механизм его действия. Стеаторея и недостаточное всасывание жирорастворимых витаминов могут служить основанием для того, чтобы заменить содержащийся в пищевом рационе жир среднецепочечными триглицеридами (СЦТ), а также назначить дополнительно (см. ниже) витамин А. Кроме того, с практической точки зрения врачу важно напомнить пациентам, что противозудный эффект отмечается не сразу, а спустя как минимум 1—2 нед после начала лечения. Если, несмотря на максимальные дозы холестирамина, зуд сохраняется, то дальнейшая борьба с ним оказывается очень трудной. В таких случаях можно попробовать назначить фенобарбитал по 60 м г на ночь. В тяжелых случаях иногда требуется увеличение дозы до 180 мг/сут. Понятно, что при такой дозе фенобарбитала возникают значительные трудности, связанные с его снотворным действием. Эффективным оказывается также плазмаферез. Как правило, он приводит к быстрому уменьшению зуда, причем продолжительность эффекта может быть различной, иногда несколько месяцев. Этот метод оказывается достаточно дорогостоящим. Вопрос о его применении целесообразно ставить в первую очередь тогда, когда у больных ПБЦ отмечается еще и болевой синдром вследствие нейропатии (ксантоматозной). При неэффективности этих терапевтических мероприятий обсуждается возможность применения иммуносупрессивных средств, а в отдельных случаях и антигистаминных препаратов, со слабым седативным действием. Назначение рифампицина в дозе 600 мг/сут оказывается эффективным у больных, которые резистентны к лечению холестирамином или лишь частично отвечают на него. Препарат можно применять на протяжении нескольких месяцев. При сравнении с плацебо рифампицин оказался достоверно более эффективным. Таким образом, этот препарат обогатил арсенал лекарственных средств, применяемых для лечения столь мучительного симптома ПБЦ, как зуд. Иногда рифампицин вызывает аллергические реакции. 10—2437 Противозудное действие оказывают также андрогены. Однако, учитывая способность данных препаратов вызывать холестаз, мы отказываемся от их применения в случаях ПБЦ. На не очень далеко зашедшей стадии заболевания можно также обсуждать вопрос о проведении фототерапии, которая способна, по крайней мере, в ранних стадиях ПБЦ временно уменьшить зуд. На поздних стадиях заболевания этот метод оказывается неэффективным. Первые результаты японских исследований свидетельствуют, что урсо-дезоксихолевая кислота (хотя лишь после 4 мес ее применения) способствует уменьшению зуда. В общем, при лечении больных следует исходить из того, что зуд, однажды появившись, сам по себе не исчезает. В таких случаях, как правило, требуется длительная терапия, значительно повышающая качество жизни больных. Каковы методы лечения печеночной остеодистрофии? Лечение печеночной остеодистрофии по-прежнему остается трудной задачей и редко дает удовлетворительные результаты. С целью лечения остеомаляции обычно назначаются витамин D2 по 100 ООО ЕД в месяц внутримышечно. Однако положительное влияние этих мер в отношении устранения нарушений обмена в костной ткани или их предупреждения пока не нашло подтверждения. Мы назначаем больным витаминотерапию — в первую очередь пациенткам в постменопаузальном периоде. Чрезвычайно трудной задачей оказывается предупреждение развития ос-теопороза у больных ПБЦ. Обычно рекомендуют прием кальция по 1,5 г в день, богатую витаминами пищу, регулярное солнечное освещение (в необходимых случаях «горное солнце» по 10 мин в день), физические упражнения. Вопрос о том, является ли поддерживающий прием гидроксиапатита оптимальной формой применения кальция, пока остается открытым. В тяжелых случаях ПБЦ с болями в костях и спонтанными переломами успешным может оказаться внутривенное введение кальция из расчета 15 мг/кг в виде глюконата кальция, вводимого внутривенно капельно на 500 мл 5% раствора глюкозы в течение 4 ч. Сначала ограничиваются 7-дневным курсом лечения. У некоторых больных удается на какое-то время уменьшить болевые ощущения. Данных об эффективности кальцитонина при лечении больных ПБЦ нет. Изучаются возможности применения дифосфонатов. На практике пациенткам в постменопаузальном периоде мы назначаем витамин D в дозе 1000 ЕД вдень в сочетании с кальцием (1 — 1,5 г/сут) под контролем уровня кальция в сыворотке. Вне декомпенсированной стадии цирроза печени сохраняют значение физические упраженения, а также регулярное солнечное облучение. Нужна ли дополнительная витаминотерапия? У больных ПБЦ обнаруживается недостаточное всасывание витамина Е. Однако неврологические симптомы, свойственные такому дефициту, как правило, отсутствуют. Если терапия витамином Е и показана, то только при очень низком содержании этого витамина (меньше Юмкг/мл), поскольку при выраженном нарушении всасывания витамина Е имеется риск клинических проявлений его дефицита. У больных ПБЦ часто бывает недостаток витамина А. Однако низкий уровень витамина А объясняется не его дефицитом, а сниженной мобилизацией из печени. Если принять во внимание опасность гепатотоксического эффекта при длительном применении витамина А, а также то, что по низким концентрациям витамина А в сыворотке (с учетом нарушенного синтеза ретинол-связывающего протеина у больных ПБЦ) нельзя делать выводы о его концентрации в тканях, то от рутинного профилактического применения витамина А стоит отказаться. Последние данные свидетельствуют, что, хотя концентрации жирорастворимых витаминов (A, D, Е, К) в сыворотке у значительного процента больных ПБЦ низкие, клинические проявления витаминной недостаточности обнаруживаются лишь у 2% пациентов. Дефицит жирорастворимых витаминов коррелирует с недостаточным всасыванием жиров, что в свою очередь коррелирует с выраженностью холестаза и снижением секреции желчных кислот. Для клинической практики это означает, что указанные состояния, связанные с дефицитом витаминов, чаще наблюдаются при желтухе и клинических симптомах нарушенного гепатобилиарного пищеварения (прежде всего при хронической диарее). Обычная терапия жирорастворимыми витаминами у большинства больных ПБЦ, по-видимому, не нужна. На поздних стадиях заболевания с прогрессирующей желтухой целесообразно определять концентрацию витаминов A, D, Е в плазме и протромбиновое время (как индикатора дефицита витамина К), чтобы на основании полученных данных решать вопрос о витаминотерапии. Какие общие мероприятия следует рекомендовать для лечения нарушений жирового обмена при ПБЦ9 Нарушение жирового обмена в виде выраженных ксантелазм, обусловленных увеличением содержания холестерина в сыворотке, представляет собой характерный признак холестатических поражений печени. В терапевтическом аспекте холестирамин является в таких случаях препаратом выбора. Это лечение положительно влияет и в отношении отложения ли-пидов в периферических нервах. Как известно, уровень холестерина у больных ПБЦ может быть очень высоким. Однако исследования электрофореза липидов показали, что артери-осклеротический потенциал нарушенного жирового обмена при ПБЦ, очевидно, не очень значительный. Тем не менее по-прежнему предпринимаются попытки симптоматического воздействия на гиперхолестеринемию при ПБЦ с помощью препаратов, снижающих уровень липидов (типа клофибрата). Применение подобных препаратов все же следует считать противопоказанным. Они вызывают, возможно, из-за влияния на секрецию холестерина, парадоксальное повышение уровня общего холестерина в сыворотке. Это повышение приводит в свою очередь к увеличению образования холестериновых желчных камней и, что было хорошо продемонстрировано отдельными наблюдениями, к увеличению образования камней во внутрипе-ченочных желчных протоках. Обобщая приведенные данные, можно заключить, что нарушение жирового обмена при ПБЦ не является существенным фактором риска поражения сосудов (если вообще является таковым). Предпочтение при его лечении следует отдавать холестирамину. Иначе складывается ситуация при ксантоматозной нейропатии, которая в типичных случаях клинически проявляется интенсивными болями в пальцах и кистях при захвате твердых предметов, значительно нарушающими самочувствие пациентов. Если эти осложнения сохраняются на фоне лечения анионообменными препаратами, то необходимо ставить вопрос о проведении плазмафереза. Необходима ли при ПБЦ специальная диета? Данных, свидетельствующих о преимуществах при лечении больных ПБЦ тех или иных диетических рекомендаций, нет. В то же время стеаторея у больных с ПБЦ обусловливается сниженным поступлением желчных кислот в тонкую кишку, что влечет за собой недостаточное всасывание жиров. Это должно служить основанием для уменьшения содержания жиров в пище до 40 г/сут. Если указанная мера оказывается недостаточной, то примерно половину жиров в пищевом рационе заменяют среднецепочечными триг-лицеридами (церес (Ceres)). При поносах у больных ПБЦ необходимо иметь в виду, что в редких случаях синдром недостаточного всасывания может быть связан со спру или внешнесекреторной недостаточностью поджелудочной железы. Эти заболевания требуют специфической терапии. Примерно 40% больных ПБЦ к моменту первичного установления диагноза имеют недостаточную массу тела (для сравнения: недостаточная масса тела выявляется лишь у 29% пациентов с алкогольным циррозом печени). Таким больным при отсутствии признаков печеночной энцефалопатии рекомендуется, по возможности, питание повышенной энергетической ценности с включением продуктов, богатых белками и витаминами. б) Различные лекарственные препараты Для лечения больных ПБЦ с целью замедления прогрессирования заболевания применялись многочисленные препараты. Однако анализ всех работ, опубликованных с 1950 г., показал, что ни один препарат не в состоянии остановить гистологическое прогрессирование заболевания или вызвать его полную ремиссию, как, например, наблюдается у некоторых больных аутоиммунным агрессивным гепатитом под влиянием иммуносупрессив-ной терапии. Начальные, потенциально обратимые стадии ПБЦ (I стадия) в последние годы предпочитают лечить иммуносупрессивными препаратами, например, преднизолоном и азатиоприном. При лечении II стадии, обратимость которой остается неясной, обсуждается назначение различных лекарственных препаратов типа метотрексата или циклоспорина А. И далеко зашедших и уже точно необратимых стадиях (III-IV стадии), когда имеется фиброзирование, применяют колхицин, а также лекарственные средства, улучшающие отток желчи, например, урсодезоксихолевую кислоту. Высказывается единодушное мнение, что в финале ПБЦ единственным эффективным методом лечения становится трансплантация печени. К сожалению, до сих пор отсутствуют контролируемые исследования по оценке названных прогностических факторов в сходных группах больных. Характеристика отдельных препаратов, применяемых при лечении ПБЦ, приводится ниже. 1. Глюкокортикоиды. Поданным ряда неконтролируемых исследований, препараты этой группы не оказывают положительного влияния на клиническое или гистологическое течение ПБЦ. По нашему мнению, отказ от глюкокортикоидной терапии был преждевременным (не в последнюю очередь этот отказ был связан с тем, что течение остеодистрофии, которая так или иначе обнаруживается у больных с далеко зашедшими стадиями ПБЦ, заметно ухудшалось на фоне глюкокортикоидной терапии). Лишь недавно глюкокортикоиды вновь привлекли к себе внимание. Было проведено контролируемое исследование эффективности их применения у 36 пациентов. Старое правило, согласно которому «кортикостероиды хороши для печени, но плохи для костей», подтвердилось и в этой работе. Вместе с тем у больных, получавших преднизолон (в поддерживающей дозе 10 мг), через 1 год было достоверное уменьшение зуда и утомляемости, а также улучшение функциональных печеночных проб (включая результаты исследования проколлаген-3-пептида) и гистологической картины печени. Однако плотность костной ткани при этом уменьшалась. В настоящее время опубликованы результаты плацебо контролируемо- ' го исследования, проводившегося в течение 3 лет, в котором сравнивались результаты применения преднизолона (у 19 больных) и плацебо (у 17 пациентов). 3 из 19 больных, получавших преднизолон, и 5 из 17 пациентов, получавших плацебо, умерли. Уровень иммуноглобулинов у больных, леченных преднизолоном, достоверно снижался. Улучшились показатели всех сывороточных печеночных проб, при количественном определении снизилась концентрация АМА. Ухудшение гистологической картины печени чаще отмечалось у больных, получавших плацебо. Достоверных различий содержания минеральных веществ в костной ткани у больных двух групп через 3 года не выявлено. На основании полученных результатов сделан вывод, что применение преднизолона у больных ПБЦ ведет к ослаблению клинических симптомов, улучшению лабораторных показателей и гистологической картины, в связи с чем этот препарат можно применять с целью замедления прогрессирования заболевания. Как показала недавно проведенная работа, поддерживающее применение кальция, витамина D и кальцитонина у 38 больных ПБЦ было эффективным в плане снижения резорбции костной ткани при тяжелой остеодистрофии. Эти препараты можно назначать с целью соответствующей профилактической терапии одновременно с длительным лечением кортикостероидами. Полученные в последние годы результаты позволяют рекомендовать кортикостероидную терапию в раннюю фазу ПБЦ (стадии I— II), комбинируя ее при необходимости с другими препаратами (например, с урсодезоксихолевой кислотой). В связи с этим необходимо напомнить о возможности дополнительного назначения азатиоприна (в дозе 75—100 мг/сут), позволяющего уменьшить дозу кортикостероидов. Является ли длительное применение глюкокортикоидов (в сочетании с азатиоприном) с урсодезоксихолевой кислотой и биофосфонатами под регулярным контролем плотности костной ткани идеальной схемой лечения ранних стадий ПБЦ, еще нуждается в подтверждении. Мы рекомендовали бы применение кортикостероидов в первую очередь тогда, когда заболевание осложняется присоединением коллагеноза (например, системной красной волчанки) или имеется «смешанная форма» ПБЦ и хронического агрессивного гепатита.
Результаты международного многоцентрового исследования у 248 пациентов подтвердили тенденцию к улучшению выживаемости, если у пациентов, получавших азатиоприн и не получавших его, было идентичное распределение факторов риска. Выживаемость больных, получавших азатиоприн в дозе 1 мг/кг, достигала в таких случаях 20 мес. Однако вывод о том, что подобные больные должны получать лечение азатиоприном, разделяют не все гепатологи, поскольку протокол указанного исследования не был лишен ряда недостатков. Мы в настоящее время не рекомендуем монотерапию азатиоприном при ПБЦ.
В настоящее время целесообразность монотерапии циклоспорином А считается спорной. Смогут ли новые производные циклоспорина изменить такую оценку, покажет будущее.
Эти первые работы французских авторов дали обнадеживающие результаты как в отношении влияния препарата на клинические симптомы (в частности, уменьшение зуда), так и применительно к названным лабораторным параметрам. После этой работы другие сообщения подтвердили и дополнили приведенные результаты. Греческие авторы на материале 45 больных установили снижение активности ферментов через 3 мес лечения. Через 6 мес терапии это снижение становилось максимальным, после чего оно было уже не столь выраженным. У 3 больных на далеко зашедшей стадии ПБЦ и уровнем билирубина выше 10 мг/дл не было изменений лабораторных показателей. Однако отдельные наблюдения показывают, что применение урсодезоксихолевой кислоты на поздних стадиях заболевания может привести к ухудшению его клинического течения. В редких случаях на фоне терапии урсодезоксихолевой кислотой уменьшается выраженность клинических симптомов (особенно зуда и утомляемости в сочетании со снижением концентрации билирубина, активности щелочной фосфатазы и ГПТ. Несмотря на положительную динамику, это сопровождается прогрессированием гистологических изменений в направлении цирроза печени. Последние данные, полученные при рандомизированном, плацебо контролируемом, двойном слепом исследовании у 153 больных, говорят о необходимости сопоставлять эффективность урсодезоксихолевой кислоты с концентрацией билирубина. У бальных, у которых уровень билирубина был ниже 2 мг/дл, лабораторные параметры на фоне лечения отчетливо улучшались, тогда как у пациентов с уровнем билирубина заметно выше 2 мг/дл (в среднем 5,1 мг/дл) лабораторные показатели если и улучшались, то очень незначительно. Результаты большого многоцентрового контролируемого исследования у 73 больных, получавших урсодезоксихолевую кислоту, и у стольких же пациентов, получавших плацебо, свидетельствовали о неэффективности терапии у 6 больных основной группы и у 13 пациентов контрольной группы. Исследование 95 биоптатов печени показало отчетливое улучшение гистологических параметров. После лечения значительно ослабевал зуд, улучшались функциональные печеночные пробы, уменьшались многие гистологические изменения, характерные для ПБЦ (вплоть до фиброза). На основании полученных результатов авторы сделали вывод, что урсодезок-сихолевая кислота эффективна и безопасна в первую очередь при лечении ранних форм ПБЦ. Последние данные свидетельствуют о том, что этот в целом благоприятный эффект сохраняется в течение 4 лет! Однако только что опубликованные результаты исследования, включавшего 61 пациента, показывают, что на фоне терапии в течение 2 лет, по крайней мере, гистологическое течение заболевания у больных, получавших лечение урсодезоксихолевой кислотой и не получавших такого лечения не изменяется. Может ли применение более высокой дозы урсодезоксихолевой кислоты в течение более длительного периода улучшить эту ситуацию, покажет ближайшее будущее. Как и при применении колхицина (см. ниже), существенное преимущество терапии урсодезоксихолевой кислотой заключается в ее хорошей переносимости, особенно в сравнении с хлорамбуцилом или азатиоприном. Оценивая механизм действия урсодезоксихолевой кислоты, можно сделать вывод, что она положительно влияет на те факторы заболевания, которые отвечают за нарушение выделения первичных желчных кислот, но не действует на патогенетические звенья, обусловливающие развитие иммунных реакций с поражением эпителия желчных протоков. С учетом указанного обстоятельства при ПБЦ целесообразна комбинированная терапия, включающая в себя, например, урсодезоксихолевую кислоту вместе с иммуносупрессивными препаратами (см. выше: 1. Глюкокортикоиды).
При применении колхицина в дозе 1 — 1,2 мг/сут побочные эффекты встречались очень редко или же вообще отсутствовали. У небольшой части больных наблюдались поносы и нехарактерные боли в верхней половине живота. С учетом опубликованных в настоящее время данных мы считаем, что эффективность монотерапии колхицином при ПБЦ недостаточно доказана, в связи с чем не рекомендуем ее проведение у таких больных. Тенденции к улучшению функциональных печеночных проб, а возможно, и показателей выживаемости пациентов при длительном применении колхицина противостоит очень незначительное влияние препарата на гистологические изменения печени или даже его полное отсутствие. Это несоответствие пока не нашло объяснения.
Авторы пришли к заключению о незначительной эффективности мало-тилата, в связи с чем его не стоит рекомендовать в виде монотерапии для лечения больных ПБЦ. в)Хирургическое лечение при ПБЦ Из-за развивающейся при ПБЦ выраженной портальной гипертензии кровотечения из варикозно расширенных вен пищевода могут возникать сравнительно рано, т.е. еще до завершения полной цирротической перестройки печени. Если повторное склерозирование узлов не дает длительного терапевтического эффекта, то следует ставить вопрос о внутрипече-ночном портосистемном шунтировании через яремные вены, поскольку на этой стадии заболевания функция печени еще сохранена и печеночная энцефалопатия наблюдается редко. Если, однако, у больного прогрессируют признаки печеночной недостаточности (усиливается желтуха, увеличивается асцит, нарастают явления печеночной энцефалопатии), то прогноз заболевания становится очень плохим. При повышении уровня билирубина в сыворотке выше 6 мг/дл выживаемость больных уменьшается примерно до 2 лет (см. табл. 93). Однако введение с 1980 г. в клиническую практику трансплантации печени значительно улучшило прогноз. Больные ПБЦ рассматриваются в настоящее время как оптимальные кандидаты на трансплантацию печени, поскольку чаще это женщины среднего возраста без сопутствующих заболеваний. Однако многие вопросы, связанные с трансплантацией печени при ПБЦ, еще остаются открытыми. Это касается в первую очередь времени проведения трансплантации и отбора больных. Какие критерии отбора могут помочь в определении больных, больше всего нуждающихся в трансплантации печени? Исследования у большого числа больных ПБЦ показали, что для трансплантации печени достаточно, по-видимому, нескольких простых критериев. Таковыми могут быть:
Плохое общее состояние и тяжелые сопутствующие заболевания должны рассматриваться как противопоказания. Долго существовавшие возрастные ограничения (60 лет) в настоящее время смягчены в связи с изменением рамок «биологического возраста». Термин «плохое общее состояние» трудно объективизировать. Хирурги-трансплантологи из Голландии оценивают состояние питания больных (а тем самым и общее состояние) главным образом на основании простого определения мышечной массы с помощью измерения окружности плеча. Каковы шансы на успех при трансплантации печени ? В списке показаний для пересадки печени ПБЦ стоит на 2-м месте. С 1980 по 1985 г. было проведено в обшей сложности 97 операций трансплантации печени у 76 больных на далеко зашедших стадиях ПБЦ. 5-летняя выживаемость пациентов составила 66%. С дальнейшим прогрессом операционной техники и улучшением послеоперационного ухода выживаемость в течение 1 года возросла почти до 70%. При этом 90% больных, которые пережили 1-й год после операции, переживают в дальнейшем 3-й и 5-й годы. Из 161 больного с ПБЦ выживаемость в течение 1-го года после операции составила 75%, а выживаемость в течение 5 лет — 70%. Эти данные свидетельствуют, что трансплантация печени значительно улучшает выживаемость больных по сравнению с естественным течением заболевания (см. табл. 93). Правда, примерно у 25% пациентов с пересаженной печенью в дальнейшем приходится проводить повторную трансплантацию. В начальном периоде после трансплантации титр антител падает. Однако эти антитела сохраняются еще долго. Возможность развития в трансплантате печени повторного заболевания оценивается противоречиво. В одном из исследований у 9 из 10 больных в биоптате трансплантата наблюдались признаки заболевания, сходные с таковыми при ПБЦ. Однако другие авторы не смогли подтвердить эти данные. При успешно выполненной трансплантации печени отдаленный прогноз больных ПБЦ следует считать благоприятным, даже если в первые месяцы после операции, возможно, вследствие сочетания постельного режима и иммуносупрессивной терапии, возникают значительные нарушения костной системы. Важно подчеркнуть, что операцию не следует отодвигать на очень поздний срок. Если трансплантация печени проводится по неотложным показаниям, то прогноз остается по-прежнему плохим: выживаемость в течение I года составляет лишь 29%. Насколько хорошие результаты может давать трансплантация печени у больных на далеко зашедших стадиях ПБЦ, видно хотя бы по тому, что после успешной трансплантации более 80% пациентов возвращаются к повседневным занятиям! 12.9.5.ПРАКТИЧЕСКИЕ ВЫВОДЫ ПБЦ представляет собой заболевание женщин среднего возраста, у мужчин оно встречается крайне редко. В клиническом плане выделяют бессим-помную форму ПБЦ, которая по меньшей мере в течение первых 5 лет протекает сравнительно благоприятно, а затем дополняется клиническими проявлениями и приобретает прогрессирующее течение и форму с клиническими симптомами, которая с самого начала склонна к прогрессированию. При бессимптомном течении диагноз ПБЦ ставится обычно на основании лабораторных изменений, свидетельствующих о внутрипеченочном холестазе (повышение активности ферментов холестаза, щелочной фосфатазы, гамма-ГТ, нормальный уровень билирубина в сыворотке). Если заболевание сопровождается клиническими проявлениями, о ПБЦ можно думать при характерных симптомах (утомляемость, зуд, гиперпигментации и ксантелазмы), сочетающихся с перечисленными выше лабораторными изменениями. В обоих случаях диагноз подтверждается при обнаружении повышенного уровня IgM и положительных антимитохондриальных антител (анти-М2), а также при соответствующей гистологической картине. В лечении больных ПБЦ выделяют симптоматические мероприятия, консервативную терапию с использованием различных лекарственных препаратов и активное хирургическое лечение (трансплантация печени). Говоря об общих мероприятиях, необходимо подчеркнуть, что каждый 3-й больной ПБЦ имеет недостаточную массу тела. Таким пациентам при отсутствии явлений печеночной недостаточности (признаки печеночной энцефалопатии) рекомендуется питание повышенной энергетической ценности с высоким содержанием белков. Ограничение жиров или переход на прием среднецепочечных триглицери-дов (торговое название препарата церес (Ceres)) необходимы только при признаках нарушения гепатобилиарного пищеварения (поносы). У всех больным с желтухой на поздней стадии заболевания оправданно назначение терапии жирорастворимыми витаминами (А, Е, К). Напротив, регулярное введением витамина D в ежемесячной дозе 100 000 ЕД внутримышечно для лечения гепатогенной остеодистрофии показано в первую очередь пациенткам в постменопаузальном периоде. Дополнительно целесообразны назначения кальция в дозе 1—1,5 г в день, физические упражнения, регулярное солнечное облучение. Необходимо контролировать уровень кальция в сыворотке. Для симптоматического лечения зуда в настоящее время препаратом выбора остается холестирамин в наименьших эффективных дозах (4—12 г). Анионообменные препараты могут связывать лекарственные средства, поэтому мы рекомендуем назначать другие лекарственные препараты самое раннее через 4 ч после приема холестирамина. Если на фоне терапии холестирамином усиливаются поносы, то показано включение в пищевой рацион среднецепочечных триглицеридов. Для лечения тяжелых форм зуда, резистентных к терапии, применяют плазмаферез, фототерапию, урсоде-зоксихолевую кислоту и рифампицин. Полезными могут оказаться короткие курсы лечения кортикостероидными препаратами в небольших дозах. Гиперлипидемия служит симптоматическим проявлением ПБЦ, свойственным любому холестатическому заболеванию печени. Для ее лечения используется холестирамин. Препараты, снижающие уровень липидов (типа клофибрата), противопоказаны. Длительный эффект различных лекарственных препаратов при ПБЦ пока не установлен. Доказана бесперспективность использования D-пени-цилламина. Рискованным представляется назначение хлорамбуцила. Эффективность циклоспорина А незначительна, а побочные явления могут быть очень выраженными. Вопрос о месте метотрексата в лечении ПБЦ остается открытым. Монотерапия колхицином или азатиоприном, несмотря на хорошую переносимость обоих препаратов, бывает недостаточно эффективной. Применение урсодезоксихолевой кислоты ведет на ранних стадиях заболевания к отчетливому клиническому улучшению и положительной динамике лабораторных параметров. Влияние данного препарата на гистологические изменения печени так же благоприятное. На ранних стадиях заболевания хороший эффект может дать иммуносупрессивная терапия глю-кокортикоидами в сочетании с урсодезоксихолевой кислотой (иногда-в комбинации с азатиоприном). Необходимо дополнительное лечение гепатогенной остеодистрофии. Текущие исследования призваны в первую очередь ответить на вопрос, эффективнее ли комбинированная терапия ПБЦ, чем монотерапия. Поздние стадии ПБЦ служат твердо установленным показанием для трансплантации печени. Важно наладить своевременные контакты с центром трансплантации печени, чтобы подобрать трансплантат в плановом порядке, а не проводить экстренную операцию. Результаты трансплантации печени при ПБЦ обнадеживают. Более 3/4 всех больных, у которых трансплантация печени оказалась успешной, полностью восстанавливают физическую активность. 12.10. ПЕРВИЧНЫЙ СКЛЕРОЗИРУЮЩИЙ ХОЛАНГИТ |
