Патфиз ч.1. Патфиз ч. Гл. 1 Введение в предмет Гл. 2 Общая нозология
 Скачать 9.21 Mb. Скачать 9.21 Mb.
|
|
ГЕНЕЗ РЕАКТИВНОСТИ Формирование реактивности произошло по мере сочетанного усложнения следующих кардинальных характеристик живых существ: • реакции — ответа организма или его части на внешнее или внутреннее воздействие; • чувственности— способности воспринимать и определять характер (качество), силу, локализацию и периодичность воздействующего на организм агента; • раздражимости — свойства организма воспринимать воздействие факторов внешней и внутренней среды и отвечать на них, как правило, генерализованной, малодифференцированной реакцией, например изменением обмена веществ, формы, размеров и др.; • резистентности — сопротивления, противодействия: устойчивости организма или его части к воздействию определённых факторов внешней и внутренней среды. КАТЕГОРИИ РЕАКТИВНОСТИ Реактивность определяется многими факторами и проявляется разнообразными формами изменений жизнедеятельности индивида. В связи с этим различают несколько категорий реактивности. Критериями выделения разновидностей реактивности являются основные биологические свойства организма, степень специфичности ответа организма, выраженность реакции организма на воздействие, природа агента, вызывающего ответ организма, биологическая значимость ответа организма. БИОЛОГИЧЕСКИЕ СВОЙСТВА ОРГАНИЗМА В зависимости от основных биологических свойств организма выделены видовая, групповая и индивидуальная категории (виды) реактивности. • Видовая реактивность детерминируется видовыми особенностями (например, атеросклероз часто наблюдается у людей, но не выявляется в такой форме у кроликов; у кроликов, в отличие от человека, также не развивается сифилис при инфицировании их возбудителем болезни). В ходе эволюции видовые особенности реактивности организма формируются в результате изменчивости (в связи с мутациями), наследственного закрепления кардинальных свойств вида и естественного отбора особей этого вида. • Групповая реактивность. В ней выделяют реактивность возрастную, половую и конституциональную. – Возрастная реактивность (например, дети в большей мере, чем взрослые, подвержены инфБ в связи с незрелостью их иммунной системы). – Половая: характеризуется, в частности, разной устойчивостью мужчин и женщин к кровопотере (у женщин она выше), физической нагрузке (выше у мужчин). – Конституциональная: относительно стабильные морфофункциональные, в том числе психические, особенности организма, определяемые наследственностью и длительным влиянием факторов окружающей среды. Известно, например, что так называемые астеники, в отличие от нормостеников, менее устойчивы к сильным и длительным физическим и психическим нагрузкам. • Индивидуальная реактивность определяется наследуемой информацией, индивидуальной изменчивостью и собственным «жизненным опытом» организма. В отличие от видовой и конституциональной, индивидуальная реактивность организма может быть физиологической и патологической. Последняя проявляется, например, развитием у отдельных индивидов аллергических реакций на факторы, которые у других такого ответа не вызывают. СТЕПЕНЬ СПЕЦИФИЧНОСТИ, ДИФФЕРЕНЦИРОВАННОСТИ ОТВЕТА ОРГАНИЗМА Степень специфичности, дифференцированности ответа организма позволяет выделить реактивность специфическую и неспецифическую. • Специфическая реактивность: например, развитие иммунного ответа на антигенное воздействие. • Неспецифическая реактивность: например, активация фагоцитарной реакции лейкоцитов при их контакте с чужеродными клетками, неорганическими частицами, бактериями, вирусами, паразитами. ВЫРАЖЕННОСТЬ РЕАКЦИИ ОРГАНИЗМА НА ВОЗДЕЙСТВИЕ Выраженность реакции организма на воздействие определяет реактивность нормергическую, гиперергическую, гипергическую и анергию. • Нормергическая реактивность выражается количественно и качественно адекватной реакцией на воздействие какого-либо агента. • Гиперергическая реактивность проявляется чрезмерной реакцией на раздражитель, например развитием анафилактического шока на повторное попадание в кровь Аг. • Гипергическая реактивность характеризуется неадекватно слабой реакцией на воздействие, например неэффективным иммунным ответом на чужеродный Аг при развитии иммунодефицитного состояния. • Анергия характеризуется отсутствием реакции на воздействие, что свидельствует о грубых нарушениях жизнедетельности организма, должной формировать ответ (например, отсутствие реакции на болевой раздражитель при коме). ПРИРОДА АГЕНТА В зависимости от природы агента, вызывающего ответ организма, выделяют иммуногенную и неиммуногенную реактивность. • Неиммуногенная реактивность: изменения жизнедеятельности организма, вызванные воздействием различных агентов психического, физического, химического или биологического характера, не обладающих антигенными свойствами. • Иммуногенная реактивность: изменения жизнедеятельности организма, обусловленные антигенными факторами. БИОЛОГИЧЕСКАЯ ЗНАЧИМОСТЬ ОТВЕТА Биологическая значимость ответа организма определяет физиологическую и патологическую реактивность. • Физиологическая реактивность — ответ, адекватный характеру и интенсивности воздействия, а также имеющий адаптивное значение для организма. Примером может служить одна из разновидностей иммуногенной реактивности — иммунитет. • Патологическая реактивность — реакция, неадекватная по выраженности и/или характеру изменения жизнедеятельности организма, сопровождающаяся снижением его адаптивных возможностей. Пример: аллергическая реакция на какой-либо продукт питания или пыльцу растения. Таким образом, реактивность — динамичное, постоянно меняющееся свойство целостного организма. С позиции врача важно, что это свойство можно изменять целенаправленно с целью повышения устойчивости организма к действию различных патогенных факторов. ПРИНЦИПЫ ЭТИОТРОПНОЙ ПРОФИЛАКТИКИ И ТЕРАПИИ Важная задача раздела патофизиологии «общая этиология» — разработка принципов этиотропного лечения и профилактики болезней и патологических процессов. Этиотропная профилактика и терапия болезней преследуют две главные цели: • Выявление причины болезни или патологического процесса и проведение мероприятий, направленных на предотвращение её воздействия на организм (профилактические мероприятия). • Выявление факторов, способствующих и препятствующих реализации патогенного действия причинного агента, и проведение мероприятий по устранению или подавлению эффектов первых и потенцированию вторых. В качестве примеров профилактических мероприятий могут быть названы меры по устранению условий, благоприятных для реализации действия микроорганизмов или возникновения злокачественных опухолей при иммунодефицитах, и/или активация факторов системы ИБН. Примерами профилактических мероприятий могут служить меры, направленные на предупреждение действия на организм патогенных химических (в том числе канцерогенных) агентов, болезнетворных микроорганизмов, проникающей радиации и других физических факторов. Эти меры реализуются медикаментозным путём (с использованием радиопротекторов, гормонов, ферментов, цитокинов, дезинфицирующих средств и др.) или с помощью немедикаментозных воздействий (например, использования защитной одежды; УФ-облучения, обладающего бактерицидными свойствами; повторного воздействия данного агента на организм в умеренной дозе с целью повышения резистентности к нему). В последнем случае речь идёт о тренировке организма, например, умеренной гипоксией, охлаждением, физической нагрузкой, некоторыми потенциально патогенными веществами. Если причинный агент уже воздействует на организм, то принимаются меры по прекращению либо по уменьшению интенсивности и/или длительности его действия (лечебные мероприятия). Примерами могут служить применение противомикробных и антипаразитарных средств при инфицировании организма; остановка кровотечения, переливание препаратов крови и кровозаменителей при нарушении целостности сосудистой стенки. ОБЩИЙ ПАТОГЕНЕЗ Термином «общий патогенез» обозначают раздел общей нозологии, посвящённый разработке представлений об общих закономерностях возникновения и развития болезней и патологических процессов (включая механизмы выздоровления и умирания), а также формулированию и обоснованию принципов и методов их патогенетического лечения и профилактики. Термин «патогенез» (или частный патогенез) применяют для обозначения механизма развития конкретной болезни (нозологической формы) или конкретного патологического процесса. Патогенез — комплекс взаимосвязанных процессов повреждения и адаптации организма, лежащих в основе возникновения, развития и исходов болезней и патологических процессов. Положения общего учения о закономерностях развития болезней и представления о частном патогенезе отдельных нозологий и патологических процессов тесно связаны и дополняют друг друга. Данные о механизмах возникновения, становления и исходов конкретных болезней обобщаются и на этой основе выявляются общие закономерности их развития, формулируются заключения и теоретические представления общего учения о патогенезе болезней, а также о принципах их терапии и профилактики. Отсюда следует, что общий патогенез является важным компонентом общего учения о болезни — общей нозологии. В свою очередь, положения общего учения о патогенезе используются при анализе конкретных звеньев патогенеза отдельных нозологий и патологических процессов. Источником сведений для разработки представлений общего и частного патогенеза являются клинические данные, а также результаты моделирования болезней и патологических процессов (как на материальных объектах, главным образом на животных, так и формализованного — математического, интеллектуального, компьютерного и др. ОСНОВНЫЕ ПОЛОЖЕНИЯ ОБЩЕГО УЧЕНИЯ О ПАТОГЕНЕЗЕ Ниже рассмотрены наиболее важные характеристики общего учения о патогенезе: наличие этиологического фактора, порочный круг (лат. circulus vitiosus), пусковой механизм, цепной процесс, основное звено патогенеза, специфические и неспецифические звенья , местные и общие явления, патогенные и адаптивные реакции. НАЛИЧИЕ ЭТИОЛОГИЧЕСКОГО ФАКТОРА Присутствие или отсутствие этиологического фактора при уже возникшей болезни определяет особенности ее развития. • При одних болезнях патогенный фактор действует по принципу «включателя» — он запускает инициальное звено патогенеза. В дальнейшем формируется более или менее разветвлённая цепь причинно-следственно связанных процессов, которая уже не нуждается в наличии причины болезни — «Мавр сделал своё дело, мавр может уйти». Примерами таких болезней и патологических процессов могут быть опухоли, лучевая болезнь, инфаркт миокарда, ожог или отморожение ткани. • При ряде болезней их причина постоянно присутствует в организме. Это относится, например, к СД, гипертиреоидным состояниям, многим инфБ, так называемым симптоматическим артериальным гипертензиям и др. При указанных патологических состояниях механизм их развития поддерживается и аранжируется наличием в организме этиологического факторов. ПОРОЧНЫЙ КРУГ Для патогенеза ряда болезней и патологических процессов характерно формирование порочных кругов. Это явление заключается в том, что одно из звеньев патогенеза является причиной расстройств, поддерживающих и/или потенцирующих действие данного звена. Например, при тепловом ударе существенное повышение температуры тела увеличивает нервно-мышечную возбудимость, что приводит к развитию судорог и усилению сократительного термогенеза. Последнее потенцирует повышение температуры и дальнейшее увеличение возбудимости нервных центров и мышц. ПУСКОВОЙ МЕХАНИЗМ В патогенезе болезней и патологических процессов всегда имеется стартовый, инициальный, пусковой механизм. Этот механизм во многом определяет специфику болезненного состояния независимо от того, работает ли он на протяжении всего заболевания или лишь запускает его. Важность обнаружения и понимания сути пускового механизма болезни заключается, с одной стороны, в возможности эффективного патогенетического лечения путём устранения этого механизма, а с другой — в прогнозировании дальнейших этапов патогенеза болезни. Так, знание того, что инициальным звеном патогенеза почечно-ишемической артериальной гипертензии является активация системы ренинангиотензинальдостерон, позволяет врачу блокировать это звено при помощи лекарственных средств (ЛС) и эффективно лечить пациента. Однако наличие лишь одного такого пускового механизма и/или продолжительное его действие характерны не для всех болезней. Так, формирующееся при гипертонической болезни стартовое патогенетическое звено в виде корково-подкоркового комплекса возбуждения сравнительно быстро активизирует другие механизмы повышения и стабилизации АД на высоком уровне: нейрогенный, почечный, эндокринный, гемический. После активации перечисленных звеньев патогенеза гипертонической болезни пусковой фактор может утратить инициирующее значение. ОСНОВНОЕ ЗВЕНО Патогенез болезней имеет основное (главное, ведущее, ключевое, организующее) звено или несколько звеньев. Как правило, оно (они) выявляется от начала до завершения процесса. Так, при заболеваниях с воспалительным компонентом в качестве основного звена выделяют образование и реализацию эффектов медиаторов воспаления; при различных видах анемии — гипоксию; при аллергических болезнях — образование и эффекты аллергических АТ, сенсибилизированных лимфоцитов и медиаторов аллергии. Выявление ключевого звена или звеньев патогенеза лежит в основе проведения эффективной патогенетической терапии и профилактики болезней и патологических процессов. Вместе с тем при ряде болезней в настоящее время трудно выявить такое главное звено. ЦЕПНОЙ ПРОЦЕСС Патогенез болезней и патологических процессов — динамичный цепной процесс. Это определяется тем, что пусковой патогенетический фактор вызывает более или менее разветвлённую цепь других процессов — вторичных, третичных и последующих патогенных изменений. Так, при СД ведущий патогенетический фактор — гипоинсулинизм (недостаточность инсулина и/или его эффектов) — обусловливает нарушение транспорта глюкозы в клетки, что приводит к расстройствам энергетического обеспечения, трансмембранного переноса ионов, субстратов обмена веществ и метаболитов, повреждению мембран и уменьшению активности ферментов. Указанные изменения в свою очередь вызывают нарушение функции органов, тканей и их систем, пластических процессов и каскад иных расстройств. В конечном счёте видно, что СД — заболевание, характеризующееся существенными нарушениями метаболизма, структуры и функции органов и тканей, жизнедеятельности организма в целом. СПЕЦИФИЧЕСКИЕ И НЕСПЕЦИФИЧЕСКИЕ ЗВЕНЬЯ Среди звеньев патогенеза болезни или патологического процесса наряду со специфическими выявляются и неспецифические звенья. Так, для различных видов наследуемых анемий характерно наличие специфических дефектов Hb: при талассемиях — несбалансированный синтез одной из цепей глобина — МЕСТНЫЕ И ОБЩИЕ ЯВЛЕНИЯ Патогенез болезней и большинства патологических процессов включает комплекс тесно взаимосвязанных местных и общих (системных) звеньев. Значимость этих двух категорий патогенетических звеньев, как правило, различна и нередко меняется по ходу формирования болезни. Например, на начальных этапах патогенеза нефрита или цирроза печени важное значение имеют местные механизмы. Вместе с тем по мере прогрессирования названных форм патологии и особенно при развитии недостаточности функций печени или почек общие звенья патогенеза начинают играть доминирующую роль в нарушении жизнедеятельности организма. В отличие от этого, механизм развития, например, большинства эндокринопатий уже на ранних стадиях их развития включает системные, генерализованные патогенетические звенья. Примером может служить гиперкортицизм, сопровождающийся избыточным выделением в кровь глюко-, минерало- и андрогенных стероидов. При этой болезни развиваются как локальные изменения в ткани коры надпочечников, имеющие свои характерные патогенетические звенья (приводящие к гиперпродукции гормонов, гиперплазии и гипертрофии гистологических элементов надпочечников и другим изменениям), так и общие. Последние связаны с эффектами избытка кортикостероидов. К ним относятся патогенетические звенья артериальной гипертензии, гипергликемии, иммунодепрессии, дисбаланса ионов в крови и тканях, кардиопатии и др. Взаимозависимость общих и местных механизмов развития болезней и патологических состояний проявляется также и тем, что регионарные (тканевые и/или органные) патологические процессы могут возникать в результате системных патогенных изменений, и наоборот. Примером первой ситуации могут быть местные патологические процессы (например, опухоли или воспаление в отдельных тканях и органах при иммунодефиците); примером второй — формирование недостаточности иммунной системы организма в результате опухолевого роста. ПАТОГЕННЫЕ И АДАПТИВНЫЕ РЕАКЦИИ Патогенез всех болезней и патологических процессов закономерно включает как патогенные, так и адаптивные (компенсаторные, защитные, репаративные, саногенетические) реакции и процессы. Конкретная их комбинация, выраженность и значимость реакций и процессов широко варьируют у различных пациентов не только с разными формами патологии, но даже с одной и той же. Например, при аллергической форме бронхиальной астмы выявляются как патогенные эффекты (бронхоспазм, нарушение вентиляции и перфузии лёгких, диффузии газов через аэрогематический барьер), так одновременно и адаптивные. Последние направлены на обнаружение, фиксацию, деструкцию и элиминацию из организма аллергена, повышение эффективности доставки и утилизации тканями кислорода, компенсацию сдвигов кислотно-щелочного равновесия (КЩР) организма и ряд других. Общее учение о патогенезе содержит и ряд других положений. Они характеризуются в учебнике при изложении типовых или частных форм патологии. ПРИНЦИПЫ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ И ПРОФИЛАКТИКИ Цель патогенетического лечения больного — прерывание и/или снижение эффективности механизмов повреждения и одновременно — активация адаптивных (саногенетических) реакций и процессов. Иногда эти группы мероприятий называют патогенетической и саногенетической терапией соответственно. ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ В качестве примера лечебного воздействия, направленного на прерывание патогенетических реакций повреждения, можно назвать применение антигистаминных препаратов при развитии воспаления или аллергических реакций. При указанных патологических процессах образуется избыток гистамина, играющего одну из ключевых ролей в их патогенезе. Торможение синтеза и/или эффектов гистамина даёт существенный терапевтический эффект. Одновременно достижение этого эффекта предупреждает развитие и других последствий: отёка, расстройств крово- и лимфообращения, чувства боли и др. САНОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ Примером терапевтических мероприятий, направленных на активацию адаптивных процессов в организме, может быть применение комплекса иммуномодулирующих и иммуностимулирующих препаратов. Последние тормозят или предупреждают формирование иммунопатологических состояний, например, у пациентов с воспалительным или аллергическим компонентом патогенеза различных болезней (бронхиальной астмы, диффузного гломерулонефрита, хронического гепатита, ревматоидного артрита и многих других). ЗАМЕСТИТЕЛЬНАЯ ТЕРАПИЯ Важный метод реализации патогенетического принципа лечения — заместительная терапия. Она предусматривает использование агентов, ликвидирующих дефицит или отсутствие в организме какого-либо фактора или факторов. Именно с этой целью применяют препараты гормонов (у пациентов с недостаточностью самих гормонов или их эффектов, например, при СД, надпочечниковой недостаточности, гипофункции гипофиза, половых желёз), ферментов (например, желудка и кишечника при нарушении полостного или мембранного пищеварения при синдромах мальабсорбции), витаминов (при гипо- или дисвитаминозах). Эффективность лечения значительно повышается при сочетании (в тех случаях, когда для этого есть основания) этиотропного и патогенетического лечения (например, при воспалении, иммунопатологических процессах, лихорадке, гипоксиях и др.).
Эволюция живого на Земле связана с двумя фундаментальными свойствами организмов — наследственностью и изменчивостью. НАСЛЕДСТВЕННОСТЬ Наследственность — свойство организмов сохранять и обеспечивать передачу признаков потомкам, а также программировать особенности их индивидуального развития в конкретных условиях среды. Отсюда следует, что состояние здоровья и нездоровья (болезнь) являются результатом взаимодействия наследственных и средовых факторов. • Наследование — процесс передачи генетической информации о признаках — осуществляется через гаметы (в случае полового размножения) и через соматические клетки (при бесполом). • Наследуемость — доля фенотипической изменчивости, обусловленная генетическими различиями между особями. Показатель наследуемости (h2) — доля участия генетических факторов в общей (фенотипической) изменчивости признака. Обычно показатель наследуемости рассчитывают для количественных признаков: рост, масса тела, АД, ГПК и т.д. При полной генетической детерминации признака h2=1,0, при h2=0 влияние наследственности не обнаруживается. Генетика — наука, изучающая закономерности наследственности и изменчивости организмов. • Генетика человека изучает явления наследственности и изменчивости у человека на всех уровнях организации: молекулярном, хромосомном, клеточном, организменном и популяционном. • Медицинская генетика изучает роль наследственности и изменчивости в возникновении, развитии и исходах патологии человека, разрабатывает методы диагностики, лечения и профилактики наследственных и ненаследственных заболеваний. ИЗМЕНЧИВОСТЬ Изменчивость — свойство организма приобретать новые признаки и особенности индивидуального развития, отличающиеся его от родительских. Выделяют фенотипическую (или ненаследственную) и генотипическую (или наследственную) изменчивость (рис. 3-1). Новые признаки могут служить основой для эволюции вида при условии их наследования.  Рис. 3-1. Виды изменчивости. ФЕНОТИПИЧЕСКАЯ ИЗМЕНЧИВОСТЬ При фенотипической изменчивости наследственный материал не меняется: изменения касаются только признаков индивида. Они не передаются по наследству даже при длительном и/или повторном воздействии (например, обряд инициации у некоторых народов в виде нанесения повреждений: обрезание крайней плоти , перфорация носовой перегородки или губ, удаление клыков и т.д.); изменение формы грудной клетки при ношении корсетов или удалении рёбер с целью коррекции фигуры; изменение формы стопы при использовании узкой обуви и т.п.. МОДИФИКАЦИОННАЯ ИЗМЕНЧИВОСТЬ Модификационными называют такие фенотипические изменения, которые по своей выраженности не выходят за пределы диапазона нормы реакции. Наиболее выраженно модификационная изменчивость проявляется при реакциях организма на изменения факторов среды, например условий проживания в различных географических зонах, интенсивности солнечной радиации, характера питания и т.д. Модификационная изменчивость имеет адаптивное значение. ФЕНОКОПИИ Фенокопии — одно из проявлений модификационной изменчивости в ответ на действие факторов среды. Термин «фенокопия» используют для обозначения признаков, болезней, фенотипов или врождённых пороков развития (ВПР), формирующихся под воздействием определённых условий среды и фенотипически (клинически) похожих на наследственные формы патологии. Пример Микроцефалия — уменьшение размеров черепа и головного мозга, сопровождающееся умственной отсталостью и определёнными неврологическими нарушениями. Микроцефалия может быть первичной или вторичной. • Первичная (истинная, генетическая) микроцефалия характеризуется первичным недоразвитием головного мозга. • Вторичная (ложная, негенетическая) микроцефалия характеризуется ранним заращением черепных швов. В обоих случаях многие клинические проявления, методы терапии, психолого-педагогической коррекции, реабилитации и адаптации больных весьма схожи. Однако, при решении вопроса о повторном риске рождения больного ребёнка необходимо точное знание причины патологии в данной семье. ГЕНОТИПИЧЕСКАЯ ИЗМЕНЧИВОСТЬ При генотипической (или наследственной) изменчивости отклонения происходят в геноме. В зависимости от вида клеток (половые или соматические) с изменённой наследственной информацией выделяют генеративную и соматическую изменчивость. • Генеративная изменчивость характеризуется изменениями в наследственном аппарате гамет. • Соматическая изменчивость заключается в модификации наследственного материала неполовых клеток тела (соматические клетки). Генеративная и соматическая изменчивость могут быть мутационной и комбинативной. • Мутационная изменчивость определяется мутацией — устойчивым изменением генетического материала и как следствие — наследуемого признака. • Комбинативная изменчивость развивается вследствие случайной комбинации родительских аллелей в генотипе потомков. Сами гены при этом не изменяются, но генотипы родителей и детей различны. Выделяют три механизма комбинативной изменчивости. – Независимое расхождение хромосом в мейозе. – Рекомбинация генов при кроссинговере. – Случайная встреча гамет при оплодотворении. ПРЕДРАСПОЛОЖЕННОСТЬ К ЗАБОЛЕВАНИЯМ В связи с постоянным расширением территории обитания и увеличением числа факторов, влияющих на человека, возникают ситуации, когда полезные в определённых условиях сочетания конкретных нормальных генов не обеспечивают оптимальных условий функционирования организма. Это приводит к тому, что неблагоприятное сочетание «непатогенных» генов может стать основой развития болезней с наследственным предрасположением. УСТОЙЧИВОСТЬ К ЗАБОЛЕВАНИЯМ Существуют механизмы генетической изменчивости, определяющие устойчивость к некоторым заболеваниям. Так, гетерозиготное носительство серповидно-клеточного Hb (HbS) обеспечивает высокую резистентность к малярийному плазмодию (внутриклеточному паразиту эритроцитов). ЭТИОЛОГИЯ И ПАТОГЕНЕЗ НАСЛЕДСТВЕННЫХ БОЛЕЗНЕЙ Инициальным звеном патогенеза наследственных заболеваний являются мутации — нарушения структуры генов, хромосом или изменение их числа. МУТАЦИИ Термин «мутация» применяют в двух значениях — расширительном и узком. В расширительном значении термин «мутация» относят ко всему генетическому материалу (пара нуклеотидов, ген, цистрон, аллели, хромосомы, ядерный и митохондриальный геном). В узком значении термин «мутация» относят к изменениям на уровне гена (в этом случае изменения хромосом обозначают термином «аберрация»). Причинами мутаций могут быть различные факторы. Их обозначают как мутагены, а изменения, приводящие к возникновению мутаций, называют мутационным процессом (мутагенезом). В результате мутационного процесса возникают разные виды мутаций. Мутации могут быть спонтанными и индуцированными. Изменения генетического материала разнообразны (делеции, вставки и т.д.), что позволяет подразделить мутации по механизму дефекта генетического материала (типы мутаций). В зависимости от уровня организации генетического материала (ген, хромосома, геном) говорят о мутациях генных, хромосомных и геномных. МУТАГЕНЫ Мутагены (равно и вызываемые ими мутации) классифицируют по происхождению (источнику) на эндогенные и экзогенные, а по природе на физические, химические и биологические. • Экзогенные мутагены. Их большинство, к ним относятся различные и многочисленные факторы внешней среды (например, радиационное излучение, алкилирующие агенты, окислители, многие вирусы). • Эндогенные мутагены образуются в процессе жизнедеятельности организма (например, мутации могут возникать под влиянием свободных радикалов, продуктов липопероксидации). • Физические мутагены — ионизирующее излучение и температурный фактор – ионизирующее излучение (например, – радиоактивные элементы (например, радий, радон, изотопы калия, углерода и т.д. — источники ионизирующего излучения); – УФизлучение; – чрезмерно высокая или низкая температура. • Химические мутагены — самая многочисленная группа мутагенов. К химическим мутагенам относятся: – сильные окислители или восстановители (например, нитраты, нитриты, активные формы кислорода); – алкилирующие агенты (например, йодацетамид); – пестициды (например, гербициды, фунгициды); – некоторые пищевые добавки (например, ароматические углеводороды, цикламаты); – продукты переработки нефти; – органические растворители; – ЛС (например, цитостатики, содержащие ртуть средства, иммунодепрессанты); – другие химические соединения. • Биологические мутагены: – вирусы (например, кори, краснухи, гриппа); – Аг некоторых микроорганизмов. ВИДЫ МУТАЦИЙ Различные группы видов мутаций приведены на рис. 3-2. 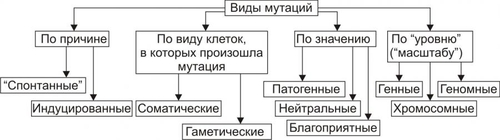 Рис. 3-2. Виды мутаций. • Спонтанные мутации возникают под влиянием естественных мутагенов экзо- или эндогенного происхождения, без специального (целенаправленного) вмешательства человека. Спонтанные мутации возникают, например, в результате действия химических веществ, образующихся в процессе метаболизма; воздействия естественного фона радиации или УФ-излучения; ошибок репликации и т.д. • Индуцированные мутации вызваны направленным воздействием факторов внешней или внутренней среды. Индуцированный мутационный процесс может быть контролируемым и неконтролируемым. – Контролируемые мутации возникают, например, в эксперименте с целью изучения механизмов мутагенеза и/или его последствий. – Неконтролируемые мутации, например при случайном выбросе радиоактивных элементов в среду обитания. • Гаметические мутации — мутации в половых клетках. Они наследуются потомками и, как правило, обнаруживаются во всех клетках организма. • Соматические мутации — мутации в неполовых (соматических) клетках — проявляются у того индивида, у которого они возникают. Они передаются при делении только дочерним соматическим клеткам и не наследуются следующим поколением индивида. Мозаики. Если соматическая мутация возникает на ранних стадиях дробления зиготы (но не первого деления) возникают клеточные линии с различными генотипами. Чем раньше в онтогенезе происходит соматическая мутация, тем больше клеток содержит данную мутацию. Подобные организмы получили название мозаичных. У человека мозаицизм наиболее характерен для половых хромосом. • Патогенные мутации приводят к гибели эмбриона (или плода) и к развитию наследственных и врождённых заболеваний. • Нейтральные мутации обычно не влияют на жизнедеятельность организма (например, мутации, вызывающие веснушки, изменение цвета волос, радужной оболочки глаза). • Благоприятные мутации повышают жизнеспособность организма или вида (например, тёмная окраска кожных покровов у жителей африканского континента). • Генные (точковые) мутации — любые изменения молекулярной структуры ДНК. Некоторые мутации не оказывают влияния на функцию соответствующего полипептида (например, замена нуклеотидов, не приводящая к замене аминокислоты в силу вырождённости генетического кода). Значительная часть точковых мутаций нарушает функционирование гена и приводит к развитию генных (моногенных) болезней. Фенотипически генные болезни проявляются признаками нарушений метаболизма (например, фенилкетонурия, нейрофиброматоз, муковисцидоз, мышечная дистрофия Дюшенна–Беккера). ГЕННЫЕ МУТАЦИИ По характеру изменений в составе гена различают следующие типы мутаций (рис. 3-3): 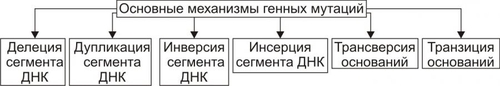 Рис. 3-3. Механизмы генных мутаций. • Делеции — утрата сегмента ДНК размером от одного нуклеотида до гена. • Дупликации — удвоение или повторное дублирование сегмента ДНК от одного нуклеотида до целых генов. • Инверсии — поворот на 180° сегмента ДНК размером от двух нуклеотидов до фрагмента, включающего несколько генов. • Инсерции — вставка фрагментов ДНК размером от одного нуклеотида до целого гена. • Трансверсии — замена пуринового основания на пиримидиновое или наоборот в одном из кодонов. • Транзиции — замена одного пуринового основания на другое пуриновое или одного пиримидинового на другое в структуре кодона. По последствиям генных мутаций их классифицируют на нейтральные, регуляторные и динамические, а также на миссенс- и нонсенс-мутации. • Нейтральная мутации (молчащая мутация) — мутация не имеет фенотипического выражения (например, в результате вырождённости генетического кода). • Миссенс-мутация — замена нуклеотида в кодирующей части гена — приводит к замене аминокислоты в полипептиде. • Нонсенс-мутация — замена нуклеотида в кодирующей части гена — приводит к образованию кодона-терминатора (стоп-кодона) и прекращению трансляции. • Регуляторная мутация — мутация в 5′- или 3′-нетранслируемых областях гена, такая мутация нарушает экспрессию гена. • Динамические мутации — мутации, обусловленные увеличением числа тринуклеотидных повторов в функционально значимых частях гена. Такие мутации могут привести к торможению или блокаде транскрипции, приобретению белковыми молекулами свойств, нарушающих их нормальный метаболизм. ХРОМОСОМНЫЕ АБЕРРАЦИИ Хромосомные мутации (аберрации) характеризуются изменением структуры отдельных хромосом. При них последовательность нуклеотидов в генах обычно не меняется, но изменение числа или положения генов при аберрациях может привести к генетическому дисбалансу, что пагубно сказывается на нормальном развитии организма. Виды аберраций и их механизмы представлены на рис. 3-4. 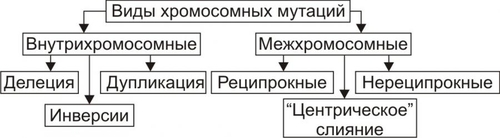 Рис. 3-4. Виды хромосомных мутаций. Различают внутрихромосомные, межхромосомные и изохромосомные аберрации. • Внутрихромосомные аберрации — аберрации в пределах одной хромосомы. К ним относят делеции, инверсии и дупликации. – Делеция — утрата одного из участков хромосомы (внутреннего или терминального), что может стать причиной нарушения эмбриогенеза и формирования множественных аномалий развития (например, делеция в регионе короткого плеча хромосомы 5, обозначаемая как 5р–, приводит к недоразвитию гортани, ВПР сердца, отставанию умственного развития). Этот симптомокомплекс обозначен как синдром кошачьего крика, поскольку у больных детей из-за аномалии гортани плач напоминает кошачье мяуканье. – Инверсия — встраивание фрагмента хромосомы на прежнее место после поворота на 180 °. В результате нарушается порядок расположения генов. – Дупликация — удвоение (или умножение) какого-либо участка хромосомы (например, трисомия по короткому плечу хромосомы 9 приводит к появлению множественных ВПР, включая микроцефалию, задержку физического, психического и интеллектуального развития). • Межхромосомные аберрации — обмен фрагментами между негомологичными хромосомами. Они получили название транслокаций. Различают три варианта транслокаций: реципрокные (обмен фрагментами двух хромосом), нереципрокные (перенос фрагмента одной хромосомы на другую), робертсоновские (соединение двух акроцентрических хромосом в районе их центромер с потерей коротких плеч, в результате образуется одна метацентрическая хромосома вместо двух акроцентрических). • Изохромосомные аберрации — образование одинаковых, но зеркальных фрагментов двух разных хромосом, содержащих одни и те же наборы генов. Это происходит в результате поперечного разрыва хроматид через центромеры (отсюда другое название — центрическое соединение). ИЗМЕНЕНИЯ ГЕНОМА Геномные мутации (рис. 3-5) характеризуются изменением числа хромосом. У человека известны полиплоидия (в том числе тетраплоидия и триплоидия) и анеуплоидия.  Рис. 3-5. Виды геномных мутаций. • Полиплоидия — увеличение числа наборов хромосом, кратное гаплоидному (3n, 4n, 5n и т.д.). Причины: двойное оплодотворение и отсутствие первого мейотического деления. У человека полиплоидия, а также большинство анеуплоидий приводят к формированию леталей. • Анеуплоидия — изменение (уменьшение — моносомия, увеличение — трисомия) числа хромосом в диплоидном наборе, т.е. не кратное гаплоидному (2n+1, 2n–1 и т.д.). Механизмы возникновения: нерасхождение хромосом (хромосомы в анафазе отходят к одному полюсу, при этом на каждую гамету с одной лишней хромосомой приходится другая — без одной хромосомы) и «анафазное отставание» (в анафазе одна из передвигаемых хромосом отстаёт от всех других). – Трисомия — наличие трёх гомологичных хромосом в кариотипе (например, по 21-й паре, что приводит к развитию синдрома Дауна; по 18-й паре — синдрома Эдвардса; по 13-й паре — синдрома Патау). – Моносомия — наличие только одной из двух гомологичных хромосом. При моносомии по любой из аутосом нормальное развитие эмбриона невозможно. Единственная совместимая с жизнью моносомия у человека — по хромосоме X — приводит к развитию синдрома Шерешевского–Тёрнера (45,Х0). ВИДЫ БОЛЕЗНЕЙ, ВЫЗЫВАЕМЫХ ИЗМЕНЕНИЯМИ В ГЕНОМЕ Подходы к дифференцировке видов болезней, вызываемых изменениями в геноме, приведены на рис. 3-6. Основные критерии классификации: вид мутантных клеток, вклад наследственных факторов и среды. 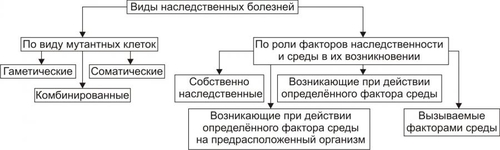 Рис. 3-6. Виды болезней, вызаваемых изменениями в геноме. В зависимости от вида первично поражённых клеток выделяют следующие группы заболеваний: • болезни вследствие мутаций в половых клетках — «гаметические», т.е. собственно наследственные болезни (например, фенилкетонурия, гемофилии); эти болезни передаются по наследству; • болезни вследствие мутаций в соматических клетках — «соматические» (например, опухоли, некоторые болезни иммунной аутоагрессии). Эти заболевания не передаются по наследству; • болезни вследствие комбинации мутаций в половых и соматических клетках (например, семейная ретинобластома). Отдельно рассматривают летальные, сублетальные и гипогенитальные болезни. • летальные болезни характеризуются гибелью индивида во время внутриутробного развития (например, при моносомии по аутосомам, гаплоидии, большинстве полиплоидий); • сублетальные заболевания завершаются гибелью индивида до периода полового созревания и возможности иметь потомство (например, наследственные иммунодефициты типа агаммаглобулинемии швейцарского типа, синдром ЛуиБар, некоторые гемофилии); • гипогенитальные заболевания сочетаются с бесплодием (например, синдромы Шерешевского–Тёрнера, Кляйнфелтера). В зависимости от роли наследственности и среды в возникновении заболеваний выделяют четыре их группы: • собственно наследственные болезни (являются вследствие мутаций); • экогенетические заболевания (развиваются вследствие мутаций под влиянием специфического фактора среды); • болезни генетической предрасположенности (вклад генетических изменений как факторов риска очевиден); • болезни, вызываемые факторами внешней среды (строго говоря, эта группа болезней не относится к наследственным болезням, так как вклад генетических факторов в их возникновение, развитие и исход может быть крайне малым, сомнительным или неизвестным). СОБСТВЕННО НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ Причина: мутации в гаметах (генные, хромосомные, геномные). Характеризуются относительно высокой пенетрантностью мутантного гена. Условия: факторы внешней среды не влияют на их возникновение, но могут модифицировать их клиническое течение. Примеры: моногенные (фенилкетонурия, гемофилии A и B, мукополисахаридозы, галактоземия, гемоглобинопатии) и хромосомные болезни (синдром Дауна, синдромы Шерешевского–Тёрнера, Кляйнфелтера, трисомии X). ЭКОГЕНЕТИЧЕСКИЕ ЗАБОЛЕВАНИЯ Экогенетические заболевания возникают при действии на организм только определённого (специфического) фактора среды. Причина: мутации (генные). Необходимое условие: действие на организм специфического фактора внешней среды. Примеры: анемия у индивидов, гетерозиготных по HbS при снижении pO2 во вдыхаемом воздухе; постанестетическое апноэ под влиянием суксаметония из группы деполяризующих миорелаксантов периферического действия; гемолиз эритроцитов при приёме сульфаниламидов (при дефекте глюкозо-6-фосфатдегидрогеназы). БОЛЕЗНИ ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТИ (МНОГОФАКТОРНЫЕ ЗАБОЛЕВАНИЯ) Эти заболевания развиваются под действием только факторов внешней среды на организм, предрасположенный к этим заболеваниям. Причина: фактор внешней среды, или чаще, комплекс этих факторов. Необходимое условие: генетически детерминированная предрасположенность индивида. Степень предрасположенности может быть у различных индивидов разной: слабой, умеренной или высокой. В связи с множеством факторов, вносящих вклад в развитие заболевания, эти болезни называют также многофакторными. Примеры: ИБС, гипертоническая болезнь, СД, псориаз, шизофрения, язвенная болезнь желудка. БОЛЕЗНИ, ВЫЗЫВАЕМЫЕ ФАКТОРАМИ СРЕДЫ Причины: факторы внешней и внутренней среды (инфекционные и неинфекционные; физической, химической и биологической природы). Генетические факторы непосредственно не влияют на возникновение болезни, но определяют особенности её течения (возможность осложнений, выраженность адаптивных реакций, степень резистентности организма, эффективность лечения и др.). Примеры: большинство инфБ, многие травмы и посттравматические состояния; болезни, вызванные химическими агентами, в том числе ЛС. НАСЛЕДСТВЕННЫЕ ФОРМЫ ПАТОЛОГИИ Наследственные заболевания передаются от родителей потомкам посредством половых клеток. Ниже приводится характеристика генных и хромосомных болезней, заболеваний с наследственным предрасположением, врождённых пороков развития (ВПР), методов диагностики наследственных заболеваний, а также принципов их терапии и профилактики. ГЕННЫЕ БОЛЕЗНИ В Каталоге наследственных заболеваний человека (OMIM, Online Mendelian Inheritance in Man |
