Патфиз ч.1. Патфиз ч. Гл. 1 Введение в предмет Гл. 2 Общая нозология
 Скачать 9.21 Mb. Скачать 9.21 Mb.
|
|
Клетка — основной гистологический элемент организма. В процессе ее пролиферации, роста, дифференцировки (специализации), функционирования и приспособления к меняющимся условиям среды в ней реализуется генетическая информация, обмен веществ и энергии, синтезируются биологически активные вещества, компоненты ее структур и интерстиция. Клетка прямо или опосредованно (совместно с другими гистологическими элементами) участвует в выполнении функций организма.
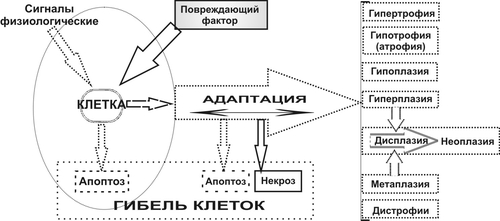 Гомеостаз, адаптация и типовые формы патологии клеток. Слева в овале — границы нормы. Существенное свойство типовых патологических процессов — их обратимость. Если степень повреждения выходит за пределы адаптивных возможностей, процесс становится необратимым (примеры — некроз, апоптоз, дисплазия, опухолевый рост — неоплазия). Учение о повреждении клетки имеет особое значение в патологии. Это определяется, по меньшей мере, тремя обстоятельствами: • Данное учение тесно связано с разработкой проблем нозологии: вопросов возникновения, развития и прогнозирования исходов болезней, поскольку любая болезнь сопровождается повреждением клетки. • Интенсивное внедрение в клиническую практику различных способов восстановления жизнедеятельности повреждённых органов и тканей (в том числе с использованием стволовых клеток и тканевых фрагментов) ставит задачи по исследованию механизмов устранения или уменьшения степени их альтерации, а также по разработке методов активации адаптивных реакций в клетках с целью оптимизации процесса выздоровления. • Понимание многих открытий молекулярной патологии становится возможным при условии определения их места и значения с позиций патологии клетки и межклеточных взаимодействий. В учении о повреждении клетки выделяют три раздела: • патология клетки в целом; • патология отдельных субклеточных структур и компонентов; • патология межклеточного взаимодействия и кооперации. ПРИЧИНЫ ПОВРЕЖДЕНИЯ КЛЕТКИ Повреждение клетки — результат воздействия на неё множества патогенных агентов. Причины повреждения клетки классифицируют по природе патогенных факторов, их происхождению и эффектам. Природа повреждающего фактора может быть физической, химической и биологической (рис. 4–1).  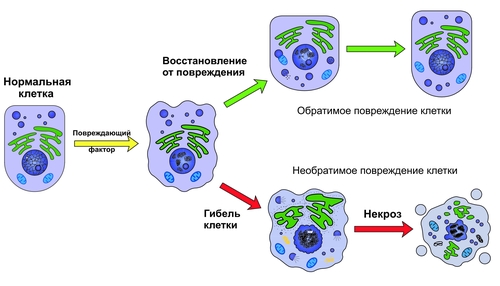 Рис. 4–1. Причины повреждения клеток. ФИЗИЧЕСКИЕ ФАКТОРЫ ПОВРЕЖДЕНИЯ Наиболее частыми причинами повреждения клетки физической природы являются механические, температурные, осмотические, свободнорадикальные (избыток свободных радикалов и продуктов активации липопероксидных процессов повреждают мембраны и денатурируют белки). Патогенное действие на клетку могут оказывать также ионизирующая радиация, электромагнитные факторы и другие агенты физического характера. МЕХАНИЧЕСКИЕ ВОЗДЕЙСТВИЯ К механически повреждающим факторам относятся удары, растяжения (например, при перерастяжении мышечной ткани или органов), сдавление (в частности, опухолью, гематомой, рубцом, экссудатом), гравитационные перегрузки и др. КОЛЕБАНИЯ ТЕМПЕРАТУРЫ Повышение температуры среды, окружающей клетку, до 40–50 °C и выше может привести к денатурации белка, нуклеиновых кислот, декомпозиции ЛП, повышению проницаемости клеточных мембран и другим изменениям. Значительное снижение температуры существенно замедляет или прекращает внутриклеточные метаболические процессы и может привести к кристаллизации внутриклеточной жидкости и разрывам мембран, что означает гибель клетки. ИЗМЕНЕНИЯ ОСМОТИЧЕСКОГО ДАВЛЕНИЯ Гиперосмия может развиться вследствие накопления в клетке продуктов неполного окисления органических субстратов или избытка ионов. Последнее, как правило, сопровождается поступлением в клетку воды по градиенту осмотического и онкотического давления, набуханием клетки и растяжением (вплоть до разрыва) плазмолеммы и мембран органелл. Снижение внутриклеточного осмотического давления или повышение его во внеклеточной среде приводит к потере клеточной жидкости, сморщиванию (пикнозу) и нередко — к гибели клетки. ХИМИЧЕСКИЕ ФАКТОРЫ ПОВРЕЖДЕНИЯ К ним относятся органические и неорганические кислоты и щёлочи, соли тяжёлых металлов, цитотоксические соединения и многие ЛС. Повреждение клетки может возникать как при избытке, так и при дефиците одного и того же агента. Например, избыточное содержание кислорода в тканях активирует процесс свободнорадикального перекисного окисления липидов (СПОЛ), продукты которого необратимо повреждают ферменты и мембраны клеток; с другой стороны, снижение содержания кислорода приводит к нарушениям окислительных процессов, понижению образования АТФ и как следствие — к расстройствам функций клетки. ЦИТОТОКСИЧЕСКИЕ СОЕДИНЕНИЯ Классические примеры цитотоксических соединений — ингибиторы ферментов. Так, цианиды подавляют активность цитохромоксидазы; этанол и его метаболиты ингибируют многие ферменты клетки; вещества, содержащие соли мышьяка, угнетают пируватоксидазу. ЛЕКАРСТВЕННЫЕ СРЕДСТВА Неправильное применение ЛС (чаще в виде передозировки) может привести к повреждению клеток. Строфантин подавляет активность мембранной Na+,K+АТФазы кардиомиоцитов, но его передозировка ведёт к дисбалансу внутриклеточного содержания ионов и воды. Инсулин обеспечивает утилизацию клеткой глюкозы, но его передозировка может вызвать истощение запасов гликогена и ухудшить энергетическое обеспечение клетки. БИОЛОГИЧЕСКИЕ ФАКТОРЫ ПОВРЕЖДЕНИЯ К ним относят главным образом инфекционные агенты и цитотоксические факторы системы ИБН. ИНФЕКЦИОННЫЕ АГЕНТЫ Инфекционные агенты (вирусы, риккетсии, микробы, гельминты, грибы, прионы) как сами по себе, так и в виде продуктов их жизнедеятельности или деградации вызывают расстройства функций клетки, нарушают течение в ней метаболических реакций, проницаемость или даже целостность мембран, подавляют активность клеточных ферментов. ЦИТОТОКСИЧЕСКИЕ ФАКТОРЫ К цитотоксическим факторам относятся эндо- и экзотоксины, аутоагрессивные T-лимфоциты, в ряде случаев — АТ (например, при явлениях молекулярной мимикрии). Эндо и экзотоксины, а также структурные компоненты бактерий, вирусов и паразитов могут изменять антигенный состав клетки. Это приводит к появлению АТ или иммунных T-лимфоцитов, повреждающих клетки организма. В результате этого могут развиться иммунопатологические процессы (аллергия, патологическая толерантность, состояния иммунной аутоагрессии). ПРОИСХОЖДЕНИЕ ПОВРЕЖДАЮЩИХ ФАКТОРОВ Причины повреждения клеток классифицируют в зависимости от их происхождения на экзогенные или эндогенные, инфекционные или неинфекционные. ЭКЗОГЕННЫЕ ФАКТОРЫ Экзогенными факторами повреждения являются физические воздействия (механические травмы, электрический ток, тепло, холод), химические агенты (кислоты, щёлочи, этанол, сильные окислители) и биологические факторы (вирусы, риккетсии, бактерии, гельминты и др.). ЭНДОГЕННЫЕ ФАКТОРЫ К эндогенным факторам повреждения относятся агенты физической природы (например, избыток в клетке или во внеклеточной среде свободных радикалов, значительные колебания осмотического давления), химические факторы (например, накопление или дефицит ионов [Н+, K+, Ca2+ и др.], кислорода, углекислого газа, перекисных соединений органических и неорганических веществ, метаболитов и др.), факторы биологической природы (например, дефицит или избыток гормонов, ферментов, Пг и др.; агенты, высвобождающиеся из повреждённых или погибших клеток: ионы, лизосомальные ферменты, метаболиты, а также цитотоксические факторы системы ИБН). ИНФЕКЦИОННОПАРАЗИТАРНЫЕ ФАКТОРЫ Примерами инфекционнопаразитарных факторов могут быть эндо и экзотоксины микроорганизмов, много и одноклеточные паразиты. ФАКТОРЫ НЕИНФЕКЦИОННОГО ГЕНЕЗА К факторам неинфекционного генеза относятся агенты физической, химической или биологической (но неинфекционной) природы. ЭФФЕКТЫ ПОВРЕЖДАЮЩИХ ФАКТОРОВ Действие повреждающих факторов на клетки осуществляется прямо (первичные факторы повреждения) или опосредованно. В последнем случае речь идет о формировании цепи вторичных, нередко многоступенчатых, реакций, реализующих повреждающее влияние первичных патогенных факторов. Примеры: • изменения нервных или эндокринных воздействий на клетки и как следствие — эффектов нейромедиаторов и гормонов (например, при стрессе, шоке); • нарушения системного кровообращения (при сердечной недостаточности); • отклонения физикохимических параметров (например, при состояниях, сопровождающихся ацидозом, алкалозом, образованием свободных радикалов, продуктов СПОЛ, дисбалансом ионов и воды). • развитие иммунных и аллергических реакций; • образование избытка или недостаток БАВ (например, факторов системы комплемента, гистамина, кининов, Пг, циклических нуклеотидов). Эффект повреждающего фактора может быть обратимым или необратимым. Признаки обратимого и необратимого повреждения. [по 4]. МЕДИАТОРЫ ПОВРЕЖДЕНИЯ Многие из вышеперечисленных агентов или воздействий, участвующих в развитии различных форм патологии клетки, получили название посредников — медиаторов повреждения. Примерами могут служить медиаторы воспаления, аллергии, канцерогенеза, лихорадки. ОБЩИЕ МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ Патогенные агенты приводят к нарушению функций клеток. В табл. 4–1 приводятся наиболее важные механизмы клеточной альтерации. Таблица 4–1. Основные механизмы повреждения клетки
РАССТРОЙСТВА ЭНЕРГЕТИЧЕСКОГО ОБЕСПЕЧЕНИЯ КЛЕТКИ Энергетическое обеспечение клеток осуществляется за счёт АТФ, образующейся преимущественно в процессе окислительного фосфоридирования в митохондриях и в меньшей мере — в реакциях гликолиза в цитозоле. Энергоснабжение клетки может расстраиваться на этапах ресинтеза, транспорта и утилизации энергии АТФ (рис. 4–2). 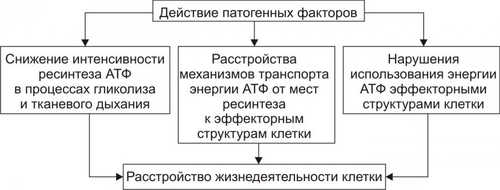 Рис. 4–2. Механизмы нарушения энергообеспечения в повреждённой клетке. НАРУШЕНИЯ РЕСИНТЕЗА АТФ Ресинтез АТФ нарушается в результате дефицита кислорода и/или субстратов метаболизма, снижения активности ферментов тканевого дыхания и гликолиза, повреждения и разрушения митохондрий, в которых осуществляются реакции цикла Кребса и перенос электронов к молекулярному кислороду, сопряжённый с фосфорилированием АДФ. РАССТРОЙСТВА ТРАНСПОРТА ЭНЕРГИИ Заключённая в макроэргических связях энергия АТФ в норме доставляется от мест ресинтеза — митохондрий и цитозоля — к эффекторным структурам (миофибриллам, мембранным ионным насосам и др.) с помощью АДФАТФтранслоказы (адениннуклеотидилтрансферазы) и КФК. Адениннуклеотидилтрансфераза обеспечивает транспорт энергии макроэргической фосфатной связи АТФ из матрикса митохондрий через их внутреннюю мембрану, а КФК переносит её далее на креатин с образованием креатинфосфата, который поступает в цитозоль (рис. 4–3). КФК эффекторных клеточных структур транспортирует фосфатную группу креатинфосфата на АДФ с образованием АТФ, который и используется в процессах жизнедеятельности клетки. 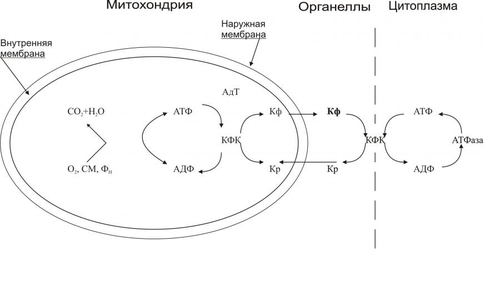 Рис. 4–3. Механизм транспорта энергии АТФ в клетке. АдТ — адениннуклеотидилтрансфераза; Кр — креатин; Кф — креатинфосфат; СМ — субстраты метаболизма; ФН — фосфат неорганический. Системы транспорта энергии могут быть повреждены различными патогенными агентами, в связи с чем (даже на фоне высокого общего содержания АТФ в клетке) может развиваться дефицит АТФ в энергорасходующих структурах. РАССТРОЙСТВО МЕХАНИЗМОВ ИСПОЛЬЗОВАНИЯ ЭНЕРГИИ Нарушения энергообеспечения клеток и расстройства их жизнедеятельности могут развиваться в результате повреждения механизмов утилизации энергии, главным образом за счёт уменьшения активности АТФаз (АТФаза миозина, Na+,K+АТФаза плазмолеммы, протонная и калиевая АТФаза, Са2+АТФаза [Са2+насос] и др.). Следовательно, расстройство жизнедеятельности клеток может развиваться даже в условиях нормального или повышенного содержания в клетке АТФ. Нарушение энергообеспечения, в свою очередь, может стать одним из факторов расстройств функции мембранного аппарата клеток, их ферментных систем, процессов транспорта ионов и воды, а также механизмов регуляции клетки. ПОВРЕЖДЕНИЕ МЕМБРАН И ФЕРМЕНТОВ Повреждение клеточных мембран и ферментов играет существенную роль в расстройстве жизнедеятельности клетки, а также — что особенно важно — в переходе обратимых изменений в ней в необратимые. Согласно жидкостно-мозаичной модели, мембрана клетки — жидкая динамическая система с мозаичным расположением белков и липидов. Основу мембраны составляют молекулы фосфолипидов (липидная фаза), полярные (ионные) «головки» которых направлены к водной среде, т.е. к гидрофильным поверхностям мембраны (гидрофильная зона), а неполярные части — «хвосты» — внутрь мембраны (гидрофобная зона). В фосфолипидной среде «взвешены» белковые молекулы, часть из которых полностью погружена в мембрану и пронизывает их толщу (так называемые интегральные белки), а часть расположена поверхностно (периферические белки). Периферические белки не проникают в толщу мембраны и удерживаются на её поверхности главным образом электростатическими силами. В плоскости мембраны белки обладают латеральной подвижностью. Интегральные белки перераспределяются в мембранах в результате взаимодействия с периферическими белками, элементами цитоскелета, молекулами в мембране соседней клетки и компонентами внеклеточного матрикса. В то же время подвижность интегральных белков в мембране ограничена вследствие их взаимодействия с периферическими белками и элементами цитоскелета, а также гидрофобного связывания с липидами. Для белков–ферментов эти обстоятельства влияют на интенсивность и характер протекания катализируемых ими реакций. Кроме того, липиды мембран обеспечивают оптимальные условия для энзиматических процессов. Например, окислительное фосфорилирование требует безводной среды, что предотвращает спонтанный гидролиз АТФ. Основные механизмы повреждения клеточных мембран приведены на рис. 4–4. Все указанные механизмы прямо или опосредованно ведут к повреждению, изменению конформации и/или кинетических свойств ферментов, многие из которых связаны с мембранами. 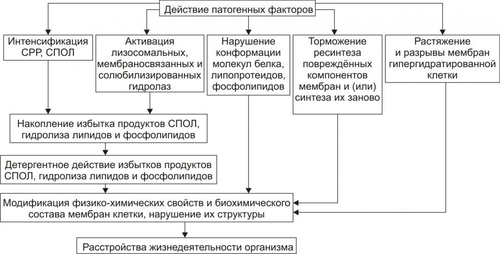 Рис. 4–4. Механизмы повреждения мембран клеток. СРР — свободнорадикальная реакция. СВОБОДНОРАДИКАЛЬНЫЕ РЕАКЦИИ Свободнорадикальные процессы и реакции СПОЛ — необходимое звено таких жизненно важных процессов, как транспорт электронов в цепи дыхательных ферментов, синтез Пг и лейкотриенов, пролиферация и дифференцировка клеток, фагоцитоз, метаболизм катехоламинов и др. В реакции СПОЛ могут вовлекаться белки, нуклеиновые кислоты, липиды, в особенности фосфолипиды. СПОЛ важна для регуляции липидного состава биомембран и активности ферментов. Последнее является результатом как прямого действия продуктов липопероксидных реакций на ферменты, так и опосредованного — через изменение состояния мембран, с которыми ассоциированы молекулы многих ферментов. |
