Интенсивная терапия заболеваний, сопровождающаясянарушением кровообращения
 Скачать 300.68 Kb. Скачать 300.68 Kb.
|
|
I. Тема занятия. ИНТЕНСИВНАЯ ТЕРАПИЯ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩАЯСЯНАРУШЕНИЕМ КРОВООБРАЩЕНИЯ II. Время занятий. 1. Введение. Обоснование важности и актуальности темы - 10 мин.
4. Отработка практических навыков в операционной и палатах ИТАР – 60 мин.. 5. Разбор протоколов наблюдения пациентов, чтение рефератов, решение ситуационных задач – 85 мин. 6. Заключительный контроль знаний и навыков-30мин. 7. Подведение итогов, задание на следующее занятие-10 мин.
Заболевания сердечно-сосудистой системы занимают первое место среди причин смерти пациентов. Сложность анатомо-физиологического строения системы кровообращения и нервно-рефлекторных механизмов компенсации, создает значительные трудности в трактовке причинно-следственных отношений в патогенезе и развитии клинической картины острых расстройств гемодинамики, в связи с чем практически отсутствует их патогенетически обоснованная классификация. Возникновение нарушения в одном из элементов системы сопровождается изменением функции всей системы гемодинамики, однако необходимость выбора патогенетической терапии требует выделения ведущего фактора. Функционально система кровообращения делится на систему макроциркуляции (сердце, сосуды, объем циркулирующей крови), которая обеспечивает транспортную функцию крови и систему микроциркуляции, влияющую на распределение сердечного выброса между органами и тканями и распределение кровотока внутри органов, таким образом выполняя главную функцию живого организма - обмен веществ. Нормальная деятельность всей системы в целом определяется взаимодействием ее составляющих (систем макро- и микроциркуляции) и влиянием на нее центральной и вегетативной нервной систем, гормональных и метаболических сдвигов. Понимание основных патофизиологических механизмов нарушений в такой сложной системе, как система кровообращения, поможет практическому врачу найти патогенетически обоснованные пути ее коррекции.
Закрепить полученные ранее знания по физиологии системы кровообращения, изучить основные патофизиологические механизмы нарушений в этой системе и патогенетически обоснованные методы их коррекции. Научить студентов понимать патофизиологические механизмы развития и течения шока, диагностировать, дифференцировать и принципиально определять тактику интенсивной терапии данного состояния в клинике. V. Задачи занятия СТУДЕНТ ДОЛЖЕН ЗНАТЬ:
СТУДЕНТ ДОЛЖЕН УМЕТЬ:
ПРАКТИЧЕСКИЕ НАВЫКИ:
VI. Требования к исходному уровню знаний:
VII. Контрольные вопросы из смежных дисциплин 1. Патогенез нарушений преднагрузки и водно-солевого обмена как причин и следствий острой сердечной недостаточности. 2. Патологические сдвиги постнагрузки как звено патогенеза острой сердечной недостаточности. 3. Патофизиология нарушений сократительной способности сердца у пациентов с острой сердечной недостаточностью. 6. Патогенез острой левожелудочковой недостаточности как причины кардиогенного отека легких. 7. Принципы терапии кардиогенного отека легких. VIII. Контрольные вопросы по теме занятия.
IX. Учебный комплекс ФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ В клинико-физиологическом аспекте систему кровообращения целесообразно рассматривать состоящей из ряда функциональных отделов: 1. Сердечный насос – главный механизм циркуляции. 2. Сосуды-буферы или артерии (некоторые авторы называют их иначе – сосуды "котла", подразумевая под ними аорту и крупные артерии) – выполняют преимущественно пассивную транспортную функцию посредника между насосом и системой микроциркуляции. 3. Сосуды-емкости, или вены, также выполняют транспортную функцию возврата крови к сердцу. Это более активная, чем артерии, часть системы кровообращения, поскольку вены способны изменять свой объем в десятки раз, активно участвуя в регуляции венозного возврата и объема циркулирующей крови. 4. Сосуды сопротивления, артериолы и венулы, включая сфинктеры, регулирующие кровоток через капилляры и являющиеся главным физиологическим средством распределения сердечного выброса по органам и тканям, в связи с чем их называют сосудами распределения. 5.Сосуды обмена – капилляры, присоединяющие систему кровообращения к общему сокообращению организма. 6. Сосуды-шунты – артерио-венозные анастомозы, регулирующие периферическое сопротивление при спазме артериол прекапиллярного и посткапиллярного сфинктеров, сокращением кровотока через капилляры. Три первые функциональные части кровообращения (сердечный насос, сосуды-буферы и сосуды-емкости) образуют систему макроциркуляции - хорошо зримую и потому кажущуюся самой главной в кровообращении организма. Но, на самом деле, в клинико-физиологическом аспекте гораздо важнее знать о состоянии системы микроциркуляции, состоящей из трех последних разделов схемы (сосуды сопротивления, сосуды обмена и шунты). Система микроциркуляции важнее для изучения патофизиологии кровообращения, потому что она поражается при критическом состоянии любой этиологии, тогда как система макроциркуляции – при первичной патологии самих органов кровообращения, а при критических состояниях она страдает вторично из-за поражения системы микроциркуляции. Главная функциональная цель системы макроциркуляции – обеспечить движение и транспорт крови. Задача микроциркуляции – присоединить систему кровообращения к общему сокообращению организма и распределить сердечный выброс между разными органами соответственно их потребности. Основные гемодинамические параметры и их соотношения Представления современной физиологии об основных параметрах кровообращения, опреде ляющих их факторах и соотношениях между ними в общем виде представлены на схеме 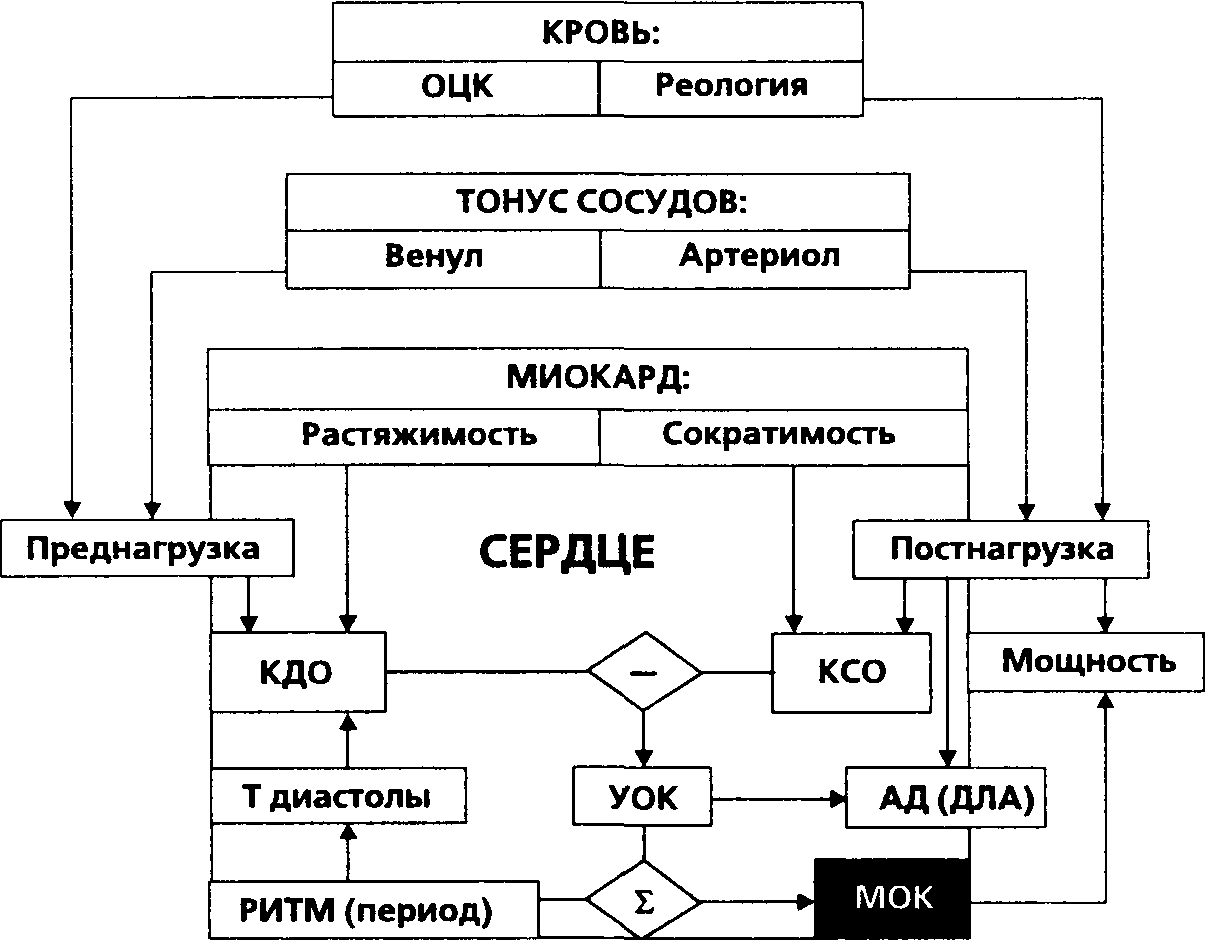 Основные показатели кровообращения и их физиологические колебания
Работа капиллярной сети здесь, возможно, даже более интенсивная, чем в большом круге кровообращения. Распределение потока зависит от силы тяжести, внутриплеврального давления, парциального давления кислорода, рН и других факторов (Marini JJ., Wheeler А.Р., 1997). Параметры центральной гемодинамики. Основными факторами, характеризующими состояние кровообращения и его эффективность, являются MOC, ОПСС и ОЦК. Эти факторы взаимообусловлены и взаимосвязаны. Измерение только АД и частоты пульса не может дать полного представления о состоянии кровообращения. Определение MOC, ОЦК, ЦВД, ДЗЛА и вычисление некоторых косвенных показателей позволяют получить необходимую информацию. Минутный объем сердца (сердечный выброс). MOC определяется объемом крови, которая выбрасывается левым желудочком в 1 мин. CB, определяемый с помощью многих методик, составляет 5—7 л/мин. В здоровом организме основным регуляторным фактором MOC являются периферические сосуды. Спазм и расширение артериол определяют динамику артериального кровообращения, регионарного и органного кровоснабжения. Венозный тонус, изменяя емкость венозной системы, обеспечивает возврат крови к сердцу (Гайтон А., 1977). При заболеваниях сердца или его функциональной перегрузке MOC практически полностью зависит от эффективности работы сердца как насоса, т.е. функциональной способности миокарда. Способность к увеличению сердечного выброса в ответ на повышение потребности тканей в кровоснабжении называется сердечным резервом. У взрослых здоровых людей он равен 300—400 % и значительно снижается при различных заболеваниях сердца. В регуляции CB основную роль играют закон Франка—Старлинга и нервно-вегетативная регуляция силы и частоты сердечных сокращений. Указанный закон отражает способность сердца увеличивать силу сокращения при увеличении наполнения его камер. Согласно этому закону, сердце перекачивает количество крови, равное венозному притоку без значительного изменения ЦВД. В целостном организме нервно-рефлекторные механизмы делают регуляцию кровообращения более тонкой и надежной, непрерывно приспосабливаясь к изменениям внутренней и внешней среды. Энергия, необходимая для сокращения миокарда, образуется при достаточном поступлении кислорода в клетки. Коронарный кровоток обеспечивает кровоснабжение миокарда в соответствии с потребностями сердечной деятельности. В норме он составляет 5 % CB, в среднем 250— 300 мл/мин. Наполнение коронарных артерий пропорционально среднему давлению в аорте. Коронарный кровоток возрастает при уменьшении насыщения крови кислородом, при увеличении концентрации углекислоты и адреналина в крови. В условиях стресса CB и коронарный кровоток увеличиваются пропорционально. При значительной физической нагрузке CB может достигать 37—40 л/мин, коронарный кровоток — 2 л/мин. При нарушении коронарного кровообращения сердечный резерв значительно снижается. В критических состояниях возрастающие метаболические потребности покрываются за счет сердечного выброса, нередко поддерживаемого инотропными агентами или при помощи седативных препаратов, анальгетиков и других средств, уменьшающих потребность тканей в кислороде. Важно помнить, что ближайший послеоперационный период, травма, шок, сепсис сопровождаются, как правило, повышенной потребностью тканей в кислороде, что достигается путем длительной и чрезвычайно интенсивной нагрузки на сердечно-сосудистую систему («гемодинамический марафон»). При этом величина CB может оказаться недостаточной для удовлетворения потребностей тканей в кислороде, что приводит к анаэробному обмену веществ. Зная основные факторы, определяющие величину MOC, врач отделения интенсивной терапии может активно воздействовать на них, улучшая гемодинамические показатели (Marini JJ., Wheeler A.P., 1997). К таким факторам относятся: • состояние венозного возврата и преднагрузки, обеспечивающей необходимую растяжимость сердечной мышцы; • состояние постнагрузки, т.е. давления, создаваемого миокардом в систолу; • сократимость миокарда. Всегда необходимо учитывать общие физиологические условия регуляции MOC, т.е. возбудимость, проводимость и сократимость. Измерение ДЗЛА позволило сделать огромный шаг вперед в оценке функции сердечно-сосудистой системы. Рассматривая варианты пред- и постнагрузки, нельзя не учитывать величину ДЗЛА, которая в норме составляет 5—12 мм рт.ст. Освоение метода катетеризации (Свана—Ганца) открыло новые возможности гемодинамического мониторинга. Стало возможным определение внутрипредсердного давления, CB, степени насыщения и парциального давления кислорода в смешанной венозной крови. Нормальные величины давления в полостях сердца и легочной артерии, мм рт.ст.
Несмотря на всю важность измерения ДЗЛА и CB, нельзя считать, что эти показатели являются абсолютными критериями адекватности тканевой перфузии. Однако применение этого метода позволяет реаниматологам контролировать величину преднагрузки и создавать условия для наиболее экономичного режима работы сердца. Сердечный индекс — отношение показателей CB и площади поверхности тела. Его определяют путем деления показателя CB на величину поверхности тела: СИ [л/(мин-м2)] = СВ/площадь поверхности тела, м2. Ударный объем — количество крови, выбрасываемое сердцем за одну систолу. Работа левого желудочка — механическая работа, выполняемая сердцем в 1 мин. Давление заклинивания легочной артерии, или давление заклинивания легочных капилляров, — давление в дистальной ветви легочной артерии при раздутом баллончике катетера Свана—Ганца. Центральное венозное давление — давление в устье полой вены или в правом предсердии. Общее периферическое сопротивление сосудов характеризует общее сопротивление всей сосудистой системы выбрасываемому сердцем потоку крови: ОПСС [дин-с/(см5-м2)] = = [(САД - ЦВД)/СИ]-80. С помощью коэффициента 80 показатели давления и объема переводят в дин-с/см5. Фактически эта величина является индексом ОПСС. Термин «общее периферическое сопротивление сосудов» обозначает суммарное сопротивление артериол большого круга кровообращения. ОПСС — важный регулятор градиента давления между артериальной и венозной системой. Возрастание этого показателя приводит к подъему среднего АД, а снижение его — к уменьшению САД. Этот важный регуляторный механизм может быть нарушен как в сторону преобладания вазоконстрикции, так и в сторону преимущественной вазодилатации. Увеличение ОПСС происходит всегда при снижении ОЦК, острой крово- и плазмопотере, травматическом шоке, повышении уровня катехоламинов в крови. Эта физиологическая реакция может сопровождаться выраженной централизацией кровообращения, вплоть до полного прекращения кровотока в коже, мышцах, ренальной и чревной областях. При длительной вазоконстрикции создаются условия для анаэробного обмена в ишемизиро-ванных тканях. При значительном увеличении ОПСС возрастает постнагрузка, что создает неблагоприятные условия для работы сердца. При повышении ОПСС в 3 раза по сравнению с нормальным MOC может уменьшиться наполовину при тех же значениях давления в правом предсердии. Многие состояния (анафилактический шок, сепсис, цирроз печени) приводят к снижению ОПСС, что сопровождается прогрессирующим падением АД. Изменение тонуса артериальных сосудов в различных отделах системного кровотока может быть различным: в одних областях возможна выраженная вазоконстрикция, в других — вазодилатация. Тем не менее, ОПСС имеет большое значение для дифференциальной диагностики вида гемодинамических нарушений. Сопротивление легочных сосудов характеризует сопротивление сосудов малого круга кровообращения. Основная функция системы кровообращения — доставка необходимого количества кислорода и питательных веществ в ткани. Кровь переносит энергетические вещества, витамины, ионы, гормоны и биологически активные вещества от места их образования к различным органам и тканям. Баланс жидкости в организме, поддержание постоянной температуры тела, освобождение клеток от шлаков и доставка их к органам экскреции осуществляются благодаря постоянной циркуляции крови по сосудам. Каждый сердечный цикл длится 0,8 с. Систола желудочков происходит в течение 0,3 с, диастола — в течение 0,5 с. Регуляция сердечного ритма в здоровом сердце осуществляется в синусовом узле, который расположен у места впадения полых вен в правое предсердие. Импульс возбуждения распространяется по предсердиям, затем к атриовентрикулярному (предсердно-желудочковому) узлу, спускается по правой и левой ветвям пучка Гиса и волокнам Пуркинье, находящимся на эндокардиальной поверхности обоих желудочков. Присасывающая сила сердца. Во время систолы желудочков атриовентрикулярная перегородка смещается по направлению к желудочкам, и, следовательно, объем предсердий увеличивается. Образующееся в предсердиях разрежение способствует присасыванию крови из центральных вен в сердце. При расслаблении желудочков напряжение их стенки обеспечивает всасывание крови из предсердий в желудочки. Дыхательные экскурсии относятся к экстракардиальным факторам регуляции MOC. Во время вдоха внутриплевральное давление становится отрицательным, что передается на предсердия и полые вены, и приток крови по этим венам в правое предсердие возрастает. При выдохе давление в брюшной полости повышается, вследствие чего кровь как бы выдавливается из брюшных вен в грудные. Отрицательное давление в плевральной полости обусловливает увеличение постнагрузки, а положительное (во время ИВЛ) оказывает противоположное действие. Этим можно объяснить снижение систолического АД во время фазы вдоха. Венозный возврат. Сердце обычно рассматривается как насос, повышающий АД и создающий направленный поток крови (сердце является «двигателем циркуляции»). Однако его можно представить и как насос, постоянно понижающий давление в правом предсердии и таким образом способствующий венозному возврату. Фактически CB является результатом взаимодействия сердца и периферических сосудов. Снижение CB можно объяснить ухудшением насосной функции сердца или развитием циркуляторных нарушений. Периферическая циркуляция играет очень большую роль в поддержании наполнения сердца и, следовательно, обеспечивает адекватный CB. Если рассматривать системный кровоток, то объем крови за единицу времени, выбрасываемый сердцем (CB), должен равняться объему крови, который возвращается к сердцу, т.е. венозному возврату. В связи с тем, что CB всегда соответствует венозному возврату, любой фактор, уменьшающий венозный возврат, соответственно снижает CB. Для выявления первичной причины снижения CB следует оценить величину давления в правом предсердии. Повышение давления свидетельствует о миокардиальной недостаточности, а снижение — об изменении тонуса периферических сосудов. В последнем случае предпочтение следует отдавать инфузионной терапии. Венозный возврат имеет точную величину потока и не является простым эквивалентом преднагрузки; он непосредственно определяется уровнем давления в правом предсердии, волемическим статусом, системным венозным тонусом. Преднагрузка. Применительно к миокарду преднагрузка определяется как сила, растягивающая сердечную мышцу перед ее сокращением. В соответствии с законом Франка— Старлинга сила сердечного сокращения зависит от длины мышечных волокон в конце диастолы. При повышении давления наполнения увеличивается объем выброса, что является важным механизмом адаптации в ответ на изменения венозного возврата. Для интактного желудочка преднагрузкой, по сути, становится конечный диастолический объем, который определяется растяжимостью стенок и давлением в полости желудочка — трансмуралъным давлением. Последнее представляет собой разницу между внутриполостным и юкстакардиальным (внекардиаль-ным) давлением. Поскольку КДО трудно определить у постели пациента, обычно пользуются такими показателями, как конечное диастолическое давление левого или правого желудочка (КДДЛЖ, КДДПЖ). Если растяжимость левого желудочка нормальная, то ДЗЛА будет равно КДДЛЖ. У пациентов, находящихся в отделениях интенсивной терапии, растяжимость левого желудочка, как правило, снижена. Это особенно характерно для ИБС, действия блокаторов кальциевых каналов, влияния положительного давления во время ИВЛ. Таким образом, ДЗЛА определяет давление в левом предсердии, но не всегда является показателем преднагрузки на левый желудочек. По сравнению с левым в правом желудочке в норме связь между трансмуральным давлением и внутрижелудочковым объемом крови относительно более выражена. При малой растяжимости желудочка, как и при повышении внутригрудного давления, требуется большее давление внутри камеры сердца для достижения определенного конечно-диастолического объема и степени растяжения мышечных волокон, предшествующих сокращению. Снижение эластичности стенок желудочка может быть следствием поражения миокарда, ограничения со стороны перикарда или сдавления сердца извне. В условиях сердечной недостаточности для достижения средних значений CB требуется большее давление наполнения. В положении пациента лежа на спине резерв преднагрузки снижается. В этом случае дальнейшее увеличение CB в основном достигается за счет увеличения ЧСС и/или фракции У О. Наибольшее значение механизм Франка—Старлинга приобретает при гиповолемии и в вертикальном положении пациента. Постнагрузка. Постнагрузку определяют как силу, препятствующую или оказывающую сопротивление сокращению желудочков. Она эквивалентна напряжению, возникающему в стенке желудочка во время систолы. Это трансмуральное напряжение стенки желудочка зависит от систолического АД, радиуса камеры (желудочка), импеданса аорты и его составляющих, растяжимости и сопротивления артерий. Постнагрузка включает преднагрузку и давление в плевральной полости (щели). Нагрузочные характеристики применительно к сердцу описывают в единицах давления и объема крови. Умеренное увеличение постнагрузки сопровождается повышением сократительной способности миокарда, преднагрузки или ЧСС. У здорового человека при этом CB обычно изменяется мало, однако при истощении резервов преднагрузки, увеличении постнагрузки он может значительно уменьшиться. Правый желудочек по сравнению с левым в норме оказывается более чувствительным к изменению постнагрузки. Дилатированные камеры сердца, как правых, так и левых отделов при декомпенсации чрезвычайно чувствительны к изменению постнагрузки. Кардиомегалия, отек легких и митральная регургитация — клинические симптомы, указывающие на необходимость медикаментозного снижения постнагрузки. В такой ситуации большое значение имеет динамическое определение ОПСС и СЛС. ОПСС помогает поддерживать АД на должном уровне, а увеличение СЛС может способствовать прогрессированию сердечной недостаточности. Возросшее сосудистое сопротивление в этом случае само по себе оказывает отрицательное воздействие на CB. Размер камер сердца также влияет на постнагрузку. В дилатированном сердце для создания необходимого внутриполостного давления требуется большее растяжение волокон во время систолы. Это особенно касается периферических волокон. Диуретики или селективные венодилататоры (нитроглицерин) способны снизить как пост-, так и преднагрузку. Помимо влияния сосудистой сети, важным показателем реологии, оказывающим влияние на постнагрузку, является вязкость крови. Вязкость крови возрастает при увеличении гематокрита. Эта зависимость имеет нелинейный характер. При увеличении гематокрита эритроциты медленнее продвигаются по капиллярам, и эффективный транспорт кислорода, значение которого зависит от ОЦК и сосудистой емкости, может достигать максимальных значений. Однако при возрастании постнагрузки CB может снизиться, в результате чего уменьшится и транспорт кислорода. Ткани обладают различной толерантностью к изменениям гематокрита и поступления кислорода. Объем циркулирующей крови. Показатель ОЦК является динамической величиной и постоянно меняется в широких пределах. В состоянии покоя не вся кровь участвует в циркуляции, и лишь некоторый ее объем, совершающий полный кругооборот за относительно короткий промежуток времени, необходим для поддержания кровообращения. В практике интенсивной терапии ОЦК — важнейший критерий состояния кровообращения. |
