Издательский дом Питер
 Скачать 5.79 Mb. Скачать 5.79 Mb.
|
|
Гены гемоглобина Каждая хромосома 16 содержит два практически идентичных гена сс-глобина, а хромосома 11 содержит подобную пару у-генов и по одной копии 5- и р-генов. Глобин синтезируется только в эритроидных клетках и только в период формирования ретикулоцитов из нормоцитов. На каждой стадии развития гены а-глобина и гены других глобинов экспрессируются координированно. Это очень важный момент. Поскольку тетрамеры, состоящие из одиночных цепей гемоглобина (например, а4 или )34), практически нерастворимы, то для его сохранения в качестве растворимого тетрамера необходим сбалансированный синтез цепей. Избыточное образование одной цепи гемоглобина, происходящее, например, при талассемии, может привести к преципитации белка в эритроците, повреждению клетки и ее преждевременной элиминации клетками ретикулоэндотелиальной системы. Подсчет ретикулоцитов Анемия может явиться результатом первичного нарушения продукции эритроцитов, острой потери крови или ускоренного разрушения эритроцитов. 176 Глава 5. Физиология крови 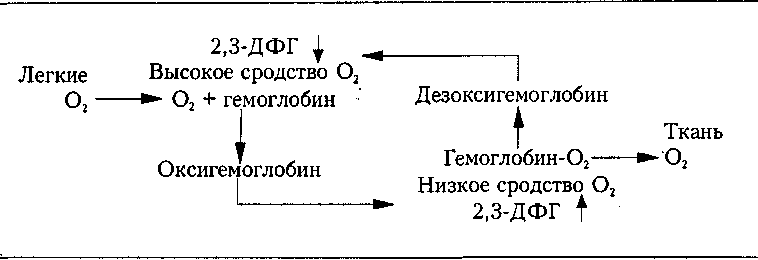 Рис. 17. Цикл диссоциации кислорода. 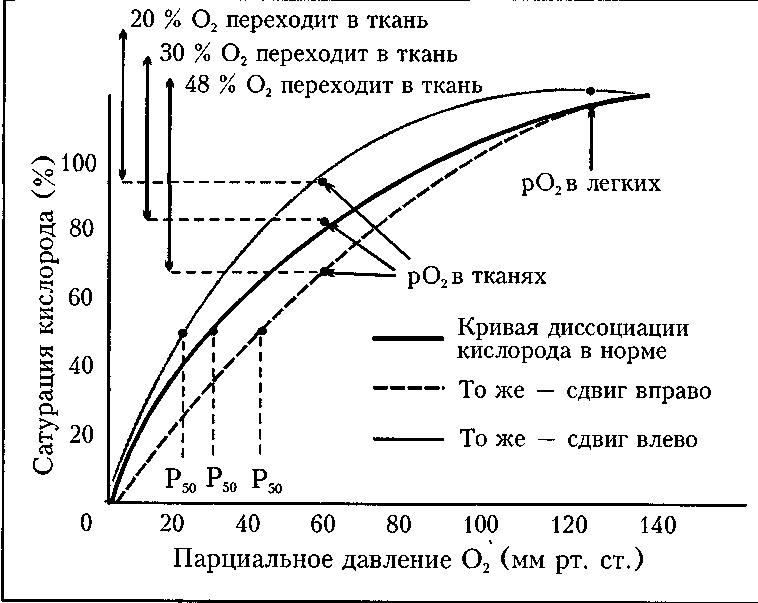 Рис. 18. Кривая диссоциации кислорода (норма, сдвиг вправо, сдвиг влево) [Walker RH. Technical Manual of the American Association of Blood Banks, 11th ed. Bethesda, MD, American Association of Blood Banks, 1993]. Эритроциты_______________________________*21 Для выяснения причин анемии чрезвычайно важно определить реакцию костного мозга. В нормальных условиях примерно 1 % эритроцитов в организме ежедневно заменяется юными клетками, которые называются ретикулоци-тами. Поскольку эти клетки все еще содержат полирибосомную РНК, их можно определить с помощью специального окрашивания мазка периферической крови. Краситель Райта, содержащий эозин и метиленовый синий, окрашивает ретикулоциты в серо-пурпурный цвет. Под действием более специфических красителей (новый метиленовый синий, бриллиантовый крезиловый синий) происходит преципитация РНК, и полирибосомы ретикулоцитов проявляются в виде сетчатого узора, что и послужило основанием для названия этих клеток. Содержание ретикулоцитов обычно выражают как процент от общего числа клеток красной крови. Эта величина может быть высокой как вследствие абсолютного увеличения количества циркулирующих ретикулоцитов, так и вследствие сокращения массы циркулирующих эритроцитов (анемия). Поэтому при анемии используют нормализованное количество ретикулоцитов (НКР), вычисляемое по формуле: ГК пациента НКР = % ретикулоцитов х ——————, ГК в норме где ГК — гематокрит. Повышение скорректированного количества ретикулоцитов свидетельствует о стимуляции костного мозга эритропоэтином, способствующей не только повышенной продукции ретикулоцитов, но и их раннему поступлению в кровь. В этих условиях в крови появляются незрелые ретикулоциты, которые и можно там обнаружить в течение более 1 дня. Конкретный срок, в течение которого циркулируют ретикулоциты, зависит от того, сколько времени потребуется для их созревания и утрате РНК. Этот срок коррелирует с уровнем ге-матокрита: при ГК, равном 45 %, ретикулоцит проведет в периферической крови только 1 день. Но если ГК составляет 35, 25 или 15 %, ретикулоцит находится в периферической крови 1,5, 2 и 2,5 сут соответственно. Индекс продукции ретикулоцитов (ИПР) позволяет уточнить время пребывания ретикулоцита в периферической крови по следующей формуле: ИПР = НКР___________________________ Время созревания ретикулоцитов (дни) Другой способ оценки продукции эритроцитов состоит в подсчете абсолютного количества ретикулоцитов, равного произведению процентного уровня ретикулоцитов на количество эритроцитов. В норме эта величина составляет 50 000 и 60 000 клеток/мкл. Подсчет абсолютного количества ретикулоцитов, по-видимому, служит наиболее информативным показателем. 178 Глава 5. Физиология крови Если причиной анемии является кровопотеря или деструкция клеток крови вне костного мозга, то секреция эритропоэтина возрастает, относительное количество ретикулоцитов поднимается выше нормального уровня (1 %), а абсолютное число ретикулоцитов превышает величину 100 000 клеток/мкл. Отсутствие соответствующего ретикулоцитоза при анемии указывает на нарушение продукции эритроцитов в костном мозге вследствие недостаточности питания, остановки созревания и/или заболеваний. Средний объем эритроцита Ориентировочно средний объем клетки (эритроцита) (СОК) можно определить при анализе мазка периферической крови. Прямое измерение осуществляется с помощью автоматического цитометра или подсчитывается путем деления гематокрита на количество эритроцитов (табл. 20). Измерение СОК особенно важно для оценки гипопролиферативных анемий (анемии с низким содержанием ретикулоцитов), которые подразделяют в соответствии с величиной СОК на три категории: — микроцитарная анемия (СОК < 80 мкм3); — нормоцитарная анемия (80 мкм3 < СОК < 100 мкм3); — макроцитарная анемия (СОК > 100 мкм3). Еще два показателя: среднее содержание гемоглобина в эритроците (ССГ= гемоглобин / число эритроцитов) и средняя концентрация гемоглобина в эритроците (СКГ = гемоглобин / гематокрит) также вычисляются с помощью автоматических цитометров, хотя их информативность не столь высока, как СОК. ССГ обычно коррелирует с величиной СОК. СКГ снижена при большинстве микроцитарных анемий, связанных с дефицитом железа, и повышена при наследственной или аутоиммунной гемолитической анемиях. Таблица 20 Эритроцитарные индексы
Эритроциты_____________________________________179 Метаболизм железа В пищевых продуктах железо находится или в качестве составной части тема, или как негемовое железо. Несмотря на то, что железо тема обычно составляет меньшую долю этого металла, поступающего с пищей, оно достаточно хорошо всасывается (в норме около 20-30 %). Негемовое железо всасывается хуже (менее 5 %), а при одновременном присутствии в пище таннинов и фосфатов — еще меньше. Несколько увеличивает абсорбцию негемового железа аскорбиновая кислота. Всасывание железа происходит в проксимальной части тонкой кишки и существенно возрастает в условиях дефицита железа, а также у пациентов с неэффективным эритропоэзом. В последнем случае при тяжелой форме нарушения эритропоэза, например при некоторых видах талассемии, несмотря на высокий уровень содержания железа в организме, его всасывание повышено. Проводимые в этих условиях переливания крови часто приводят к клинически значимой перегрузке железом (см. раздел 14.6.1). Транспорт железа осуществляется с помощью плазменного белка — трансферрина, который связывается со специфическим рецептором мембраны. Комплекс рецептор — трансферрин — железо поглощается развивающимися эритроцитами, после чего железо высвобождается, а соединение трансферрин/ трансферриновый рецептор завершает цикл на клеточной мембране. Внутриклеточный белок ферритин в нетоксичной форме депонирует железо, которое мобилизуется по мере необходимости. Каждая молекула ферритина может связываться с 4500 атомами железа, но в нормальных условиях такая молекула содержит около половины этого количества. Некоторая часть ферритина конвертируется в гемосидерин — нерастворимое в воде соединение, хранящее железо в большем количестве, но в менее доступной форме. Содержание железа в организме мужчин и женщин составляет соответственно 50 и 40 мг/кг массы тела. От 28 до 31 мг/кг железа входит в состав гемоглобина, 4-5 мг/кг — в состав миоглобина, 12 мг/кг — в состав ферритина и гемосидерина, а остальное — в состав гемсодержащих и других ферментов (табл. 21). Главным местом депонирования железа являются печень (гепатоциты и макрофаги), костный мозг, селезенка и мышцы. Внутри клетки специфический белок связывается с регуляторным участком на мРНК и координирует экспрессию ферритина, трансферрина и трансферринового рецептора. Этот белок активируется при низком внутриклеточном уровне железа и инициирует повышение синтеза трансферринового рецептора и подавляет синтез ферритина. Железодефицитная анемия (ЖДА) — наиболее распространенное заболевание. У большинства мужчин, а также у женщин в постменопаузе дефицит железа развивается вследствие кровопотери, обусловленной кровотечением из желудочно-кишечного тракта (ЖКТ) (табл. 22). Поэтому при обнаружении дефицита железа каждый мужчина или женщина в период постме- 180 Глава 5. Физиология крови Таблица 21 Распределение железа
Таблица 22 Причины дефицита железа
нопаузы должны пройти полное обследование ЖКТ на предмет поиска возможной патологии, особенно опухолей. Не удается установить причину кровотечения из ЖКТ примерно у 15 % пациентов. У женщин детородного возраста основные причины железодефицитной анемии: — вагинальное кровотечение; — беременность; — лактация. Около 15 мг железа в месяц теряется при менструации. Примерно 900 мг железа теряется в период нормальной беременности и родов, поскольку железо транспортируется в плаценту и к плоду, а также теряется при родовом кровотечении. Более редкие причины потери крови: — возвратный гемофтиз; — пневмосидероз; Эритроциты — синдром Гудпасчера; — гематурия. Дефицит железа может развиваться и без потери крови, например в период интенсивного роста детей потребность в железе превышает его поступление. Подобная ситуация характерна для новорожденных, особенно недоношенных, а также для подростков (главным образом у девушек в период становления месячного цикла). Другой причиной дефицита железа может быть нарушение всасывания, которое развивается у пациентов, подвергшихся хирургическому вмешательству на желудке, или у больных с синдромами кишечной мальабсорбции. Дефицит железа приводит к развитию объективных и субъективных симптомов, обычных для всех анемий: бледность, усиленное сердцебиение, шум в ушах, головная боль и слабость. К редким, но более специфическим симптомам относятся: извращение аппетита, странное желание съесть такие вещества, как крахмал, лед, глина (амилофагия, пагофагия, геофагия), койлонихия и голубой цвет склер. Недостаток железа в неэритроидных тканях может быть причиной глоссита, ангулярного стоматита и эзофагита. Хотя классическая ЖДА при лабораторном обследовании может проявляться как гипохромная микроцитарная анемия, у большинства пациентов в начале заболевания наблюдается нормохромная анемия. Анемия обычно предшествует микроцитозу, а гипохромия является последним проявлением прогрессирующей ЖДА. Анемия часто сопровождается реактивным тромбоцитозом. При тяжелой ЖДА в мазке периферической крови можно наблюдать микроцитоз с бледными гипохромными эритроцитами и одиночные удлиненные «карандаше-подобные» клетки, а также мишеневидные клетки. Запасы железа можно определить непрямым методом, измеряя уровни ферритина, железа и насыщения трансферрином (железосвязывающая способность). Печень продуцирует ферритин пропорционально количеству доступного железа, и небольшое определенное количество этого ферритина сек-ретируется в плазму. Таким образом, уровень ферритина в плазме является важным показателем запасов железа в организме. Уровень ниже 12 нг/мл, как правило, свидетельствует о дефиците железа, но следует иметь в виду, что гипотиреоз и дефицит аскорбиновой кислоты также иногда могут снижать уровень ферритина в плазме. Кроме того, и нормальный уровень ферритина не исключает дефицита железа, поскольку ферритин является острофазовым реактантом, и его уровень может возрастать при высокой температуре тела, инфекции, воспалительном процессе, поражении печени, злокачественных новообразованиях, гемолизе, неэффективном эритропоэзе. Однако подобные состояния сами по себе не должны повышать уровень ферритина выше 50-100 нг/мл; ферритин выше этого уровня обычно исключает дефицит железа. 182 Глава 5. Физиология крови О корреции железодефицитной анемии и восстановлении запасов железа см. раздел 13.7. 5.3. Лейкоциты Клетки «белой крови», или лейкоциты, являются основой антимикробной защиты организма. В эту разнородную группу клеток входят основные эффекторы иммунных и воспалительных реакций. Термин «лейкоцит» относится более к внешнему виду клеток (leukos — с греч. белый), наблюдаемому в образце крови после центрифугирования. Лейкоциты представляют собой гетерогенную группу клеток, возможные классификации которых приведены ниже. Лейкоциты можно классифицировать по нескольким характеристикам. По происхождению: миелоидные; лимфоидные. По функции: иммуноциты; фагоциты: макрофаги; микрофаги. По морфологии ядра: полиморфно-ядерные; мононуклеарные. По наличию цитоплазматических включений: гранулоциты. Нейтрофилы Нейтрофильные гранулоциты составляют самую большую группу циркулирующих лейкоцитов. Термин «нейтрофильный» характеризует внешний вид цитоплазматических гранул при окрашивании по Райту-Гимзе. Вместе с эозинофилами и базофилами нейтрофилы относятся к классу гранулоци-тов. В связи с характерным многодолевым ядром нейтрофил называют также полиморфно-ядерным лейкоцитом (ПМЯЛ). Эти высокоспециализированные клетки мигрируют в очаги инфекции, где распознают, захватывают и уничтожают бактерии. Для осуществления этой задачи нейтрофилы способны к хемотаксису, адгезии, передвижению и фагоцитозу. У них имеется метаболический аппарат для продуцирования токсических веществ и ферментов, разрушающих микроорганизмы. Развитие нейтрофилов. В костном мозге можно наблюдать 6 определенных последовательных морфологических стадий созревания нейтрофилов: Лейкоциты____________________________________ 183 миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерная и сег-ментоядерная клетка. Кроме того, в костном мозге имеются более ранние, морфологически не идентифицируемые, коммитированные предшественники ней-трофилов (КОЕ-ГМ и КОЕ-Г). Наличие этих клеток-предшественников считается доказанным с учетом способности костного мозга порождать коммитированные миелоидные колонии invitroи с возобновлением гранулоци-топоэза после трансплантации костного мозга. Созревание нейтрофилов сопровождается прогрессирующим снижением размера ядра за счет конденсации хроматина и потери ядрышек. По мере созревания нейтрофила ядро зазубривается и наконец приобретает свой характерный многодолевой внешний вид. Параллельно происходят изменения и в цитоплазме нейтрофила, где накапливаются гранулы, содержащие соединения, которые в последующем сыграют столь важную роль в защите организма. Первичные (азурофильные) гранулы — включения синего цвета размером приблизительно 0,3 мкм, содержащие эластазу и миелопероксидазу. Впервые они появляются на промиелоцитарной стадии; их количество и интенсивность окрашивания снижаются в период последующего созревания нейтрофилов. Вторичные (специфические) гранулы, которые содержат ли-зоцим и другие протеазы, появляются на стадии миелоцита. Окрашивающие свойства этих вторичных гранул обусловливают характерный нейтрофиль-ный вид цитоплазмы. Продукция нейтрофилов. Нейтрофилы непрерывно поступают в кожу, слизистые оболочки и другие периферические ткани. Ежедневный оборот нейтрофилов — около 100 млрд клеток. Особенность нейтрофилов — уникальная возможность увеличения численности как за счет расширения пула про-лиферирующих клеток, так и за счет «рекрутирования» зрелых нейтрофилов. В отличие от большинства других клеток крови нейтрофилы проводят во внутрисосудистом пространстве очень небольшую часть своей жизни. Поэтому количество циркулирующих нейтрофилов не вполне отражает кинетику образования этих клеток. Большую часть своей 15-дневной жизни клетки нейтрофильного ряда проводят в костном мозге, где происходит расширение пула нейтрофильных предшественников. Митотический, или пролиферативный, пул клеток состоит из коммитированных миелоидных клеток-предшественников КОЕ-ГМ и КОЕ-Г и нейтрофильных предшественников вплоть до стадии миелоцита. Расширение этого костномозгового пула ускоряется воспалительными цито-кинами - Г-КСФ и ГМ-КСФ. На пути к периферическим тканям нейтрофилы проводят примерно 10 ч, находясь во внутрисосудистом пространстве. Этот внутрисосудистый компар-тмснт является для гранулоцитов не просто коридором, ведущим от костного мозга к периферическим тканям; в любой момент времени только половина внутрисосудистых гранулоцитов находится в движении, другая половина 184 _________________Глава 5. Физиология крови обратимо прилипает к эндотелиальной поверхности микрососудистого русла. Эти так называемые пристеночные клетки составляют запасной пул зрелых клеток, которые могут быть востребованы при необходимости в случае инфекции или воспаления. Функция нейтрофилов. Функция нейтрофилов — защита организма от инфекции — включает три составляющие: — хемотаксис; — фагоцитоз; — уничтожение микроогранизмов. Хемотаксис — способность к обнаружению и целенаправленному движению к микроорганизмам и очагам воспаления. Нейтрофилы имеют специфические рецепторы в отношении С5а — компонента системы комплемента (вырабатываемого в классическом или альтернативном путях активации комплемента) и протеаз, выделяемых при повреждении тканей или при непосредственном бактериальном воздействии. Кроме того, нейтрофилы имеют рецепторы для N-формильных пептидов, выделяемых бактериями и пораженными митохондриями. Эти рецепторы реагируют на продукты воспаления — лей-котриен LTB4 и фибринопептиды. Локомоторная система, напоминающая сократительный аппарат мышцы, позволяет нейтрофилу продвигаться по эндотелиальной поверхности к месту воспаления. Нити актина взаимодействуют с сократительным белком миозином в процессе, при котором потребляется АТФ. Медленно двигаясь, нейтрофилы распространяют псевдоподии в направлении воспалительных хемотак-синов. Нейтрофилы распознают инородные организмы посредством рецепторов к опсонинам (термин взят из греческого языка и означает «подготовиться к обеду»). Фиксация сывороточного IgG и комплемента на бактериях делает их распознаваемыми для гранулоцитов. Нейтрофил имеет рецепторы для Fc-фрагмента молекулы иммуноглобулина и продуктов каскада комплемента. Эти рецепторы инициируют процессы захвата, поглощения и адгезии инородных объектов. Нейтрофилы поглощают опсонированные микроорганизмы с помощью цитоплазматических пузырьков — фагосом. Эти пузырьки продвигаются от складчатых псевдоподий и сливаются с первичными и вторичными гранулами в ходе энергетически зависимого процесса, во время которого в фагоцитах происходит взрывной процесс гликолиза и гликогенолиза. При деграну-ляции клетки содержимое гранул попадает в фагосому с выделением ферментов, реализующих его деградацию: — лизоцим; — кислая фосфатаза; — щелочная фосфатаза; — эластаза; Лейкоциты_____________________________________185 — лактоферрин. Также нейтрофилы разрушают бактерии, метаболизируя кислород с образованием его активных форм — продуктов, токсичных для поглощенных микроорганизмов. Аппарат оксидазы, генерирующий эти продукты, состоит из флавин- и гемсодержащего цитохрома b558. При этих реакциях используется восстанавливающий агент никотинамидадениндинуклеотидфостат (НАДФ), а стимуляторами их является глюкозо-6-фосфатдегидрогеназа и другие ферменты гексозомонофосфатного шунта. За счет этого клетка генерирует супероксид (О2-) и перекись водорода (Н2О2), которые выделяются в фагосому для уничтожения бактерий. Лактоферрин участвует в образовании свободных гидроксильных радикалов, а миелопероксидаза, используя галоиды в качестве кофакторов, еще и в продукции гипохлорной кислоты (НОС1) и токсичных хлораминов. Активные формы кислорода токсичны как для микроорганизма, так и для самой клетки. Но благодаря тому, что местом их локализации является фагоцитарная вакуоль, поражение других участков клетки ограничено. К другим механизмам защиты клетки от воздействия этих продуктов относятся: супероксиддисмутаза, превращающая супероксид в перекись водорода; ка-талаза, разрушающая перекись водорода; восстановленный глютатион, также разрушающий перекись водорода (и способствующий тем самым регенерации НАДФ-Н, который в дальнейшем может вновь использоваться для образования перекиси). Наряду с токсическими активными формами кислорода нейтрофил обладает и другими механизмами бактерицидного действия: губительной для микроорганизмов кислой средой фагосомы; лизоцимом, гидролизирующим му-копептидную клеточную мембрану некоторых бактерий; вырабатываемыми в фагосоме бактерицидными белками (дефензинами и перфоринами), изменяющими проницаемость мембран клеток-мишеней. Наряду с многочисленными врожденными и приобретенными возможными нарушениями функции нейтрофилов для трансфузиологии принципиально важное значение имеет нейтропения. Нейтропения (количество нейтрофилов менее 1,8х109/л), как и нейтро-филия, может быть вызвана временными или постоянными изменениями различных нейтрофильных пулов и подтверждается рядом последовательных анализов крови. Если абсолютное количество нейтрофилов составляет более 0,5x109 /л, обычно существенного нарушения в защите макроорганизма не происходит. Однако тяжелая нейтропения (особенно при показателях ниже 0,2х109 /л) всегда связана с повышенным риском инфекции, особенно если снижение уровня нейтрофилов происходит быстро. Тяжелая острая нейтропения может быть вызвана истощением резерва нейтрофилов в связи с септицемией, лихорадкой, прострацией. Эта форма нейтропении, особенно связанная с лихорадочным состоянием, требует быстрой оценки и раннего лечения 186 _____________ Глава 5. Физиология крови антибиотиками широкого спектра действия. Хроническое постоянное истощение нейтрофильного резерва может не давать клинических симптомов и проявляться незначительным повышением температуры, стоматитом, лимфадено-патией и рецидивирующими абсцессами. Нейтропения может быть вызвана различными лекарственными препаратами, чаще всего сульфапроизводными антибиотиками, фенотиазинами, анти-тиреоидными средствами и анальгетиком фенилбутазоном. При многих видах химиотерапии происходит дозозависимая супрессия гранулоцитообразо-вания; эти препараты могут быть наиболее частой причиной ятрогенной гра-нулоцитопении. Содержание гранулоцитов в крови снижается при таких системных нарушениях, как ревматоидный артрит и системная красная волчанка. В некоторых случаях причиной могут быть антинейтрофильные антитела, которые участвуют в интрамедуллярной деструкции созревающих нейтрофилов или влияют на выживание и пролиферацию предшественников нейтрофилов. Псевдонейтропения обусловлена повышенной маргинацией (краевое стояние) гранулоцитов. Такие временные сдвиги могут быть вызваны реакциями повышенной чувствительности, виремией, гемолизом или ге-модинамическими изменениями. |
