Химия лабы и индивид зад. Лабораторная работа по теме гальванические элементы Опыт Гальванический элемент с деполяризатором катионом металла. По заданию преподавателя из перечисленных электродов составьте элемент
 Скачать 5.58 Mb. Скачать 5.58 Mb.
|
Лабораторная работа 6 по теме «Химические эквиваленты веществ» Опыт 1. Приготовление раствора соляной кислоты заданной нормальности из более концентрированного раствора Опыт выполняется по следующей общей схеме (рис.1). Приготовить раствор соляной кислоты в объеме V1 = 100 мл (в мерной колбе) с концентрацией А (концентрацию для каждой бригады определяет преподаватель) из более концентрированного раствора (…г/мл и С...%). Для этого рассчитать требуемый объем концентрированной кислоты и расчет показать преподавателю. Предлагается один из вариантов решения задачи: V1Сн1 = V2Сн2, V2 = (V1Сн1)/ Сн2, Сн2 = С10/Э, V2 = V1Сн1Э/ С10, где V1 = 100 мл, V2 – требуемый объем кислоты, Сн1 и Сн2 – молярная концентрация эквивалента, С% - массовая доля, Э – мольная масса эквивалента, - плотность раствора. 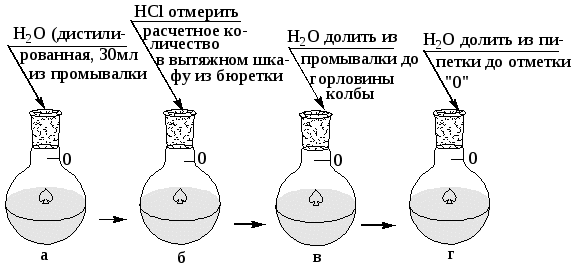 Рис.1. Схема приготовления раствора: а – мерная колба (V1 = 100 мл); б – мерная колба с Н2О ( 30 мл); в – мерная колба с HCl и Н2О; г – мерная колба с раствором заданной концентрации HCl. При заполнении раствором мерных колб необходимо исходить из того, чтобы нижний мениск раствора касался метки или нулевого деления, а глаз экспериментатора находился на уровне мениска. Опыт 2. Определение молярной концентрации эквивалента, приготовленного раствора соляной кислоты методом титрования Расход этилового спирта на 1 опыт: 0,30 мл. Опыт выполняется в следующей последовательности (рис. 2, 3): 1) бюретку А ополоскать приготовленным раствором НСl (расход около 10 мл); 2) заполнить бюретку А приготовленным раствором из мерной колбы (из опыта 1); 3) вытеснить воздух из кончика бюретки А, и установить уровень раствора НСl на ноль по нижнему мениску; 4) отмерить раствор НСl из бюретки А в коническую колбу в количестве 1 мл; 5) подготовить бюретку Д со щелочью для титрования (заполнить до 0 уровня с 0,1 н растворы NаОН, вытеснить воздух из кончика бюретки); 6) произвести титрование приготовленного раствора НСl (V=1мл) со щелочью NаОН из бюретки А до получения раствора устойчивой окраски розового цвета от последней капли щелочи (опыт повторить 2-3 раза до получения одинаковых результатов по объему израсходованной щелочи).
Рис. 2. Схема выполнения опыта: а – бюретка А с приготовленным раствором НСl; б – бюретка Д с раствором NаОН; в – коническая колба для титрования приготовленного раствора НCl (из опыта 1) и г – коническая колба с раствором HCl и Н2О для титрования со щелочью. Результаты титрования запишите в виде табл. 1. Таблица 1
Опыт 3. Экспериментальная проверка закона эквивалентов – определение массы металла (навески) и молярной массы эквивалента (или эквивалентной массы) металла методом вытеснения водорода Опыт выполняется при помощи прибора, который показан на рис. 3, в следующей последовательности: 1) заполните приготовленным раствором HCl бюретку Г до нулевой отметки; 2) получите у лаборанта реакционную колбу с металла В, запишите номер навески в журнале и соедините колбу с бюреткой Г; 3) проверьте герметичность бюреток Г, Б и колбы В путем поднятия или опускания одной из бюреток (Б или Г) на 10 см, при этом разность уровня раствора ( 10 см) должна сохраниться без изменения; 4) проверьте уровень раствора в бюретках А и Б (в бюретке Б уровень должен быть больше, чем в бюретке А) и записываем начальный уровень раствора в бюретках Б и А (h1); 5) путем постепенного введения до 1,5-2,0 мл (V1) раствора HCl из бюретки Г в колбу В осуществите реакцию Mg + HCl MgCl2 + H2, запишите показания барометра и термометра; 6) после завершения реакции запишите прилитый объем кислоты и после 4-5 минут, не нарушая герметичность прибора, приведите уровень раствора в бюретках Б и В к одинаковому уровню, запишите уровень воды в бюретках h2 и определите объем выделившегося водорода υН2 = h1 – h2; 7) определите избыток HCl в колбе Б (V2) путем титрования как в опыте 2, по формуле VHClCHCl = VNaOH СNaOH; 8) определите объем кислоты (V3), который прореагировал со взятой навеской металла и через V3 определите массу магния mMg = ЭV3Cн(оп), где Э – эквивалентная масса магния (теоретическая) и Cн(оп), - нормальная концентрация раствора (опытная). 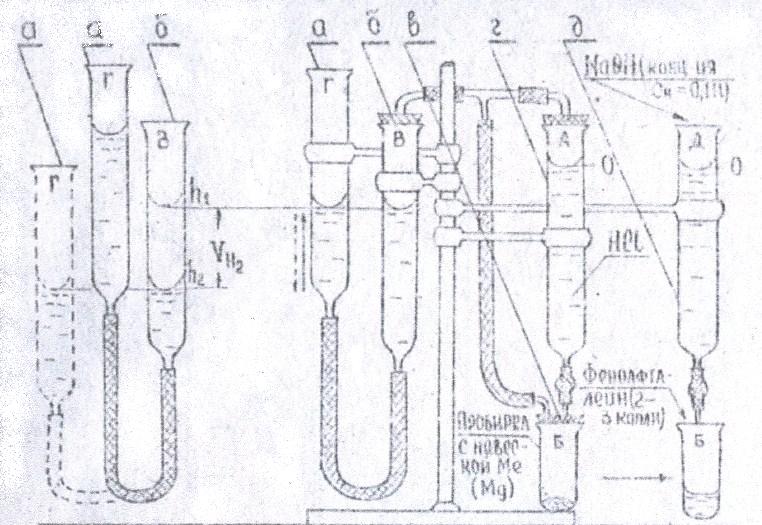 Рис 3. Прибор для определения эквивалентной массы металлов: а(Г)- и б(В)- бюретки с раствором; в(Б)- реакционная колба с навеской металла; г(А)- бюретка с приготовленным раствором HCl и д(Д)- бюретка с раствором NaOH Для определения опытного значения молярной массы эквивалента (или эквивалентной массы) магния (Эоп) необходимо определить объем водорода в нормальных условиях Vоп(Н2) = КVH2, где К- множитель, который определите по номограмме (рис. 4) или по уровню газового состояния: Vоп(Н2) = VH2(Р - РН2О)То/ТРо, где Р – атмосферное давление (определите по барометру); РН2О - давление насыщенного пара воды в бюретке Б, которое приведено в табл.2. Таблица 2
 Рис. 4. Номограмма для определения множителя К: а-температурная шкала; б-давление насыщенного пара воды; в-шкала множителя К; г-шкала атмосферного давления. Опытное значение молярной массы эквивалента: Эоп = m Vэ(H2)/ Vоп(H2), где Vэ(H2) -объем, занимаемый молярной массы эквивалента водорода (Vэ(H2) =11,2 л) и Vоп(H2) - объем водорода в нормальных условиях. Относительная ошибка Сн(HCl), m(Mg), Эоп. Её определяют по формуле П = (аоп - атеор)100/атеор. Запишите уравнения протекающих реакций, зарисуйте схему прибора. ИНДИВИДУАЛЬНЫЕ ЗАДАНИЯ Вариант I. 1. Сколько эквивалентов заключается в одном моле CH3COOH, NH4OH, Na2O, Al(OH3), Al2(SO4)3, H2? 2. Какова молярность 3н раствора FeCl3? 3. При взаимодействии кислорода и фосфора израсходовано 2,8 л кислорода (н.у.). Сколько эквивалентов P2O5 получилось? 4. Из 0,4635 г оксида металла получено 0,4135 г металла. Определите эквивалентную массу оксида и металла. 5. Для нейтрализации некоторого объема H2SO4 израсходовано 24,2 мл 0,1 М раствора щелочи. Вычислите, сколько граммов было в растворе. 6. Определите молярность и нормальность 30% HCl с ρ = 1,15 г/мл. Сколько этой кислоты потребуется для приготовления 100 мл 1н раствора? Вариант 2. 1. Сколько эквивалентов заключается в одном моле O2, P2O5, Na2CO3, HBr, Ca(OH)2, Ca3(PO4)2? 2. Какова нормальность 1,5 М раствора NiSO4? 3. Сколько граммов щелочи NaOH потребуется для растворения 4 моль Zn(OH)2? 4. Сколько граммов цинка и серной кислоты вступили в реакцию, если при этом выделилось 5,6 л водорода (н.у.)? 5. Сколько 0,5М раствора KOH потребуется для полной нейтрализации раствора, содержащего 6,5 г? 6. Определить молярность и нормальность 70% HClO4 с ρ = 1,7 г/мл. Сколько мл этой кислоты потребуется для приготовления 200 мл 4 М раствора? Вариант 3. 1. Сколько эквивалентов заключается в одном моле N2, H2S, CO2, CaCO3, Cr2O3, H3PO4? 2. Какова молярность 1,5н раствора H3PO4 ? 3. Для полного окисления 2,25 г металла потребовалось 1400 мл кислорода (н.у.). Определите эквивалентную массу металла и оксида. 4. Смешали растворы, содержащие по 1 г HCl и KOH. Какая будет среда (кислая, щелочная или нейтральная)? 5. Вычислить, сколько граммов Ba(OH)2 потребуется для полной нейтрализации 100 мл 1 М раствора H2SO4. 6. Определить молярность и нормальность 13,5% HCl с ρ = 1,065 г/мл. Сколько этой кислоты потребуется для приготовления 250 мл 0,5 М раствора? Вариант 4. 1. Сколько эквивалентов заключается в одном моле Cl2, N2O5, Al(NO)3, NH4NO3, Cu(OH)2, H2SO4? 2. Какова нормальность 0,1 М раствора NH4NO3 и Ba(OH)2? 3. При взаимодействии водорода и азота получили 2 эквивалента аммиака. Какие объемы водорода и азота вступили во взаимодействии (н.у.)? 4.При сжигании 3,4г металла было получено 5,4г оксида. Определите атомную массу металла, зная, что его валентность равна двум, и составьте формулу оксида. 5. Какой объем 0,4м раствора НСl следует прибавить к раствору Ag NO3 для получения 0,2867г AgCl? 6. Определить молярность и нормальность 80% H2SO4 с ρ=1,73 г/мл. Сколько этой кислоты потребуется для приготовления 500 мл 0,1н раствора? Вариант 5. 1. Сколько эквивалентов в одном моле CaSO4, SO3,,Fe(OH)3,HF, F, Fe2(SO4)3? 2. Какова нормальность 1М раствора NH4OH и 1М раствора Ba(OH)2? 3. При растворении в кислоте 3,06 г металла выделилось 2,8 л водорода, измеренного при 0оС и давлении 101,325 кПа (760 мм рт. ст.). Вычислите эквивалентную массу металла. 4. Сколько эквивалентов и граммов едкого натра содержалось в растворе, если в результате его взаимодействия с раствором сернокислой меди образовалось 3 моль гидроксида меди (II)? 5. Какой объем 0,1н раствора можно приготовить из 2 л 2М раствора? 6. Определите молярность и нормальность 50% H3PO4 c = 1,3 г/мл. Сколько этой кислоты потребуется для приготовления 400 мл 3М раствора? Вариант 6. 1. Сколько эквивалентов в одном моле Zn(OH)2, Al, Mn2O7, Na2SO4, H2SiO3, Cr2(SO4)3? 2. Какова молярность 0,2н раствора Ва(OH)2? 3. Некоторое количество металла, эквивалентная масса которого 28 г/моль, вытесняет из кислоты 700 мл водорода (н.у.). Определите массу металла. 4. Сколько эквивалентов находится в 2 моль сернокислого алюминия и сколько эквивалентов и граммов NH4OH потребуется для осаждения алюминия в виде Al(ОН)3? 5. Определите, сколько 2М раствора NaOH потребуется для полного растворения 9,9 г Zn(OH)2? 6. Определите молярность и нормальность 96% H2SO4 c = 1,84 г/моль. Сколько этой кислоты потребуется для приготовления 100 мл 0,1н раствора? Вариант 7. 1. Сколько эквивалентов в одном моле J2, NO2, HJ, CuSO4, Cr(OH)3, KNO3? 2. Какова нормальность 0,5М раствора HJ? 0,5М раствора H2CeO4? 3. Определите эквивалентную массу металла, если 0,72 г его вытеснили из кислоты 711 мл водорода при температуре 15оC и давлении 100 кПа (750 мм рт. ст.). Давление насыщенного водяного пара при указанной температуре равно 1,69 кПа (12,7 мм рт. ст.) . 4. Определите эквивалентную массу меди в оксиде, содержащем 20% кислорода. 5. Сколько граммов KOH нужно растворить в воде, чтобы получить 200 мл 2 М раствора? 6. Определите молярность и нормальность 20 % раствора Ba(OH)2 с ρ = 1,5 г/мл. Сколько этого раствора потребуется для приготовления 1 л 1М раствора гидроксида бария? Вариант 8. 1. Сколько эквивалентов в одном моле NH4OH, N2, Fe2O3, NaBr, Al2S3, H2SO3? 2. Какова молярность 4н. раствора CuSO4? 3. Смешали растворы, содержащие по одному грамму H3PO4 и NaOH . 4. 0,604 г двухвалентного металла вытеснили из кислоты 581 мл водорода, собранного над водой при 10оC и давлении 105,6 кПа. Давление насыщенного пара воды при 18оC составляет 2,1 кПа. Найдите относительную атомную массу металла. 5. Какой объем 4 М раствора соляной кислоты требуется для нейтрализации 10 г едкого натра? 6. Определите молярность и нормальность 80 % с HNO3 ρ = 1,45 г/мл. Сколько этой кислоты потребуется для приготовления 400 мл 5М раствора? Вариант 9. 1. Сколько эквивалентов в одном моле MgSO4, H2Te, O2, K2O, CH3COOH, Ca3(PO4)2? 2. Какова нормальность 2 М раствора H3PO4? 3. Вычислите валентность меди в оксиде, в котором на 1 г кислорода приходится 3,973 г меди. 4. Сколько граммов алюминия и серной кислоты вступили в реакцию, если на сжигание выделившегося в результате реакции водорода потребовалось 2,24 л кислорода (н.у.)? 5. На нейтрализацию 20 мл 1 М раствора едкого натра использовали 20 мл раствора серной кислоты. Сколько граммов серной кислоты содержится в 1 л такого раствора ? 6. Определите молярность и нормальность 4 % H2SO4 с ρ = 1,03 г/мл. Сколько этой кислоты потребуется для приготовления 500 мл 0,01 М. раствора? Вариант 10. 1. Сколько эквивалентов в одном моле MgO, Cl2, K2CO3, Mn(OH)2, H2S, Ba3(PO)2? 2. Какова молярность 3н раствора Al2(SO4)3? 3. Какие объемы водорода и кислорода прореагировали, если образовалось 2 эквивалента воды (н.у.)? 4. На нейтрализацию I г кислоты израсходовано 1,24 г KOH. Вычислите эквивалентную массу кислоты. 5. Сколько граммов NaOH требуется для осаждения железа, содержащегося в 20,1 мл 1,6 М раствора FeCl3. 6. Определите молярность и нормальность 30% HNO3 c p=1,2г/мл. Сколько кислоты потребуется для приготовления I л C,1 M раствора? Вариант 11. 1. Сколько эквивалентов в одном моле Ca, BaO, Cl2O7, HClO4, Ba(OH)2 , Fe2(SO4)3? 2. Какова нормальность 2 М раствора Fe2(SO4)3? 3. В какой массе NaOH содержится столько же эквивалентных масс, сколько в 140 г KOH? 4. 0,350 г металла вытеснили из кислоты 209 мл водорода, собранного над водой при 20°С и давлении 104,3 кПа. Давление насыщенного пара воды при этой температуре составляет 2,3 кПа. Найти эквивалентную массу металла. 5. Для реакции с FeCl3, содержащимся в 25 мл 2 М раствора, взято 100 мл I М раствора КОН. Вычислите, в избытке или а недостатке взят раствор КОН . 6. Определите полярность и нормальность 20 % серной кислоты с =1,14 г/мл. Сколько этой кислоты потребуется для приготовления 100 мл 2 М раствора? Вариант 12. 1. Сколько эквивалентов в одном моле CO, Na2CO3, Al2O3, Al, HNO3, Cd(OH)2? 2. Какова молярность 3нраствора CuCl2 ? 3. При восстановлении 1,34 г оксида металла до металла образовалось 0,24 г воды. Вычислите эквивалентную массу металла. 4. Какая среда кислая, щелочная или нейтральная, получается при смешивании 8 г NаOH с 10 г? 5. Сколько граммов NаOH требуется, чтобы осадить в виде всю медь, содержащуюся в 15 сл 1,2 М раствора. 6. Определите молярность и нормальность 4 %раствора Na2CO3 с =1,04 г/мл. Сколько этого раствора потребуется для получения I л углекислого газа? |