Лекции ОХТ для заочников. Лекция 1 Предмет и содержание курса охт
 Скачать 1.88 Mb. Скачать 1.88 Mb.
|
|
Лекция № 4 Сырье в химической промышленности Сырье – исходный материал для производства химического продукта, обладающий стоимостью. Классификация сырья По происхождению сырье бывает природное и синтетическое.  Растительное и животное сырье обычно подразделяют на пищевое и техническое. По запасам сырье бывает возобновляемое (вода, воздух, растительное и животное сырье) и невозобновляемое ( руды, горячие ископаемые). По химическому составу сырье бывает неорганическое (руды, минералы) и органическое (нефть, уголь, природный газ). По агрегатному состоянию сырье бывает твердое (руды, уголь, древесина), жидкое (вода, нефть) и газообразное (воздух, природный газ). Сырье для промышленности органического синтеза - это углеводороды, получаемые из горючих ископаемых (нефти, угля, природного газа). Нефть - это тяжелая маслянистая жидкость, содержащая: 1) парафиновые углеводороды (алканы) газообразные С1 – С4, жидкие С5 – С15 и твердые >С15.; 2) нафтеновые углеводороды (циклоалканы) – моно-, би- и полициклические структуры с боковыми цепями; 3) ароматические углеводороды (арены) – моноциклические (бензол, толуол, ксилолы) и полициклические (нафталин, фенантрен, антрацен и др.); 4) кислородсодержащие соединения (нафтеновые кислоты, фенолы, крезолы и др.); 5) сернистые соединения (сероводород, сульфиды, дисульфиды, меркаптаны, тиофены и др.); 6) азотистые соединения (пиридин, хинолин и их производные); 7) соли минеральных кислот; 8) органические комплексы ванадия, никеля и других металлов; 9) другие соединения. Переработка нефти осуществляется с использованием физических и химических методов в следующей технологической последовательности: 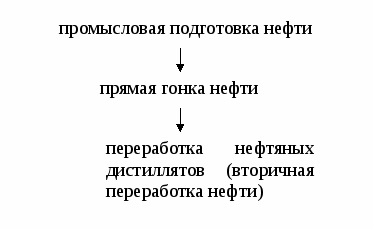 Промысловая подготовка нефти заключается в удалении из нее минеральных примесей (вода, песок, соли), растворенных газов (попутного газа) и легколетучих жидкостей (газового бензина). Нефть освобождается от примесей в ходе следующих операций: 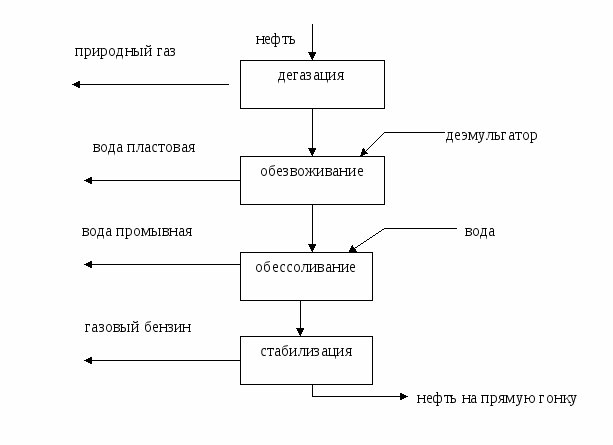 Прямая гонка нефти предназначена для разделения нефти на отдельные фракции, отличающиеся по температурам выкипания. В зависимости от направления использования полученных дистиллятов различают топливный и топливно-масляный варианты прямой гонки. Нефтеперерабатывающие заводы топливного профиля ориентированы только на производство топлив и используют установки прямой гонки АТ (атмосферная трубчатка). При этом получают следующие фракции: - прямогонный бензин , t начала кип. = 1400; - лигроин, tкип. = 140-1800; - керосин, tкип. = 180-2400; - дизельное топливо, tкип. =180-3500; - мазут – > 3500. Прямогонный бензин имеет низкое октановое число и используется в качестве топлива для автомобильных двигателей внутреннего сгорания (карбюраторное топливо) только после добавки соединений, повышающих детонационную стойкость (тетраэтилсвинца, алкилатов, метил-трет-бутилового эфира и др.). Бензин, содержащий тетраэтилсвинец, называется этилированным; он является экологически опасным и запрещен к применению в странах Европы. Большая часть отечественного бензина А-76 содержит тетраэтилсвинец. Бензины АИ-95, АИ-98 относятся к неэтилированным (около 60% от общего количества отечественного бензина). Кроме автомобильных бензинов нефтеперерабатывающая промышленность выпускает также бензины-растворители и бензины-экстрагенты. Лишь незначительная часть бензиновой фракции используется в качестве нефтехимического сырья. Керосин применяют в качестве топлива для авиационных двигателей (реактивное топливо). Дизельное топливо используют для двигателей с воспламенением от сжатия (дизели). Мазут применяют в качестве топлива для паровых котлов, промышленных печей и газовых турбин (котельное топливо, газотурбинное топливо); большая часть его идет на вторичную переработку. Если нефтеперерабатывающий завод ориентирован на топливно-масляный вариант, то, используя установки АВТ (атмосферно-вакуумная трубчатка), кроме перечисленных продуктов получают вакуумный газойль (tкип. = 350-5000 и из мазута под вакуумом отгоняют масляные дистиллаты (трансформаторный, tкип. = 300-4000, машинный, tкип. = 400-4500 и цилиндровый, tкип. = 450-4900). Эти фракции являются основой для получения высококачественных масел. Нефтяные масла в зависимости от направления использования разделяют на: - моторные (для карбюраторных, дизельных и авиационных двигателей); - турбинные; - компрессорные; - индустриальные; - приборные; - электроизоляционные и др. Кроме того, на основе масляных дистиллатов изготавливают смазки (консистентные, атифрикционные, фрикционные, протекционные, диспергирующие и др.) и специальные жидкости (охлаждающие, гидравлические, антикоррозионные и др.). Остаток вакуумной перегонки, выкипающий выше 5000 – гудрон, используют для получения битумов (дорожных, строительных, изоляционных), а также в качестве сырья в процессах коксования и деасфальтизации. Из дистиллатов прямой гонки нефти получают такие нефтепродукты как парафин, церезин, нафтеновые кислоты, нафталин и др. Наиболее ценные компоненты нефти – «светлые» нефтепродукты, выкипающие при температуре ниже 3500 при атмосферном давлении. Они находят наиболее широкое применение. Однако их содержание в нефти невелико, не более 45% (бензин 17%, керосин 10-%, дизельное топливо 17%). Поэтому так называемые «тяжелые» фракции нефти подвергают специальной переработке, заключающейся в уменьшении молекулярной массы и химического состава углеводородов с целью снижения их температур кипения. Применяемые при этом процессы называют вторичными и по своей природе они, в отличие от первичной переработки нефти, являются химическими. В основе всех этих процессов лежат следующие реакции: - реакции расщепления связи С-С с образованием алканов и алкенов с более короткой цепочкой; - реакции расщепления связи С-Н с образованием алкенов с той же длиной цепи и молекулярного водорода; - реакции изомеризации; - реакции полимеризации, конденсации, алкилирования и др., приводящие к укрупнению молекул. Все эти реакции являются радикальными; вклад каждого типа реакций зависит от условий проведения процесса и состава нефтяной фракции, подвергающейся переработке. Различают термические и каталитические вторичные процессы. Назовем самые важные вторичные процессы переработки нефти: 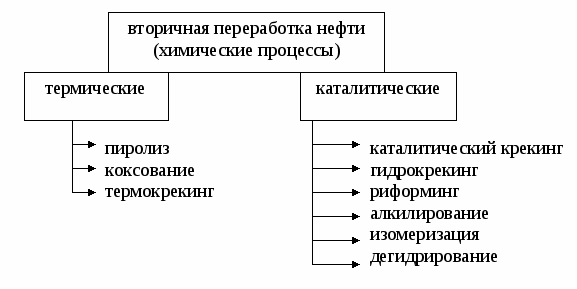 Термокрекинг – расщепление тяжелых углеводородов при их нагревании до 450-5000С без доступа воздуха, под повышенным давлением. Это наиболее старый метод вторичной переработки; разработан в 1890 г. В.Г. Шуховым. В настоящее время термокрекинг имеет ограниченное применение. Его используют для получения котельного топлива из гудрона (висбрекинг) и в некоторых других случаях. В промышленности в зависимости от конкретных условий используют жидкофазный и парофазный крекинг, а также пиролиз как особый вид высокотемпературного крекинга (600-9000С), осуществляемого из различных видов сырья с целью получения олефинов, прежде всего, этилена и пропилена. Коксование – высокотемпературное (600-11000С) разложение гудрона и тяжелых нефтяных остатков с целью получения нефтяного кокса (материал для производства электродов и металлургическое топливо). Коксование проводят в таких условиях, при которых происходит реакция конденсации продуктов термического распада углеводородов. Использование катализатора меняет механизм реакций разложения на ионный, это в сотни и тысячи раз увеличивает скорость некоторых реакций. Применение катализаторов позволяет снизить температуру процессов распада и менять относительный вклад отдельный реакций, т.е. направлять процесс преимущественно в направлении получения требуемых продуктов. 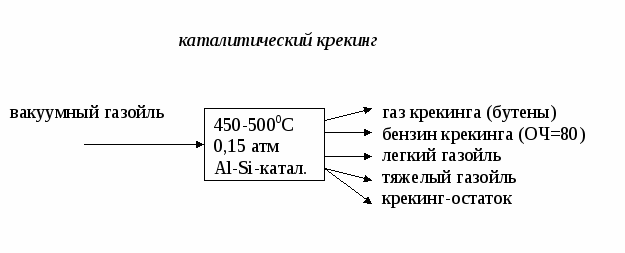 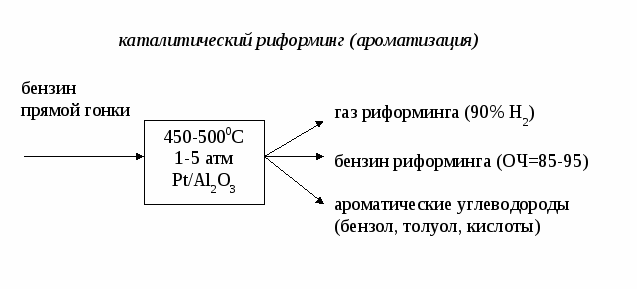 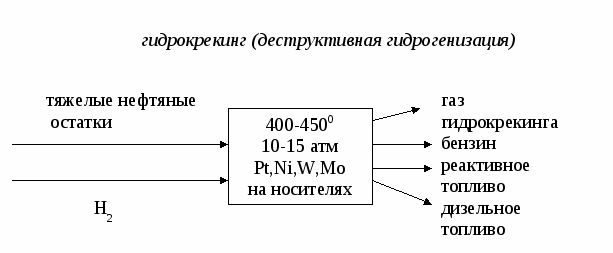 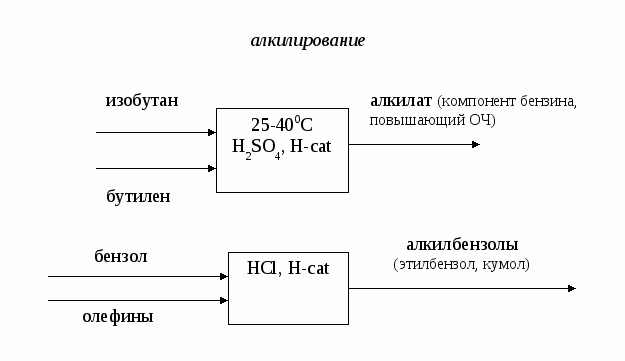 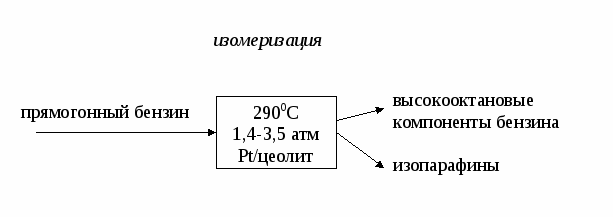 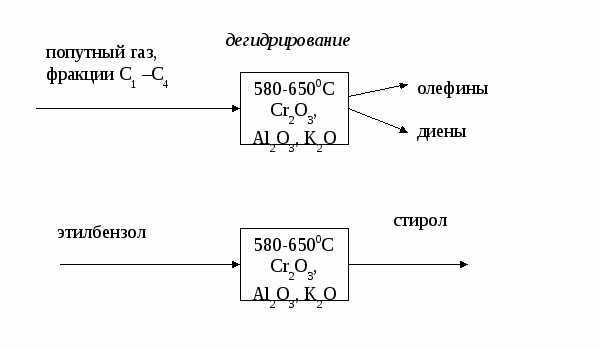 Углеводородные газы Углеводородные газы являются более перспективным видом сырья, чем нефть, так как характеризуются лучшими экономическими показателями, более высокой технологичностью, легко транспортируются, содержат меньше примесей и перерабатываются по непрерывным легко автоматизируемым технологическим схемам. По происхождению углеводные газы делятся на природные, попутные и нефтезаводские. Природные газы добываются из пластов, не содержащих нефть, и содержат 80-98% метана, 0,5-2% углеводородов С2-С4 и не более 0,7% углеводородов С5, Н2S и СО2. Различают тощие (96-98% метана) и жирные (менее 96% метана) природные газы. В группу природных газов включают также газы газоконденсатных месторождений. При добыче из них выделяется конденсат, содержащий жидкие углеводороды и значительное количество сероводорода. Из природных газов получают формальдегид, уксусную кислоту, синтез-газ, водород, ацетилен, сажу, метанол, растворители и хладоагенты (хлор- и фторпроизводные метана), нитросоединения и др. Большое количество природных газов используется в качестве бытового и промышленного топлива. Попутные газы добываются вместе с нефтью в количестве порядка 50 м3/т. Они относятся к группе жирных газов, так как содержат значительное количество гомологов метана. Многие попутные газы содержат также благородные газы (гелий и аргон). Из попутных газов получают олефины, диены, благородные газы и используют в качестве топлива. Предварительно попутные газы разделяются на отдельные компоненты и газовый бензин на газофракционирующих установках (ЦГФУ) газобензиновых заводов. Нефтезаводские газы образуются в процессах вторичной переработки нефти и угля; состав этих газов и направления их использования зависят от их происхождения. В каталитических процессах выход газов составляет 15-20%, в термических – 7-8%. Уголь Этот вид сырья является альтернативой нефти и газу, запасы которых быстро истощаются. Уголь содержит органическую и неорганическую часть. Органическая часть представляет собой макроциклические полимеры сложного состава и строения. Неорганическая часть представлена производными кремния, алюминия, кальция, железа. Основные процессы переработки угля – пиролиз (коксование и полукоксование), ожижение и газификация. Пиролиз– нагрев угля до 500-6000С (полукоксование) или до 900-12000С (коксование) без доступа воздуха. При этом образуется некоторое количество горючего газа, выделяются жидкие углеводороды, в основном, ароматические и получается кокс для металлургической промышленности. Ожижение (гидрогенизация) осуществляется с целью получения искусственной нефти, которую затем перерабатывают в моторные топлива. Уголь в виде пасты гидрируется водорододонорными растворителями в присутствии катализаторов. Газификация твердого топлива производится с целью получения искусственного газообразного топлива, восстановительных газов, синтез-газа (СО + Н2). Суть процесса заключается в пропускании через раскаленный уголь газов различной природы. При использовании паров воды получают водяной газ, воздуха и кислорода – паровоздушные и парокислородные газы; иногда используют СО2, Н2 и другие газы. Процессы газификации могут быть термическими и каталитическими. Сырье для промышленности неорганического синтеза Промышленность неорганического синтеза использует, в основном, минеральные виды сырья рудного и нерудного типа. Переработка такого вида сырья начинается с обогащения. Обогащение – это совокупность физических и физико-химических методов повышения содержания основного компонента. При этом нужный минерал получают в виде концентрата, а примеси и пустую породу - в виде отхода («хвостов»). В тех случаях, когда в сырье содержится несколько полезных составляющих, его делят на отдельные части (фракции), обогащенные тем или иным компонентом. Методы обогащения сырья зависят от его фазового состояния. Для твердого сырья используют следующие методы: - гравитационное обогащение, основанное на различие скорости осаждения частиц в жидкости или газе в зависимости от плотности или размера этих частиц. Осаждение в жидкости (чаще всего в воде) называют мокрым обогащением, в газе (чаще всего в воздухе) – сухим гравитационным обогащением. Мокрое обогащение осуществляют в классификаторах, сухое – в воздушных сепараторах различного устройства. - рассеивание (грохочение), основанное на различной прочности отдельных компонентов сырья, вследствие чего при дроблении они дают частицы разного размера. Измельченное сырье просеивают через сита с отверстиями разного размера. - флотация, основанная на различной смачиваемости частиц отдельных минералов водой. Несмачиваемые частицы остаются на поверхности, смачиваемые – опускаются на дно аппарата. Для усиления разницы в смачиваемости применяют флотореагенты – вещества, уменьшающие (олеиновая кислота, нафтеновые кислоты и др,) или увеличивающие (щелочи, соли щелочных металлов и др.) смачиваемость. - магнитная сепарация – отделение магнитовосприимчивых материалов от немагнитных. - электростатическое обогащение (сухое и мокрое), основанное на разнице электропроводности различных компонентов сырья. - термическое обогащение, основанное на разности температур плавления или возгонки. - химическое обогащение, основанное на разном отношении к химическим реагентам. Жидкое сырье концентрируют - упариванием растворителя; - вымораживанием; - выделением примесей в осадок; - выделением примесей в газовую фазу. Газовые смеси разделяют на компоненты - последовательной конденсацией, то есть, переводя их в жидкое состояние при постепенном понижении температуры и сжатии; - последовательным испарением, когда газовую смесь сначала полностью конденсируют, а затем, постепенно повышая температуру, переводят отдельные компоненты смеси в газовое состояние; - поглощением отдельных компонентов смеси жидкостью (абсорбцией) или твердыми веществами (адсорбцией) с последующим выделением их из сорбентов в концентрированном виде. Воздух Воздух в химической технологии используется в качестве: - сырья в процессах окисления, при получении кислорода, азота, благородных газов; - окислителя при получении тепловой энергии (сжигании топлива); - теплоносителя и хладоагента; - для перемешивания и распыления жидкостей. Степень и способ очистки воздуха зависит от характера его применения. Обычно его очищают от пыли и влаги, а при использовании воздуха в качестве сырья – от контактных ядов. Вода Современная химическая промышленность является крупнейшим потребителем воды. По объему водопотребления химический завод средней мощности может быть приравнен к городу с 800 тысячным населением, т.е. 10-20 млн. м3 в год. Вода используется как: - реагент (в процессах гидратации, гидролиза, в производстве Н2 и др.); - промывной агент; - растворитель; - разбавитель (в процессах пиролиза, крекинга, дегидрирования и др.); - теплоноситель (перегретая вода, водяной пар, хладоагент). Вода является самым распространенным на Земле соединением. Но запасы пресной воды, пригодной для использования, составляют всего 0,3% объема гидросферы. Все природные воды обычно подразделяют на атмосферные, поверхностные и подземные. Атмосферные воды выпадают на землю в виде дождя и снега. Они содержат наименьшее количество примесей. В основном, это растворенные газы (кислород, углекислый газ, азот и др.), соли, бактерии. Атмосферные воды используются как источник водоснабжения только в безводных и засушливых районах. Поверхностные воды – это воды открытых водоемов : рек, озер, морей. В состав этих вод входят разнообразные минеральные и органические вещества. Подземные воды – воды артезианских скважин, колодцев, ключей, гейзеров. Они характеризуются значительным содержанием минеральных солей. В зависимости от солесодержания природные воды подразделяют на: - пресные (до 1 г/кг солей), - солоноватые (1-10 г/кг), - соленые (более 10 г/кг). Природные воды представляют собой сложную динамическую систему, содержащую газы, минеральные и органические вещества, находящиеся в истинно растворенном, коллоидном или взвешенном состоянии. В истинно растворенном состоянии находятся, в основном, минеральные соли, содержащие катионы Са2+, Мg2+, Na+ , К+ и анионы SO42-, CO32-, HCO3-, Cl-. В виде недиссоциированных молекул могут находиться некоторые органические соединения, а также растворенные газы (О2, СО2, Н2S и др.). В коллоидном состоянии в воде находятся недиссоциированные и малодиссоциированные соединения алюмо- и железосиликатов, гидроксид железа, кремниевая кислота и др., различные органические соединения. Органические коллоиды состоят, в основном, из гуминовых кислот, фульвокислот, лигнина, протеина, клетчатки, различных смол и других сложных соединений. Во взвешенном состоянии природные воды содержат глинистые, песчаные, известковые и гипсовые частицы. Они могут также содержать живые организмы в виде различных бактерий, грибков, водорослей и т.п. В зависимости от назначения потребляемая вода условно подразделяется на промышленную и питьевую; содержание примесей в них регламентируется соответствующими стандартами. Пресная природная вода используется без предварительной очистки в процессах первичной обработки сырья, для охлаждения продуктов и аппаратов и для различных вспомогательных операций. Во всех остальных случаях она подвергается очистке различными методами в зависимости от характера примесей и предъявляемых требований. Можно выделить следующие группы методов очистки воды: - механические методы: 1) отстаивание – осаждение песка и тяжелых минеральных примесей под действием силы тяжести; 2) фильтрация (через кварцевый песок, коксовую мелочь, мраморную крошку, неактивный уголь и др.) – выделение тонкодисперсных соединений; Особым видом фильтрации являются ультрафильтрация и обратный осмос (мембранные методы). Это наиболее современные способы очистки воды. Мембраны задерживают частицы размером 0,05-0,1 мкм, что позволяет отделить мелкодисперсные или даже растворенные частицы. Ультрафильтрация очень часто используется для разрушения эмульсий. Мембраны могут быть уплотняющие (полимерные), жесткие (металлические, керамические, стеклянные) и динамические (получаемые путем нанесения разделяющего слоя на пористую подложку до или в процессе фильтрации). Наиболее распространены полимерные мембраны. Ультрафильтрация и обратный осмос проводятся под давлением и отличаются друг от друга его величиной. Поскольку при обратном осмосе используются мембраны, обладающие меньшей проницаемостью для молекул растворителя, этот метод требует более высоких давлений. - механо-химические методы: 1) коагуляция – адсорбция мелкодисперсных примесей на хлопьях коагулянта и их совместное осаждение. Для ускорения процесса к воде добавляют флокулянты (например, полиакриламид), которые способствуют слипанию и укрупнению хлопьев коагулянта. Наиболее распространенными коагулянтами являются сульфаты алюминия и железа в присутствии едкого натра или извести. 2) флотация – выделение гидрофобных частиц примесей вместе с пузырьками воздуха и удаление их с поверхности воды. - термические методы: 1) кипячение; 2) дистилляция – последовательное испарение воды с конденсацией пара; - физические методы: 1) радиационный метод, основанный на разрушении примесей излучениями высоких энергий; 2) магнитная обработка, используемая для предотвращения образования накипи; 3) вымораживание; 4) ультрафиолетовое облучение; 5) ультразвуковая обработка. - физико-химические методы: 1) метод ионного обмена, основанный на способности некоторых материалов, обмениваться ионами с водой. Такими материалы называют катионитами или анионитами. Катиониты отдают воде катион натрия (Na-катиониты) или катион водорода (Н-катиониты); аниониты - ОН- группу. Обмен ионов кальция и магния на Na+ или Н+ называется умягчением воды, процесс полного освобождения воды от ионов – обессоливанием. - химические методы: 1) хлорирование; 2) озонирование; 3) насыщение ионами серебра; 4) известково-содовый метод умягчения жесткой воды; 5) фосфатный метод умягчения жесткой воды; 6) каталитическое сжигание. Первые три метода обычно используются для обеззараживания питьевой воды; последний - для обезвреживания очень загрязненных стоков. - биохимические методы: 1) аэробный (в присутствии кислорода) 2) анаэробный (без кислорода). Эти методы используются для очистки стоков и основаны на способности микроорганизмов использовать в качестве источников питания неорганические и органические соединения, содержащиеся в воде. - биогидроботанический метод - доочистка воды в биологических прудах перед сбросом в водоемы. Выбор и обоснование сырьевой базы При выборе сырья для производства химического продукта следует учитывать: - ожидаемый объем производства, который определяет объем потребляемого сырья. Следует убедиться в наличии достаточных запасов сырья. - стоимость и доступность сырья; возможность и целесообразность его транспортировки. - ресурсоемкость сырья. Переработка различного сырья требует использования разных технологических схем, а, следовательно, разного количества материальных, энергетических и трудовых ресурсов. - содержание полезного компонента в сырье. Наличие примесей создает ряд проблем и требует дополнительных затрат на концентрирование и очистку сырья или разделение реакционной смеси и очистку целевого продукта. Также нежелательны колебания в составе сырья; они приводят к нарушению технологического режима, снижению производительности установки и качества целевого продукта. - число химических стадий. Выбранное сырье должно перерабатываться по технологии с минимальным числом стадий. - количество побочных продуктов. Количество побочных продуктов должно быть минимальным или побочные продукты должны находить применение в качестве вторичного сырья. - возможность утилизации тепла и других видов энергии при переработке выбранного вида сырья. - количество стоков и выбросов. Большое количество стоков и выбросов приводит к загрязнению окружающей среды; очистка и нейтрализация их повышает затраты на производство продукта. - переработка сырья должна проводиться с высокой скоростью, конверсией и селективностью. |
