ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савельева. ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савель. Media medica 2003 п од редакцией академика B. C. Савельева
 Скачать 9.44 Mb. Скачать 9.44 Mb.
|
|
История вопроса Первое вмешательство по поводу опухоли левой доли печени было выполнено в 1887 г. немецким хирургом Карлом Лангенбушем. В то же время регулярные элективные оперативные вмешательства на печени по поводу метастазов злокачественных опухолей стали производиться лишь в 70-80 годы прошлого столетия. Это было связано с несколькими факторами. К этому периоду был накоплен опыт консервативного лечения метастазов в печени различного генеза, который свидетельствовал о неудовлетворительных результатах различных вариантов изолированного химиотерапевтического и лучевого воздействия. В то же время анализ результатов резекций печени говорил о возможности значительного продления жизни при ряде онкологических заболеваний, сопровождавшихся метастазами в печени. Первые клинические классификации метастазов в печени были предложены Pettavel (1978), Taylor (1981) и Gennari (1982, 1985). КI стадии метастатического поражения печени относят единичный метастаз, занимающий не более 25% объема печени, ко II стадии - множественные и билобарные метастазы объемом не более 25% , а также единичный метастаз объемом от 25 до 50%, к III стадии -множественные и билобарные метастазы объемом 25-50%, а также метастазы общим объемом более 50% (LGennari et al., 1982; 1985). В последние годы при колоректальных метастазах в печени стали чаще использовать m TNM-классификацию, предложенную S.C.Iwatsuki и соавт. в 1986 г. Мы в своей практике предпочитаем mTNM-клас-сификацию, позволяющую более точно оценить стадию процесса и его прогноз. До сих пор отсутствует единая классификация неколоректальных ме- тастазов, в этих случаях целесообразно использовать классификацию Gennari. Единый подход к классификации крайне важен для сравнения результатов лечения в различных клиниках. Первые работы, обобщающие данные по терапии метастатического рака печени, были представлены MAAdson, J.A. van Heerden (1980) и G.H.Foster, J.Lundy(1981). Этиология и патогенез При метастазировании злокачественных опухолей различной локализации наиболее часто поражается печень. По секционным данным, метастазы в печени выявляются у 36% больных со злокачественными опухолями (Foster G.H., LundyJ., 1981). Наиболее частыми первичными очагами при этом являются опухоли толстой и тонкой кишки, желудка, поджелудочной железы, гениталий. Реже в печень метастазируют злокачественные опухоли почек, простаты, легких, кожи, мягких тканей, костей и головного мозга. Наиболее частыми путями распространения злокачественных клеток являются лимфогенный и гематогенный. В этой связи большое значение имеет абластичное выполнение операций по поводу первичных опухолей (лимфодиссекция, предварительная перевязка сосудов, кровоснабжающих резецируемый орган), а также системная химиотерапия после радикальных оперативных вмешательств. Скорость роста метастазов определяется прежде всего биологией первичной опухоли, а также состоянием иммунной системы пациента. Многочисленные исследования показали, что метастазы имеют преимущественно артериальное кровоснабжение, индуцируют неоангиогенез с формированием патологических сосудов. Быстрый рост метастазов в виду активного метаболизма и деления опухолевых клеток приводит к ишемии в центральных участках узлов с их последующим некрозом. Соотношение процессов роста, некроза и перифокальной реакции здоровой паренхимы печени обусловливает разнообразие семиотики метастатических образований по данным ультразвукового исследования (УЗИ), компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ). 194 абдоминальная хирургия Время удвоения метастазов колоректального рака в печени составляет от 50 до 112 дней, при этом большая часть МТС выявляется при размерах 1 см* (10 млрд клеток). Таким образом, если объем очага составляет 1 мм^, то его теоретически можно выявить через 10 мес (Bozzetti F. et al., 1987). Диагностика метастазов в печени При выявлении очагов в печени следует иметь в виду, что в 95% случаев опухолевого поражения печени оно является метастатическим. Это правило относится прежде всего к Европейским странам. В странах Юго-Восточного региона преобладающей патологией является первичный рак печени. Онкологическая настороженность особенно важна у больных, ранее оперированных по поводу злокачественных опухолей. Регулярные динамические обследования в группах высокого риска позволяют выявлять метастазы на ранних стадиях, что влияет на результаты лечения. Диагностика метастазов включает обязательное выполнение комплексного ультразвукового исследования, спиральной компьютерной томографии (СКТ), а также определение уровня опухолевых маркеров. Для колоректальных метастазов при УЗИ характерным признаком является симптом "бычьего глаза" и наличие кальцинатов (рис.1), при СКТ - не- ровность и неоднородность контрастирования и появление гиперконтрастного ободка в артериальную фазу (рис.2). Метастазы рака яичника и матки могут иметь кистозно-солидную структуру (рис.3). Метастазы хорошо васкуляризированы, что подтверждается при СКТ, ангиографии (рис.4) и цветном дуплексном картировании (рис.5). Трудности диагностики возникают при небольших ги-пер- и гипоэхогенных метастазах, когда их приходится дифференцировать с гемангио-мами, кистами и абсцессами печени. В данной ситуации целесообразно произвести пункцион-ную биопсию печени, чувствительность последней при МТС составляет, по нашим данным, 94,2%, специфичность - 100%, общая точность - 94,4%. Для исключения метастатического поражения костной системы выполняется сцинтиграфия скелета, детально обследуются легкие и желудочно-кишечный тракт. При перенесенных ранее вмешательствах на прямой кишке показана компьютерная томография органов малого таза для исключения местного рецидива. При массивном унилобарном метастатическом поражении печени в предоперационном периоде возможно выполнение химиоэмюолизации, а также портальной эмболизации пораженной доли с целью стимуляции регенерации непораженной части печени.  Рис. 1. УЗИ-картина при МТС колоректального рака Р 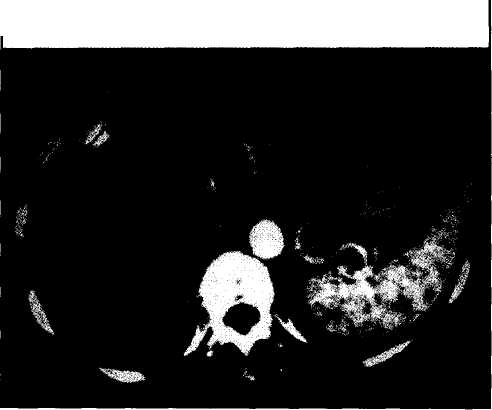 ис.3. УЗИ и СКТ при метастазах кистозно-солидной структуры. ис.3. УЗИ и СКТ при метастазах кистозно-солидной структуры.  Рис.2. СКТ. Артериальная фаза. Метастазы в печени. Р  ис.4. Ангиографическая картина при МТС в печени. ис.4. Ангиографическая картина при МТС в печени. 195 абдоминальная хирургия   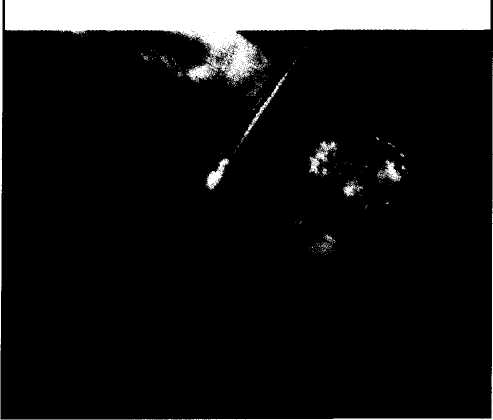 Рис.7. ИОУЗИ при МТС в печени. Рис.5. Цветное дуплексное картирование. МТС в печени. Рис.6. Стандартная анатомическая резекция печени (момент операции). 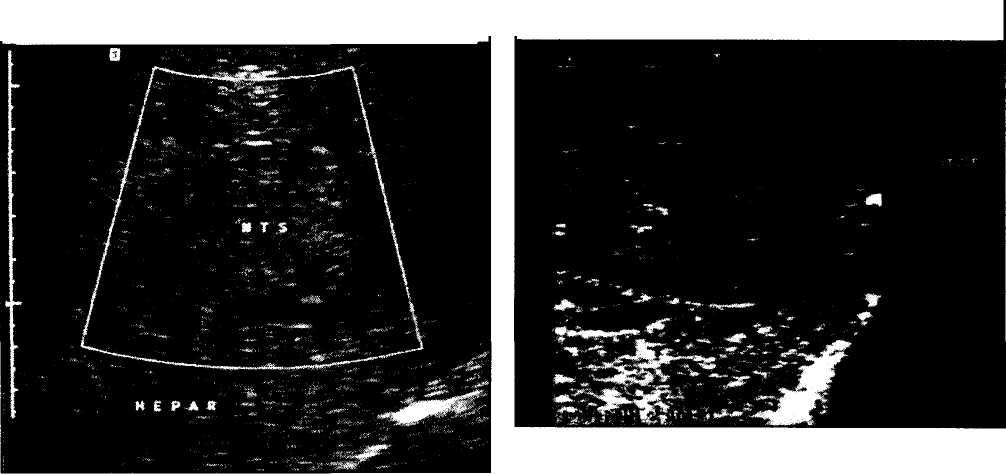 Принципы хирургического лечения Принципы хирургического лечения Резектабельность метастазов печени, по данным различных авторов, составляет от 25 до 30% (D.A. August et al, 1985). В большинстве случаев показанием к выполнению резекции печени являются метастазы колоректального рака, реже - злокачественных опухолей тонкой кишки, почек, надпочечников, желудка, молочных желез, матки, яичников, поджелудочной железы и меланомы (Iwatsuki S. et al., 1989). Противопоказанием к оперативному вмешательству является наличие отдаленных внепеченочных метастазов. В то же время при вовлечении в процесс таких органов, как диафрагма, надпочечник и почка, возможно выполнение сочетанных операций. Другими необходимыми условиями резекции печени по поводу ее метастатического поражения являются радикальное удаление первичного очага, а также достаточные функциональные резервы остающейся печени. Вариант резекции определяется размерами, расположением и числом метастатических узлов, их соотношением с трубчатыми структурами печени. Неанатомические резекции печени выполняют при поверхностно расположенных «легко доступ- ных» метастазах размерами не более 5 см. При глубоко расположенных метастазах размером более 5 см необходимо проведение стандартных анатомических резекций печени (рис.6). Сегментэктомии в различных сочетаниях выполняются при циррозе печени, когда операции большего объема не переносимы или при изолированном поражении сегментов печени. Радикальными следует считать те операции, при которых резекция выполняется на расстоянии не менее 1,0 см от видимых границ опухоли. Основные моменты хирургического вмешательства Операция выполняется из стандартного J- или Т-образного доступа. При операциях по поводу метастатического поражения печени прежде всего необходима тщательная ревизия органов брюшной полости и забрюшинного пространства с целью исключения отдаленных метастазов и местного рецидива первичной опухоли. После визуальной и пальпаторной оценки печени обязательным является проведение интраоперационного ультразвукового исследования (ИОУЗИ). ИОУЗИ позволяет вьывить небольшие (менее 1,0 см) глубокие метастазы, не выявленные до операции, что в 10-15% случаев приводит к необходимости изменения предварительно намеченного плана операции (рис.7). Важным этапом является лимфаденэктомия из гепатодуоденальной связки. Дальнейшие этапы операции зависят от варианта предпринимаемой резекции печени и мало отличаются от таковых при операциях по поводу поражений печени другого генеза. Использование атравматичной сосудистой хирургической техники, предварительная сосудистая изоляция удаляемого участка печени, применение кавитационного ультразвукового хирургического аспиратора, аргон усиленной коагуляции, а также пленкообразующих клеющихся композиций позволили значительно уменьшить объем интраопе-рационной кровопотери и риск оперативного вмешательства. Операция завершается контрольным ИОУЗИ печени и дренированием брюшной полости. После получения данных гистологического исследования окончательно устанавливается стадия метастатического поражения печени, что опреде- 196 абдоминальная хирургия ляет прогноз заболевания и необходимость проведения того или иного варианта комбинированного лечения. Особенности послеоперационного ведения В первые часы после операции проводится непрерывное мониторирование основных жизненно важных функций (давление, пульс, сатурация крови, ЦВД, КЩС, гемоглобин и гематокрит, почасовой диурез), контроль отделяемого по дренажам. Особое значение придается ранней экстубации больных, сбалансированному парентеральному и энте-ральному питанию. При резекциях печени большого объема отмечается значительное снижение синтетической функции печени, в связи с чем необходима коррекция гипоальбуминемии, переливание коллоидных и кристаллоидных растворов, а также аминокислот и витаминов. Крайне важным является регулярное ультразвуковое исследование брюшной и плевральных полостей с целью раннего выявления жидкостных скоплений в зоне операции. При значимых скоплениях жидкости проводятся пункция и эвакуация содержимого под УЗИ-контролем с последующим бактериологическим исследованием. Дренажи из брюшной полости, как правило, удаляются на 5-7-е сутки. При благоприятном течении, больные на 2-3-и сутки после операции переводятся из палаты интенсивной терапии в обычную палату и выписываются из стационара на 14-17-е сутки. Перед выпиской у больных после резекции печени по поводу метастатического поражения обязательно определяется уровень специфического для конкретной патологии онкомаркера, что важно для последующего динамического наблюдения. Регулярное обследование больных осуществляется 1 раз в 3 мес на протяжении первых 2 лет после вмешательства. При метастатических поражениях печени III-IVA стадиЬ в обязательном порядке проводится системная химиотерапия. Ближайшие перспективы развития хирургии метастазов в печени Частота послеоперационных осложнений составляет от 19 до 43%. Послеоперационная летальность колеблется в пределах от 4 до 7%. При этом летальность у больных с сопутствующим циррозом печени составляет 37%, в то же время при отсутствии цирроза - 2% (Iwatsuki S. et al, 1989). Средняя продолжительность жизни при метастатическом поражении печени без лечения составляет 6 мес. Системная химиотерапия увеличивает продолжительность жизни до 9— 12 мес. Разительный контраст представляют результаты оперативного лечения. Продолжительность жизни от 1 года до 5 лет после операций по поводу метастазов колоректального рака составляет 90, 69, 52, 40 и 37%. Практически столько же живут больные, оперированные по поводу метастазов из других первичных источников: 75, 54,47, 38 и 20%. Разница в продолжительности жизни при этом статистически не достоверна (Iwatsuki S. et al., 1989)- Продолжительность жизни после операций по поводу солитарных и множественных метастазов достоверно не отличается, однако при количестве метастазов 4 и более она достоверно ниже. При анализе продолжительности жизни при колорек-тальных метастазах в зависимости от стадии первичной опухоли была выявлена достоверная разница между группами В и С по Дюку и отсутствие различий между С и D (синхронные с первичной опухолью метастазы в печени). При этом 5-летняя продолжительность жизни при стадии В составила 36%, при С - 25% (Iwatsuki S. et al., 1986). Статистически достоверные различия в длительности жизни после операции отмечены при различных стадиях метастатического поражения печени. При I стадии 3 года живут 73% больных, оперированных по поводу метастазов колоректального рака, при II стадии - 60%, при III стадии - 29%. При сравнении продолжительности жизни в зависимости от объема операции, худшие результаты были отмечены при расширенных гемигепатэктомиях по сравнению с лобэктомиями и резекциями печени меньшего объема. Длительность жизни после лобэкто-мий, левосторонних латеральных сегментэктомий и краевых резекций печени была одинаковой. Это объясняется тем, что расширенные резекции печени предпринимаются по поводу больших, центрально расположенных метастазов, тогда как краевые резекции - при небольших периферических поражениях. При проведении системной химиотерапии после резекции печени до появления признаков рецидива заболевания была отмечена большая продолжительность жизни, чем в группе больных, которые ее не получали. Продолжительность жизни после резекции печени по поводу ее метастатического поражения не отличается в различных возрастных группах, а также не зависит от половой принадлежности. Продолжительность жизни без рецидива метастазов составляет 9-Ю мес, 2 года без рецидива живут 46% больных, перенесших резекцию печени по поводу ее метастатического поражения, 3 года - 28%. У всех больных с III стадией метастазов печени отмечается рецидив в пределах 2 лет после резекции печени, в те же сроки при I стадии рецидив отмечается лишь в 28%. В среднем интервалы времени от операции до возникновения рецидива при I, И и III стадиях составляют соответственно 15,9 и 7 мес. В 39% случаев местом повторного метастазирова-ния является печень, в 17% - легкие, в 21% - малый таз, в 13% - ретроперитонеальные лимфатические узлы, в 3,5% - головной мозг. Наиболее часто рецидивы возникают при раке прямой кишки (75%). В ряде случаев даже после обширных резекций печени возможно выполнение ререзек-ций при повторном метастазировании. В последние годы оперативное лечение метастазов печени все шире комбинируется с региональной химиотерапией, внутрипортальной и внутричревной химиоэмболизацией, чрескожной алкоголизацией, криодеструкцией и СВЧ- и лазер-деструкцией небольших метастатических узлов, а также имму-номоделирующей терапией. Несмотря на большое количество публикаций, свидетельствующих о бесспорной эффективности хирургического лечения метастазов печени, до сих пор в среде врачей бытует мнение о фатальности поражения, в связи с чем значительное количество больных не направляются в специализированные гепатологические стационары и центры. Введение семинаров по хирургической гепатологии в программы высших меди- 197 абдоминальная хирургия цинских заведений, а также факультетов усовер шенствования врачей различных специальностей позволит значительно улучшить результаты лече ния пациентов с онкологическими заболеваниями. Перспективные направления исследований на ходятся в области ранней диагностики метастазов печени, разработке мультимодальных методов те рапии, в том числе и малоинвазивных методов ле чения первичных и рецидивных метастазов в пече ни. Необходимо проведение мультицентровых ис следований по согласованным протоколам, только такой подход позволит выработать оптимальный алгоритм терапии метастатического поражения печени. , Литература
patients with colorectal cancer // Cancer., 1985.- Vol 55- P. 1490-4.
10. Taylor I. Stadies on the treatment and prevention of colorectal liver metastases// Ann.R. Coll.Surg. Eng.,1981.- Vol.63- P. 270-6.  Хирургическое лечение желчно-каменной болезни Хирургическое лечение желчно-каменной болезниA.M. Шулутко  Лечение желчно-каменной болезни (ЖКБ) сегодня пока еще является в основном хирургической проблемой, хотя целый ряд ситуаций требуют интегрального решения с привлечением терапевтов, эндоскопистов, рентгенологов и других специалистов. |
