Хирургия печени и желчных путей. Нежизнеспособности ее у больного или для борьбы с тяжелой печеночной недостаточностью
 Скачать 11.68 Mb. Скачать 11.68 Mb.
|
|
Иннервация печени осуществляется из 2 источников. Элементы парасимпатической системы идут от правого блуждающего нерва. Симпатическая иннервация происходит за счет веточек pi. sollaris, главным образом через правый п. splanchi- Рис. 4. Схема вариантов начала и хода пузырной артерии (по Rio—Branco). cus. Веточки солнечного сплетения, оплетая печеночную артерию, образуют plexus hepaticus. Из правой веточки сплетения, идущей к желчному пузырю, образуется пузырное сплетение. Такие же веточки симпатической системы идут к холедоху, располагаясь на боковой и задней его поверхности. Веточки блуждающего нерва вплетаются в указанные сплетения, проходя предварительно через солнечное сплетение, и не отличаются от симпатических волокон. Желчевыводящая система печени. Печеночная ткань состоит из множества долек, разделенных между собой прослойками соединительной ткани,в которой проходят желчные протоки, разветвления воротной вены, печеночной артерии и нервов, оплетающих дольки густой сеткой. Печеночные клетки в дольках расположены так, что один полюс их обращен к кровеносным сосудам, другой — к желчным канальцам. Внутрипеченочные желчные ходы идут параллельно разветвлениям воротной вены и печеночной артерии, соединяясь между собой, образуют более крупные внутрипеченочные протоки и в конечном итоге формируют внеорганные печеночные протоки для правой и левой долей печени. Установлено, что в правой доле для оттока желчи из переднего и заднего сегмента имеется 2 главных протока — передний сегментарный и задний, которые в свою очередь образовались из слияния протоков верхних и нижних зон — субсегментов. Передний и задний протоки распространяются к воротам печени, причем задний расположен несколько выше и является более длинным. Сливаясь, они образуют правый печеночный проток. В ряде случаев (28 %) слияния не происходит, и нижний сегментарный проток рассматривается как правый дополнительный печеночный, что является неправильным, так как в этих случаях проток не является дополнительным — он осуществляет отток желчи из определен- ного участка печени. Часто в ложе желчного пузыря можно найти тонкий проток, осуществляющий отток из V сегмента правой доли и имеющий непосредственную связь с правым печеночным протоком. Повреждение его во время холецистэктомии является нежелательным. Прямого сообщения этого протока с желчным пузырем не установлено. Отток желчи из левой доли, подобно правой, осуществляется по 2 сегментарным протокам — латеральному и медиальному. Латеральный сегментарный проток осуществляет отток желчи из левой анатомической доли и образуется путем слияния протоков верхних и нижних зон. Место слияния расположено по линии левой сагиттальной борозды (в 50%) или несколько правее от нее (42 %), (Schwartz, 1964). Медиальный проток образуется из нескольких протоков верхних и нижних зон (обычно по 2) и присоединяется к латеральному в воротах печени, образуя левый печеночный проток. В хвостатой доле протоки делятся на 2 системы. Из правого отдела желчь оттекает в правый печеночный проток, из левого — в левый. Вну-трипеченочного сообщения между левым и правым печеночными протока- ми в области хвостатой доли не установлено. Печеночныепротоки(ductus he-paticus dex. et sin). Обычно слияние левого и правого протока хотя и происходит чаще (у 95% больных) вне печени в 0,75 — 1,5 см от ее поверхности, а иногда и дальше, все же у ряда больных (5%) слияние происходит в печеночной паренхиме (И. М. Тальман, 1965). Левый печеночный проток шире и длиннее правого. Диаметр левого печеночного протока 4—5 мм, длина — 2,5—5 еж с колебаниями от 1 до 10 см. Расположен левый печеночный проток впереди правого края воротной вены, спереди его довольно часто перекрещивает пузырная артерия и правая ветвь печеночной артерии. Левый печеночный проток собирает желчь из I, II, III, IV сегментов печени, правый дренирует V, VI, VII, VIII сегменты. Хотя следует оговориться, что I сегмент отдает веточки желчных ходов, впадающие непосредственно и в левый, и в правый печеночные протоки. Изучение внутрипеченочной архитектоники желчных протоков и проекций этих протоков на поверхности печени (А. Ф. Ханжинов, 1958; Г. Е. Островерхов, В. В. Виноградов, В. Ф. Забродская, 1966; А. И. Краковский, 1966) послужило основанием для создания точных схем отыскивания наиболее доступных внутрипеченочных протоков и создания билиодегистивных анастомозов (о чем речь будет идти в соответствующей главе). Указанные исследования потребовали пересмотра вопроса о резекции части печени и целой доли для отыскивания внутри-печеночных желчных протоков, предлагаемые Е. С.Футуряноми Б. М.Шубиным (1966), Longmire (1948), Couinaud (1953), Dogliotti (1958). Общий печеночный проток. После слияния в воротах печени правого и левого печеночных протоков образуется общий печеночный (ductus hepaticus communis). В тех случаях, когда слияние печеночных протоков бывает у края двенадцатиперстной кишки, оба протока идут параллельно, а пузырный может впадать в один из них на различном уровне. Общий печеночный проток идет в составе печеночно-две-надцатиперстной связки по ее правому краю впереди правого края воротной вены. Диаметр его около 4 мм, длина колеблется от 1 до 10 см (обычно 3—7 см) в зависимости от места слияния печеночных протоков и уровня впадения пузырного протока. Общий желчный проток. От места впадения пузырного протока к двенадцатиперстной кишке идет общий желчный проток ductus choledochus или холедох. Длина его колеблется в зависимости от уровня впадения пузырного протока (в среднем 5— 8 см). Диаметр протока 5 мм. Перед входом в ткань поджелудочной железы холедох несколько расширяется, затем постепенно суживается, проходя через ткань железы особенно в месте впадения в двенадцатиперстную кишку. В патологических условиях холедох способен расширяться до 2—3 см и более. Стенка его тонкая и состоит из адвентиции, фиброзного слоя, небольшого количества пучков гладких мышечных волокон и толстой слизистой оболочки с большим количеством слизистых желез. Общепризнанным является деление холедоха на 4 части.
головкой поджелудочной железы и двенадцатиперстной кишкой. Чаще (у 90% людей) холедох проходит через поджелудочную железу, у части он располагается на ее дорсальной поверхности. Следует сказать, что холедох, проходя через поджелудочную железу, чаще имеет желоб и не полностью окружен паренхимой железы, как сообщает И. М. Тальман (1963), хотя Hess (1961), наоборот, отмечает, что у 90% людей холедох в этой части находится внутри паренхимы поджелудочной железы. 4. Интрамуральная часть холедоха. Внедрение его в двенадцатиперстную кишку происходит по левому медиальному краю вертикального ее отдела на границе с задней стенкой в 12—14 см от привратника при измерении по кишке (М. Д. Ани-ханова, 1960; И. М. Тальман, 1963), то есть в средней части вертикального отдела. В ряде случаев место впадения может находиться и в 2 еж от пилоруса или даже в желудке, а также в области flexura duodeno jejuna Us (Hess, 1955; Hen-rard, 1957; Arianoff, 1958). Bayens (1960) на 210 препаратах констатировал расположение места впадения холедоха в дуоденум в верхней горизонтальной части ее у 8 больных, в верхней половине вертикальной части — у 34, в нижней — у 112, у перехода в нижнюю горизонтальную часть — у 36, в нижней горизонтальной части — у 6, слева от средней линии около двенадцати-перстно-тонкокишечного изгиба — у 4 больных. Все это, безусловно, необходимо иметь в виду при оперативных вмешательствах на большом дуоденальном соске и дистальном отделе холедоха. Чем выше место впадения холедоха, тем он прямее прободает стенку кишки, а в связи с изменением угла впадения в сторону прямого создается и большая предрасположенность к дуоденально-папилляр-ному рефлюксу. 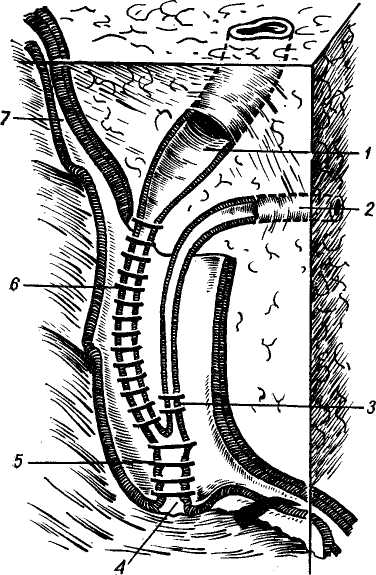 Рис. 5. Большей дуоденальный сосок (схема по В. В. Виноградову). 1 — общий желчный проток; 2 — главный панкреатический проток; 3 — мускулатура панкреатического протока; 4 — устье большого дуоденального соска; 5 — ампула большого дуоденального соска и мускулатура сфинктера Одди; 6 — мускулатура общего желчного протока; 7— мышечный слой стенки двенадцатиперстной кишки. Четвертная, внутристеночная часть холедоха имеет протяженность 10— 15 мм и косо прободает стенку двенадцатиперстной кишки, образуя со стороны слизистой оболочки большой дуоденальный сосок (papulla duode-ni major — Vateri). Большой дуоденальный сосок. В месте прохождения стенки кишки холедох несколько суживается и затем в подслизистом слое расширяется, образуя ампулярное расширение длиной 9 мм, иногда — 4,5 мм (Vater, 1920; Lichtman, 1953). Ампула заканчивается в просвете кишки сосочком величиной с просяное зерно. Сосочек располагается на продольной складке, образованной самой слизистой оболочкой. В дуоденальном сосочке имеется мышечный аппарат, состоящий из циркулярных и продольных волокон — сфинктера Одди. Продольные волокна разделяются на восходящие и нисходящие, при этом восходящие являются продолжением мышечных волокон двенадцатиперстной кишки, а нисходящие идут по дуоденальной стороне холедоха и заканчиваются на одном уровне с циркулярными волокнами (рис. 5). Рядом с холедохом несколько ниже его прободают стенку дуоденум и выводной проток поджелудочной железы (ductus Wirsungianus). Слияние холедоха и панкреатического протока очень непостоянно как в смысле места слияния, так и в смысле угла впадения. Этот вопрос достаточно изучен многочисленными исследователями (С. П. Федоров, 1918; А. В. Мельников, 1922, 1935; И. И. Киселев, 1939; Opie, 1901; Ludd, 1931; Milbourn, 1944; Hjorth, 1947; Caroli и Nora, 1951; Hess, 1955; Hewman с соавт., 1965, и др.), что позволило принять деление всех вариантов на 3 группы, предложенное Milbourn и в 1944 г.
Schumacher (1928) предложил свою схему вариаций соединения холедоха с выводным протоком поджелудочной железы (рис. 6). Ввиду нередких вмешательств на соске двенадцатиперстной кишки эта схема имеет определенный практический интерес. Сам сосочек является терминальным отделом общего желчного про- 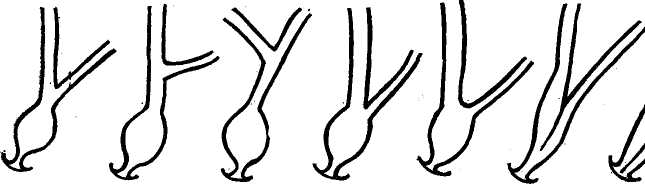 Рис. 6. Схема вариаций соединения холедоха с выводным протоком поджелудочной железы (по Schumacher). тока, длина его от 2 до 12 мм. Кровоснабжение большого сосочка двенадцатиперстной кишки происходит за счет мелких ветвей желудочно-двенадцатиперстной, поджелудочно-двенадцатиперстной и верхней брыжеечной артерии. Желчный пузырь (vesica felle) расположен в продольной борозде нижней поверхности печени. Этот тонкостенный орган покрыт в большинстве случаев па 2/3 брюшиной, а на 1/3 прилегает к печени. Стенка желчного пузыря состоит из серозной, слизистой оболочек, субсерозного и фибромускулярного слоев. Грушевидный по форме желчный пузырь имеет 3 отдела: дно (fundus), тело (corpus) и шейку (col-lum vesicae felle). Обычно у места перехода тела желчного пузыря в шейку имеется изгиб. Здесь же вблизи шейки стенка желчного пузыря образует 1, реже 2 кармана, которые часто являются местом расположения камней и сдавления ими пузырного протока. Вследствие деятельности мышечных волокон, расположенных в шейке и пузырном протоке, благодаря изгибу между ними, имеется перепад давления между полостью желчного пузыря и желчными протоками. Располагается обычно желчный пузырь на висцеральной поверхности печени в sulcus vesicae felle. Кроме типичного расположения желчного пузыря, встречаются и значительные отклонения в его топографоанатомическом положении,
3. Дистопия желчного пузыря встречается относительно редко. С. П. Федоров (1933) находил его в круглой связке печени, под левой долей и у серповидной связки. Bachlth (1944) обнаружил желчный пузырь под двенадцатиперстной кишкой, В. И. Гордиенко (1953) — в левой доле печени и т. д. 4. Удвоение желчного пузыря, по данным Borkus (1962), встречается у 0,02% больных. Особенно следует помнить об аномалиях впадения в желчный пузырь печеночного протока, пересечение которого без перевязки ведет к развитию желчного перитонита, а перевязка выключает из функции участок печени, дающий отток желчи через него. Kher (1913) и Andersen с соавторами (1960) отмечают возможность впадения правого печеночного протока в пузырный, Holzamer (1960) и Eisold (1961) — возможность впадения пузырного протока в двенадцатиперстную кишку без сообщения с печеночным протоком. Пузырный проток представляет собой несколько суженную в передне- 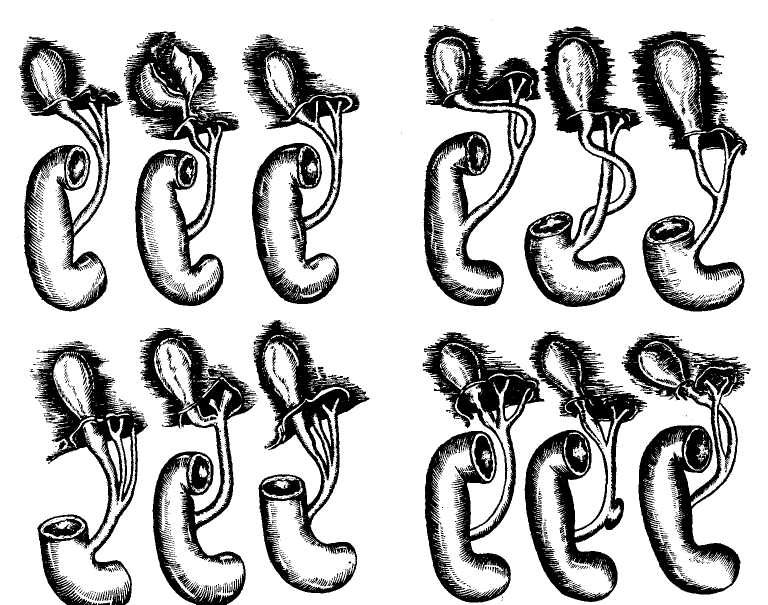 Рис. 7. Варианты слияния пузырного и печеночного протоков по И. Л. Брегадзе и А . И. Иванову. заднем направлении трубку длиной ченочному (на протяжении 1 — 5 см и от 3 до 10 мм, берущую начало от более) и впадает под очень острым поверхности шейки желчного пузыря, углом. обращенной к воротам печени, где 3-й тип (8—33%) — пузырный он изгибаясь направляется к ним, проток спирально обходит печеноч- а затем под углом уходит вниз к пе- ньтй сзади и впадает в заднюю или ченочному протоку. Просвет прокси- левую, а иногда и переднюю его мального отрезка пузырного прото- поверхность. Б. И. Школьник (1959) ка напоминает своим видом штопор на 250 трупах взрослых людей тща- неправильной формы вследствие спи- тельно изучил варианты слияния тер- ралеобразного строения его слизи- минального отдела пузырного и пе- стой оболочки. ченочного протока и при этом уста- Руге, Kunze, Descomps, Eisend- новил, что у 141 больного это слияние rath (1956) различают 3 основных располагалось ниже внешнеопреде- типа соединения пузырного протока ляемого соприкосновения стенки на ■с печеночным: 4—8 мм, у 92 — на 15 мм, у 8 — 1-й тип (33—80%) — короткий пу- на 25—30 мм, а у 10% больных сди- зырный проток впадает в общий пе- яние происходило позади двенадца- ченочный на его правой боковой по- типерстной кишки. И. Л. Брегадзе, верхности под умеренно острым А. И. Иванов (1961) также изучали углом. варианты слияния пузырного и пе- 2-й тип (12—49%) — длинный пу- ченочного протоков и представили зырный проток идет параллельно пе- следующую схему (рис. 7). Глава вторая Ф  УНКЦИОНАЛЬНЫЕ И СПЕЦИАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПЕЧЕНИ И ЖЕЛЧНЫХ ПРОТОКОВ УНКЦИОНАЛЬНЫЕ И СПЕЦИАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПЕЧЕНИ И ЖЕЛЧНЫХ ПРОТОКОВОбъем и характер специальных исследований в каждом частном случае определяется предварительным диагнозом. Однако окончательная диагностика и выбор наиболее подходящего метода лечения в настоящее время невозможны без применения комплекса функциональных и морфологических методов исследования. ИССЛЕДОВАНИЯ ДО ОПЕРАЦИИ Целью этих исследований является уточнение диагноза и оценка функционального состояния печени и желчных путей, обоснование показаний к хирургическому вмешательству и выявление возможных противопоказаний к нему. Биохимические исследования. К настоящему времени предложено большое количество функциональных биохимических проб печени, но систематизация и окончательная клиническая оценка их еще не завершена. Наибольшие успехи достигнуты в изучении пигментного и белкового обменов, имеют определенное значение и пробы, отражающие состояние обмена жиров и углеводов. В последнее десятилетие все большее значение придается изучению ферментов печени. Поскольку для практических целей приходится ограничить набор функциональных проб гепатобилиар-ной системы минимальным количе- ством тестов, мы в настоящем разделе обсуждаем лишь наиболее чувствительные и практически ценные показатели. Билирубин. Определение его содержания в сыворотке крови является наиболее точным методом оценки пигментной функции печени. Различают 2 фракции билирубина — непрямой (гемобилирубин) и прямой (холебилирубин). Последний дает покраснение сыворотки крови при добавлении к ней диазореактива Эрли-ха, сразу (реакция прямая, быстрая) или через 3—5 минут (реакция прямая, замедленная). Непрямой билирубин дает покраснение сыворотки только после предварительной обработки ее спиртом (реакция непрямая). Непрямой билирубин образуется в ретикулоэндотелиальной системе из гемоглобина, поступающего в сыворотку вследствие гемолиза, постоянно происходящего в организме в определенных пределах. Считается, что непрямой билирубин содержит белковый компонент, не растворяется в воде и поэтому не выделяется почками. Проходя через печень, он освобождается от этого белка и превращается в водорастворимый прямой билирубин, который и выделяется с желчью в кишечник. В настоящее время утверждается, что непрямой билирубин, проходя через печень, соединяется с глю-куроновой кислотой, превращаясь в моноглюкуронид-билирубин (пигмент I, прямой билирубин I) и ди-глюкуронид-билирубин (пигмент II, прямой билирубин II). Поэтому некоторые авторы считают более правильным именовать непрямой билирубин свободным, а прямой — связанным. Предполагается, что диглю-куронид-билирубин образуется исключительно в печени, в то время как моноглюкуронид-билирубин может быть и внепеченочного происхождения. В норме прямой билирубин сыворотки составляет не более 25% от общего билирубина, непрямой билирубин — 75% и более. Отдельные авторы считают, что в норме прямой билирубин в сыворотке крови отсутствует. Прямой билирубин желчи под влиянием окислительных процессов частично превращается в уробилин, а основная часть в толстой кишке — в стеркобилин и в таком виде выделяется с калом. Часть уробилина в кишечнике всасывается и, возвращаясь через систему воротной вены в печень, снова превращается в билирубин. Незначительная часть уробилина выделяется с мочой. Повышение содержания билирубина в крови сверх нормы может быть результатом повышенного распада эритроцитов (гемолитическая желтуха), неспособности печеночных клеток к переработке и выделению билирубина (паренхиматозная желтуха) или следствием препятствия на пути оттока желчи (механическая желтуха). Определение фракций билирубина помогает до некоторой степени дифференцировать различные формы желтух. Для гемолитической желтухи характерно избыточное содержание в крови непрямого билирубина, увеличение количества стеркобилина в кале и уробилина в моче. При полной непроходимости главных желчных путей исчезают стеркобилин в кале и уробилин в моче, резко увеличивается содержание прямого и непрямого билирубина крови, по- являются желчные пигменты в моче. Следует отметить, что в норме моча не содержит такого количества желчных пигментов, которые улавливались бы обычными лабораторными методами. Почечный порог для прямого билирубина равен 0,8 — 2 мг%. Видимая глазом желтушная окраска кожных покровов, слизистых оболочек и конъюнктив определяется при содержании общего билирубина выше 2 мг%. Если видимой желтухи нет, но содержание билирубина в крови выше нормы, то говорят о так называемой скрытой или субклинической желтухе. Моча в присутствии желчных пигментов приобретает темный желто-зеленый цвет, а кал при отсутствии в нем стеркобилина теряет коричневую окраску и становится бело-глинистого цвета. На высоте паренхиматозной желтухи, как и при механической, отмечается уменьшение или даже полное исчезновение стеркобилина в кале и уробилина в моче, увеличение билирубина в моче. В крови увеличивается количество преимущественно прямого билирубина. Определение прямого и непрямого билирубина позволяет отличить только гемолитическую желтуху, при которой это соотношение составляет 25%, а при механической или паренхиматозной — более 40%. Дифференцировать с уверенностью механическую и паренхиматозную желтуху только на основании этих фракций — уробилина в моче и стеркобилина в кале — невозможно. Новые исследования с раздельным определением глюкуронидов билирубина якобы дают такую возможность. Известно, что при желтухах процесс глюкуро-нидирования нарушается и в первую очередь нарушается образование ди-глюкуронид-билирубина, в связи с этим установлено, что, если в норме на долю пигмента II приходится 70% прямого билирубина, а на долю пигмента I — 30 %, то при механической желтухе или этот процесс вовсе не нарушается, или увеличивается количество пигмента II до 79%, при паренхиматозной желтухе, наоборот, повышается содержание пигмента I до 42% относительно пигмента II. Однако диагностическое значение этих исследований еще не может считаться общепризнанным. То же можно сказать и в отношение эфиро-растворимой фракции билирубина, появление которой предположительно считалось признаком непроходимости холедоха вследствие периам-пулярного рака. Более ценной для дифференциальной диагностики оказалась предни-золоновая проба: в течение 5—8 дней вводят преднизолон (около 300 мг на курс) и повторяют исследование билирубина. При паренхиматозной желтухе определяется отчетливое снижение уровня сывороточного билирубина и улучшение самочувствия больного, в то время как при механической желтухе внепеченочного происхождения содержание его практически не меняется или снижается медленно и незначительно. Наибольшее распространение для определения сывороточного билирубина получил метод ван ден Берга. Однако этот метод не дает возможности количественного определения прямого и непрямого билирубина. Б этом отношении выгодно отличается метод Ендрассика, которому и отдается предпочтение в настоящее время. Трансаминазы (аминоферазы). Наиболее изучены и широко используются для диагностических целей 2 траисаминазы — глютаминоаланино-вая, или глютаминопировиноград-ная трапсаминазы (ГАЛТ, ГПТ) и глютамииоаспарагиновая, или глю-таминощавелевокислая трансамина-за (ГАСТ, ГЩТ). Они являются представителями индикаторных ферментов, выполняют определенные внутриклеточные функции и сосредоточены в цитоплазме (ГПТ) или в обеих клеточных структурах — цитоплазме и митохондриях (ГЩТ). Наибольшая часть трансаминаз — печеночного происхождения. Особенно это относится к ГПТ. Наряду с печеночными клетками трансаминазы в больших количествах содержатся в мышцах и других тканях. Поэтому повышение уровня индикаторных ферментов в сыворотке наблюдается не только при болезнях печени, но и при выраженных дистрофических изменениях органов и систем богатых этими ферментами,— инфаркте миокарда, остром панкреатите, гемолитических состояниях, ревматическом миокардите, остром нефрите, обширных травмах и других состояниях. Трансаминазы частично проникают через клеточные мембраны и поэтому даже в нормальных условиях небольшое количество их находится в плазме крови. ГПТ сравнительно легко проходит клеточную мембрану, ГЩТ — медленно. В сыворотке крови они быстро разрушаются. Нормальное содержание ГПТ и ГЩТ в сыворотке крови от 0 до 40 ед., соотношение ГПТ/ТЩТ (коэффициент де Ритиса) 1,3—1,4. Индикаторная гиперферментемия в первую очередь свидетельствует о повышении проницаемости клеточных мембран, а не о некрозе клеток, как предполагали ранее (А. И. Ха-занов, 1968). Наиболее высокие цифры трансаминаз (до 120—440 ед.) отмечаются при болезни Боткина и быстро текущих циррозах печени (почти у 100% больных) с максимумом повышения на 2—3-й неделе заболевания. К 5—6-й неделе болезни Боткина уровень трансамипаз нормализуется. Коэффициент де Ритиса при остром вирусном гепатите снижается до 0,65 и ниже. Ценным является закономерное повышение трансаминаз еще в преджелтушном периоде, а также при безжелтушных формах болезни Боткина. При механической желтухе иногда наблюдается подъем трансами- наз, но он бывает кратковременным и менее высоким (до 60—80 ед. с коэффициентом де Ритиса 0,8). Более умеренное повышение трансаминаз со снижением коэффициента де Ритиса ниже 1,0 наблюдается в некоторых случаях хронического гепатита, при первичном и метастатическом раке печени. При явных циррозах печени в активной фазе повышение ГПТ отмечено у 60,2% больных (А. И. Хазанов, 1968). Исследование сывороточных трансаминаз является довольно чувствительным и ценным методом дифференциальной диагностики желтух и поэтому широко применяется в клинической практике. Фруктозе- 1-фосфаталъдолаза (мо-нофосфатфруктоалъдолаза). В норме этот фермент в сыворотке отсутствует или активность его составляет лишь 0,5—2,8 ед. в 100 мл сыворотки крови (3. А. Бондарь, 1970). При острых гепатитах активность его возрастает в 12—30 раз (Д. М. Брагинский, 1965), в то время как при механической желтухе, метастазах рака в печень и пораженных желчных путях гиперферментэмия отсутствует, а при циррозах печени подъем фермента незначителен (А. И. Хазанов, 1965). Сорбитдегидрогеназа. Она является также «органоспецифическим» ферментом печени и «ведет» себя почти аналогично фруктозо-1-фосфаталь-долазе. При циррозах печени и хронических гепатитах активность его колеблется в пределах 1,3— 3,5 ед. Диагностическое значение этих 2 ферментов при заболеваниях печени приравнивается к результатам исследования глютаминопировиноградной трансамина зы. Глютаминовая дегидрогеназа. Это — чисто митохондриальный фермент и появляется в сыворотке крови только при разрушении печеночных клеток. Исследование глютаминовой дегидрогеназы позволяет поэтому обнаруживать некротические изменения при остром гепатите в период обострений хронических гепатитов и особенно циррозов печени, а также в ранних стадиях острой закупорки желчных путей. Большинство исследователей очень высоко оценивают диагностическое значение глютаминовой дегидрогеназы, потому что быстрое и существенное возрастание ее активности может наблюдаться при отсутствии гипертрансаминаземии и нормальных показателях фруктозо-1-фосфатальдолазы, сорбитдегидроге-назы и щелочной фосфатазы. Щелочная фосфатаза. ЩФ — один из экскреционных ферментов печени, имеющий значение в диагностике заболеваний печени. Печень вырабатывает лишь небольшую часть щелочной фосфатазы (примерно до 10%), остальная часть этого фермента вырабатывается преимущественно в костной системе. Однако в нормальных условиях почти вся щелочная фосфатаза выделяется печенью в желчь. При нарушениях оттока желчи концентрация этого фермента в сыворотке возрастает, на чем и основывается диагностическая ценность определения щелочной фосфатазы. При определении по методу Бо-данского нормальное содержание ще-лочпой фосфатазы составляет 2— 5 ед., по методу Кинга-Армстронга — 3—14 ед. По данным А. И. Хазаиова, отчетливое повышение щелочной фосфатазы свыше 10 ед. по Боданскому наблюдается в 61 % случаев механической желтухи, в 26,1% —болезни Боткина, в 8,6% — циррозов печени и в 63,1 % случаев метастатического рака печени. Диагностическая ценность гипер-фосфатаземии несколько снижается тем обстоятельством, что отчетливое повышение щелочной фосфатазы обнаруживается относительно поздно»— на 4—10-й день обтурационной желтухи. Следует также учитывать, что иногда значительное повышение щелочной фосфатазы наблюдается при воспалительных заболеваниях костной системы и переломах. Хининоксидаза. В крови здорового человека активной хининоксида-зы практически не содержится. Значительная ферментемия возникает при активном циррозе печени и паренхиматозной желтухе (от 10 до 40 ед.). При механических желтухах выраженного изменения активности хи-ниноксидазы не происходит. Результаты исследования этого фермента равноценны результатам осадочных реакций (Linder и Sachs, 1963). Холинэстераза. Определение этого фермента имеет значение для функционального исследования печени, так как активность холинэстеразы существенно уменьшается при поражениях паренхимы печени, в то время, как при механической желтухе (в начальных стадиях) она в пределах нормы. В норме у здоровых людей уровень холинэстеразы колеблется от 0,285 до 0,490 усл. ед. Наиболее резко холинэстераза снижается при циррозах печени. Тяжелое течение острого гепатита ведет к снижению активности фермента до 0,006 ед., а характер изменения активности в процессе болезни имеет значение в определении прогноза заболевания. При доброкачественном течении гепатита или при хроническом активность фермента относительно невелика, но при переходе хронического гепатита в цирроз снижение активности становится отчетливым. Это отражает нарушение синтетических процессов в печени. Довольно низкая активность фермента отмечена при первичном раке, особенно с вовлечением паренхимы печени, а также, хотя и в меньшей мере, при метастатическом ее поражении. Холестерин. Исследование холестерина сыворотки является тестом для определения роли печени в ли-пидном обмене, так как печень играет доминирующую роль в синтезе холестерина (из уксусной и пирови- ноградной кислот) и она же в основ-ном регулирует уровень холестерина в крови. Кроме того, в печени осуществляется эстерификация холестерина — соединение его с жирными кислотами. Небольшая часть холестерина выделяется с желчью в неизмененном виде, большая часть превращается в желчные кислоты. Общее содержание холестерина в сыворотке крови 150—200 мг%. Эфиры холестерина составляют 90— 130 мг%, свободный холестерин — в среднем около 60 мг% (20—40% общего холестерина). Коэффициент эстерификации (отношение эфиров холестерина к общему холестерину) в норме равен 0,6—0,8. Этот коэффициент является ценным тестом, отражающим состояние функции печени. При холестазе (механическая желтуха, острые холангиолитические гепатиты, хронические холангиогепа-титы, билиарные циррозы печени) наряду с другими составными частями желчи накапливается в крови и холестерин. В этом отношении имеется явный параллелизм между ги-перхолестеринемией, гипербилируби-немией и гиперфосфатаземией. При тяжелых паренхиматозных поражениях печени (острые гепатиты, циррозы, активная дистрофия и диффузные опухоли) наблюдается резкое снижение уровня сывороточного холестерина — признак печеночной недостаточности, а значительное падение коэффициента эстерификации (до 0,3—0,2) является уже плохим прогностическим признаком. Напротив, нарастание этого коэффициента в процессе заболевания следует расценивать как благоприятный признак. Считается, что феномен снижения холестеринэстеров зависит от блокады особого фермента — эсте-разы. При механической желтухе, хо-лангиогепатите и первичном били-арном циррозе количество эфиров холестерина у большинства больных пропорционально общему холестерину, и для практической работы можно ограничиться именно этим исследованием. |
