Хирургия печени и желчных путей. Нежизнеспособности ее у больного или для борьбы с тяжелой печеночной недостаточностью
 Скачать 11.68 Mb. Скачать 11.68 Mb.
|
|
Пластика устья вирсунгова протока. Как уже подчеркивалось, после рассечения сфинктера Одди необходимо отыскать отверстие вирсунгова протока и тщательно исследовать его, чтобы определить, нет ли какого-нибудь нарушения проходимости главного панкреатического протока. Это особенно необходимо при повышении уровня сывороточной амилазы и наличии изменений поджелудочной железы, обнаруживаемых на лапаротомии. В норме отверстие вирсунгова протока свободно пропускает зонд или катетер диаметром 3 мм. Если же обнаруживается стеноз этого отверстия, то должны быть приложены все усилия, чтобы устранить его. 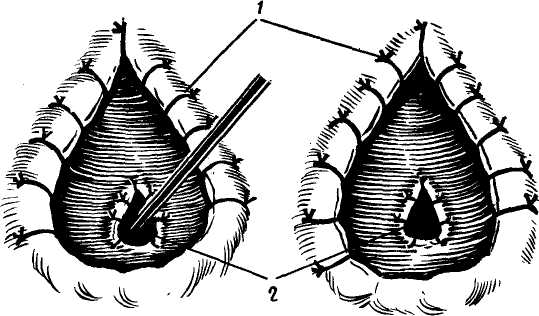 Рис. 43. Пластика устья вирсунгова протока. Обычная сфинктеропластика, какой бы широкой она ни была, оказывается недостаточной, так как патологические изменения, вызывающие сужение ампулы, распространяются так, что включают и терминальный сегмент панкреатического протока, то есть ту часть сфинктера Одди, которая составляет собственный сфинктер вирсунгова протока. Более того, возможен изолированный стеноз отверстия вирсунгова протока, без стеноза ампулы (Hess, 1966; Acosta и со-авт., 1970). В таких случаях через кишечное отверстие удается ввести только самый тонкий зонд, причем характерно, что вслед за удалением этого зонда из вирсунгова протока под давлением вытекает несколько капель панкреатического сока, иногда с примесью беловатых крошечных цилиндров, представляющих слепки мельчайших панкреатических канальцев. Необходимо помнить, что зондирование панкреатического протока должно быть проведено с максимальной осторожностью, так как любая излишняя травма может вызвать вспышку панкреатита. При стенозировании отверстия вирсунгова протока необходимо выполнить не только обычную сфинкте-ропластику, но и применить пластику отверстия панкреатического протока. Эта операция упоминается в литературе под разными названиями: резекция шпоры между общим желчным и панкреатическим протоками, рассечение (или иссечение) перегородки между дистальными отделами общего желчного и панкреатического протоков, сфинктеротомия вирсунгова протока, У-образная сфинктеротомия, двойная сфинктеротомия. Ее применяют Д. Г. Мамамтавришвили (1970), Hess (1965), Gones и соавт. (1969), Acosta и соавт. (1970) и другие. Техника этой операции состоит в следующем. После удаления пуговчатого зонда или катетера в отверстие вирсунгова протока на глубину в среднем около 1 см вводят лезвие тонких ножниц. Проток разрезают вдоль его продольной оси в том месте, где имеется шпора между общим желчным и вирсунговым протоком. Это соответствует переднезаднему квадранту отверстия. В этом месте нет панкреатической паренхимы, поэтому не существует опасности поранить поджелудочную железу. При необходимости из указанной шпоры удаляют клин ткани с основанием около 2 мм (рис. 43). Фактически этот клин является частью перегородки, разделяющей нижние концы общего желчного и вирсунгова протока. Удаление его расширяет отверстие панкреатического протока и, кроме того, дает материал для биопсии. Слизистая оболочка панкреатического протока сближается со слизистой общего желчного протока и ампулы тонкими узловатыми швами (от 3 до 5). Очень важно, чтобы разрез захватывал на всем протяжении участок стеноза. Безопасно рассекать панкреатический проток до 1,5 см от его отверстия. Если же стеноз более распространенный или локализован в нескольких местах (что необходимо проверить операционной панкреато- графией), то мы предпочитали наложить обходные панкреатоеюнальные анастомозы по методу Duval (1961) или Puestow (1965), если только не показана резекция поджелудочной железы. Когда операция сделана без излишней травмы, нет необходимости прибегать к наружному дренированию вирсунгова протока. Лишь в сомнительном случае мы с успехом применили дренаж вирсунгова протока по модифицированному методу Leger. У одного больного мы встретились с редкой патологией — стенозирова-нием устья вирсунгова и санторини-ева протоков. Мы ограничились пластикой вирсунгова протока, но, ретроспективно оценивая это наблюдение, можно сказать, что дополнительная пластика санториниева протока была бы целесообразней. Bart-lett и Nordi в 1960 г. описали редкий случай, когда санториниев проток являлся главным протоком поджелудочной железы и его отверстие было сильно стенозировано. Произведена пластическая операция на отверстии этого протока, и у больного прекратились симптомы рецидивирующего панкреатита. Если отверстие вирсунгова протока после трансдуоденальной сфинк-теротомии не удается найти в ампуле или на верхушке большого дуодена-нального сосочка, то следует искать его на малом сосочке двенадцатиперстной кишки. Это крошечное анатомическое образование можно определить по оттоку панкреатического секрета. Patel и соавторы (1969) описывают сфинктеротомию вирсунгова протока «слева направо» при помощи сфинктеротома Leger. Это возможно только при значительном расширении вирсунгова протока. После вскрытия его в области тела поджелудочной железы, панкреатографии и возможной экстракции панкреатических камней сфинктеротом с закрытой гильотиной проводят по протоку в сторону головки поджелудоч- ной железы и затем в область большого дуоденального соска. Надавливая на рукоятку инструмента, его тупой конец проталкивают через сосочек под контролем пальпации через стенку двенадцатиперстной кишки. Раскрывая гильотину и затем извлекая сфинктеротом, производят резекцию сфинктера вирсунгова протока. Сообщений о клиническом применении подобной методики мы не обнаружили. В кратком последовательном изложении наша стандартная техника трансдуоденальной сфинктеропласти-ки состоит в следующем: холецистэк-томия и ушивание пузырного ложа; интубация культи пузырного протока и измерение остаточного давления, дебитометрия и операционная холан-гиография; мобилизация двенадцатиперстной кишки и головки поджелудочной железы, пальпаторное исследование желчных путей, фатерова сосочка и головки поджелудочной железы; удаление камней и детрита (если он есть) из желчных путей через культю пузырного протока или холедохотомическое отверстие; проведение трехмиллиметрового пугов-чатого зонда через культю пузырного протока или холедох и через частично стенозированный сфинктер Одди; короткая продольная дуоде-нотомия на передней стенке нисходящей части двенадцатиперстной кишки, в точке, противоположной пу-говчатому концу зонда; наложение 3 держалок в области большого дуоденального соска; расширение отверстия и ампулы большого дуоденального соска снизу для того, чтобы способствовать прохождению пугов-чатого зонда сверху, если его не удалось провести перед дуоденотомией; укрепление прочной нити на пуговча-том конце зонда и захватывание ее изогнутым зажимом с длинными тонкими браншами; протягивание нити кверху с помощью обратного хода пуговчатого зонда для проведения конца зажима через отверстие большого дуоденального соска на глуби- ну около 20 мм; раскрытие зажима и разведение его браншей для максимального растягивания отверстия сосочка; проведение одного лезвия тонких ножниц через отверстие большого дуоденального соска вверх, в общий желчный проток, на глубину 10—20 мм; рассечение сфинктера (или иссечение клина его ткани) на протяжении 10—20 мм в направлении стрелки на 10—11 часов; определение отверстия вирсунгова протока у края большого дуоденального сосочка и осторожное введение в него пуговча-того зонда; сближение слизистых оболочек общего желчного протока и двенадцатиперстной кишки 7—9 тонкими узловатыми швами по линии рассечения сфинктера; определение ширины отверстия вирсунгова протока и, если необходимо, катетеризация его и панкреатография; дилата-ция отверстия вирсунгова протока (если оно стенозировано зажимом) «москит» для того, чтобы ввести одно лезвие остроконечных ножниц на 5— 10 мм в вирсунгов проток; рассечение устья вирсунгова протока или иссечение клина ткани из перегородки между дистальными концами холе-доха и вирсунгова протока длиной 5—10 мм; наложение 3—5 тонких узловых швов между слизистыми оболочками общего желчного и вирсунгова протоков; промывание общего желчного протока с помощью введенной снизу хлорвиниловой трубки; закрытие дуоденотомического отверстия в поперечном направлении непрерывным швом из тонкого кетгута через все слои и П-образными серо-серозными швами с дополнительной перитонизацией брыжейкой поперечно-ободочной кишки; введение тонкой хлорвиниловой трубки в культю пузырного протока и перевязка его на этой трубке. Ушивание холедохо-томического отверстия (если была сделана холедохотомия); контрольная холангиоманометрия и дебитометрия; выведение второго конца хлорвиниловой трубки через отдельный прокол брюшной стенки в правом под- реберье и прикрепление ее к коже; дренирование подпеченочного пространства резиновой трубкой, обвернутой перчаточной резиной, и выведение дренажа через отдельный небольшой разрез брюшной стенки в правом фланке; закрытие разреза брюшной стенки. Необходимо подчеркнуть, что следует очень строго придерживаться всех деталей оперативной техники при трансдуоденальной сфинктеро-пластике. Тогда эта операция будет достаточно безопасной и обеспечит хорошие непосредственные и отдаленные результаты. Эту операцию должны производить высококвалифицированные хирурги в специализированных лечебных учреждениях. Последствия трансдуоденальной сфинктеропластики. Для изучения функционального состояния рассеченного сфинктера Одди мы провели послеоперационные измерения остаточного давления в общем желчном протоке и дебита через трубку в культе пузырного протока; послеоперационную холангиографию под контролем рентгенотелевидения и кинохо-лангиографию. Измерения остаточного давления и дебита производили во время опе рации — до и после сфинктеропла- стики, а затем на 1, 2, 3, 7 и 14-й день после нее. Для оценки способ ности сфинктера Одди к сокращению, измерения, производимые на 13-й день, повторяли после внутривенного введения 5 мг сернокислого морфи на. Всего таким образом исследова но 16 больных, перенесших трансду оденальную сфинктеропластику. У всех в послеоперационном периоде проводили прямую (через трубку) холангиографию под контролем рент- генотелевизионного наблюдения, а у 12 больных, кроме того, сделали ки- нохолангиографию до и после инъек ции морфина. Аналогичные исследования проведены у 15 больных после холецистэк-томии и у 10 — после холецистэк-томии, дополненной селективной 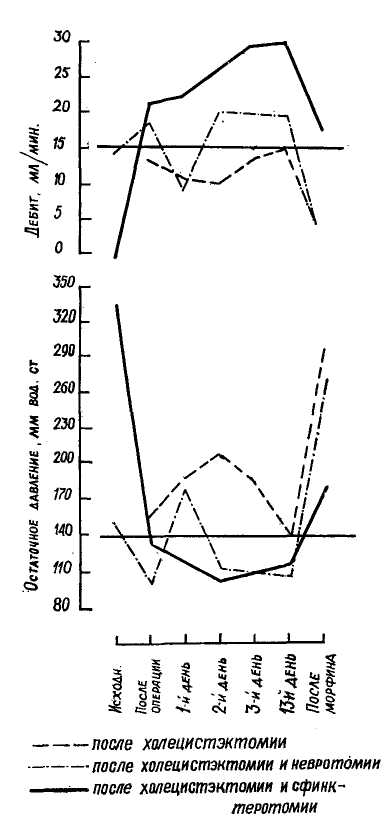 Рис. 44. Динамика остаточного давления и дебита после трансдуоденальной сфинк-теропластики в сравнении с динамикой тех же показателей после простой холецистэк-томии и холецистэктомии с селективной ретрохоледохальной невротомией. ретрохоледохальной невротомией. Показанием к дренированию пузырного протока после холецистэктомии было повышение остаточного давления и уменьшение дебита, которое можно приписать легкому стенозу или спазму сфинктера Одди. На основании статистической обработки результатов проведенных исследований построен график (рис. 44) динамики изменения остаточного давления и дебита в послеоперационном периоде после некоторых видов вмешательств на желчных протоках. Из данных графика вытекает, что трансдуоденальную сфинктеропла-стику производили при очень высоком остаточном давлении и низком дебите, но эти показатели нормализовались сразу же после операции и оставались в пределах нормальных величин на протяжении всего послеоперационного периода. Селективную ретрохоледохалъную невротомию производили при показателях, лишь умеренно отклоняющихся от нормы. После нее обнаружено некоторое снижение остаточного давления и легкое увеличение дебита. Однако, к исходу первых суток давление в холедохе значительно превышало норму, но еще через день давление и дебит определялись на нормальном уровне в течение всего послеоперационного периода. В противоположность этому, одна холеци-стэктомия, сделанная при наименее выраженных отклонениях давления и дебита, не привела их к нормализации на протяжении всего времени изучения, хотя микродренаж холе-доха и оставался открытым все это время. Внутривенное введение морфина у больных после простой холецистэктомии или холецистэктомии с ретрохоледохальной невротомией вызывает быстрый и резкий подъем остаточного давления в холедохе, сохраняющийся в течение 1 часа и более. Дебит после введения морфина у этих больных снижается почти до нуля. Напротив, после сфинктеропластики введение морфина вызывает лишь кратковременный и слабо выраженный подъем остаточного давления и не такое резкое снижение дебита. Это временное повышение давления и уменьшение дебита обусловлено, по-видимому, рефлюксом дуоденального содержимого в холедох, так как вентильный механизм устранен сфин-ктеропластикой. На основании этих данных можно считать, что трансдуоденальная сфинктеропластика стойко снижает сопротивление патологического сфинктера Одди. Поэтому в наружном профилактическом дренировании хо-ледоха после сфинктеропластики нет никакой необходимости. Ретрохоле-дохальная невротомия может быть применена взамен сфинктеропластики при легких степенях стеноза и спазма сфинктера, но самостоятельного значения как метода лечения, она, по-видимому, не имеет. Простая холецистэктомия с временным наружным микродренажом холедоха даже при легких поражениях сфинктера Одди не оказывает нормализующего действия на его тонус. После адекватной трансдуоденальной сфинктеропластики сохраняется ритмическая деятельность сфинктер-ного сегмента холедоха, но ритм сокращений явно изменен — фаза раскрытия удлиняется, а фаза сокращения укорачивается по сравнению с нормой. Введение морфина мало изменяет характер холедоходуоденаль-ного оттока. Перистальтические сокращения двенадцатиперстной кишки после тотальной сфинктеропластики вызывают интермиттирующий реф-люкс контрастного вещества вверх, в общий желчный проток, что свидетельствует о нарушении запира-тельной функции сфинктера Одди. При быстром введении контрастного раствора после сфинктеропластики не определяется видимое расширение проксимального сегмента холедоха и больные не испытывают никаких болевых ощущений. Ни разу после трансдуоденальной сфинктеропластики мы не наблюдали реф-люкса контрастного вещества в вир-сунгов проток. Это еще раз подтверждает наличие собственного сфинктера вирсунгова протока. В противоположность только что описанной картине, после простой холецистэктомии или селектив-вой ретрохоледохальной невротомии отчетливо определяются перисталь- тические сокращения сфинктерного сегмента с порционным поступлением контрастного вещества в двенадцатиперстную кишку. После введения морфина отток в двенадцатиперстную кишку при обычном давлении прекращается, а повышение перфу-зионного давления сопровождается видимой дилатацией холедоха и выраженными субъективными симптомами — коликообразной болью в животе и тошнотой. Послеоперационное бариевое исследование желудка и двенадцатиперстной кишки в сроки от 2 месяцев до 2 лет после трансдуоденальной сфинктеропластики было произведено у 47 больных. У 19 из них отмечено наличие газа в желчных путях (рис. 45а), и рефлюкс бария в холе-дох (рис. 45б). Рефлюкс был незначительным и очень кратковременным. Эти симптомы мы рассматривали как доказательство адекватности сфинктеропластики. Холангит не развился ни в одном из случаев с наличием рефлюкса. Это можно объяснить отсутствием какого-либо стаза в желчных путях благодаря хорошему их дренированию в двенадцатиперстную кишку. Приведенные данные позволяют сказать, что правильно сделанная трансдуоденальная сфинктеропластика не сопровождается рубцовым сужением вновь сформированного холе-доходуоденального соустья. ОСЛОЖНЕНИЯ И ЛЕТАЛЬНОСТЬ Операционные осложнения транс-дуоденальной сфинктеропластики могут быть разделены на 2 группы: наступающие при обнаружении большого дуоденального сосочка и связанные с самой сфинктеропластикой. Наиболее частым осложнением у больных I группы является образование ложного хода. Он возникает при перфорации холедоха инструментом, вводимым для зондирования большого дуоденального сосочка свер- 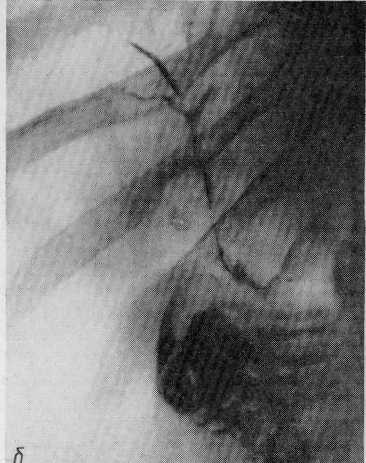 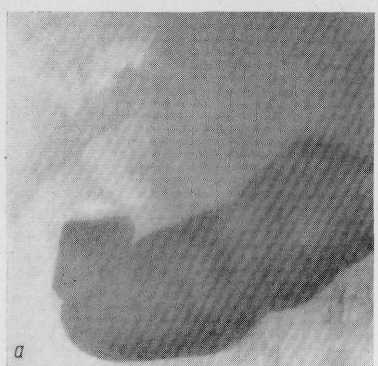 Рис. 45. Послеоперационное исследование с бар ием; а — газ в желчных протоках после трансдуоденальной сфинктеропластики; б — рефлюкс бария в желчные протоки после трансдуоденальной сфинктеротомии. ху. Нерр (цит. по Patel и соавт., 1969) на 1753 случаях сфинктеротомии наблюдал это осложнение у 17 больных (1%). Как правило, перфорация происходит в терминальном сегменте холедоха, и зонд (или другой инструмент), пройдя через ложный ход, проникает в просвет двенадцатиперстной кишки выше сосочка. Если используемый инструмент тонкий, то лечение этого осложнения не представляет сложностей: отыскав отверстие сосочка, сфинктеротомию проводят так, чтобы соединить оба отверстия. Иногда для этого необходимо произвести довольно длинный разрез. Необходимо тщательно сопоставить швами стенки холедоха и двенадцатиперстной кишки для ликвидации этого отверстия. При использовании более грубого инструмента возможна тяжелая травма. Мы наблюдали отрыв большого дуоденального сосочка при его зондировании и были вынуждены завершить операцию холедохоеюно-стомией. Сфинктеропластика изолированным трансдуоденальным путем также сопряжена с опасностью обра- зования ложного хода. При неаккуратном зондировании отверстия сосочка зонд может проникнуть в под-слизистый слой двенадцатиперстной кишки вдоль холедоха и выйти в свободную брюшную полость или за-брюшинное пространство. Мы дважды наблюдали подобное осложнение. В одном случае ложный ход был ушит при сфинктеропластике без дальнейших осложнений, но в другом случае образовался дуоденальный свищ и забрюшинная некротическая флегмона, ставшая причиной летального исхода. Осложнения сфинктеротомии и сфинктеропластики: образование сквозного дефекта в задней дуоденальной стенке при слишком глубоком рассечении собственного сфинктера холедоха, а также прошивание вирсунгова протока с последующим панкреонекрозом, который является грозным послеоперационным осложнением. Истинную частоту «чистого» послеоперационного панкреатита трудно установить, так как у многих больных он развивается как обострение хронического рецидивирующего. Раз- витию этого осложнения способствуют послеоперационный дуоденальный стаз и прямая травма терминального сегмента холедоха, вирсунгова протока и ткани поджелудочной железы. Исследуя амилазу, липазу и трипсин в дооперационном периоде и в первые дни после операции, мы обнаружили довольно частые функциональные и органические изменения поджелудочной железы после вмешательства на общем желчном протоке и сфинктере Одди. После трансдуоденальной сфинк-теропластики амилаза сыворотки и мочи была повышена у 12 больных (10%). Одна из них умерла в результате панкреонекроза. Можно предполагать, что причиной его в этом случае была техническая погрешность — случайное прошивание вирсунгова протока. Диагностика острого панкреатита после сфинктеропластики трудна, особенно в ранние сроки после операции. Прогрессирующее падение артериального давления, олигурия, возбуждение, частая рвота или большое количество отсасываемого из желудка содержимого должны наводить на мысль о развитии этого осложнения. Систематическое исследование панкреатических ферментов в первые послеоперационные дни может дать хирургу полезные сведения о состоянии поджелудочной железы и дать возможность своевременно предупредить послеоперационный острый панкреатит. Многие авторы преувеличивают опасность панкреатита, относя его к специфическим осложнениям трансдуоденальной сфинктеропластики. Полностью согласиться с этим мнением нельзя. Ведь послеоперационные панкреатиты в хирургии были известны еще до введения операций на сфинктере и не так уж редко. После простой холедохотомии Hess находил острый панкреатит у 9,8%, Mil-lbourn — у 9%, a Block — даже у 13,8% больных (цит. по Hess, 1966). Каждому опытному хирургу хорошо знакомы случаи панкреонекроза даже после простых резекций желудка и других несложных операций. Маигег при 674 операциях на желудке у 27% больных и при 1032 вмешательствах на желчных путях у 18% больных отметил повышение уровня амилазы в моче. Сопоставление приведенных данных свидетельствует о том, что послеоперационные панкреатиты после сфинктеротомии и сфинктеропластики встречаются не чаще, чем после других вмешательств на желчных путях. Следующим осложнением, на которое особенно указывают противники трансдуоденальной сфинктеротомии, являются дуоденальные свищи, связанные с дуоденотомией. Hess (1961) наблюдал 2 больных с дуоденальным свищом с летальным исходом из 113 больных, которым была произведена трансдуоденальная сфинктеротомия. В обоих случаях автор отметил недостаток техники. Stiller (1963) также описал два случая с недостаточностью шва двенадцатиперстной кишки, но с полным правом ссылался на то, что эта опасность существует и при супрадуоденальной холедоходуоденостомии. Мы наблюдали недостаточность швов двенадцатиперстной кишки у 4 больных. У 1 больного свищ был небольшим и зажил самостоятельно. У 2 — развился перитоните летальным исходом. У 2 остальных больных дуоденальный свищ сочетался с панкреонекрозом и ложным ходом с забрюшинной флегмоной, которые послужили причиной летального исхода. Во всех этих случаях причина образования дуоденального свища была связана с техническими погрешностями во время операции. Можно утверждать, что при хорошей технике и правильном двухрядном шве нет опасности образования дуоденального свища. Niedner (1956) не имел этого осложнения при выполнении 52 операций, Heiss (1965) — при 138 операциях. Полезным профилактическим мероприятием является систематическая аспирация желудочного и дуоденального содержимого в первые 3—5 дней после операции. В качестве возможного осложнения необходимо иметь в виду кишечное кровотечение из дуоденального разреза или из разреза сфинктера. Wense (1970) описал 2 больных с тяжелыми кровотечениями после сфинктеротомии. Мы, применяя шов по линии разреза сфинктера, ни разу не сталкивались с подобным осложнением. Желудочный стаз собственно нельзя назвать осложнением, так как он развивается в каждом случае вследствие частичной дуоденальной непроходимости в первые послеоперационные дни. Аспирация желудочного содержимого по зонду поэтому является необходимой у каждого больного и устраняет стаз в течение 3—4 дней. Продолжительность симптомов желудочного стаза в большой степени зависит от техники ушивания дуоденотомического разреза. Дуоденальные стенозы, вызванные неадекватным ушиванием двенадцатиперстной кишки, очень редки, но им благоприятствует слишком длинная вертикальная дуоденотомия и грубое ушивание. Частота поздних холангитов после сфинктеротомии специально изучена Lataste и Lenriot (1967). На 120 сфинктеротомии они отметили 5 больных с тяжелым холангитом, потребовавшим повторного вмешательства. Характерно, что сфинкте-ротомия у этих больных была сделана при атоничном и резко расширенном холедохе, то есть при условиях, когда мы сфинктеропластику не рекомендуем. Авторы не обнаружили в этих случаях препятствия к оттоку желчи в виде камней или рестеноза, но выявили значительное увеличение диаметра общего желчного протока. У 3 больных на реопе-рации наложен холедоходуоденаль-ный анастомоз и у 2 — холедохо- еюноанастомоз с отличными резуль-тами. Kourias и Fierris (1966) также наблюдали холангит с гепатитом, тяжелый у 2 больных и умеренный у 2 больных. Все 4 больных вылечены без повторных операций. Приступы умеренного холангита в отдаленном периоде мы отмечали у 3 больных. Холангитические симптомы удавалось ликвидировать проведением консервативной терапии в условиях стационара, и повторное хирургическое вмешательство не потребовалось. Ни разу не отмечено холангита у тех больных, у которых имелось широкое холедохо дуоденальное сообщение при свободном дуоденоби-лиарном рефлюксе. На основании этого мы считали, что опасность такого рефлюкса и восходящего холангита преувеличена. Холангит является следствием недостаточного дренирования холедоха после неполных сфинктеротомии. Можно утверждать, что чем шире сфинктеропластика, тем меньше опасность послеоперационного холангита. Явно незначительной представляется опасность истинного рестеноза сфинктера Одди (Taubert, 1965; Boh-mig и соавт., 1971). Нашим 2 больным чаще применяли неадекватную сфинктеротомию, чем истинное ресте-нозирование. И все же рестеноз может встречаться вопреки всем предосторожностям, ибо он встречается при любых других операциях с наложением анастомоза. Удовлетворительные результаты при рестенозе вполне могут быть достигнуты повторной тотальной сфинктеропластикой (Nordi и Acosta, 1966). Поскольку показания и техника вмешательства еще очень разнообразны, единая оценка результатов трансдуоденальной сфинктеропластики едва ли возможна. Все же находим полезным привести табл. 9. Мы произвели 166 операций трансдуоденальной сфинктеротомии и сфинктеропластики и было всего 6 летальных исходов (3,6%), из них Таблица 9 |
