Клиническая химия в диагностике и лечении. Обмен натрия и воды обмен калия лечение диуретиками гомеостаз ионов водорода
 Скачать 3.99 Mb. Скачать 3.99 Mb.
|
ОБМЕН ЖЕЛЕЗАУ человека находящийся в кровяном русле железосодержащий пигмент гемоглобин переносит кислород от легких к тканям, где происходят процессы метаболизма; в мышцах миоглобин усиливает локальное потребление кислорода. Свойство переносить кислород зависит, наряду с другими факторами, от наличия в молекуле гема двухвалентного железа. Недостаточность железа сопровождается угнетением синтеза гема; симптомы апемии обусловлены тканевой гипоксией. Цитохромы и некоторые ферменты, катализирующие перенос электронов, также содержат железо. При недостаточности железа, наблюдаемой р клинике (за исключением очень тяжелых случаев), возможность изменения свойств указанных макромолекул представляется сомнительной. ОБМЕН ЖЕЛЕЗА В НОРМЕ Распределение железа в организме На рис. 45 схематически представлено распределение железа в организме. Общее содержание железа в организме примерно от 50 до 70 ммоль (3—4г). Около 70% общего количества железа циркулирует в составе гемоглобина эритроцитов. До 25% имеющегося в организме железа резервировано в ретикулоэндотелиальной системе, в печени, селезенке и тканях костного мозга. Это резервное железо комплексируется с белком, образуя ферритин и гемосидерин. Железо ферритина более легко высвобождается из белка, чем железо гемосидерина. Гемосидерин (возможно, образующийся при агрегации ферритина) можно видеть с помощью светового микроскопа на неокрашенных срезах. Как ферритин, так и гемосидерин (в отличие от железа, не включенного в гем) окрашиваются ферроцианидом кальция (реакция образования берлинской лазури). Это окрашивание является характерным и может быть использовано для оценки величины запасов железа в организме. Недостаточность железа становится очевидной только в тех случаях, когда на мазках костного мозга в клетках ретикулоэндотелиальной системы не удается обнаружить окрашиваемого железа, которое в норме используется при биосинтезе гемоглобина. Перегрузка железом представляется вероятной в тех случаях, когда в пробах печени, полученных методом биопсии, удается обнаружить окрашиваемое железо. Такие отложения железа в паренхиму печени происходят, если способность ткани к образованию резерва железа исчерпана. Гистологические методы позволяют более уверенно обнаруживать недостаточность железа, чем перегрузку им. Л  ишь приблизительно от 50 до 70 мкмоль. (3—4 г, или примерна 0,1%) общего железа. организма циркулирует в плазме в связанной с белком форме. При определениях железа. плазмы крови измеряют именно содержание этой фракции. ишь приблизительно от 50 до 70 мкмоль. (3—4 г, или примерна 0,1%) общего железа. организма циркулирует в плазме в связанной с белком форме. При определениях железа. плазмы крови измеряют именно содержание этой фракции.Остальное железо организма входит в состав миоглобина, циторомов и железосодержащих ферментов. Транспорт через клеточные мембраны путем активного переноса совершается только при участии ферро (Fe2+)формы; именно в этом восстановленном состоянии находится железо. как в оксигемоглобине, так и в восстановленном гемоглобине. В ферритине и гемосидерине, а также в условиях связывания с трасферрином железо находится в ферри (Fe) форме. Регуляция распределения железа в организме изучена мало. Концентрации железа в плазме крови могут варьировать на 100% и более по чисто физиологическим причинам. На эти величины могут также влиять разнообразные патогенные факторы, не изменяющие количество железа в организме. Эти вариации в содержании железа плазмы крови, по-видимому, обусловлены его перераспределением между тканевыми резервами и плазмой. Баланс железа Как показано на рис. 45, железо, попавшее в организм, находится фактически в замкнутой системе. Экскреция железа. Экскреция железа, по-видимому, не регули руется. Потери железа организмом, вероятно, зависят от содержания железа в клетках, подвергающихся десквамации (преимущественно клетки желудочнокишечного тракта и кожи). Таким путем организм теряет приблизительно 18 мкмоль (1 мг) железа за сутки. Таблица 30. Сопоставление потерь железа
В моче появляются незначительные количества железа, что соответствует представлениям о наличии в кровотоке только связанного с белком железа. У женщин потери железа в связи с менструациями составляют в среднем за месяц 290 мкмоль (16 мг), что соответствует ежесуточной потере 10—18 мкмоль (0,5—1 мг) при базальном уровне 18 мкмоль (1 мг). В случаях меноррагии потери организмом железа могут значительно возрастать, что может приводить к дефициту железа. При беременности средние избыточные потери организмом матери железа, обусловленные наличием плода и плаценты, составляют приблизительно 27 мкмоль (1,5 мг) за сутки. Для сравнения следует отметить, что у доноровмужчин, сдающих примерно 0,5 л крови каждые 4 мес, избыточные потери организмом железа составляют 36 мкмоль (приблизительно 2 мг) за сутки при фоновом уровне потерь 18 мкмоль (1 мг) (табл. 30). Всасывание железа. На регулировании всасывания железа основана регуляция его содержания в организме. Всасывание железа представляет собой активный процесс, осуществляемый в проксимальпых отделах тонкого кишечника. Железо может проникать через клеточные мембраны (в частности через мембраны клеток кишечника) только в ферроформе. В клетках кишечника часть железа связывается с белком апсь ферритином, образуя ферритин, который (как и ферритин всех других клеток) является резервным соединением. При десквамации клеток кишечника происходят потери ферритина. В норме примерно 18 мкмоль (1 мг) железа всасывается ежесуточно, что восполняет потери железа организмом. Обычно всасывается приблизительно 10% железа пищи, но эта величина зависит отчасти от характера диеты. По-видимому, на всасывание железа влияют следующие факторы или их сочетания: 1) парциальное давление кислорода; 2) эритропоэтическая активность костного мозга; 3) величина тканевых резервов" железа. С точки зрения клинициста, важно отметить, что всасывание железа повышено при многих анемиях, которые itp обусловлены недостаточностью железа. У большинства здоровых женщин при адекватной диете, видимо, всасывается несколько больше железа, чем у мужчин, благодаря чему достигается восполнение их более значительных потерь железа. У детей и подростков потребности организма в железе сходны (или несколько превышают) с потребностью менструирующих женщин. При адекватной диете за счет повышения всасывания железа эти потребности также могут быть удовлетворены. В норме потери организмом железа настолько малы, а его тканевые резервы так велики, что при полностью лишенной железа диете потребовалось бы приблизительно 3 года для развития недостаточности железа. Если же теряется кровь, то этот период значительно сокращается. Транспорт железа в плазме В плазме крови железо, находящееся в ферриформе и соединенное со специфическим связывающим белком трансферрином, представлено в концентрации примерно 18 мкмоль/л (100 мкг/дл). Этот белок в норме способен связать около 54 мкмоль/л (300 мкг/дл) железа; таким образом, в плазме трансферрин насыщен железом примерно на '/з Связанное с трансферрином железо транспортируется в тканевые резервы и костный мозг. В тканевых резервах оно представлено в виде ферритина и гемосидерина, а в тканях костного мозга железо частично может поступать из трансферрина непосредственно в развивающиеся эритроциты, участвуя в образовании гемоглобина. Свободное железо токсично и у здорового человека, по-видимому, отсутствует. В клетках кишечника и тканевых резервах железо, связанное с белком, представлено в виде ферритина и гемосидерина, в плазме крови оно связано с трансферрином и в эритроцитах включено в состав гемоглобина. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СОДЕРЖАНИЕ ЖЕЛЕЗА В ПЛАЗМЕ Определить содержание железа в плазме крови просят часто, но результаты таких анализов, редко имеющие важное значение для клинициста, зачастую интерпретируют ошибочно. Как мы уже видели, железо плазмы крови (подобно калию плазмы крови) составляет очень небольшую часть от его общего количества в организме. Даже учитывая только эту причину, следует признать, что вероятность использования показателя железа плазмы для суждения об общем содержании железа в организме невелика. Содержание калия в плазме крови, которое в норме относительно постоянно, имеет важное значение для организма в целом. Но железо плазмы крови, представляющее собой белковосвязанную транспортную фракцию, значительно варьирует даже при физиологических состояпнях организма. Физиологические факторы, влияющие на содержание железа в плазме Причины физиологических вариаций содержания железа в плазме крови еще мало изучены, но они совершаются очень быстро и предположительно основаны на сдвигах в содержании железа между плазмой крови и тканевыми резервами. Ниже мы анализируем факторы, воздействующие па содержание железа в плазме крови; первые три фактора могут у отдельных лиц обусловить изменения концентрации железа на 100% и более. Циклические вариации. Циркадный (суточный) ритм. В утренние часы содержание железа в плазме крови выше, чем в вечерние. Это различие может быть менее выраженным (или вообще отсутствовать), если пациент проводит бессонную ночь. У лиц, работающих в ночные часы, утром содержание железа в плазме крови ниже, чем вечером. Месячные вариации у женщин. Непосредственно перед или во время менструации содержание железа в плазме крови может быть понижено очень значительно, что, по-видимому, обусловлено не потерей крови, а воздействием гормональных факторов. Случайные вариации. Результаты определений содержания железа в плазме крови одного пациента, но полученной в разные дни, могут различаться существенно (иногда в 3 раза); на этом фоне циклические изменения уровня железа делаются незаметными. Обычно причину случайных вариаций установить не удается; иногда они связаны с физическим или психическим стрессом. Влияние беременности и пероральных контрацептивов. У женщин, принимающих некоторые пероральньге контрацептивы, содержание железа в плазме крови нарастает до величин, свойственных мужчинам. Аналогичное нарастание уровня железа происходит в течение первых нескольких недель беременности. Различия, связанные с полом и возрастом. Концентрация железа в плазме крови, подобно содержанию гемоглобина и числу эритроцитов, у мужчин выше, чем у женщин. Это различие, возможно, определяемое воздействием гормонов, становится заметным при половом созревании (до того, как происходит выраженная потеря организмом железа в связи с менструациями), исчезая при менопаузе. Андрогены обнаруживают тенденцию к повышению концентрации железа в плазме крови, тогда как эстрогены оказывают обратное действие. Патологические факторы, влияющие на содержание железа в плазме Низкая и высокая концентрации железа в плазме крови обычно обусловлены недостаточностью и перегрузкой железом. Недостаточность железа сопровождается гппохромной микроцитарной анемией и уменьшением количества окрашиваемого железа костного мозга. Перегрузка железом сопровождается увеличением количества окрашиваемого железа в ткани печени, получаемой методом биопсии. Любое заболевание, как острое, так и хроническое, вызывает гипоферремию; даже грипп может вызвать понижение концентрации железа в плазме крови. Такие хронические патологические состояния, как злокачественные новообразования, почечная недостаточность, ревматоидный артрит и хронические инфекционные болезни, часто сопровождаются нормоцитарной пормохромной анемией. Тканевые резервы железа при этом в пределах нормы или даже увеличены; анемия не поддается лечению препаратами гкелеза. При ревматоидном артрите особенно велика вероятность развития недостаточности железа на фоне анемии, сопровождающей хроническое заболевание. Используемые при лечении первичного патологического состояния салицилаты и другие противовоспалительные лекарственные средства могут вызывать небольшие кровотечения из мелких язв желудка. Наиболее чувствительным показателем развития этого осложнения является обнаружение не столько сниженного уровня железа в плазме крови, сколько гипохромных эритроцитов. При патологических состояниях, протекающих с нарушением утилизации железа костным мозгом, либо в связи с его гипоплазиеи, либо из-за отсутствия некоторых других необходимых для эритропоэза факторов (таких как витамин Bi2 или фолиевая кислота), содержание железа в плазме крови часто бывает высоким. Результаты исследования мазков крови и костного мозга могут дать типичную картину. В случаях пиридоксинчувствительной анемии и талассемии, например, при исследовании мазков крови могут быть получены результаты, напоминающие характерные для недостаточности железа. При двух указанных патологических состояниях увеличены тканевые резервы железа, что можно показать путем исследования мазков костного мозга. При гемолитической анемии железо гемоглобина из разрушенных эритроцитов высвобождается в плазму крови и поступает s ретикулоэндотелиальную систему. В плазме крови концентрация железа может быть высокой во время гемолитического приступа, но в период между приступами она обычно бывает в пределах нормы. При хронических патологических состояниях, сопровождающихся гемолизом, резервы железа в тканях мозга обычно увеличены. При острых заболеваниях печени повреждение клеток может высвобождать железо ферритина в кровоток, что вызывает транзиторное повышение концентрации железа в плазме крови. При диррозе уровни железа в плазме иногда могут быть высокими. Причины этого явления неясны. Иногда оно может быть обусловлено повышенным всасыванием железа в связи с увеличением •его поступления в организм. ТРАНСФЕРРИН И ОБЩИЙ РЕЗЕРВ СВЯЗЫВАНИЯ ЖЕЛЕЗА (ОРСЖ) Данные о концентрации железа в плазме крови сами по себе не дают полезных сведений о состоянии тканевых резервов железа. В тех редких случаях, когда и после гематологических исследований все еще остаются сомнения, можно повысить точность диагностики путем определения одновременно с измерением содержания железа в плазме крови концентрации трансферрина или способности плазмы связывать железо. Определять только содержание железа в плазме крови — это пустая трата времени и денег. Содержание трансферрина часто оценивают на основании результатов измерений способности плазмы крови связывать железо. Избыток неорганического железа смешивают с плазмой крови, после чего удаляют (обычно при помощи ионообменной смолы) все железо, которое не связалось с трансферрином. В пробе, содержащей плазму крови, измеряют содержание оставшегося железа; на основании полученных результатов оценивают общий резерв связывания железа (ОРСЖ). В настоящее время приобретают более широкое распространение методы прямого определения содержания трансферрина. Физиологические изменения уровней трансферрина. Уровень трансферрина менее лабилен, чем железа в плазме крови. Концентрация трансферрина в крови, однако, быстро нарастает после приема некоторых контрацептивных препаратов, о чем следует помнить при оценке результатов обследований женщин. Даже у женщин, имеющих соответствующие норме тканевые резервы железа, содержание трансферрина в плазме крови увеличивается при беременности (приблизительно после 28й недели). Патологические изменения уровнен трансферрина. Уровень трансферрина и ОРСЖ повышается при недостаточности железа, ио понижается при перегрузке им. Уровень трансферрина и ОРСЖ понижается при хронических заболеваниях, связанных с низкой концентрацией железа в плазме крови. При нефротическом синдроме возможно понижение обоих показателей в связи с тем, что трансферрин теряется из организма с мочой. При острых инфекционных заболеваниях содержание трансферрина и ОРСЖ не изменяется. Таким образом, при неосложненной недостаточности железа снижение концентрации железа в плазме крови сопровождается увеличением уровня трансферрина и ОРСЖ. Анемия, не обусловленная недостаточностью железа, связала с низким уровнем ОРСЖ. При сочетании недостаточности железа с анемией, сопровождающей хронические инфекционные заболевания, противоположные эффекты этих двух патологических состояний на концентрацию трансферрина затрудняют интерпретацию результатов определений этого параметра, а также измерений содержания железа. ПРОЦЕНТ НАСЫЩЕНИЯ ОРСЖ Предположение, что в норме ОРСЖ насыщен железом на '/з, довольно приблизительное. Физиологические варианты содержания железа в плазме крови редко сопровождаются существенными изменениями ОРСЖ, и степень насыщения белка железом колеблется в широких пределах. В процентах степень насыщения равна: 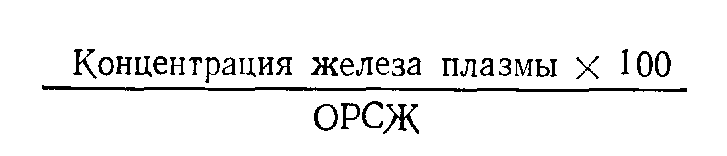 Полагают, что выраженная в процентах степень насыщения является более адекватным показателем, характеризующим резервы железа, чем концентрация железа в плазме крови сама по себе. Если степень насыщения составляет величину, меньшую 16%, то можно считать вероятным наличие недостаточности железа. Первое из этих положений, очевидно, справедливо, так как при недостаточности железа понижение уровня железа в плазме сопровождается повышением ОРСЖ. Таким образом, при недостаточности железа величина процента насыщения будет относительно ниже, чем в норме при одинаковой концентрации железа в плазме. Насыщение на величину порядка 16%, однако, можно обнаружить, например, в периоды, предшествующие менструации, и при острых инфекционных заболеваниях на фоне отсутствия изменения ОРСЖ или запасов железа. По-видимому, более целесообразно учитывать результаты как определений содержания железа в плазме, так и ОРСЖ, чем вычислять процент насыщения. В табл. 31 представлены результаты лабораторных исследований при заболеваниях, которые могут оказать влияние на сотдержание в плазме железа и трансферрина и ОРСЖ. Таблица 31. Изменения в плазме содержания железа (Fe) и трансферрина или общего резерва связывания железа (ОРСЖ)
СОДЕРЖАНИЕ ФЕРРИТИНА В ПЛАЗМЕ КРОВИ В норме плазма крови содержит приблизительно 100 мкг/л ферритина. Ферритин циркулирующей крови находится в состоянии равновесия с ферритином тканевых резервов. По-видимому, если концентрация ферритина в крови меньше 10 мкг/л, то это свидетельствует о недостаточности железа. Эти результаты, однако, редко помогают в постановке диагноза. Более важное значение имеют данные о повышении концентрации ферритина, полученные в случаях перегрузки железом или заболеваний печени. ЛЕЧЕНИЕ ЖЕЛЕЗОМ Парентеральная терапия препаратами железа может легко приводить к перегрузке организма железом, поскольку экскреция железа не поддается активной регуляции и его содержание в организме контролируется процессами его всасывания. Перегрузки организма железом следует опасаться и при повторных переливаниях крови. В 0,5 л донорской крови содержится приблизительно 4,5 ммоль (250 мг) железа. При анемиях, не связанных с истинной недостаточностью железа, его тканевые резервы и пределах нормы или даже повышены. Назначать препараты же леза, даже при доказанной его недостаточности, рекомендуется внутрь, но пе парентерально. Повторные переливания крови могут требоваться при лечении тяжелых анемий, например, в случаях хронических заболеваний почек и гипопластпческой анемии. Но назначать таким больным переливания крови следует с осторожностью, помня об опасности перегрузки железом. Даже в тех случаях, когда тканевые резервы железа повышены, анемия повышает скорость всасывания железа. Лечение. например, хронической гомолитической анемии препаратами железа, назначаемыми внутрь, может в некоторых случаях при нести к перегрузке организма железом. Применение этих препаратов пе облегчает точение анемии, которая связана с повышенной скоростью распада эритроцитов по сравнению со скоростью их образования, но пе с недостаточностью железа. Высвобождаемое железо остается в организме. Аналогичная опасность существует и при других апемпях, не связанных с недостаточностью железа. Хотя всасывание железа в определенной степени регулируется, зта система регуляции неэффективна; в редких случаях она может быть нарушена большими нагрузками железа, даже к отсутствие анемии. Имеется сообщение о перегрузке железом организма женщины, пе страдавшей анемией, но принимавшей внутрь годами препараты железа вопреки рекомендациям врачей. Лечение железом потенциально опасно; его следует назначать с осторожностью и лишь в тех случаях, когда его недостаточность доказана. ПЕРЕГРУЗКА ЖЕЛЕЗОМ Как уже указывалось выше, железо из организма фактически не экскретируется. Железо, всасываемое из желудочнокишечного тракта или вводимое парентерально в количествах, превосходящих суточные потери, накапливается в тканевых резервах. Если такой положительный баланс существует длительно, то резервы железа могут превысить 350 ммоль (20 г), что приблизительно в 5 раз выше пормы. Причины перегрузки железом. Повышенное всасывание железа в кишечнике может происходить в следующих случаях: 1) идиопатический гемохроматоз; 2) анемия с повышенным, но неэффективным эритропоэзом; 3) заболевание печени (редко); 4) избыток железа в диете; 5) неадекватная терапия препаратами железа, назначаемыми внутрь. Парентеральное введение железа может быть при повторных переливаниях крови или при неадекватной терапии препаратами железа, назначаемыми парентерально. В очень редких случаях причиной перегрузки железом является врожденная недостаточность трансферрина. Последствия перегрузки железом. Воздействия накапливающегося железа зависят от его распределения в организме. В свою очередь распределение в организме отчасти зависит от путей поступления железа. Результаты исследований секционного материала пли тканей, полученных методом биопсии, указывают на существование двух основных типов патологических изменений: перегрузки железом паренхиматозных тканей и ретикулоэндотелиальной системы. Перегрузка железом паренхиматозных тканей встречается при идиопатпческом гемохроматозе и у больных с неэффективным эритропоэзом. Железо накапливается в паренхиматозных клетках печени, поджелудочной железы, сердца и других органов. Обычно эти явления сопровождаются функциональными расстройствами n/iii повреждониямп тканей. Перегрузку железом ретпкулоэндотелиальпой системы отмечают после парентерального введения препаратов железа в чрезмерных количествах или после многократных переливаний кровп. Первоначально железо накапливается в клетках ретпкулоэндотелиальной системы печени, селезенки и костного мозга. Патогенные эффекты при этом малочисленны, но существуют обстоятельства, при которых распределение железа может изменяться таким образом, что развиваются поражения паренхиматозных органов. При перегрузке, связанной с избытком железа в диете, возможно развитие перегрузки железом как ретикулоэндотелиальной системы, так и паренхиматозных органов, что сопровождается явлениями цинги и остеопороза. Вне зависимости от причины значительной перегрузки железом, при этом может происходить накопление железа в паренхиматозных органах и поражение тканей. Следует дать определения широко используемых терминов: гемосидероз и гемохроматоз. Гемосидероз представляет собой гистологический термин, обозначающий повышение содержания гемосидерина в тканевых резервах железа. Наличие гемосидероза пе обязательно свидетельствует об увеличении общего содержания железа в организме. Так, например, при анемиях многих типов содержание железа гемоглобина понижено (меньше гемоглобина), но железо тканевых резервов нарастает. Гемохроматоз — термин, обозначающий клинический симптом, обусловленный поражением паренхиматозных органов в связи с накоплением железа. Синдромы перегрузки железом Идиопатический гемохроматоз. Идиопатический гемохроматоз представляет собой генетически детерминированное заболевание, при котором повышенное всасывание железа в кишечнике приводит в течение многих лет к накоплению больших количеств же леза в паренхиматозных органах. К числу клинических проявлений, наблюдаемых впервые обычно у больных среднего возраста, относятся цирроз в сочетании с сахарным диабетом, гипогонадизм и усиленная пигментация кожи. Из-за потемнения кожи (обусловленного повышением содержания меланина, но не отложением железа) это патологическое состояние назвали бронзовым диабетом, хотя пигментация выглядит в большей мере серой, чем бронзовой. Нарушения сердечной деятельности могут занимать важное место среди проявлений заболевания, особенно у относительно молодых больных, многие из которых погибают от сердечной недостаточности. Развитие гепатоцеллюлярной карциномы было отмечено примерно в 10—20% случаев. Идиопатический гемохроматоз наследуется по аутосомнорецессивному типу. При обследованиях родственников больных важно учитывать факт тесной взаимосвязи гена, участвующего в развитии данного заболевания, с генным локусом HLA. У членов семьи, имеющих гаплотип HLA, идентичный таковому больного, может развиться идиопатический гемохроматоз. Такие факторы, как злоупотребление алкоголем, могут ускорить накопление железа и способствовать развитию поражений печени. Идиопатический гемохроматоз бывает трудно дифференцировать от алкогольного цирроза. При обоих патологических состояниях возможны сахарный диабет и гипогонадизм. Хотя частота таких осложнений выше при идиопатическом гемохроматозе, это не помогает в постановке диагноза каждого отдельного случая. Результаты исследований ткани печени, полученной методом биопсии, могут еще больше дезориентировать. Нередко при алкогольном циррозе в печени повышено содержание окрашиваемого железа. Некоторые алкогольные напитки, в частности вина, содержат значительные количества железа. Доказано, что при циррозе всасывание железа может быть усилено, по-видимому, в связи с воздействием алкоголя. Однако у большинства больных с циррозом, по данным химического тестирования, тканевые резервы железа не повышены; результаты исследований тканей печени, полученных методом биопсии, указывают на преимущественную локализацию железа в портальном тракте. При циррозе патологические изменения, выявляемые клиническими, гистологическими и биохимическими методами, обычно выражены в большей степени, чем сдвиги в содержании железа, тогда как для гемохроматоза характерна обратная картина на фоне, казалось бы, одинакового накопления железа. В редких случаях у больных с циррозом печени или портокавальным шунтом может быть истинная перегрузка железом, поэтому дифференциальная диагностика с идиопатическим гемохроматозом может быть крайне затруднена. Данные семейного анамнеза или результаты обследований близких родственников больного могут помочь в диагностике. В любом случае методы лечения перегрузки железом идентичны. Если идиопатический гемохроматоз диагностирован, обследования других членов семьи пациента обязательны; лицам с повышенным содержанием железа назначают соответствующее лечение. Лечение перегрузки железом. Больным с идиопатическим гемохроматозом обычно 1 раз в неделю делают кровопускание (после венесекции) для удаления избытка железа до тех пор, пока не понизится уровень гемоглобина. С каждой порцией 0,5 л крови выводится 4,5 ммоль (250 мг) железа. Анемия и перегрузка железом. Перегрузка жолезол! может сопровождаться развитием анемии нескольких типов. В некоторых случаях, как, например, при апластической анемии и анемии, сопровождающей хроническую почечную недостаточность, перегрузка железом обусловлена повторными многократными переливаниями крови, llpii этом железо сначала накапливается в рстикулоэндотелиальной системе. При значительной перегрузке (свыше 100 порций крови, приблизительно 0,5 л каждая) может развиться перегрузка железом паренхиматозных органов и гемохроматоз. При таких анемиях, как талассемический синдром и спдеробластическая анемия (характеризующихся эритроидной гиперплазией костного мозга на фоне недостаточности эритропоэза), повышается также всасывание железа. В условиях переливания крови гемохроматоз развивается при меньшей нагрузке железом, чем в случае апластической анемии. Перегрузку железом, связанную с анемией, безусловно, нельзя лечить кровопусканиями, которые привели бы к ухудшению состояния больных с анемией вследствие удаления из кровяного русла дополнительных количеств гемоглобина. Усугубление перегрузки железом в результате переливания крови можно снизить, назначая каждый раз дефероксамин, образующий с любым введенным железом, не входящим в состав гемоглобина, внутрикомплексные соединения, экскретирующиеся с мочой. Алиментарная перегрузка железом. Повышенное всасывание железа, обусловленное его чрезмерным содержанием в диете, встречается редко. Источником железа может быть пиво в металлических сосудах. Обычно избыток железа обнаруживают только в ретикулоэндотелиальной системе и печени (как в портальном тракте, так и паренхиматозных клетках); при этом повреждения тканей отсутствуют. В редких случаях, когда происходит отложение железа в паренхиматозных клетках других органов, клиническая картина сходна с таковой идиопатического гемохроматоза. Алиментарную перегрузку железом можно отличить по его высоким концентрациям в ретикулоэндотелиальной системе, что устанавливают в ходе исследований костного мозга и селезенки (при аутопсии). При этой форме перегрузки железом возможны цинга и остеопороз. Недостаточность аскорбиновой кислоты может быть обусловлена ее необратимым окислением в присутствии чрезмерного количества железа; остеопороз иногда сопровождает цингу. Недостаточность аскорбиновой кислоты препятствует также нормальной мобилизации железа из ретикулоэндотелиальных клеток; содержание железа в плазме крови при этом может быть низким, а ответная реакция на воздействие комплексообразующих агентов слабой, несмотря на перегрузку железом. ЗАКЛЮЧЕНИЕ 1. Экскреции значительного количества железа из организма не происходит. Тканевые резервы железа регулируются его всасыванием. Поэтому парентеральную терапию препаратами железа следует проводить осторожно. 2. Даже в отсутствие дефицита железа, при анемии его всасыаапнс усилниастсд. Поэтому при анемии по следует назначать препараты железа внутрь с лечебными целями, за исключением тех случаев, когда анемия обусловлена недостаточностью железа. 3. При физиологических состояниях содержание железа в плазме крови варьирует в значительной степени. 4. Во многих случаях при анемии, но обусловленной недостаточностью железа, содержание железа в плазме крови понижается. 5. По этим двум причинам (3 и 4) содержание железа в плазме крови само по себе является очень ненадежным показателем состояния тканевых резервов железа в организме. 6. В плазме циркулирующей крови железо связано с белком трансферрином. О содержании трапсферрица часто судят косвенно по результатам измерения общего резерва связывания железа (ОРСЖ) плазмы крови. 7. При недостаточности железа ОРСЖ увеличивается, а при перегрузке железом — уменьшается. 8. Во многих случаях при анемии, связанной с низким содержанием железа в плазме крови, но не обусловленной его недостаточностью, ОРСЖ уменьшается. 9. Данные о низкой концентрации железа в плазме крови при высоком ОРСЖ более информативны как показатель недостаточности железа, чем только сведения о понижении его уровня в плазме крови. 10. Простые гематологические тесты—самые быстрые, дешевые и информативные показатели недостаточности железа. Прежде чем давать направление на определение содержания железа в плазме крови, следует проделать простые гематологические тесты. 11. Факторы, определяющие распределение избытка железа, полностью не изучены. Для всех форм перегрузки паренхиматозных органов общей особенностью является высокая степень (в процентах) насыщения железом трансферрина. 12. Перегрузка железом может быть следствием чрезмерного всасывания из кишечника или парентерального введения железа (обычно при переливании крови). При разных формах перегрузки железом его распределение в организме различно. 13. О перегрузке железом можно судить по реакции организма на повторные кровопускания или комплексообразующие агенты. Только при наличии значительной перегрузки железом можно диагностировать идиопатический гемохроматоз. 14. Фактически во всех случаях перегрузки железом паренхиматозных органов обнаруживают высокую концентрацию железа в плазме крови и высокую степень насыщения (в процентах) железом трансферрина. 15. Хотя концентрации ферритина в плазме крови при перегрузке железом часто повышены, результаты определений ферритина могут быть дезориентирующими. СПИСОК ЛИТЕРАТУРЫ Finch С. A., Haebers H. Perspectives of iron metabolism. — New Engl. J. Med., 1982, 306, 1520—1528. Halliday ]. W; Powell L. W. Iron overload. — Semin. Hemat., 1982, 19, 42-53. ИССЛЕДОВАНИЯ НАРУШЕНИИ ОБМЕНА ЖЕЛЕЗА Исследования анемий Анемии могут быть обусловлены недостаточностью железа плп множеством других факторов. В учебниках гематологии вопросы диагностики анемии изложены более подробно. Целесообразно, однако, рассмотреть рекомендуемую последовательность выполнения исследований прп анемии с тем, чтобы оценить возможное значение результатов определений содержания железа в плазме крови. 1. Предположение клинициста о наличии анемии следует подтвердить определением содержания гемоглобина. Возможна, одпако, недостаточность железа при содержании гемоглобина в пределах нормы. 2. Следует обратить внимание на средний эрнтроцитарпый гемоглобин (СЭГ) и средний эритроцитарньш объем (СЭО); если необходимо, исследуйте мазок крови. При недостаточности железа анемпя относится к гппохромному и микроцитарному типу; гипохромия может быть обнаружена до того, как уровень гемоглобина упадет ниже нормы. Нормоцитарпая, нормохромная анемия не является специфичной для какоголибо определенного заболевания. Она не обусловлена недостаточностью железа, если не было недавней кровопотери. Характерные особенности анемий других' типов можно обнаружить при исследовании мазка крови. В большинстве случаев анемии данные перечисленных исследований в сочетании с клиническими наблюдениями позволяют установить причину анемий. Наиболее вероятны затруднения при диагностике таких редких анемий, как талассемия и пиридоксинчувствительная анемия. Они также являются гипохромными, но нс обусловлены недостаточностью железа. 3. Исследование мазка костного мозга может потребоваться для подтверждения диагноза (например, мегалобластической анемии). Еслп такой мазок сделан, наилучшим способом характеристики резервов железа является окрашивание ферроцианидом калия. Если пункция костного мозга не представляется обоснованной п в тех редких случаях, когда диагноз остается неясным, результаты биохимических исследований иногда могут оказаться полезными. Если такие исследования необходимы, следует определить содержание железа в плазме крови и ОРСЖ или трансферрин. Результаты определений только содержания железа неинформативны. Тест на всасывание железа. Если при обследовании больного с доказанным дефицитом железа в течение нескольких недель после назначения внутрь препаратов железа не нидны признаки улучшения состояния, то он, по-видимому, не принимает назначенные таблетки. Это предположение подтверждается нормальной (но не темной) окраской фекалий (что при необходимости можно установить путем ректального обследования). Если препараты железа действительно им принимались, то иногда причиной наблюдаемых явлений может быть нарушение всасывания (обычно как часть общего дефекта всасывания). В тех случаях, когда доказательства нарушения всасывания (гл. XII) отсутствуют, адекватность всасывания железа можно оценить путем измерения увеличения содержания железа в плазме крови после приема внутрь стандартной дозы (300 мг) эликсира железа. Это увеличение будет существенным (до 40 мкмоль/л), если всасывание у больного с доказанной анемией, обусловленной недостаточностью железа, не нарушено. Если указанное увеличение очень мало, то это может быть обусловлено следующими обстоятельствами: 1) недостаточностью всасывания; 2) отсутствием анемии у обследуемого (у которого в норме не аропсходпт Есасывавия большого количества железа); 3) наличием у больного анемии, не обусловленной недостаточностью железа (всасываемое железо быстро поступает в тканевые резервы). Чтобы избежать ошибок при интерпретации, следует поставить диагноз недостаточности железа до проведения теста. Исследования при подозрении на перегрузку железом Первоначальное тестирование. Определите содержание железа в плазме крови, насыщение (в %) железом трансферрина и содержание ферритина в плазме крови. При идиопатическом гемохроматозе концентрация железа в плазме почти всегда высока; часто она превышает 36 мкмоль/л (200 мкг/дл). Это явление сочетается с уменьшением содержания трансферрина (судя по уменьшению ОРСЖ); при этом насыщение (в %) железом трансферрина обычно превышает 80%, часто достигая 100%. При злокачественных опухолях или инфекционных болезнях содержание железа в плазме крови и степень насыщения (в %) железом трансферрина может быть ниже ожидаемого; ОРСЖ остается пониженным. Мы уже упоминали о том, что при недостаточности аскорбиновой кислоты уровень железа в плазме крови снижен. При перегрузке железом (с его накоплением в ретикулоэндотелиальной системе или в паренхиматозных органах) у большинства больных уровень ферритина в плазме крови высокий. Описано лишь несколько семей с идиопатическим гемохроматоэом, несмотря на нормальные уровни ферритина в плазме крови. Вероятность перегрузки железом невелика, если все три определяемые величины находятся в пределах нормы. Доказательство повышения резервов железа. Диагноз перегрузки железом может быть поставлен только после того, как будет доказано увеличение резервов железа в организме. Реакция организма на венесекцию. Если состояние больного не улучшается в ответ на проводимые с лечебными целями повторные венесекции, то это служит наиболее убедительным (хотя и ретроспективным) доказательством увеличенных резервов железа. Если резервы железа в норме, повторные еженедельные венесекции (приблизительно по 0,5 л крови, что соответствует 4,5 ммоль, или 250 мг железа) быстро приводят к уменьшению железа в плазме крови, а вскоре и к развитию анемии вследствие недостаточности железа. Однако у больных с идиопатическим гемохроматозом можно удалить таким путем из организма 350 ммоль (20 г) и более железа, но сим птомы его недостаточности не развиваются. Применение комплексообразующих реагентов. Альтернативный подход заключается в использовании комплексообразующего действия таких веществ, как дефероксамин, которые связывают железо и затем выводятся с мочой. После введения дефероксамина больные с повышенными запасами железа экскретируют с мочой железа больше, чем здоровые. Уровни ферритина в плазме высокие в большинстве случаев перегрузка железом ретикулоэндотелиальной системы, но при идпопатическом гемохроматозе они, как правило, в норме. При многих заболеваниях печени (в том числе циррозе) содержание ферритина в плазме крови может быть повышено. Полученная путем биопсии ткань печени содержит большие количества окрашиваемого железа, которое может быть либо в паренхиматозных, либо ретикулоэндотелиальных клетках. Результаты химического определения содержания железа более надежны, чем таковые гистохпмических исследований. В тканях костного мозга содержание железа обычно в пределах нормы при гемохроматозе, когда перегрузка железом бывает преимущественно riaренхиматозного типа, но при перегрузке ретикулоэндотелиальных клеток содержание железа в костном мозге может быть резко повышено. Аналогичную перегрузку ретикулоэндотелиальных клеток обнаруживают в случаях нарушения утилизации железа костного мозга для синтеза гемоглобина, как это происходит при многих гематологических заболеваниях, злокачественных опухолях и хронических воспалительных процессах. Обследования членов семьи больного. Целесообразно обследовать родственников больного, у которого диагностирован идиопатический гемохроматоз. Наиболее чувствительными тестами являются определения содержания железа в плазме крови и насыщения (в%) железом трансферрина. Если резервы железа существенно не повышены, содержание ферритина в плазме крови может быть в пределах нормы. Для идентификации лиц с наиболее высокой вероятностью наследования гемохроматоза рекомендуется, по возможности, проводить HLAтипирование. ГЛАВА XIX |
