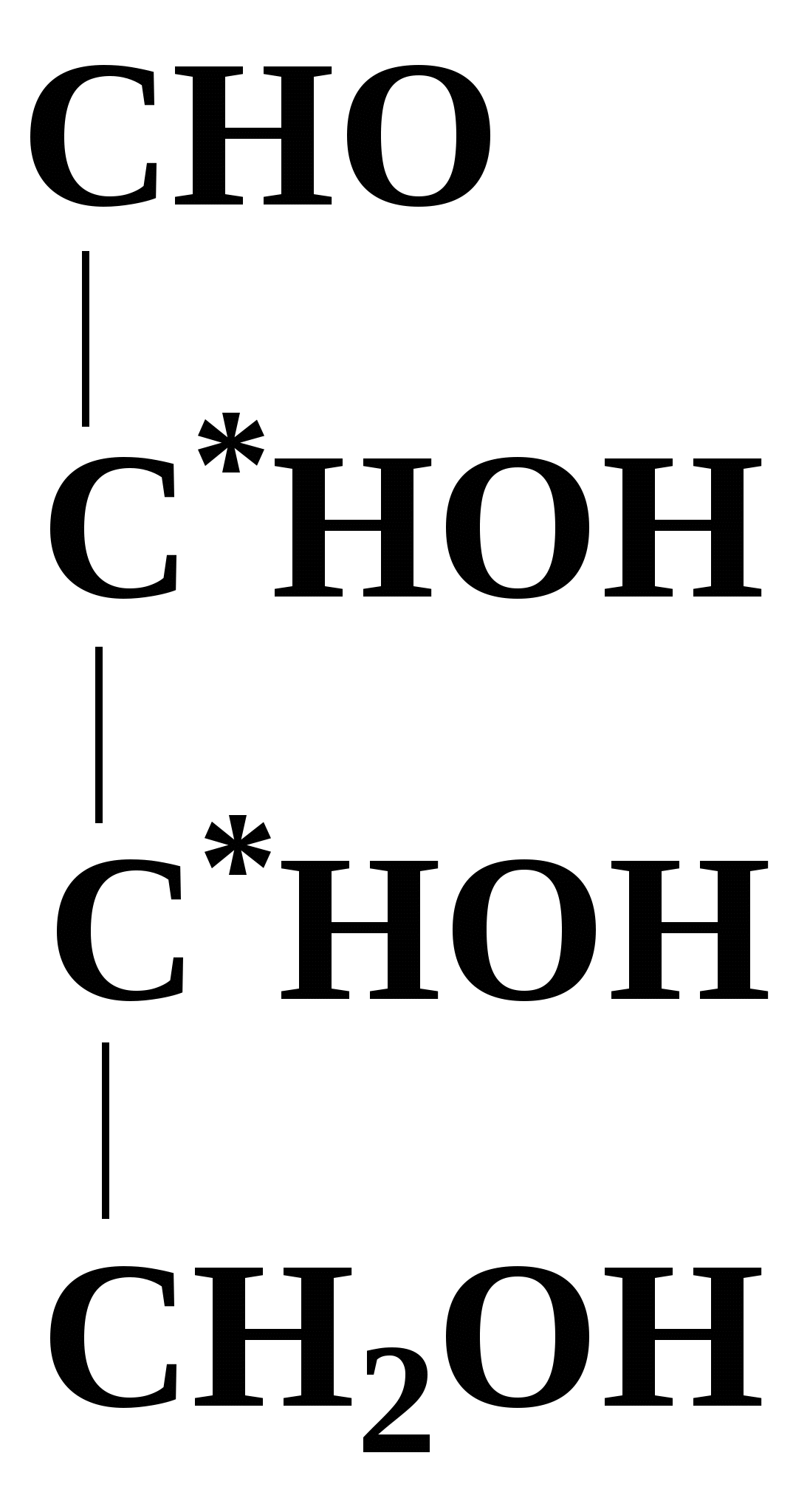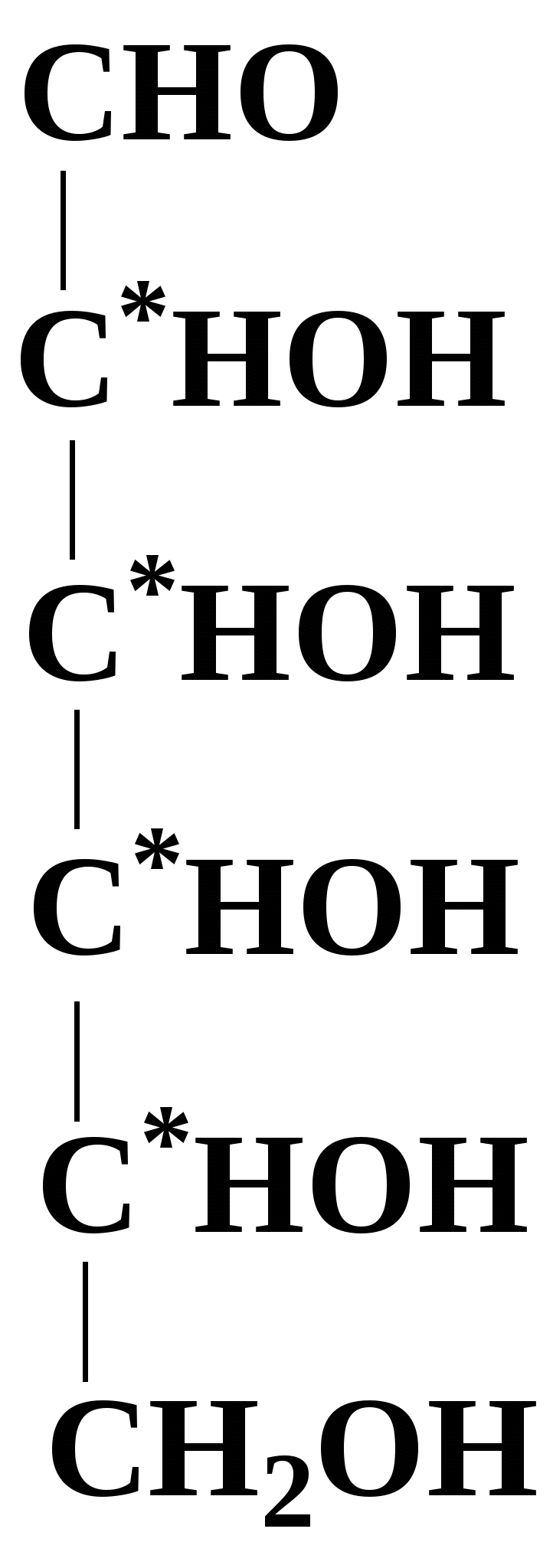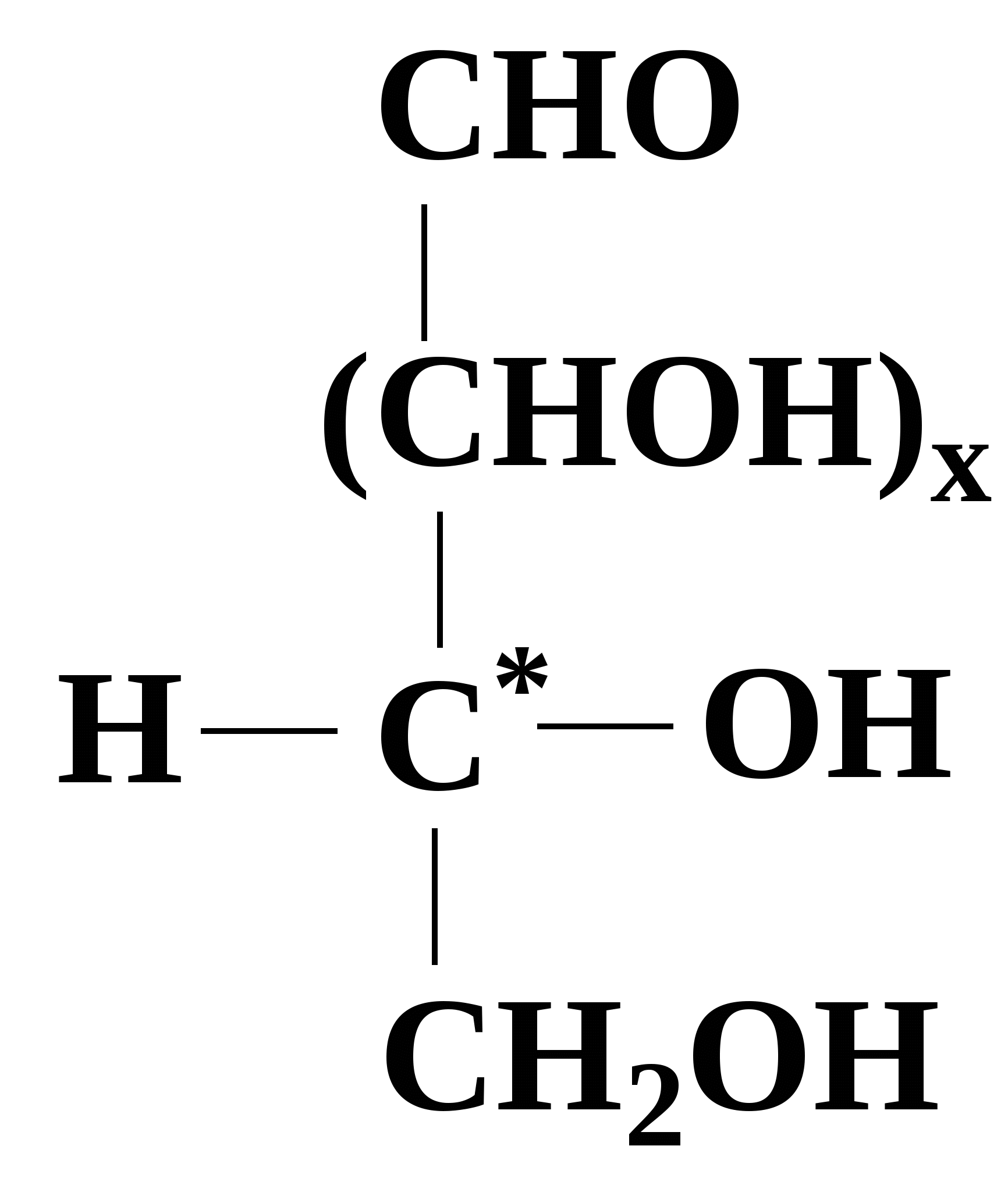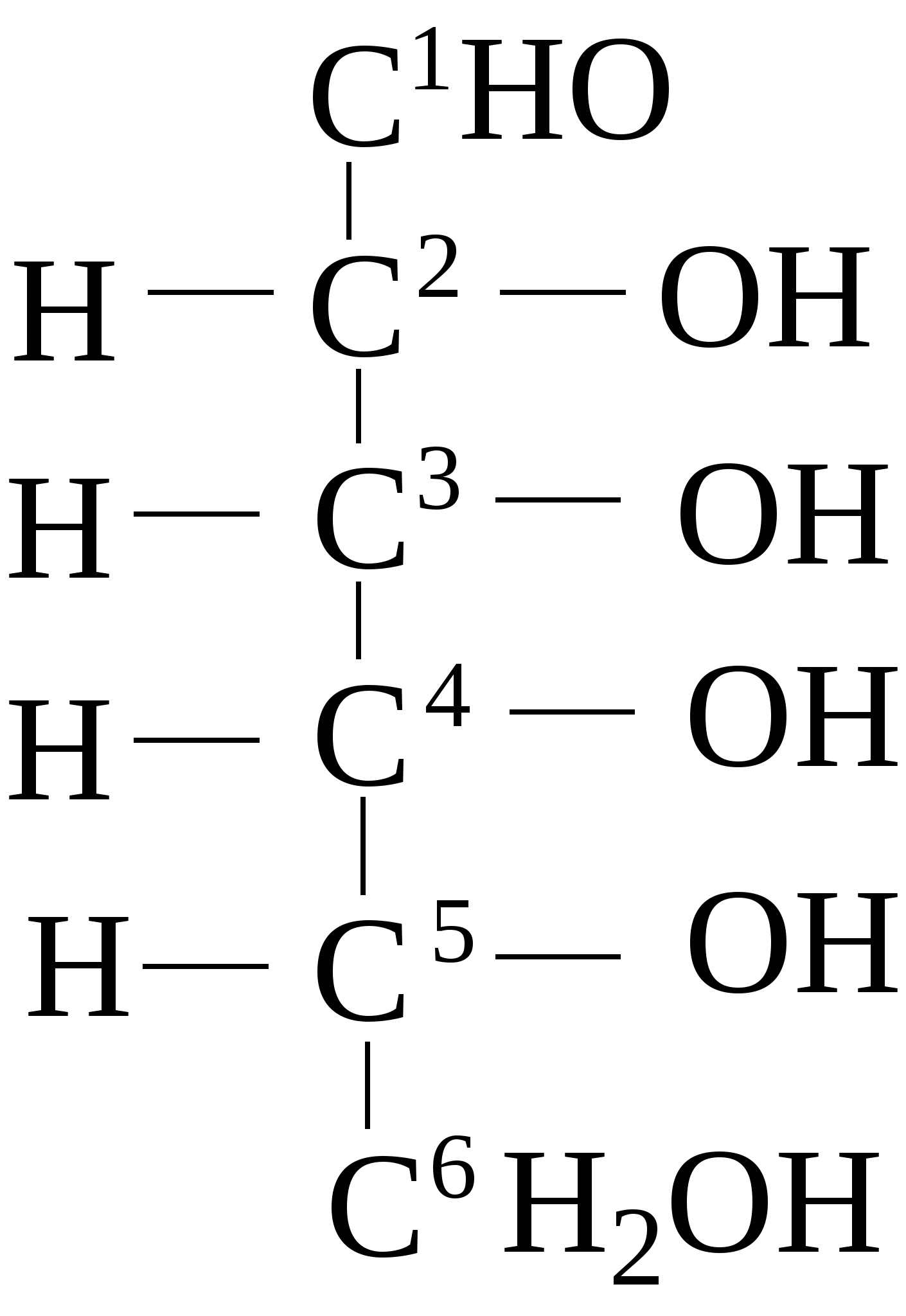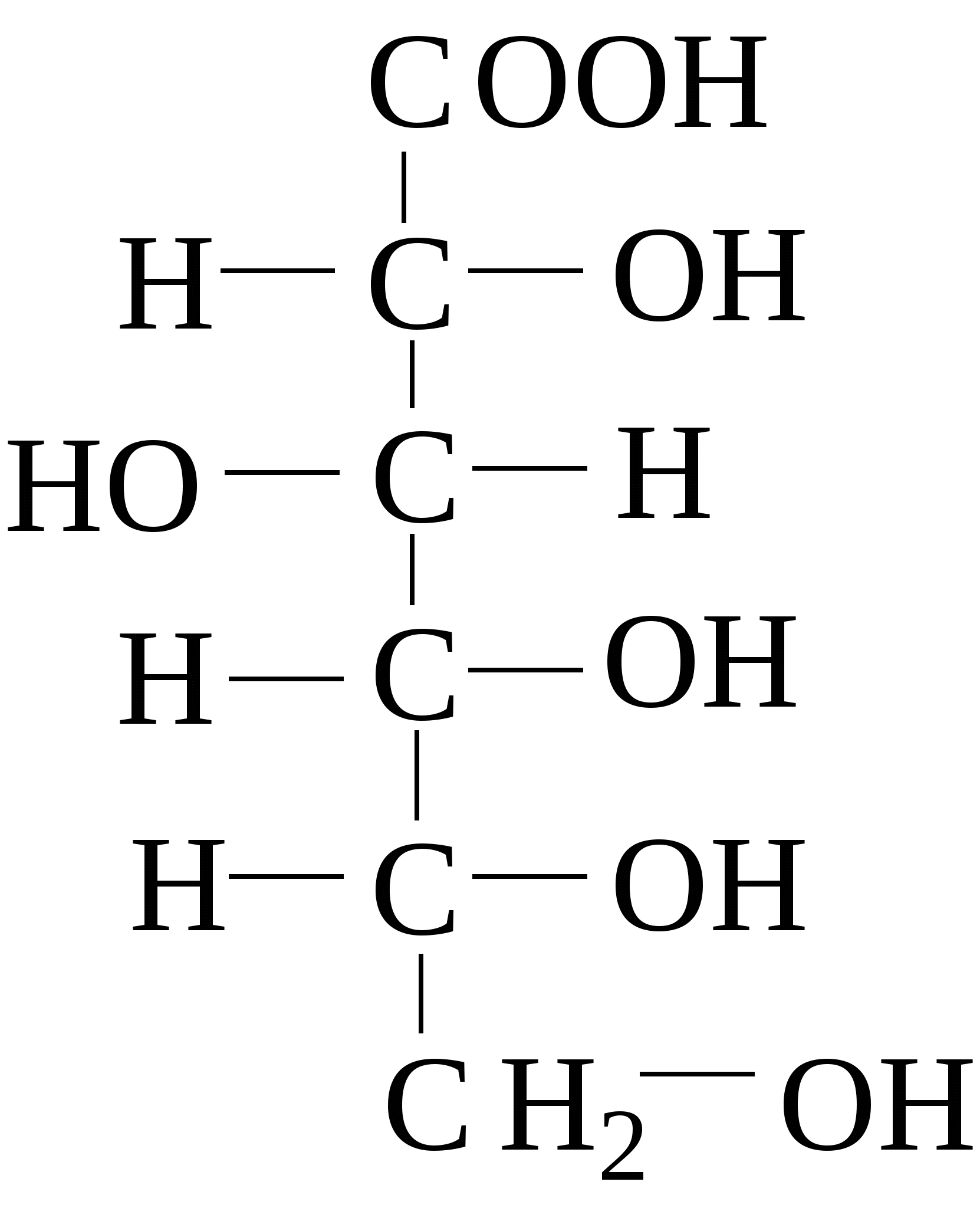Основы биологической химии предисловие
 Скачать 7.85 Mb. Скачать 7.85 Mb.
|
Глава 3. УГЛЕВОДЫ
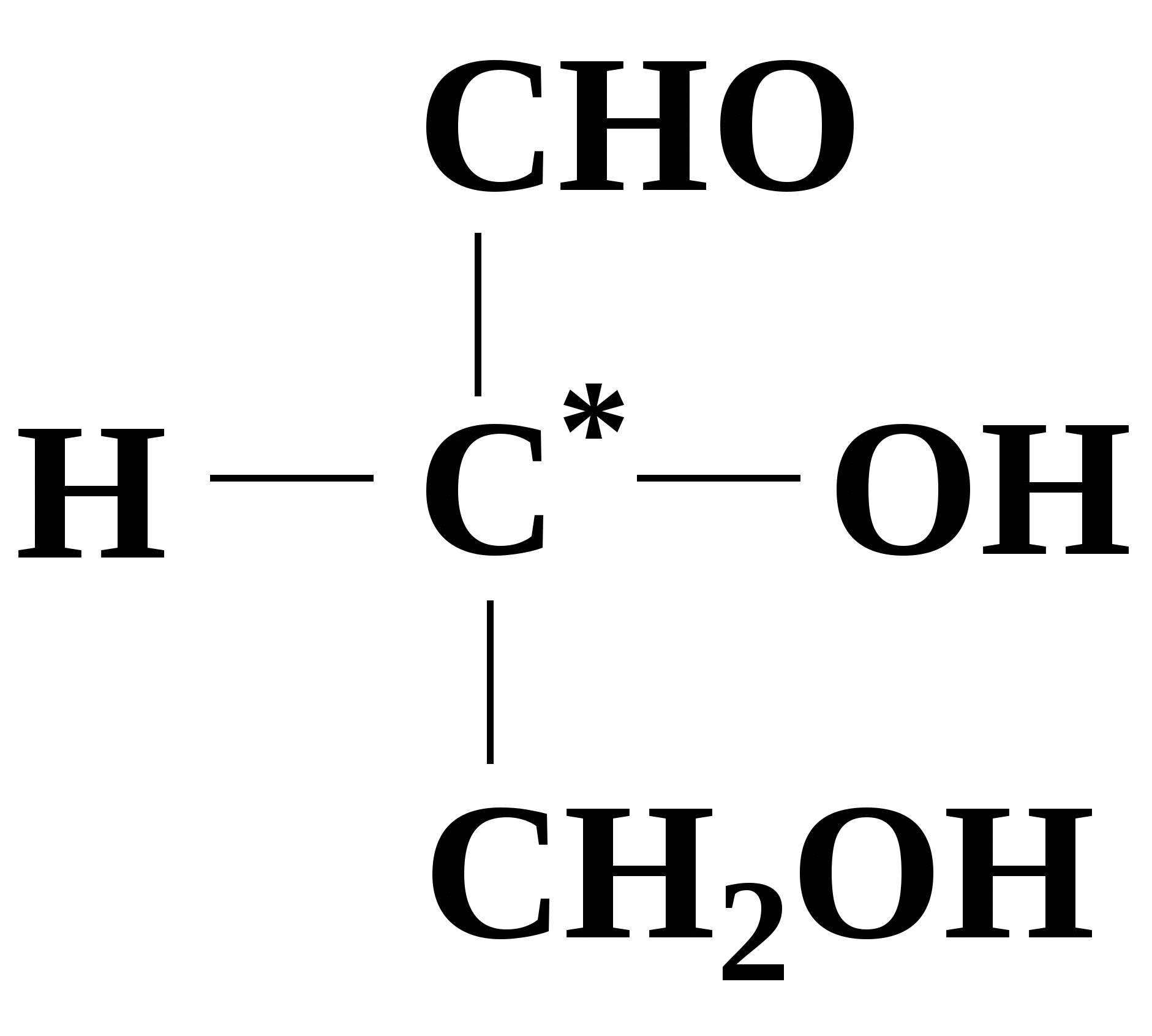
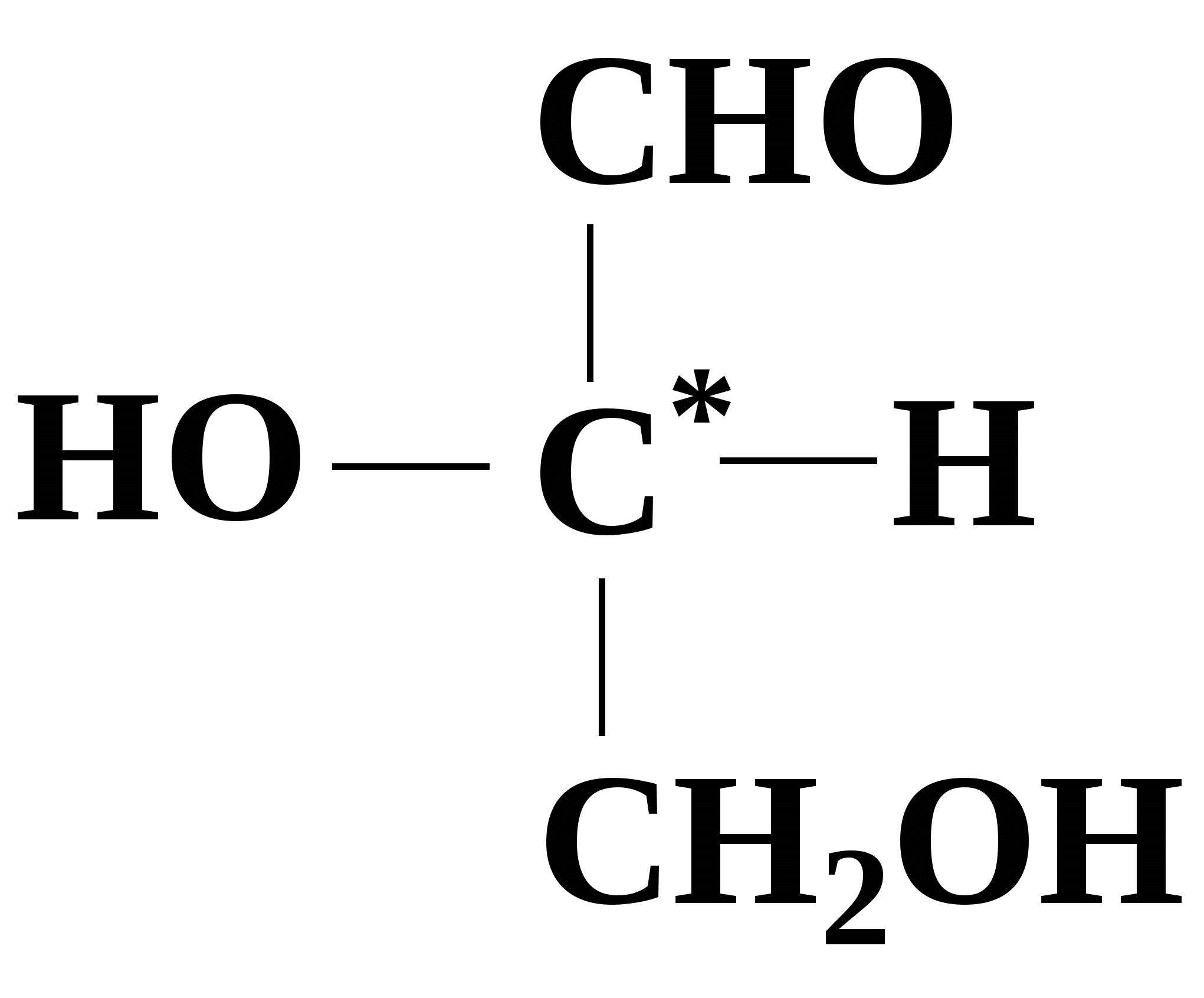
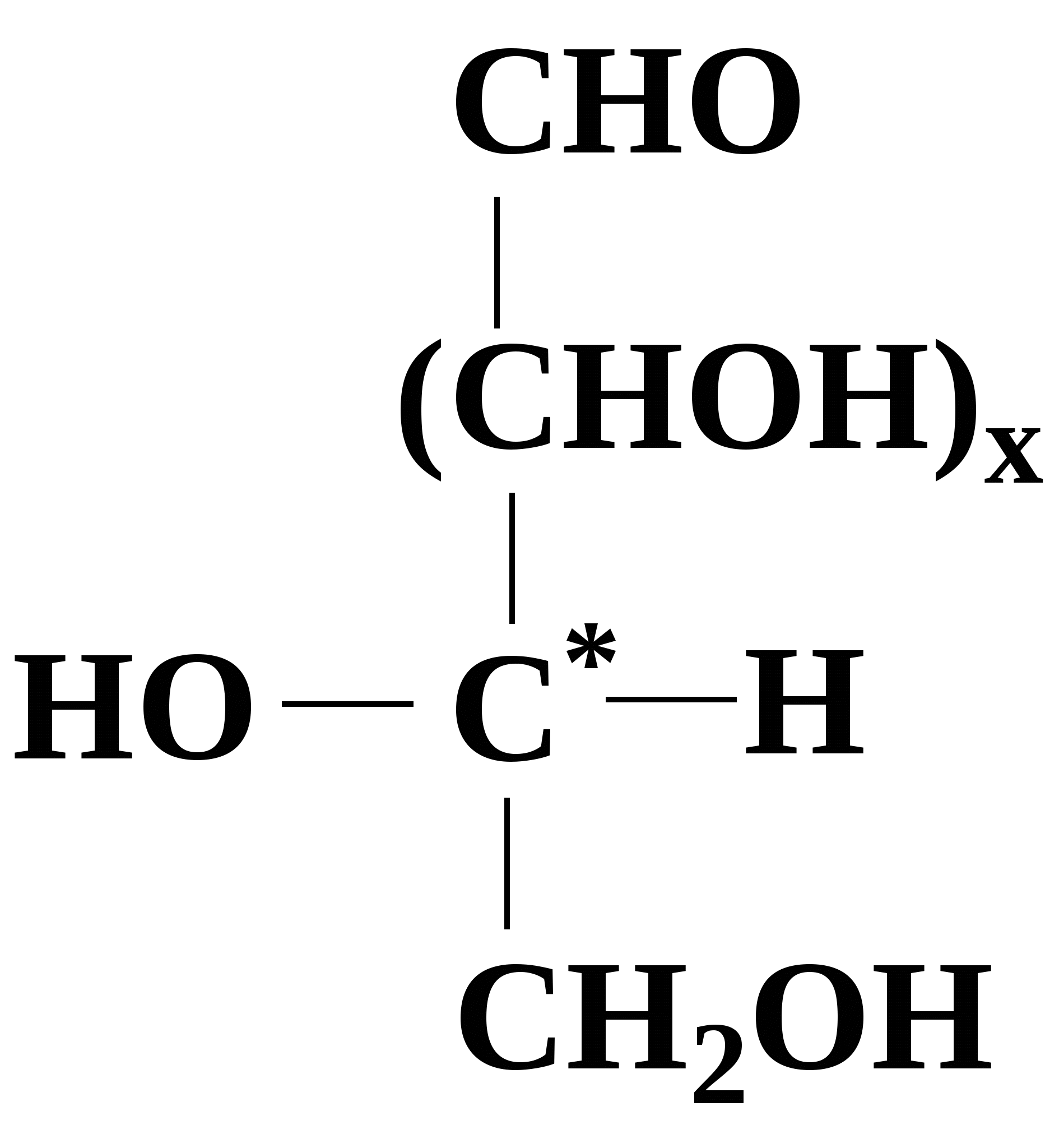
Принадлежность моносахарида к D- или L-ряду определяется расположением атома водорода и гидроксила у последнего асимметрического атома углерода по сравнению с их расположением у D- и L-глицеринового альдегида. Тот изомер, у которого при проекции на плоскость ОН-группа у асимметрического атома углерода расположена с правой стороны, принято считать D - глицеральдегидом, а зеркальное отражение - L-глицеральдегидом:
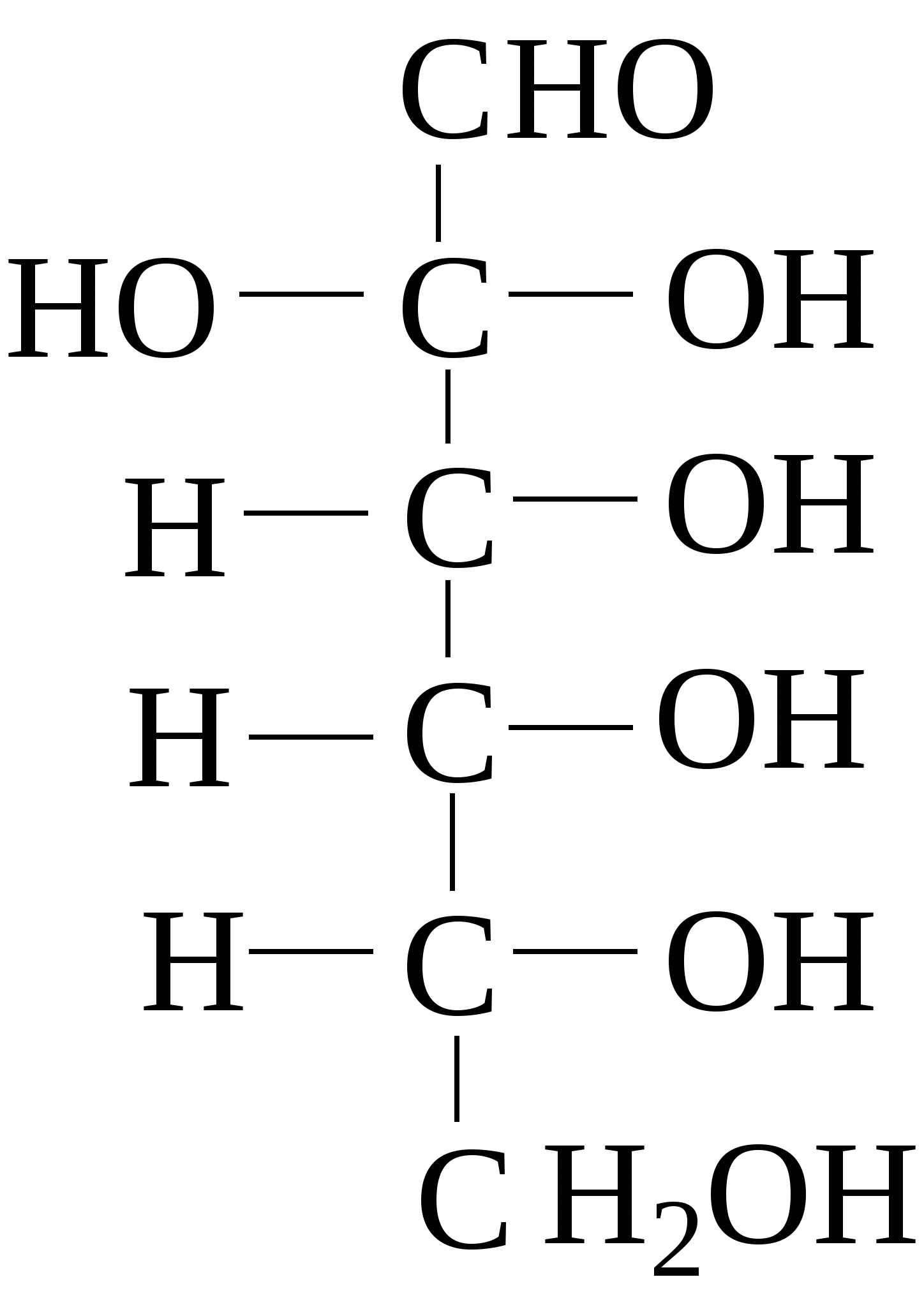
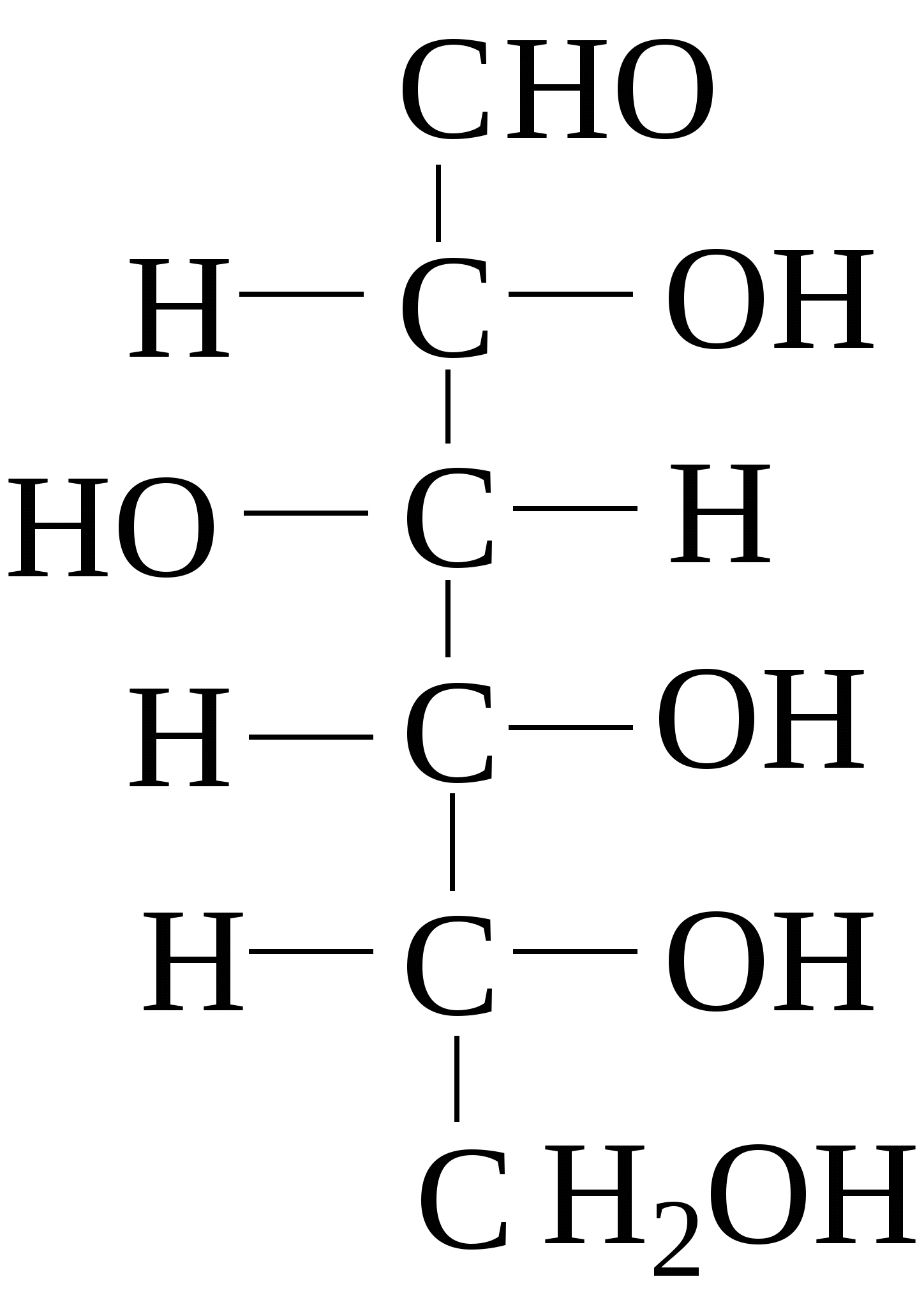
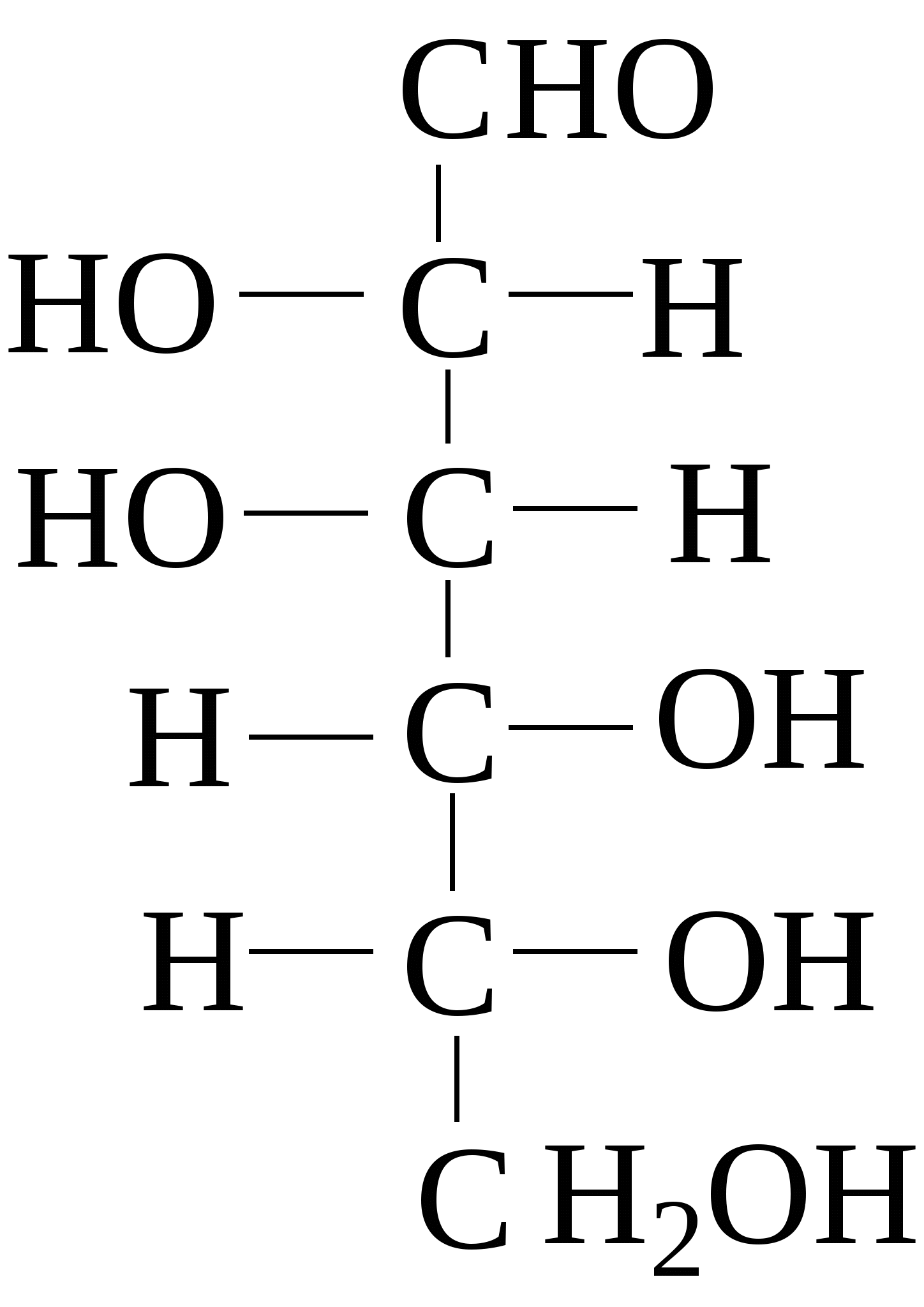
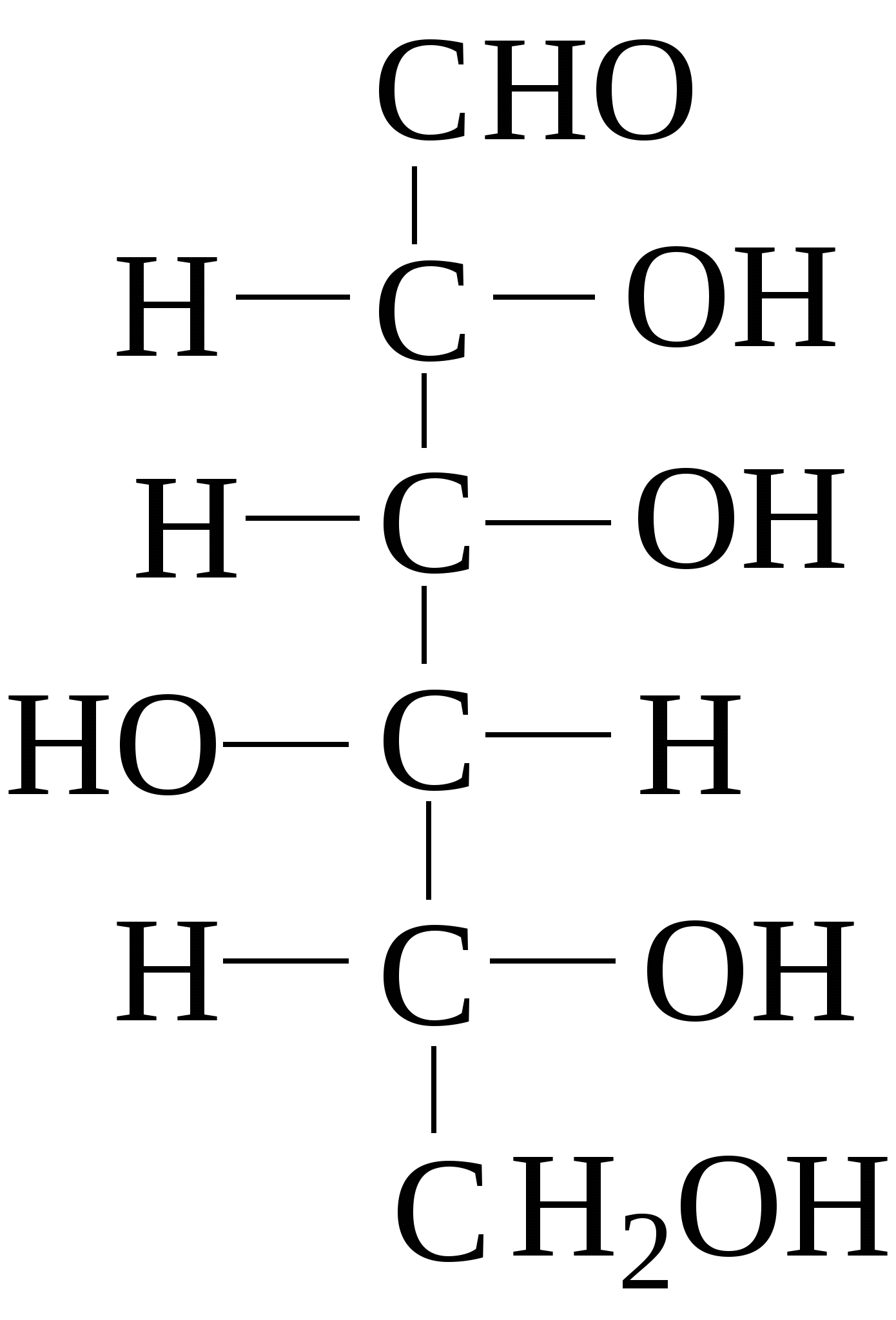
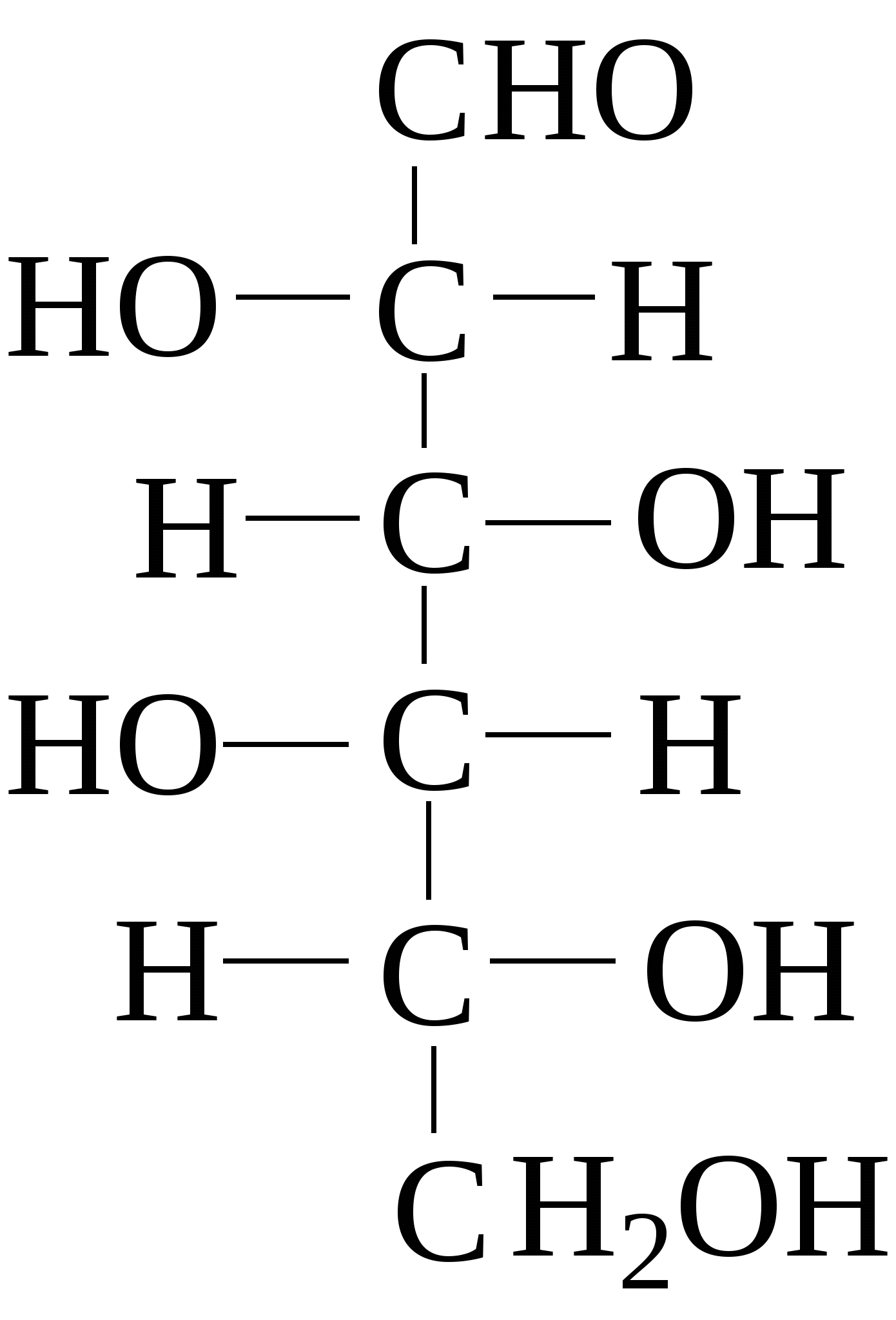
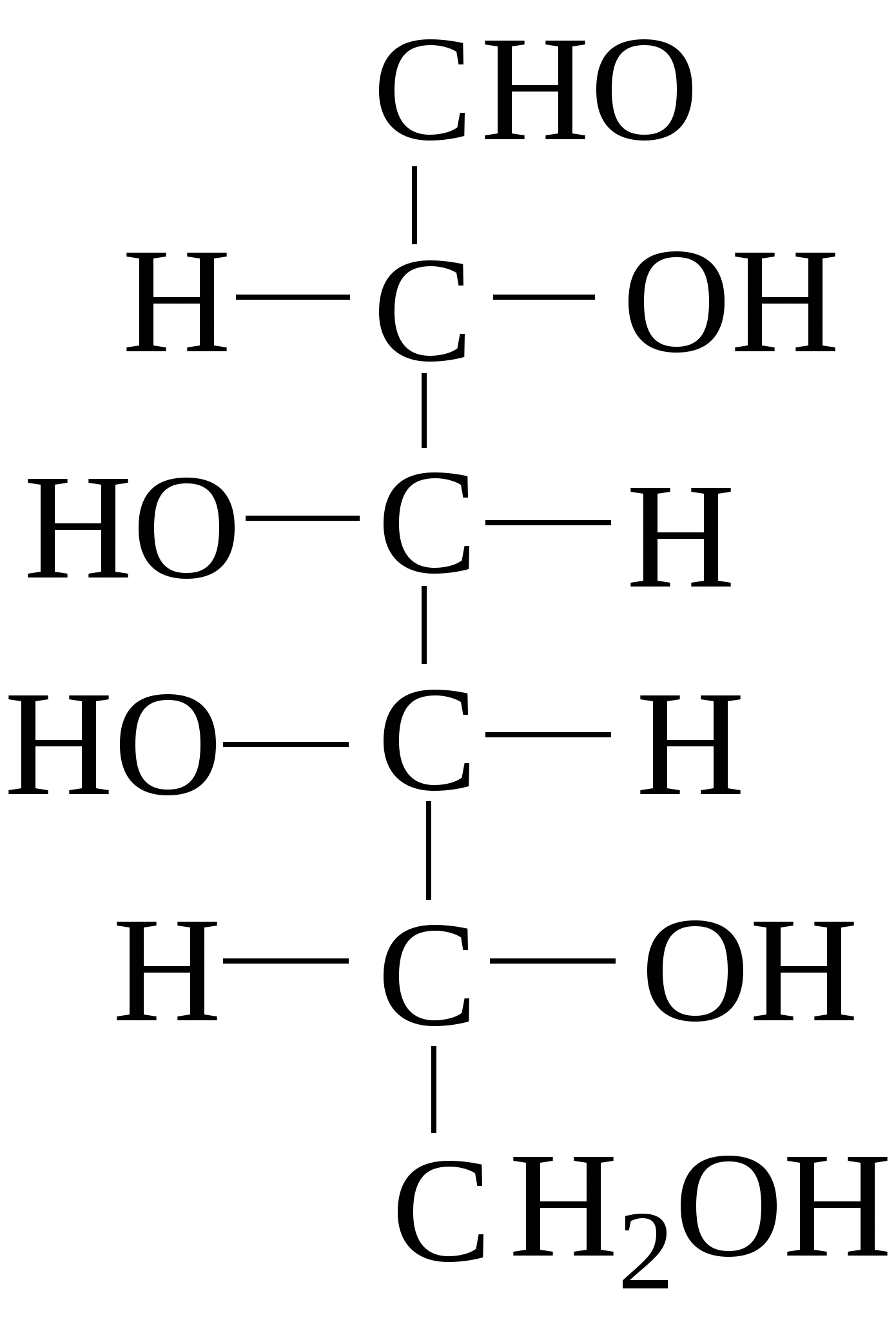
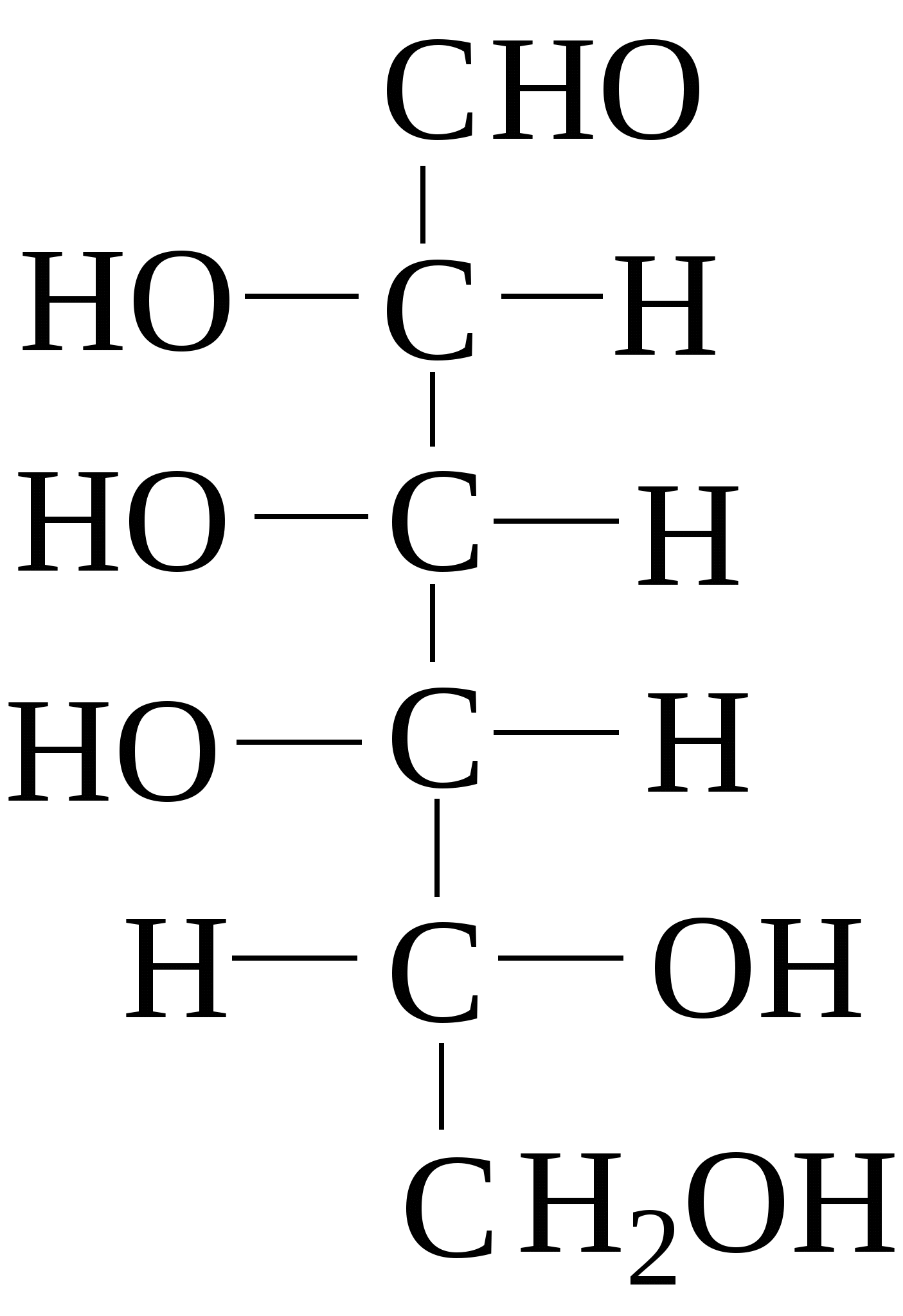
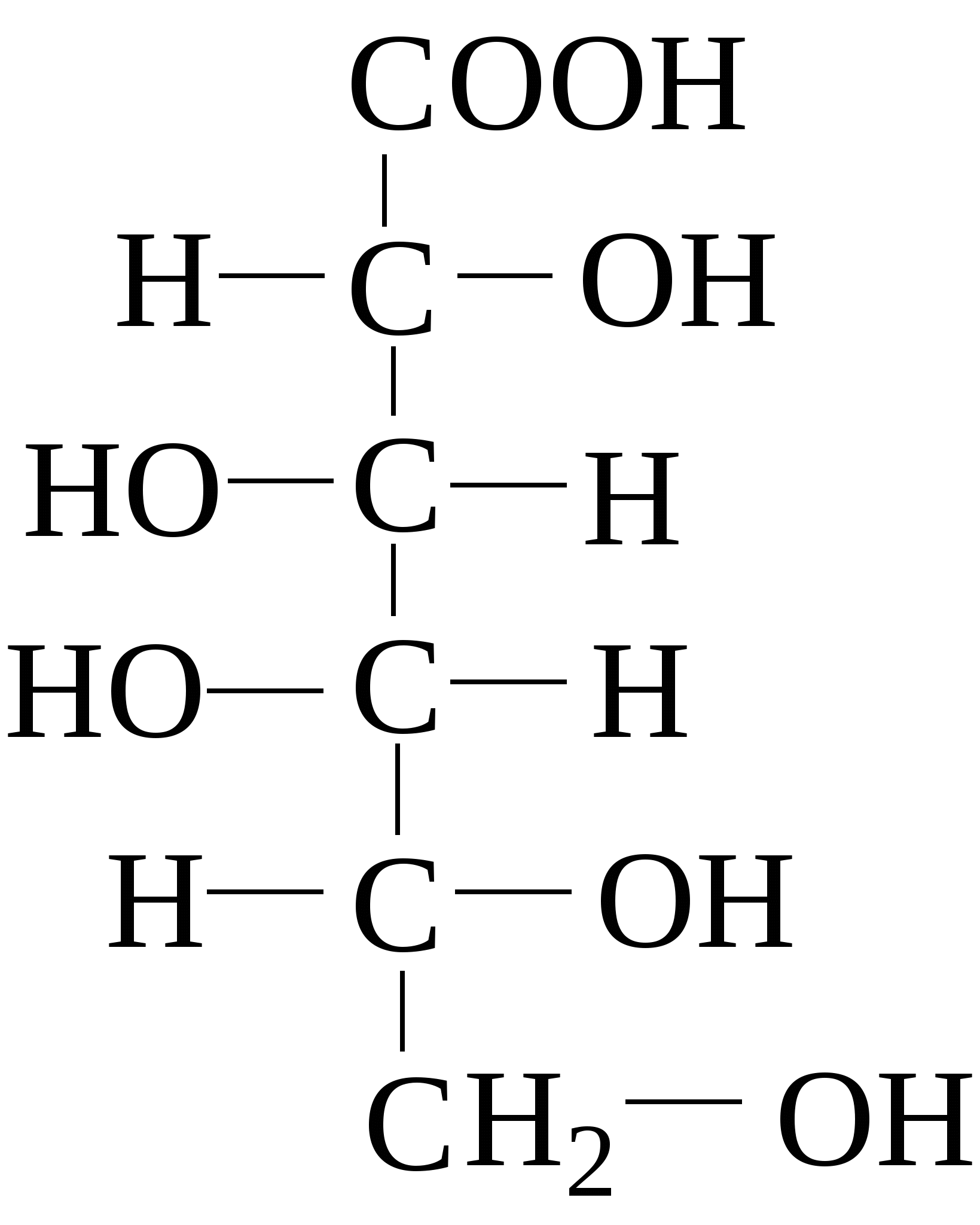
Зеркально построенные формы моносахаридов называют оптическими антиподами, а их эквимолярные смеси - рацематами. Каждый оптический изомер имеет свое название и свои особенности свойств. Ниже приведены формулы оптических изомеров гексоальдоз D-ряда:
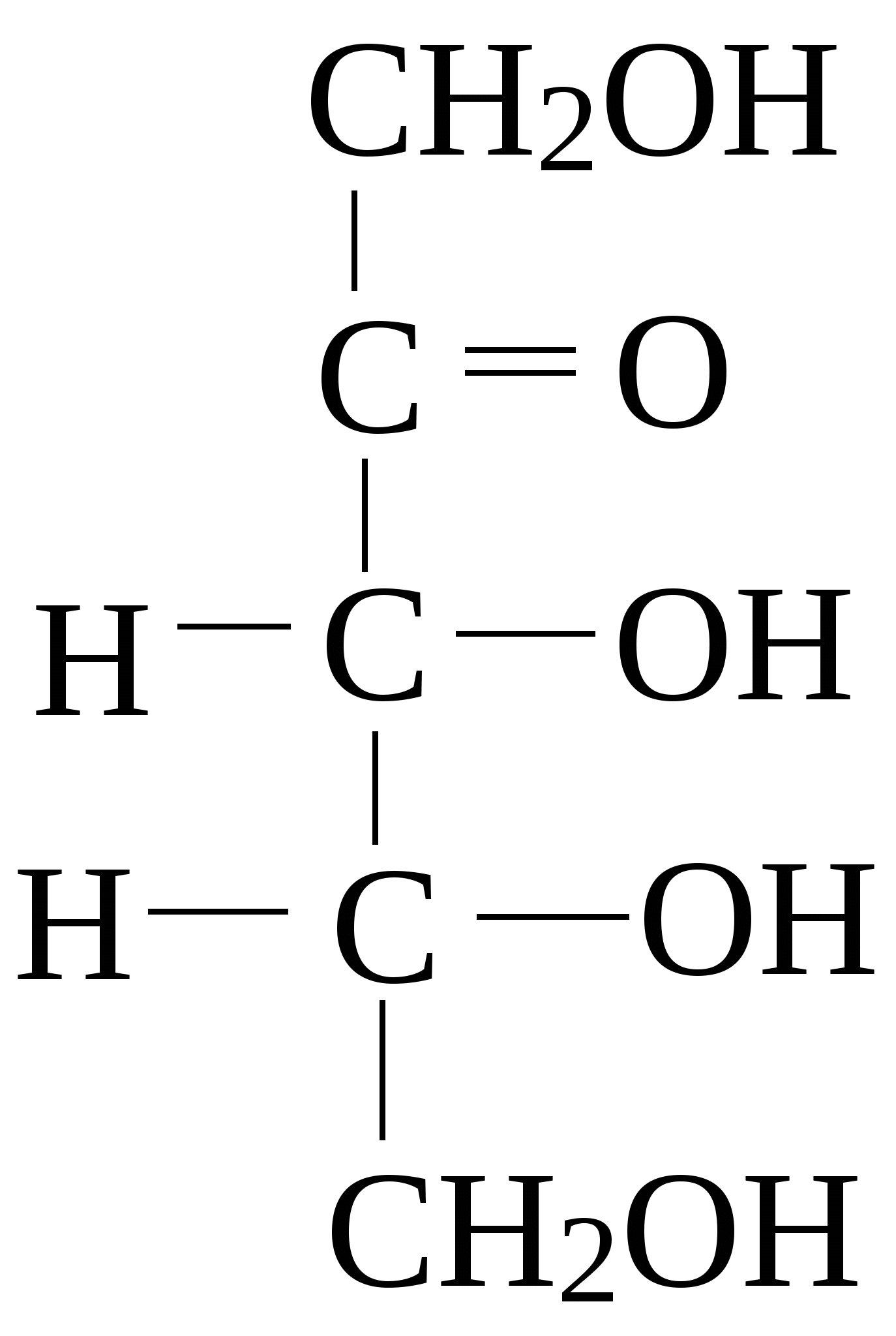
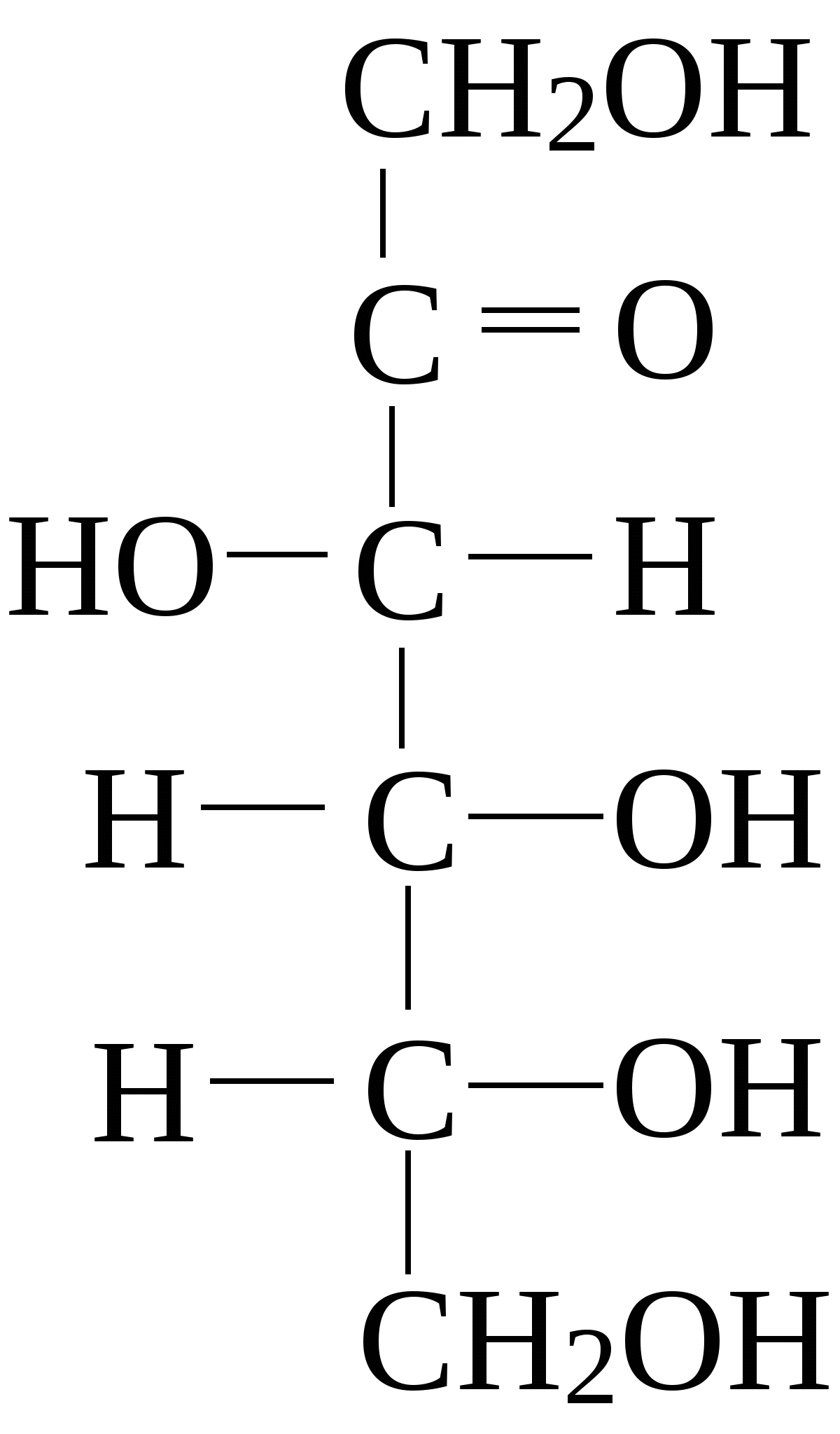
Стереоизомеры, отличающиеся пространственным расположением водорода и ОН групп у соседнего с альдегидной группой углеродного атома, называют эпимерами. Из приведенных примеров эпимерами являются аллоза и альтроза, глюкоза и манноза, гулоза и идоза, галактоза и талоза. Кетозы также способны к стереоизомерии. Наиболее известные из кетоз D-рибулоза (1), D-фруктоза (2), D-седогептулоза (3):
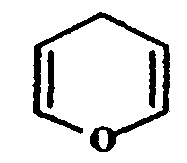
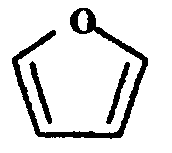
Для перехода от моносахарида D-ряда к L-ряду нужно изменить конфигурацию всех асимметрических атомов углерода на противоположную. Почему важно знать оптические свойства углеводов и аминокислот? Организм человека усваивает только L-аминокислоты и D-глюкозу и не может усваивать D-аминокислоты и L-глюкозу. В мышечных тканях содержится D-молочная кислота, а в кислом молоке в результате деятельности микроорганизмов образуется L-молочная кислота. Природные гексозы: глюкоза, фруктоза, манноза и галактоза - принадлежат, как правило, к соединениям D-ряда. Живые клетки усваивают из смеси изомеров необходимый им изомер даже в том случае, когда разделение изомеров какими-либо физическими и химическими методами практически невозможно. Структура моносахаридов Рассмотренные выше структуры оптических изомеров моносахаридов являются ациклическими и изображены с помощью проекционных формул Фишера. Однако моносахариды, начиная с пентоз, могут существовать и в циклических формах, причем в кристаллическом состоянии - это преобладающий вид структуры. В растворах устанавливается подвижное равновесие между ациклической и циклической формами (таутомерами), которое называют таутомерией. Известно, что углеродная цепь вследствие вращения атомов относительно химических связей может быть не только вытянутой, но и изогнутой. При этом циклические формы возникают за счет взаимодействия карбонильной группы и одной из гидроксильных групп с образованием внутренних полуацеталей. Альдегидная, или кетонная, группа гексоз и пентоз взаимодействует с гидроксильными группами у С4 или С5. В результате образуются пяти- или шестичленные циклы. Эти циклы структурно аналогичны кислородсодержащим гетероциклам пирану и фурану:
Поэтому циклические формы гексоз и пентоз соответственно называют пиранозными и фуранозными. Циклические формы изображают перспективными формулами Хеуорса. При написании структурных формул по Хеуорсу нумерацию атомов углерода в цикле производят по часовой стрелке, и символы атомов углерода обычно не записывают. При этом атомы и группы атомов, которые в формуле Фишера находятся справа от цепи, располагают под плоскостью цикла, и - наоборот. Исключение составляет группа –СН2ОН у 5-го атома углерода гексоз, которая всегда располагается над плоскостью цикла. В качестве примера рассмотрим схему таутомерии глюкозы: 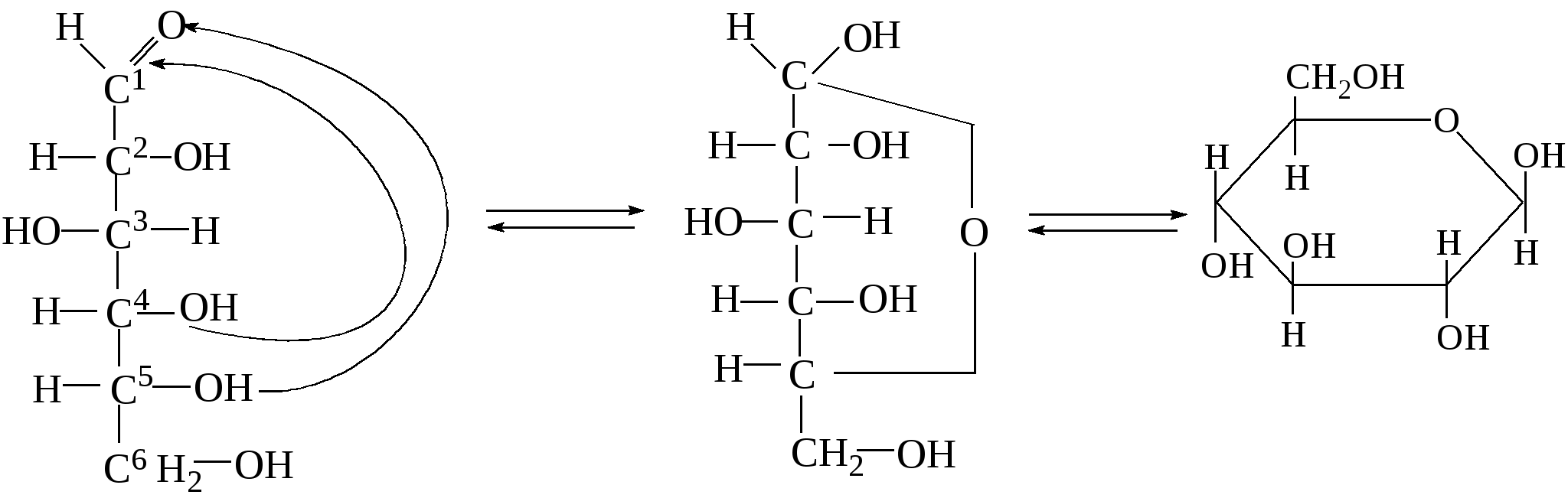 По карбонильному кислороду происходит реакция присоединения водорода от ОН-группы у С5 и появляется новый гидроксил у С1, получивший название полуацетального гликозидного и отличающийся высокой реакционной способностью. Существует два вида циклической формы глюкозы в зависимости от того, как будет расположен гликозидный гидроксил - ниже плоскости кольца (α-форма) или выше плоскости кольца (β-форма): 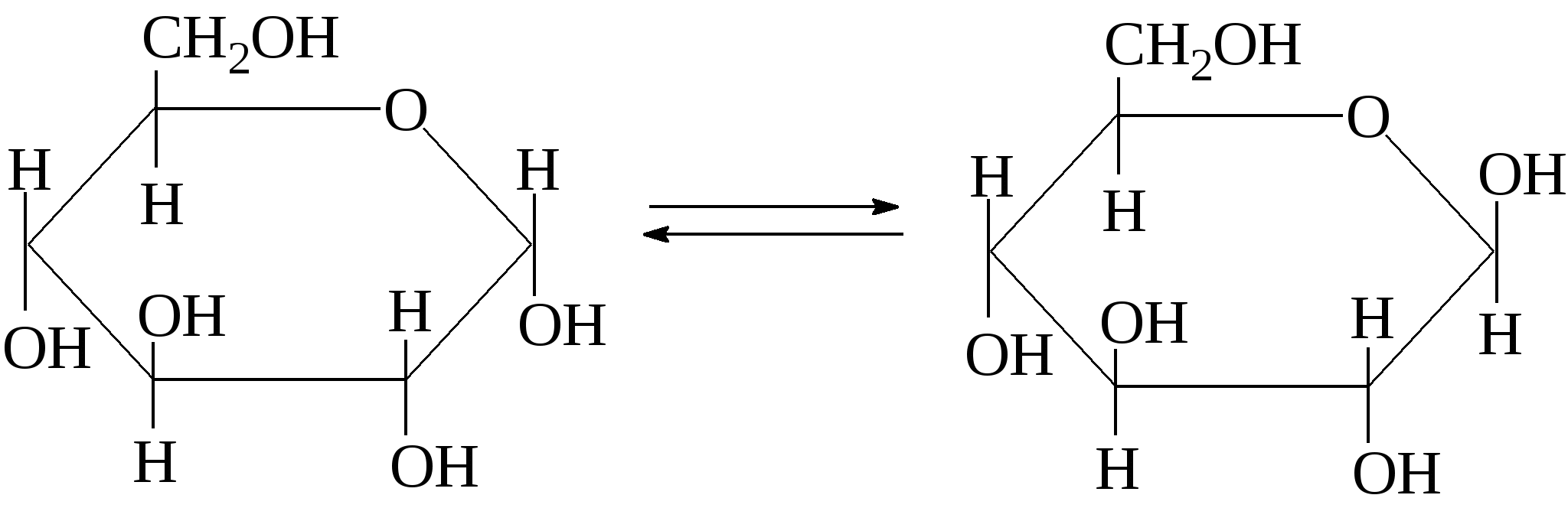
Кристаллическая глюкоза содержит молекулы α- формы. При растворении вещества в воде появляются и молекулы β-формы. Превращение идет через промежуточное образование альдегидной формы глюкозы: α-форма глюкозы <=> альдегидная форма <=> β- форма глюкозы. Аналогичная ситуация наблюдается и для остальных моносахаридов. Для других альдогексоз, как и для глюкозы, характерны пиранозные циклические формы. Циклические формы важнейшей из кетогексоз - D-фруктозы содержат пятичленный цикл: 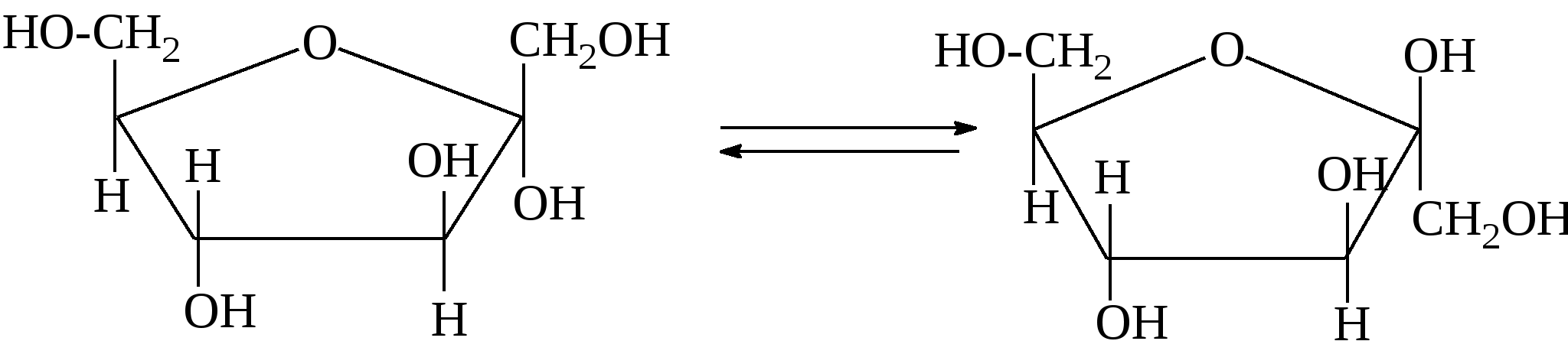
Наиболее известные из пентоз - D-рибоза и 2-дезокси-D-рибоза, входящие в состав нуклеиновых кислот, также имеют фуранозные циклические структуры, при этом возможны α- и β- формы: 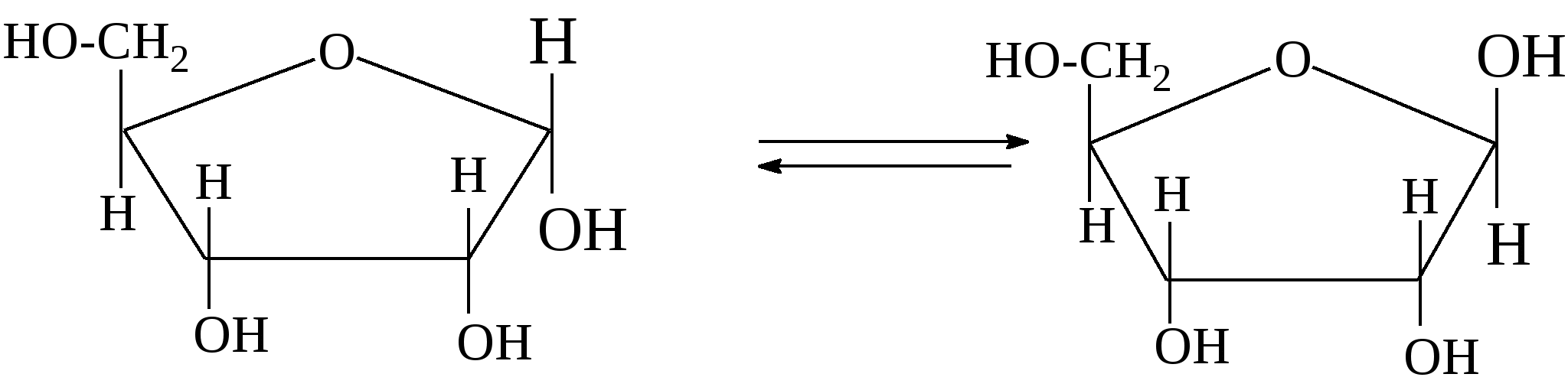
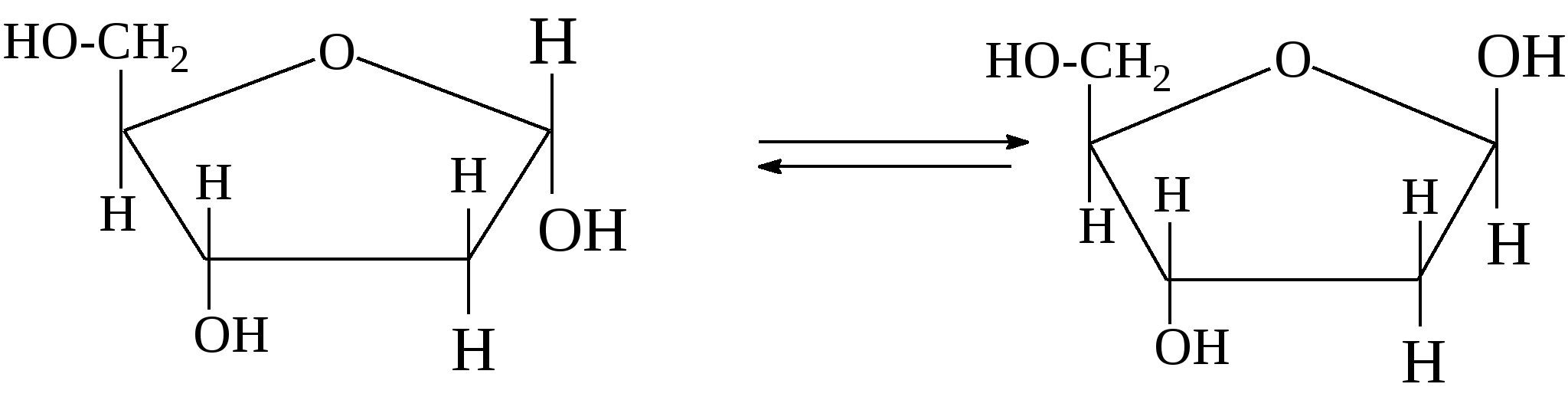
3.3. Химические свойства моносахаридов Реакции с участием карбонильной группы Хотя ациклическая форма моносахаридов присутствует и в кристаллическом состоянии, и в растворах в незначительных количествах они проявляют все свойства, присущие альдегидам (в альдозах) или кетонам (в кетозах). Так, по альдегидной группе для них характерны реакции окисления и восстановления, присоединения спиртов с образованием полуацеталей и др. Рассмотрим некоторые из этих свойств. 1. Окисление моносахаридов. При обработке альдоз слабыми окислителями (например, гипойодидом натрия) альдегидная группа превращается в карбоксильную - образуются альдоновые кислоты. В качестве примера можно привести D-глюконовую (1) и D-галактоновую (2) кислоты, образующиеся соответственно из D-глюкозы и D-галактозы:
Альдоновые кислоты являются промежуточными продуктами углеводного обмена. 2. Восстановление моносахаридов. Моносахариды под действием соответствующих ферментов легко гидрируются по связи С=О с образованием многоатомных спиртов (сахароспирты). Из D-глюкозы получается сорбит, из Д-маннозы - маннит. Восстановление D-фруктозы приводит к образованию эквимолярной смеси эпимеров - D-маннита и D-сорбита, так как в результате гидрирования второй атом углерода становится асимметричным: 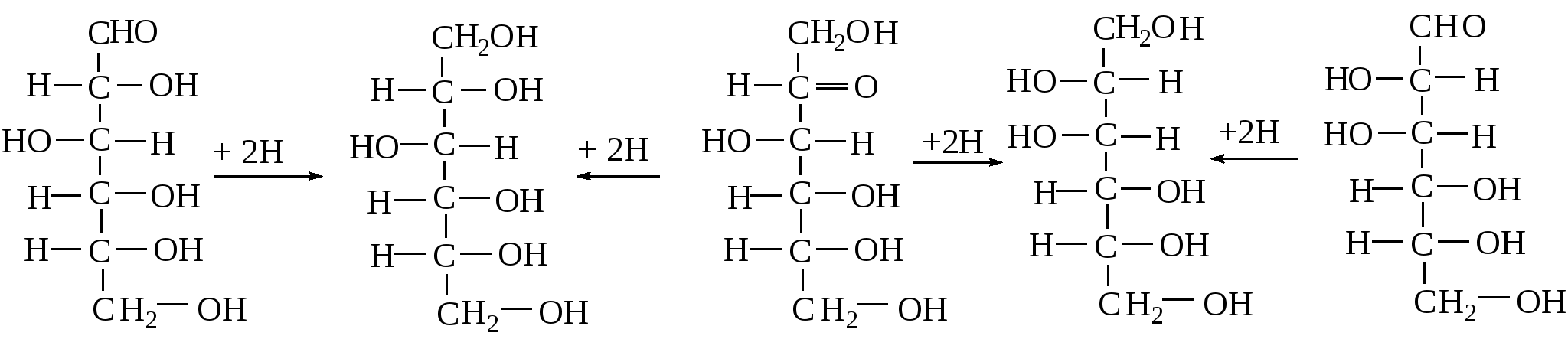
Реакции с участием гидроксильных групп Моносахариды как в кристаллическим состоянии, так и в растворе в основном существуют в полуацетальных (циклических формах). Полуацетальный (гликозидный) гидроксил отличается большей реакционной способностью, чем другие гидроксильные группы и может замещаться на различные группы в реакциях со спиртами и фенолами (простые эфиры), карбоновыми кислотами (сложные эфиры), а также может взаимодействовать с гидроксилом у С4-атома другого (других) моносахаридов с образованием β-1,4-гликозидов или α-1,4-гликозидов (дисахариды и полисахариды) и т.д. Соединение, которое действует на полуацетальный гидроксил моносахарида, называют агликоном, а продукт реакции - гликозидом. Например, при реакции метанола с β-D-глюкопиранозой в присутствии неорганических кислот образуется метил -β-D-глюкопиранозид: 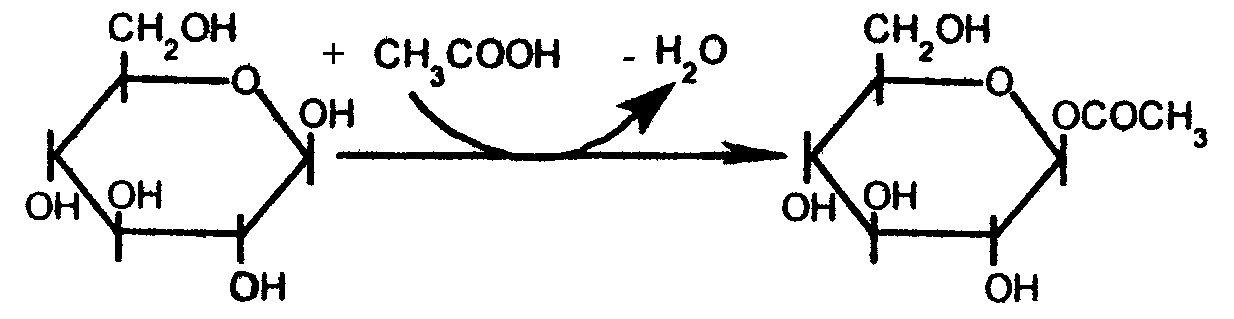
При действии на β-D-глюкопиранозу уксусной кислоты получается ацетил-β-D-глюкопиранозид: 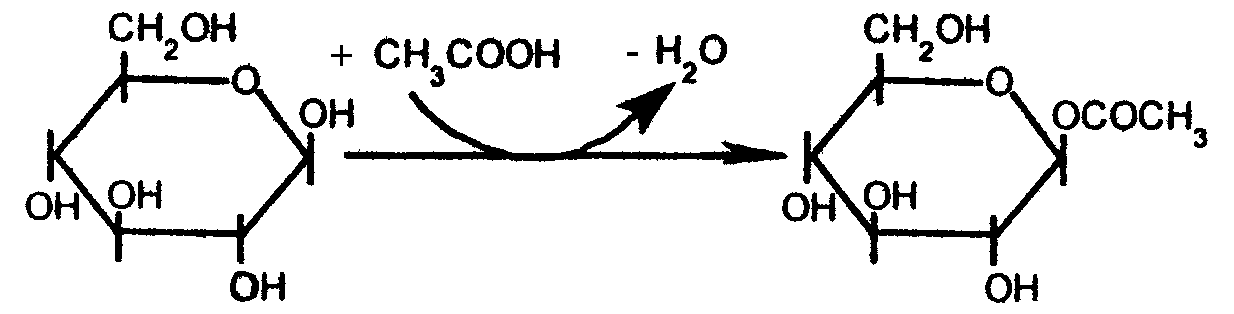
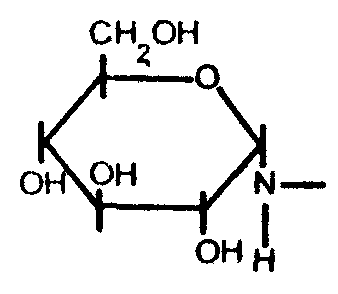
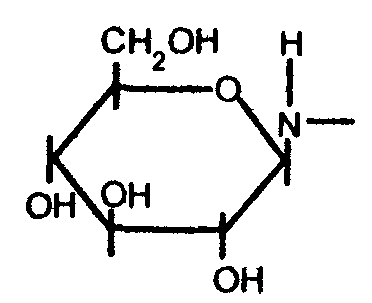
Ацилированию и алкилированию могут подвергаться и остальные гидроксильные группы моносахаридов, но в более жестких условиях. Вышеперечисленные гликозиды называют О-гликозидами. Важным свойством моносахаридов является образование N-гликозидов, в которых связь с агликоном осуществляется через азот, а не через кислород:
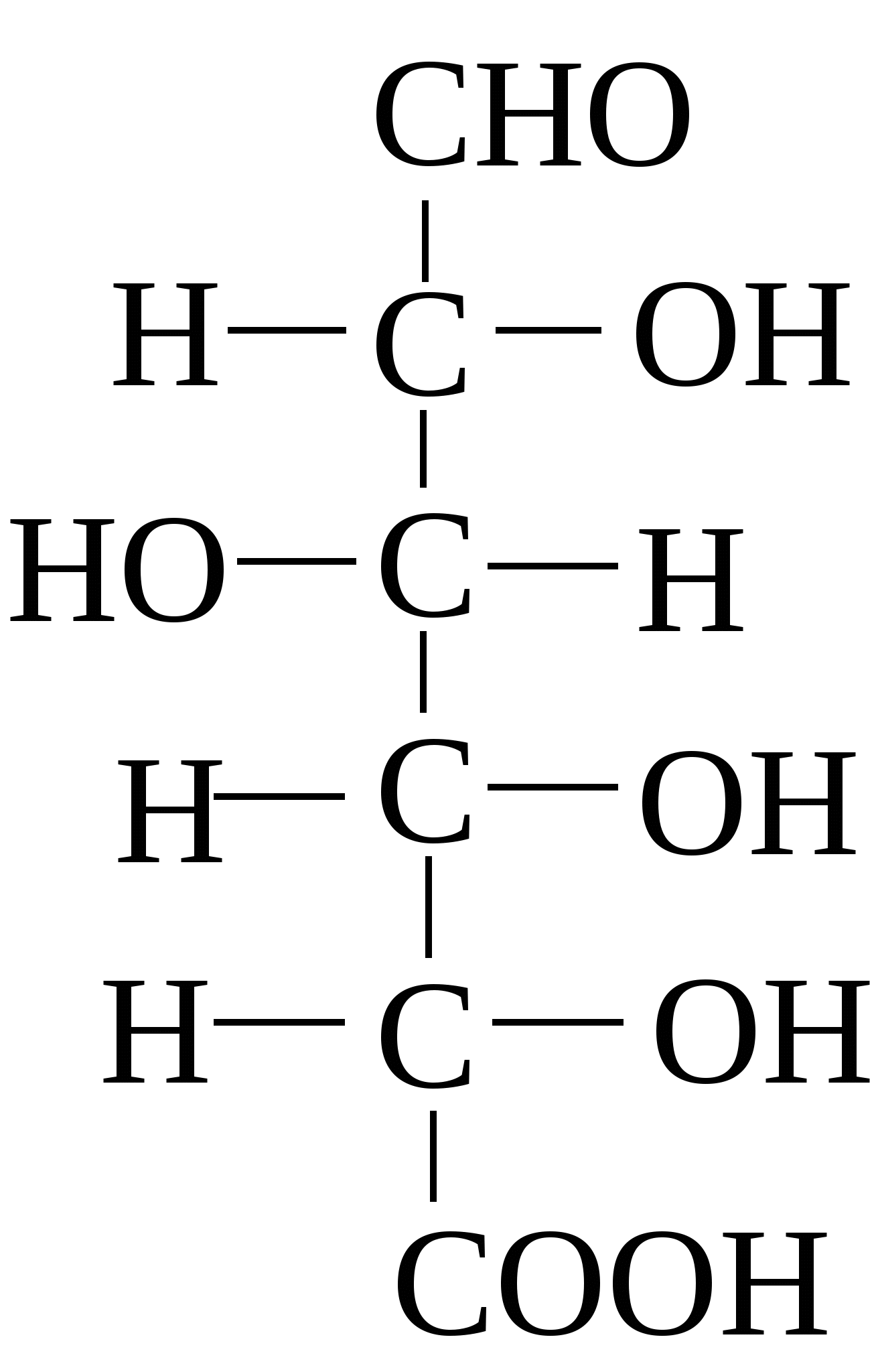
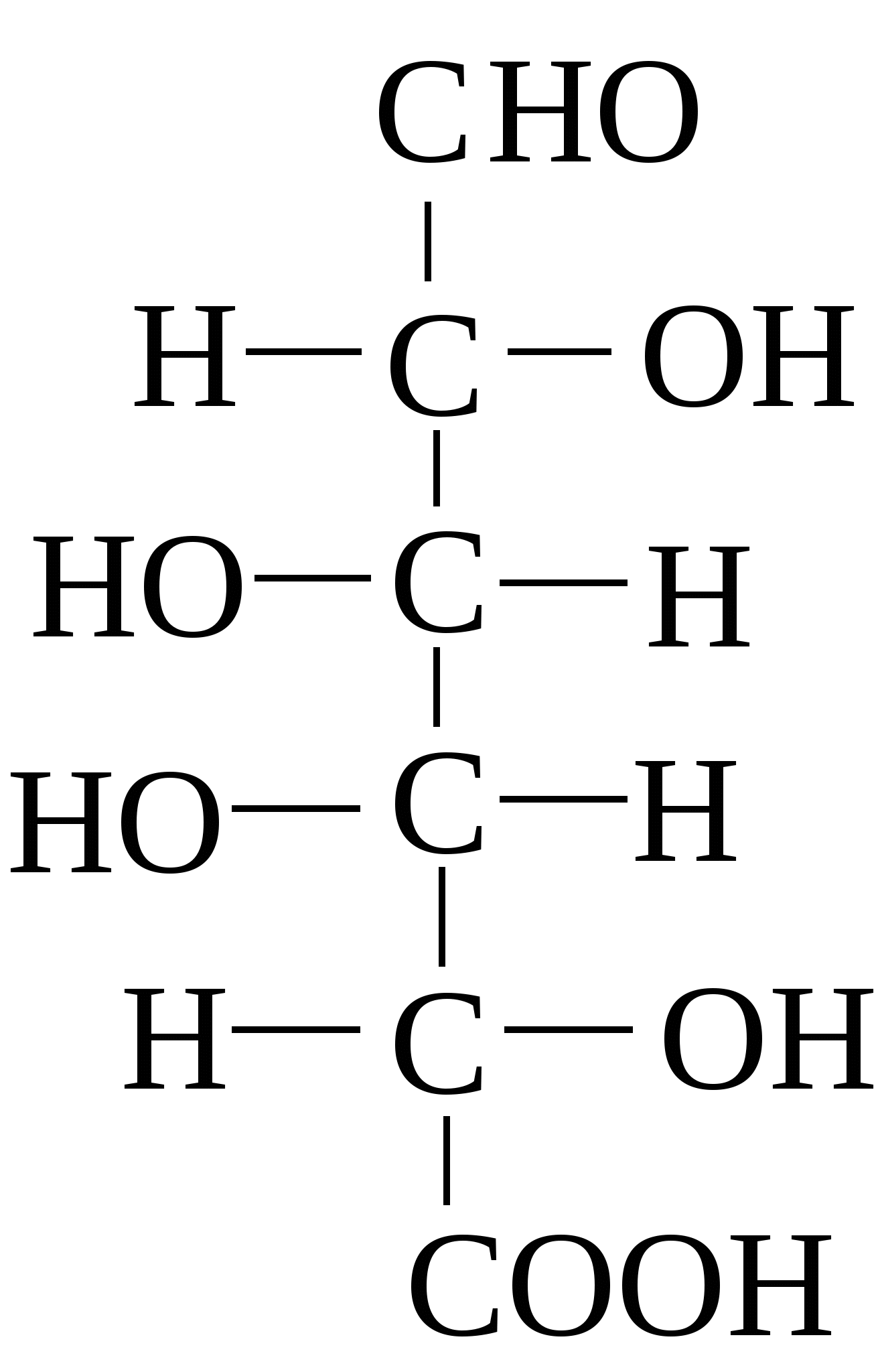
К N-гликозидам относятся исключительно важные в обмене веществ продукты расщепления нуклеиновых кислот и нуклеопротеидов (нуклеотиды и нуклеозиды), АТФ, НАД, НАДФ (см. главы 4, 7), некоторые антибиотики. При окислении первичной спиртовой группы до карбоксильной образуются уроновые кислоты, которые имеют важное биологическое значение, являясь компонентами гетерополисахаридов. Например, из D-глюкозы и D-галактозы образуются соответственно D-глюкуроновая и D-галактуроновая кислоты:
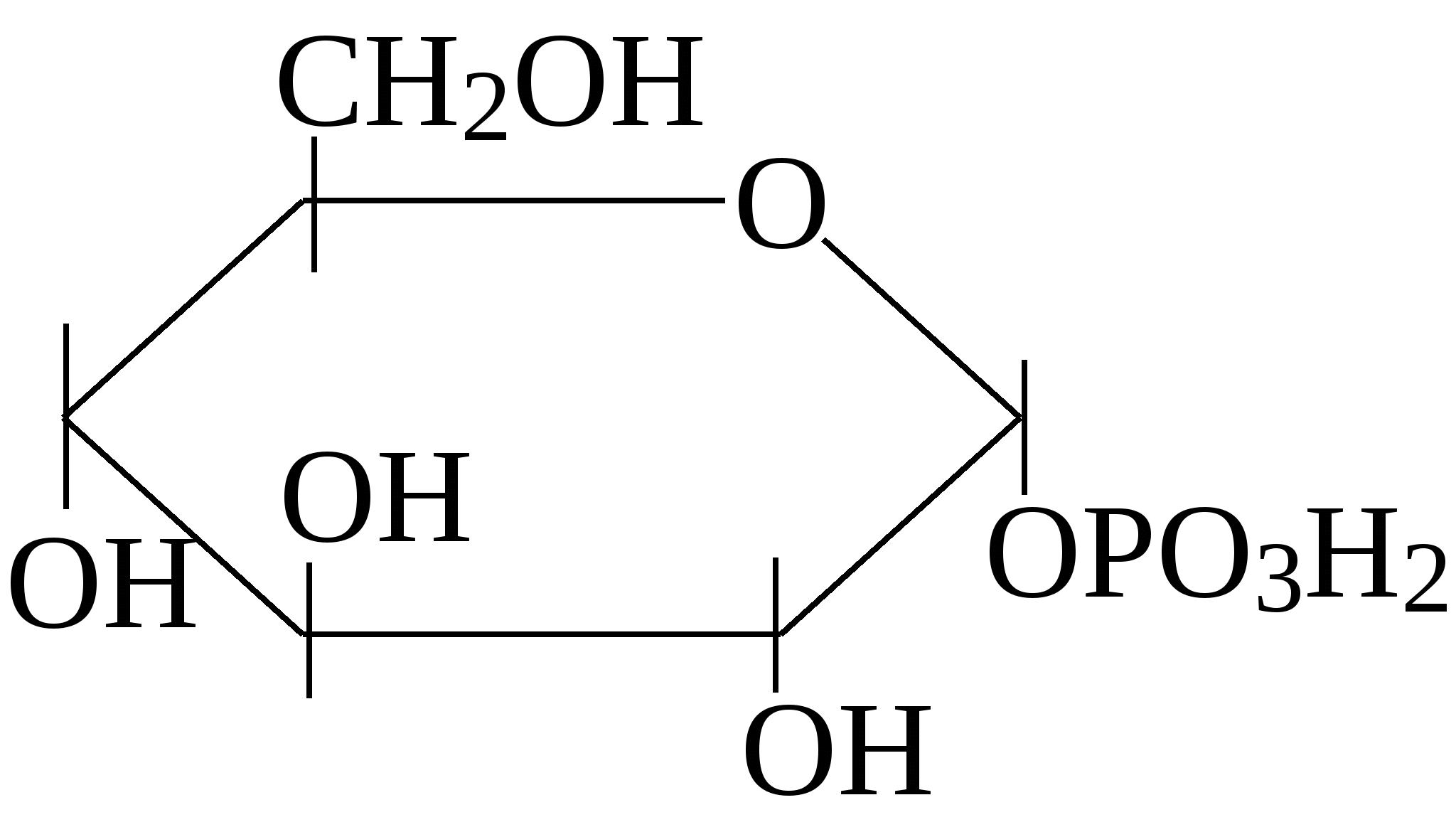
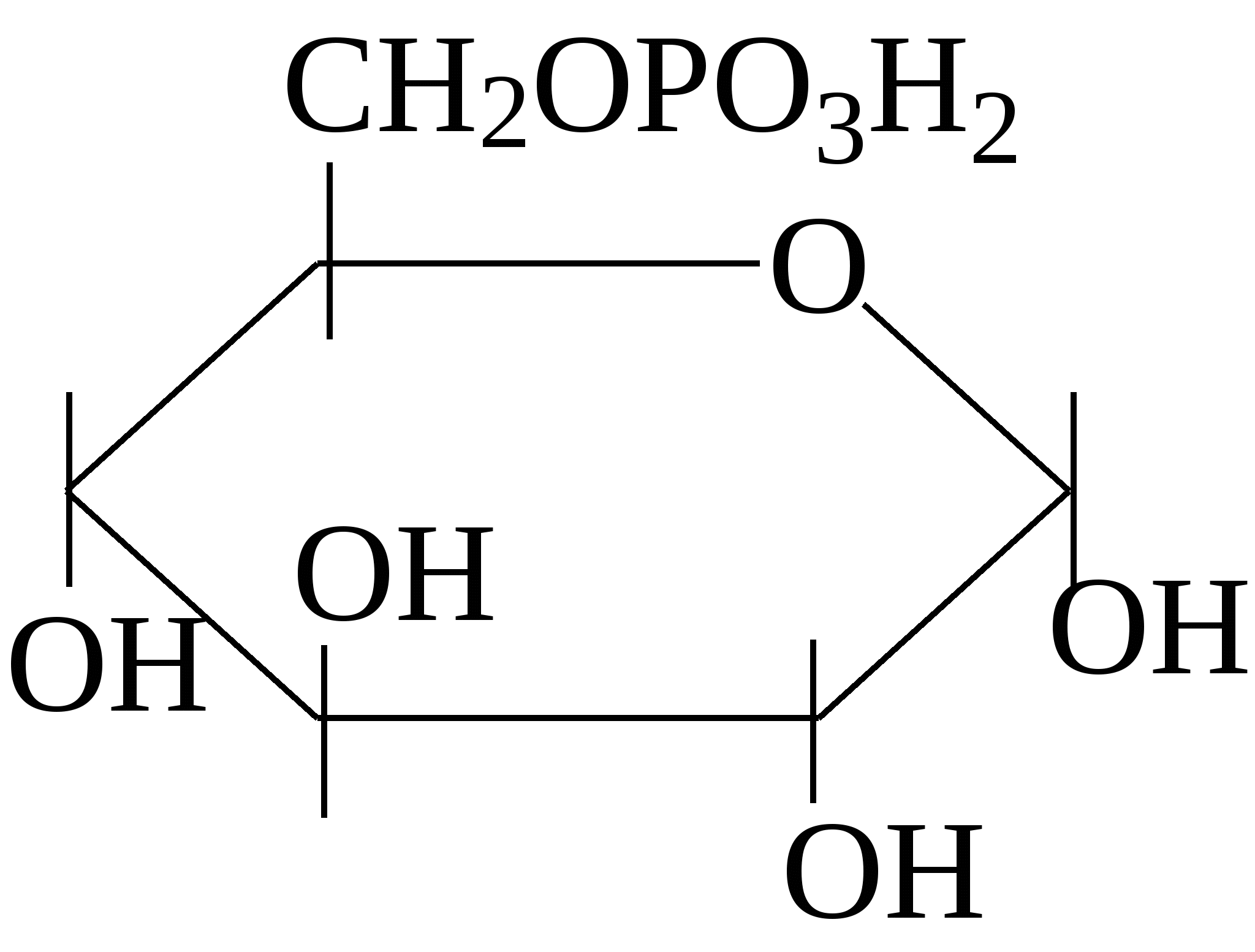
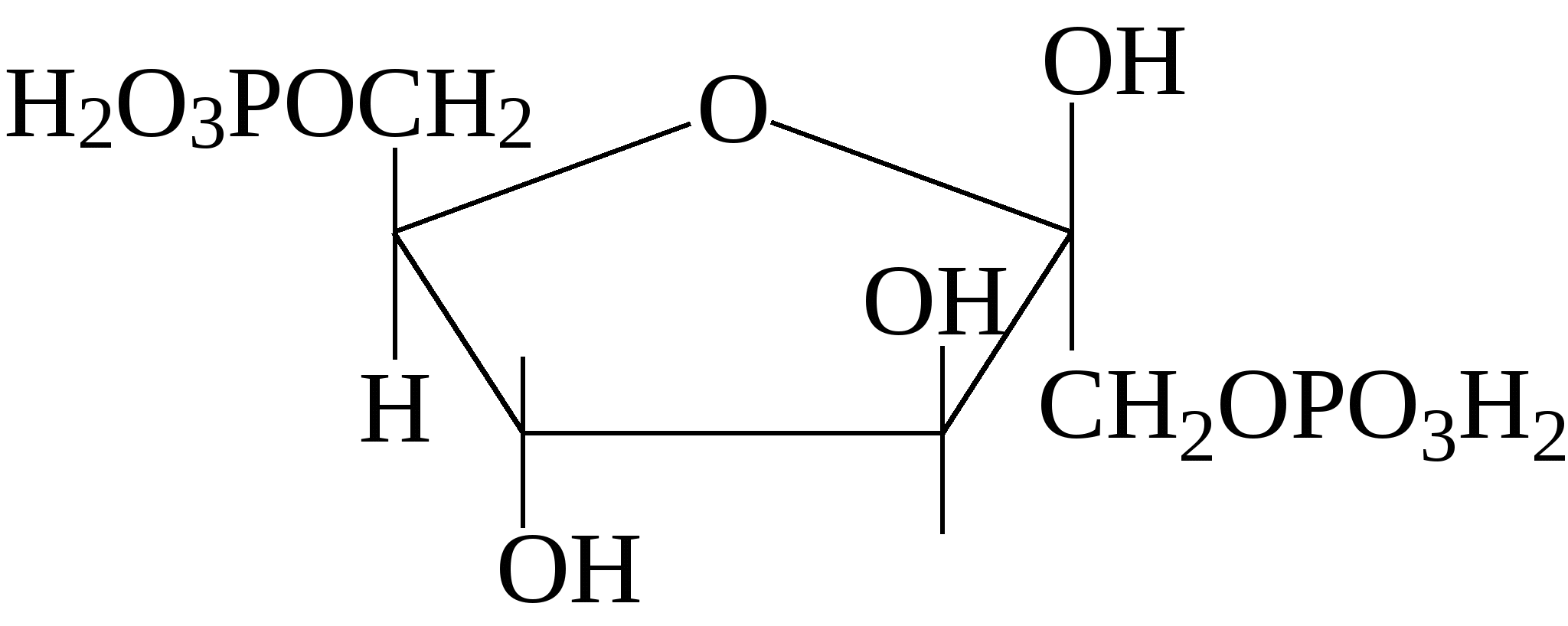
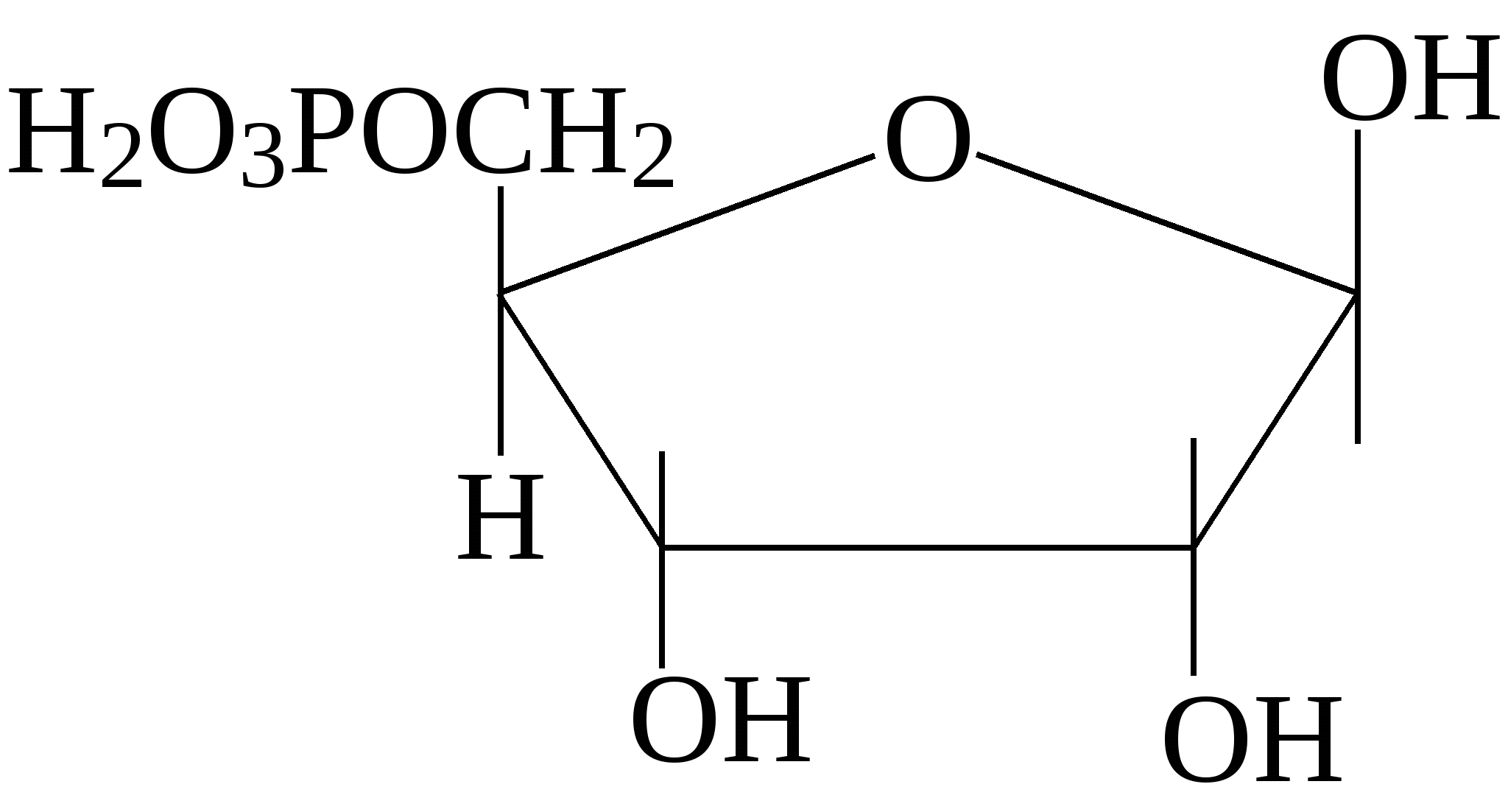
Исключительно важную роль в обмене веществ играют фосфорнокислые эфиры моносахаридов, образующиеся при взаимодействии с фосфорной кислотой. Ниже приведены формулы некоторых фосфатов моносахаридов:
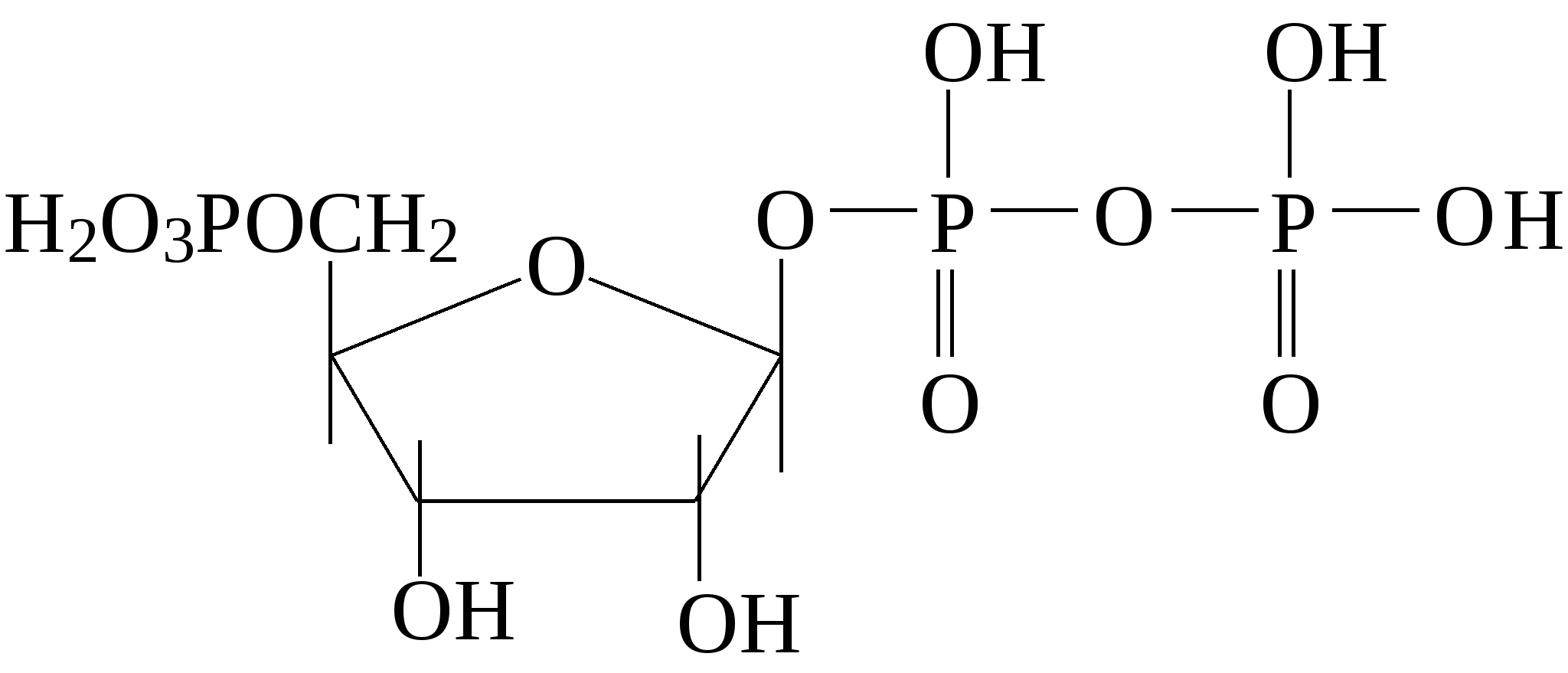 5-фосфорибозил-1-пирофосфат Важную роль играют аминосахара - производные моносахаридов, гидроксильная группа которых замещена аминогруппой. В организме человека и животных наиболее важными аминосахарами являются D-глюкозамин и D-галактозамин: Аминосахара входят в состав гетерополисахаридов животного, растительного и бактериального происхождения, являются углеводными компонентами различных гликопротеинов и гликолипидов, принимающих участие в построении клеточных мембран. На рисунке показана структура протеогликана клеточной стенки Стафилококка ауреуса, грамм-положительной бактерии.  Рис. Протеогликан клеточной стенки стафилококка, грам-положительной бактерии 3.4. Сложные углеводы Среди сложных углеводов выделяют две группы: олигосахариды и полисахариды. Олигосахариды Олигосахариды - углеводы, молекулы которых содержат от 2 до 10 остатков моносахаридов, соединенных гликозидными связями. Они хорошо растворяются в воде, легко кристаллизуются и, как правило, сладкие на вкус. Поэтому олигосахариды иначе называют сахароподобными сложными углеводами. Наиболее изучены дисахариды - сложные, сахара, при гидролизе дающие 2 молекулы моносахаридов. Среди дисахаридов, важнейшие - мальтоза, целлобиоза, лактоза и сахароза. Мальтоза - α-глюкопиранозил (1-4) -α-глюкопираноза (солодовый сахар) - состоит из двух остатков α-D-глюкозы, является промежуточным продуктом при гидролизе полисахаридов (крахмала и гликогена): 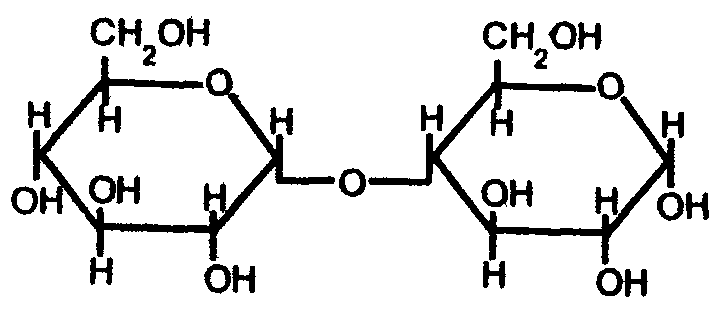 Так как в молекуле мальтозы у второго остатка глюкозы имеется свободный полуацетальный гидроксил, она обладает восстанавливающими свойствами. Целлобиоза, как и мальтоза, состоит из двух остатков D-глюкозы, но в отличие от мальтозы это β-глюкопиранозил -(1-4)-β-глюкопираноза: 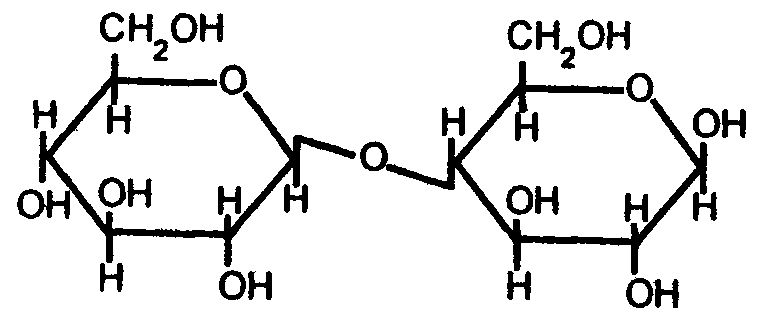 Она также как и мальтоза, легко окисляется и является хорошим восстановителем, широко распространена в растительном мире: в прорастающих семенах, косточках абрикосов, соке деревьев. Образуется при ферментативном гидролизе клетчатки (целлюлозы), из которой состоят оболочки растительных клеток. Лактоза - β-галактозил-(1-4)-α-глюкопираноза (молочный сахар)- состоит из β-D-галактозы и α-D-глюкозы, содержится только в молоке (молочный сахар); проявляет восстановительные свойства, поскольку в остатке глюкозы имеется свободный полуацетальный гидроксил: 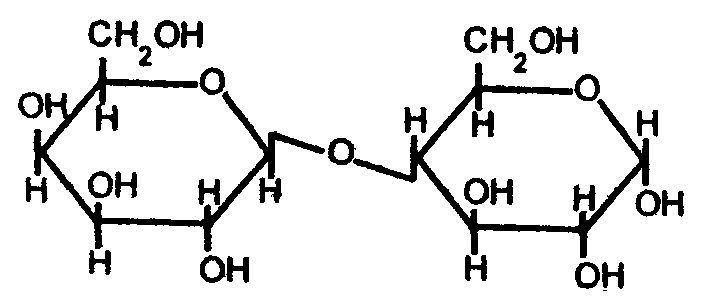 Сахароза - α-глюкопиранозил -(1-2) -β-фруктофуранозид - наиболее распространенный дисахарид - состоит из остатков α-D-глюкозы и β-D-фруктозы: 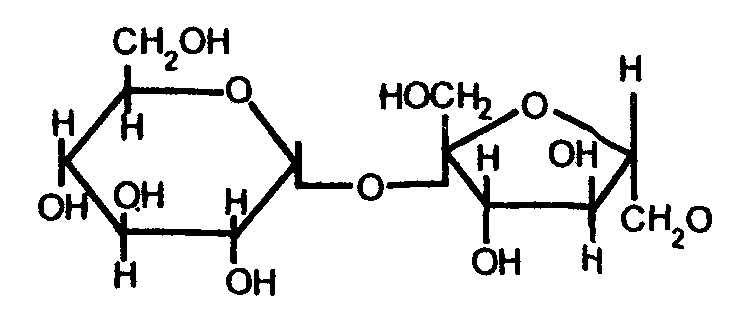 В отличие от других дисахаридов сахароза восстанавливающими свойствами не обладает, так как не имеет свободного полуацетального гидроксила. Сахароза содержится в соке многих растений: в свекле (до 27%) итростнике (14-26%), и в меньшем количестве в соке клена, березы, пальмы. Сахарозу часто называют тростниковым или свекловичным сахаром, она является важнейшим пищевым продуктом. Из трисахаридов наиболее известна рафиноза, состоящая из остатков фруктозы, глюкозы и галактозы. Она содержится в сахарной свекле и во многих других растениях. В целом олигосахариды растительных тканей разнообразнее по своему составу, чем олигосахариды животных тканей. Полисахариды Полисахариды - сложные углеводы, содержащие более десяти остатков моносахаридов. Все полисахариды можно разделить на две группы: на гомополисахариды, состоящие из моносахаридов только одного типа, и гетерополисахариды, для которых характерно наличие двух или более типов моносахаридных звеньев. Полисахариды, как и олигосахариды, легко гидролизуются при кипячении с разбавленными растворами кислот или под действием ферментов. Внешне они резко отличаются от моно- и дисахаридов: имеют аморфную структуру, не обладающую сладким вкусом, полисахаридам присущи свойства типичных высокомолекулярных соединений (ВМС), имеющих полярные группы. Поэтому полисахариды гидрофильны, при растворении в воде они набухают, а затем, частично растворяясь, дают коллоидные растворы. В зависимости от состава полисахариды обладают разной гидрофильностью, растворимостью и зарядом. Гетерополисахариды характеризуются гораздо более кислыми свойствами посравнению с гомополисахаридами и несут больший отрицательный заряд. Гомополисахариды К числу наиболее распространенных гомополисахаридов принадлежат крахмал,гликоген (животный крахмал) - резервные полисахариды и целлюлоза (клетчатка) - структурный полисахарид. Все они являются полигликозидами, в молекулах которых за счет эфирных (кислородных) мостиков объединяются сотни, тысячи и десятки тысяч остатков моносахаридов. Эфирные мостики образуются за счет взаимодействия гликозидного гидроксила одного остатка моносахарида со спиртовым гидроксилом ( чаще всего у 4-го атома С - для линейных форм, 4-го и 6-го - у разветвленных форм) другого остатка моносахарида. Крахмал - один из самых распространенныхгомополисахаридов, содержится в зернах злаков (пшеница, кукуруза) и в клубнях растений (картофель и др.). Он нерастворим в холодной воде, а в горячей образует коллоидный раствор - клейстер. Крахмал - природный полимер, мономером которого является D-глюкоза. Состоит из двух различных фракций, различающихся по своему строению и свойствам: амилозы (20%) и амилопектина, общая формула которых одинакова (С6Н10О5)n. Амилоза - линейный полисахарид - остатки D-глюкозы соединены α-1,4-глюкозидными связями; она имеет молекулярную массу от 20000, до 200000 Да, в водной среде амилоза образует двухспиральные структуры. Ее коллоидные частицы (мицеллы) дают с йодом характерное синее окрашивание. Амилопектин - разветвленный полисахарид с молекулярной массой от 100000 до 1 млн Да. Примерно через 15-25 моносахаридных звеньев у него имеются точки ветвления, образованные α-1,6-глюкозидмыми связями: 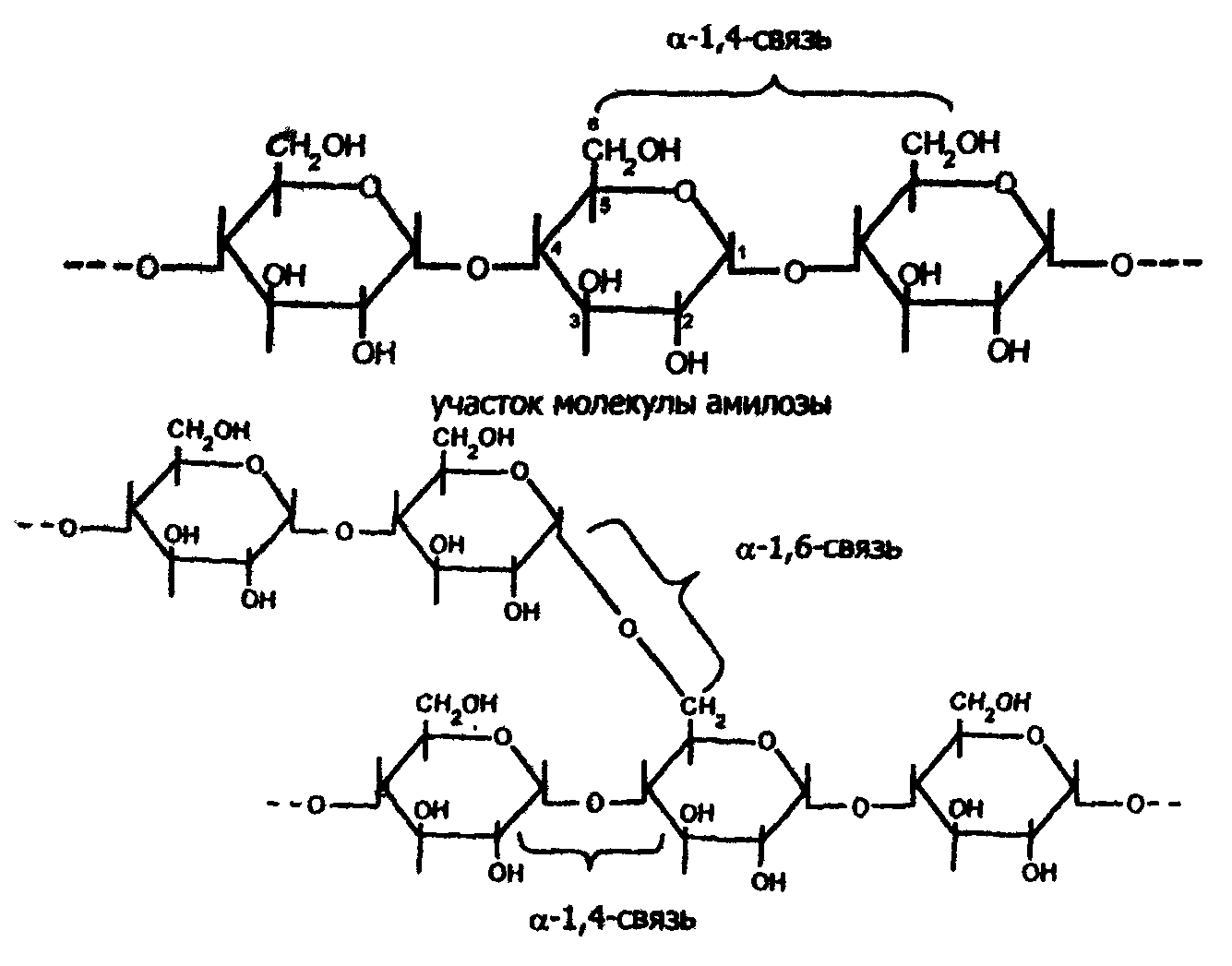 Участок молекулы амилопектина Коллоидные растворы амилолектина дают с йодом красно-фиолетовое окрашивание. Компоненты крахмала прочно связываются в клетке с белком, образуя смешанные макромолекулы. Возможно, что синтез крахмала, т.е. удлинение полисахаридных цепей, происходит на белковой основе. Очевидно, белковая часть придает полисахариду некоторую способность к диффузии внутри клетки. При частичном гидролизе крахмала образуются полисахариды с меньшей степенью полимеризации - декстрины, при полном гидролизе - мальтоза и глюкоза. Крахмал - наиболее важный пищевой углевод для человека, содержание его в муке 75-80%, в картофеле - 25%. Гликоген - является главным резервным гомополисахаридом в организме человека и животных. Поэтому его называют «животный крахмал», однако он найден в грибах, дрожжах и зернах кукурузы. Гликоген содержится почти во всех органах и тканях животных и человека, но больше всего в печени и в мышцах. Молекулярная масса гликогена 105-108Да и выше. Гликоген по строению близок к амилолектину, но отличается большой разветвленностью цепей. В молекуле гликогена различают внутренние цепи - участки полиглюкозидных цепей между точками ветвления, и наружные цепи - участки от периферической точки ветвления до конца цепи. В цепях остатки глюкозы соединены α-1,4-глюкозидными связями, а в точках ветвления - α-1,6-глюкозидные связи.  Рис. Строение молекулы гликогена (по Майеру): белые, кружки - остатки глюкозы, соединенные α-1,4 - связью; черные - остатки глюкозы, соединенные α-1,6-связью При гидролизе гликоген распадается, как и крахмал, сначала до декстринов, затем до мальтозы и, наконец, до глюкозы. Распад гликогена носит название гликогенолиза и обеспечивает потребность организма в энергии для поддержания температуры тела, осуществления мышечного сокращения, протекания биохимических реакций и т.д. В клетке гликоген, как и крахмал, связан с белком цитоплазмы и частично белком внутриклеточных мембран. Целлюлоза (клетчатка) - наиболее распространенный гомополисахарид растительного мира: в древесине 50 - 70% клетчатки, в стеблях волокнистых растений (лен) еще больше, а волокно хлопка - почти чистая, клетчатка. Она играет большую роль в построении клеточных стенок (название целлюлоза - от латинского "целлюла" - клетка). Клетчатка так же, как и крахмал, построена из остатков D-глюкозы, но в отличие от крахмала - это β-полиглюкозид: с молекулярной массой 5·104- ·106 Да. Ниже представлен фрагмент молекулы целлюлозы: 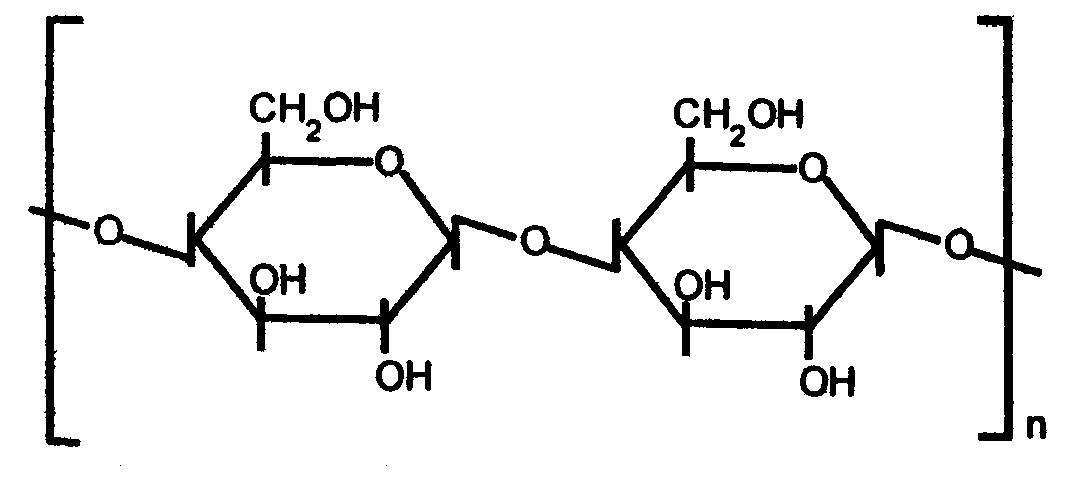 При частичном гидролизе клетчатки образуется дисахарид целлобиоза, а при полном гидролизе – D-глюкоза. Гетерополисахариды Гетерополисахариды, или мукополисахариды (от латинского mucos - слизь), представляют собой сильно гидратированные, желеподобные, липкие вещества, имеющие значительный отрицательный заряд. Они обычно находятся в межклеточном веществе и связаны с белками, вот почему зачастую их относят классу протеогликанов. На рисунках ниже представлен участок внеклеточной матрицы (гликокаликс) представляющий собой длинную молекулу гиалуроновой кислоты нековалентно связанной с примерно 100 молекулами основного белка аггрекана, который в свою очередь ковалентно связывает хондроитин сульфат и кератан сульфат. В качестве примеров изолированных гетерополисахаридов можно привести гиалуроновую кислоту, хондроитин-4-сульфат, хондроитин-6-сульфат, кератансульфат, гепарин, гепарансульфат. Гиалуроновая кислота содержит D-глюкуроновую кислоту и N-ацетил-D-глюкозамин, а остальные - сульфатированные аминосахара и D-глюкуроновую или L-идуроновую кислоты. В кератансульфате вместо гексуроновых кислот содержится D-галактоза. 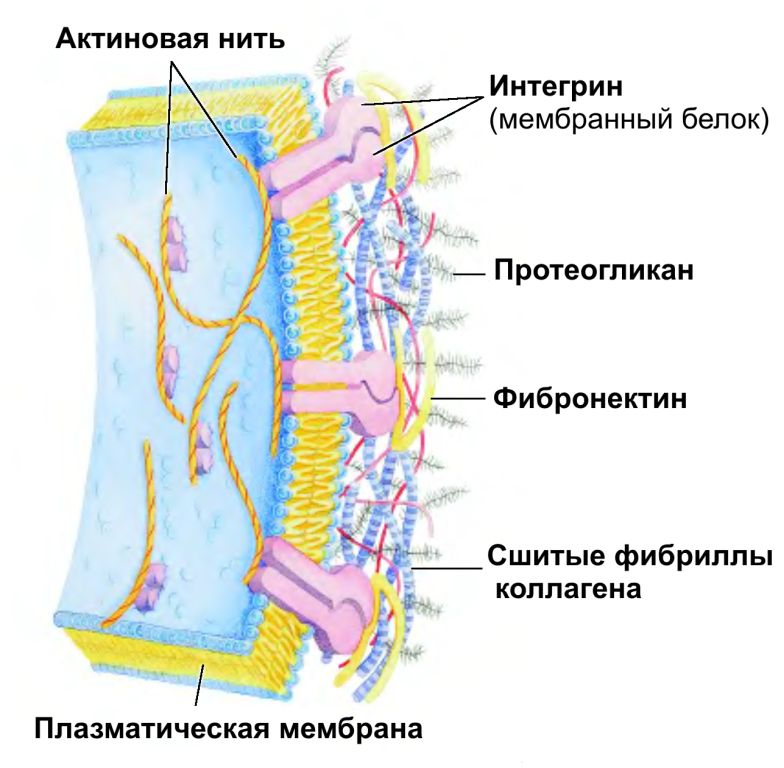 Взаимосвязь между клетками и внеклеточной матрицей осуществляется через мембранный белок интегрин и внеклеточный белок фибронектин связанный с коллагеновыми фибриллами и протеогликаном 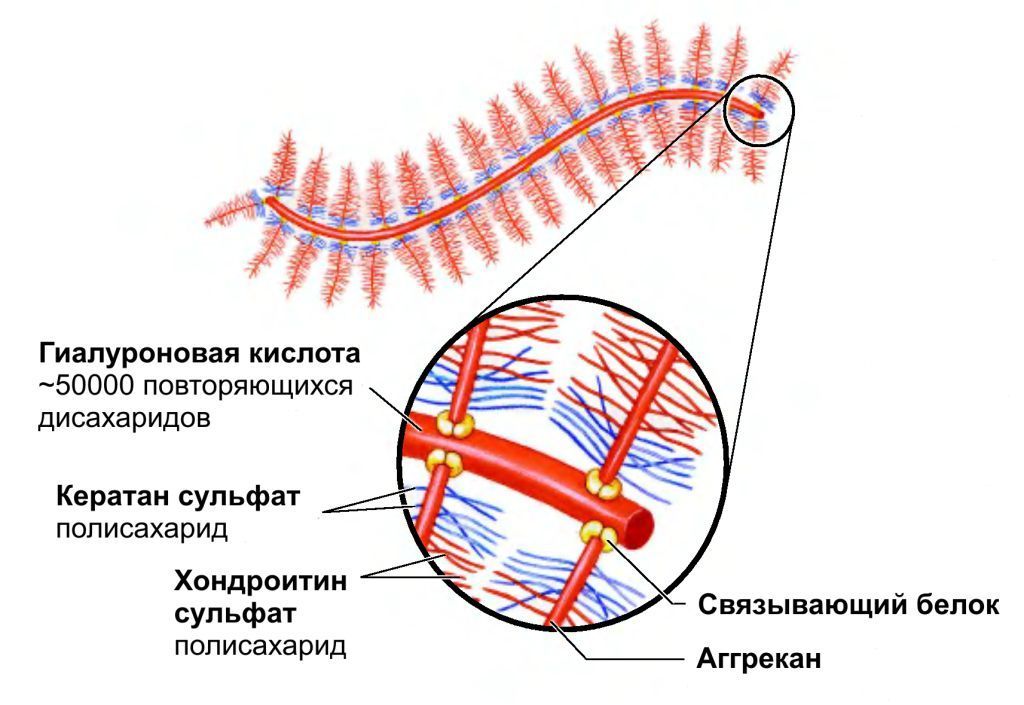 Протеогликан внеклеточной матрицы представляет собой длинную молекулу гиалуроновой кислоты нековалентно связанную с примерно 100 молекулами основного белка аггрекана, который в свою очередь ковалентно связывает хондроитин сульфат и кератан сульфат. 3.5. Биологические функции углеводов К наиболее важным функциям полисахаридов относятся: энергетическая, опорная, защитно-механическая, связующая и структурная. Энергетическая функция. Ее выполняют резервные гомополисахариды - крахмал и гликоген. При необходимости гликоген быстро расщепляется с образованием легхоусвояемого источника энергии - глюкозы. Крахмал пищи также распадается до глюкозы под действием ферментов пищеварительного тракта. За счет окисления углеводов удовлетворяется половина потребностей человека в энергии. Опорную функцию выполняет целлюлоза в растительных организмах и хондроитинсульфаты в костной ткани. Защитно-механическая - типичная функция гетерополисахаридов. Высокая вязкость и слизеподобная консистенция объясняет их роль защищающего поверхность клеток. Выстилая трущиеся поверхности сосудов, мочеполовых путей, пищеварительного тракта, слизистой носа, трахеи, бронхов, суставов (синовиальная жидкость) и т.д., они предохраняют их от механического повреждения. Связующая, или структурная, функция - кислые гетерополисахариды являются структурным межклеточным веществом, одновременно выполняющим функцию биологического цемента (например гиалуроновая кислота). Углеводы - обязательный компонент большинства внутриклеточных структур, а в растительных организмах - основа клеточных мембран. Гидроосмотическая и ионрегулирующая функции. Кислые гетерополисахариды, благодаря высокой гидрофильности и отрицательному заряду, способны удерживать большие количества воды и катионов.Например, гиалуроновая кислота связывает воду и катионы, регулируя межклеточное осмотическое давление. Подобно осмометру, эта кислота препятствует излишнему скоплению свободной воды в межклеточном пространстве. Кофакторная функция. Некоторые гетерополисахариды, такие как гепарин и гепарансульфат, действуют как кофакторы ферментов. Гепарин проявляет свойства тех ферментных белков, у которых он играет роль кофактора. Поэтому он осуществляет антисвертывающую функцию (задерживает свертывание крови) и антилипемическую (снижает уровень липидов в крови, активируя их расщепление). На практике гепарин и сульфатированные синтетические полисахариды (гепариноиды) широко применяют как антикоагулянты и противоатеросклеротические препараты. Синтетическая функция. Углеводы используются для синтеза соединений других классов: нуклеиновых кислот, нуклеотидных коферментов, липидов, белковых аминокислот, гликопептидов и т.д. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||