Практикум. Лабораторный практикум по органической химии. Практикум по органической химии оглавление Оформление лабораторного журнала 2 гидроксисоединения 3
 Скачать 295.46 Kb. Скачать 295.46 Kb.
|
4. УГЛЕВОДЫУглеводы (сахара) – соединения состава Cn(H2O)m– самые распространенные органические вещества на земле. Они имеют большое значение в живой природе (в животном и растительном мире) как источники энергии в процессах метаболизма, структурные компоненты клеточных стенок растений, бактерий и входят в состав жизненно важных веществ (нуклеиновые кислоты, витамины и др.). Они составляют значительную долю пищи млекопитающих. Углеводы пищи – основной источник энергии для организма человека. Углеводы относятся к незаменимым питательным веществам, так как животные организмы не способны синтезировать эти вещества и получают их с продуктами растительного происхождения. Все углеводы делятся на две большие группы по способности к гидролизу: простые сахара - моносахариды (не гидролизуемые вещества); продукты их конденсации в процессе биосинтеза, т.е. сложные сахара, включающие олигосахариды (при гидролизе образуются 2-10 молекул моносахаридов) и полисахариды (состоящие из сотен и тысяч молекул моносахаридов). УГЛЕВОДЫ (сахара) 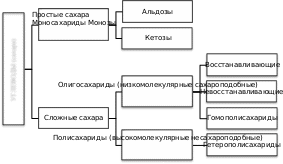 Дальнейшую классификацию углеводов можно представить следующей схемой: Дальнейшую классификацию углеводов можно представить следующей схемой: Молекулы моносахаридов имеют одну карбонильную группу, т.е. альдегидную или кетонную. Отсюда деление простых сахаров на альдозы и кетозы. Кроме альдегидной или кетонной группы все моносахариды содержат несколько гидроксильных групп, являясь многоатомными альдегидоспиртами или кетоноспиртами (полигидроксиальдегидами или полигидроксикетонами). Деление олигосахаридов на восстанавливающие, т.е. по способности легко окисляться за счет наличия свободных карбонильных групп и восстанавливать при этом катионы металлов (серебро, медь и др.), и не восстанавливающие зависит от химического строения молекулы и наличия свободного гликозидного (полуацетального) гидроксила. Молекулы полисахаридов могут состоять из остатков одного моносахарида (это гомополисахариды) или из остатков различных моносахаридов (гетерополисахариды). МоносахаридыВ зависимости от числа углеродных атомов (3 – 6) моносахариды относятся к триозам, тетрозам, пентозам и гексозам. В природе наиболее распространены и наиболее важны для жизнедеятельности пентозы С5Н10О5 и гексозы С6Н12О6. Моносахариды имеют тривиальные названия с окончанием –оза. Важнейшие представители пентоз (ксилоза, рибоза, дезоксирибоза, арабиноза) и гексоз (глюкоза, фруктоза, галактоза и манноза) даны в виде проекционных формул Фишера, из которых видно, что только фруктоза является кетозой, остальные вещества относятся к альдозам.     H O H O H O H O H O H O H O H OC C C C  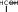     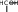 HO C H HO C HHO C H   HO C H HO C H 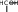 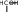 CH2OH CH2OHCH2OH CH2OH CH2OH D-ксилоза D-рибоза D-дезоксирибоза L-арабиноза    H O H O H O C CH2OH C C H O H O H O C CH2OH C C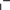  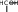 CO HO C H CO HO C H  HO C H HO C H CH2OH HO C H   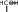 CH2OH CH2OHHO C H   HO C H HO C H CH2OH HO C H 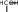 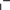  CH2OH CH2OHD-глюкоза D-фруктоза D-галактоза D-манноза Молекулы моносахаридов, как видно, имеют несколько асимметрических атомов углерода и потому моносахариды являются оптически активными веществами, т.е. способны вращать плоскость поляризованного света. Принадлежность по конфигурациям к D- или L-ряду для молекул моносахаридов определяется пространственным положением гидроксильной группы при последнем асимметрическом атоме углерода (для пентоз при четвертом атоме, для гексоз при пятом атоме). Подавляющее большинство природных моносахаридов относится к D- ряду. Живые организмы не умеют перерабатывать L-глюкозу. Например, спиртовое брожение происходит только из D-глюкозы.  H O H OC  HO C H HO C H H C OH H C OH HO C H HO C H   HO C H CH2OH HO C H CH2OHL-глюкоза Напомним, что L-изомеры являются зеркальными изомерами D-моносахаридов, т.е. все функциональные группы около асимметрических атомов углерода в D- и L- изомерах расположены в противоположные стороны (что наглядно видно в формулах Фишера для D- и L-конфигураций). Есть некоторые примеры, когда более распространенными в природе оказываются моносахариды L-ряда, например, L-арабиноза. Поскольку в молекулах моносахаридов имеются два типа функциональных групп (карбонильная и спиртовая группы), то возможно их внутримолекулярное взаимодействие, приводящие к образованию циклической формы (пиранозные – шестичленные и фуранозные – пятичленные циклы) и появлению нового гидроксила – полуацетального или гликозидного. В зависимости от расположения в пространстве полуацетального (гликозидного) гидроксила различают - и β-формы моносахаридов (- и β- аномеры). Между открытой и циклической формой молекулы моносахарида существует подвижное динамическое равновесие и возможен обратимый переход из одной формы в другую, т.е. наблюдается циклоцепная таутомерия или циклооксо- таутомерия (таутомеры – обратимые изомеры). В твердом состоянии моносахариды имеют циклическое строение. В водном растворе возможно существование 5 таутомерных форм). Ниже приведены таутомеры для глюкозы с привлечением формулы Хеуорса (гликозидный гидроксил обведен в рамку). 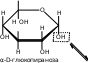 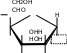 CH2OH CH2OHHO 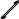 H OH H OH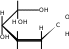 CH2OH CH2OH H OH H OHα-D-глюкофураноза   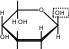 CH2OH CH2OHH O   C C CH2OH CH2OH H OH H OHH OH HO H   H OH H OH H OH H OHCH2OH HO H OH β-D-глюкопираноза ациклическая форма (оксиформа) β-D-глюкофураноза В растворе глюкозы в смеси таутомеров преобладают пиранозные формы (особенно β-пиранозная форма). Оксоформа (ациклическая) и таутомеры с фуранозными циклами содержатся в малых количествах. В растворе фруктозы в равновесной смеси таутомеров преобладают фуранозные циклы.   CH2OH O CH2OH CH2OH O CH2OHH HO H OH OH H OH H -D-фруктофураноза β-D-фруктофураноза Химические свойства моносахаридов определяются природой их функциональных групп и строением молекул). Характерные реакции окисления моносахаридов протекают легко, процесс и продукты реакции зависят от природы окислителя, температуры, рН среды. При окислении альдоз в нейтральной и кислой среде могут образоваться альдоновые (гликоновые) кислоты (при мягких условиях процесса, например, из глюкозы образуется глюконовая кислота, из галактозы – галактоновая кислота). При действии сильных окислителей (разбавленная азотная кислота) альдозы превращаются в двухосновные кислоты – гликаровые (сахарные кислоты), имеющие карбоксильные группы у первого и последнего атома углерода. При специфических условиях окисления (ферментативный процесс и др.) возможно превращение альдоз в гликуровые (уроновые кислоты), содержащие карбоксильную группу вместо последней концевой спиртовой группы (из глюкозы – глюкуроновая кислота, из галактозы – галактуроновая кислота). Окисление моносахаридов в щелочной среде приводит к восстановлению катионов металлов (меди, серебра), так как преобладающая циклическая форма таутомерно переходит в альдегидную форму (для альдоз), а кетозы в щелочной среде изомеризуются в альдозы. В щелочной среде моносахариды расщепляются, идет деструкция углеродного скелета и образуется смесь продуктов окисления. Реакции восстановления моносахаридов (альдоз и кетоз) приводят к образованию многоатомных спиртов (из глюкозы – сорбит, из ксилозы – ксилит, из маннозы – маннит). По гидроксильным группам моносахаридам возможно образование простого эфира, сложного эфира) или хелатного комплексного соединения с Cu(OH)2, что является качественной реакцией на многоатомные спирты, в молекулах которых имеются две соседние гидроксильные группы. Одна из важнейших реакций моносахаридов – взаимодействие с гидроксилсодержащими соединениями (спиртами, фенолами и др.) в условиях кислотного катализа, когда в реакции участвует только полуацетальный (гликозидный) гидроксил и образуются циклические ацетали – гликозиды. Например,  H HC  H C H C  HO C H HO C H H C H C H C H CO + CH3OH HCl газ H  C C H C H C   HO C H HO C H H C H C H C H CO + H2O CH2OH CH2OH -D-глюкопираноза α-D-метилглюкопиранозид (-D-метилглюкозид)  CH2OH CH2OHH OH + CH3OH или  HCl HClгаз CH2OH  H O H OH OH H OH H OH H OCH3 + H2O Окончание –озадля сахаров в названиях гликозидов заменяется на –озид (галактозид, фруктозид, рибозид и т.д.). |
