ответы на экзаменационные билеты. Применение изоферментов
 Скачать 6.79 Mb. Скачать 6.79 Mb.
|
ЦНС ГИПОТАЛАМУС ГИПОФИЗ ПЕРИФЕРИЧЕСКИЕ ЖЕЛЕЗЫ ТКАНИ МИШЕНИВ гипоталамусе вырабатываются специфические полипептиды: либерины и статины, они поступают в гипофиз и активизируют выработку тропных гормонов гипофиза (либерины или освобождающие факторы) или ингибируют выработку тропных гормонов (статины). В регуляции гормональной активности присутствует также и механизм обратной связи: если периферическая железа вырабатывает избыточное количество гормона, то его высокая концентрация в крови активирует синтез статинов в гипоталамусе, торможение выработки тропных гормонов и в конечном итоге снижение продукции гормона периферической железы. Два основных механизма действия сигнальных молекул по локализации рецептора: 1. Мембранный – рецептор расположен на мембране. Для этих рецепторов в зависимости от способа передачи гормонального сигнала в клетку выделяют три вида мембраносвязанных рецепторов и, соответственно, три механизма передачи сигнала. По данному механизму работают пептидные и белковые гормоны, катехоламины, эйкозаноиды. 2. Цитозольный – рецептор расположен в цитозоле. Виды мембраносвязанных рецепторов 1. Рецепторы, обладающие каталитической активностью – при взаимодействии лиганда с рецептором активируется внутриклеточная часть (домен) рецептора, имеющий тирозинкиназную или тирозинфосфатазную или гуанилатциклазную активность. По этому механизму действуют СТГ, инсулин, пролактин, интерлейкины, ростовые факторы, интерфероны α, β, γ. 2. Каналообразующие рецепторы – присоединение лиганда к рецептору вызывает открытие ионного канала на мембране. Таким образом действуют нейромедиаторы (ацетилхолин, глицин, ГАМК, серотонин, гистамин, глутамат); 3. Рецепторы, связанные с G-белками – передача сигнала от гормона происходит при посредстве G-белка. G-белок влияет на ферменты, образующиевторичные мессенджеры (посредники ). Последние передают сигнал на внутриклеточные белки. Большинство гормонов действуют по данному механизму. К третьему виду относятся аденилатциклазный и кальций-фосфолипидный механизмы. Тканевой распад пуриновых и пиримидиновых нуклеотидов. Конечные продукты обмена пуринов и пиримидинов. Гиперурикемия. Подагра. Распад пуриновых азотистых оснований      Аммиак и мочевая кислота –конечные продукты распада пуриновых азотистых оснований. •В сутки с мочой выводится до 1г мочевой кислоты. •0,21-0,42 ммоль/л –норма содержания мочевой кислоты в крови мужчин. •Мочевая кислота –плохо растворимое соединение. 40-50 мг/л мочевой кислоты выпадает в осадок. •При снижении рН появляются очаги кристаллизации мочевой кислоты. Ураты откладываются в тканях. Гиперурикемия наблюдается при •подагре, •болезни Леша-Нихана, •усиленном обмене нуклеиновых кислот (опухоли, перницитозная анемия, инфекционный мононуклеоз, миелопролиферативные состояния), •почечной недостаточности, •остром алкоголизме, •врождённом дефиците Г-6-ФДГ, •избыточной продукции лактата, •диабете. Следствием гиперурикемииявляется кристаллизация уратовв различных тканях и связках, вызывающая воспалительный процесс, который называется ПОДАГРА. Подагра связана с •увеличением синтеза мочевой кислоты, •снижением в плазме уратсвязывающего белка (α-гликопротеин), •замедлением выведения уратов с мочой. В 20 раз чаще подагра встречается у мужчин, чем у женщин, так как у них меньше экскреция уратов с мочой. •В Армении в почве и воде содержится много молибдена, поэтому в этой стране выше поражённость подагрой. Признаки подагры •подагрические кризы (ураты натрия откладываются в суставах), •тофусы (подагрические узелки) в суставах, сухожилиях, хрящах, коже, почках, •почечные камни. Тест на подагру Употребление пищи, богатой нуклеопротеинами, ведёт к увеличению мочевой кислоты и появлению боли в суставах. Лечение подагры •снижение содержания пуринов в пище, •повышение экскреции уратовс мочой (салицилаты), •уменьшение образования уратов. Аллопуринол–конкурентный ингибитор сантиноксидазы. Распад пиримидиновых азотистых оснований 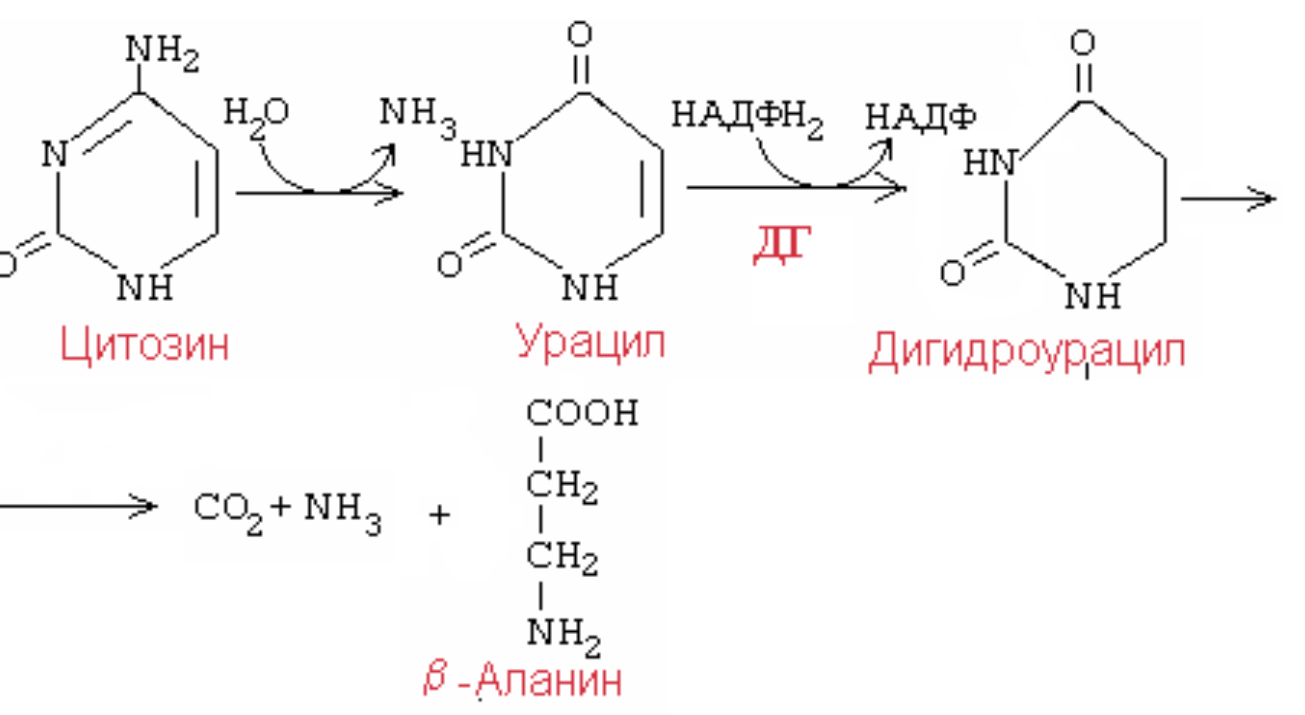 Распад тимина  Болезнь Леша-Нихана –ювенильная гиперурикемия •возникает при отсутствии фермента гипоксантин-гуанинфосфорибозилтрансферазы, •врождённое заболевание мальчиков. •При этом для синтеза пуриновых нуклеотидов не могут быть повторно использованы гипоксантин и гуанин, в результате чего происходит стимуляция образования из них уратов. Симптомы •умственная отсталость, •агрессия, •самоистязания, •церебральные параличи. У больного 67 лет установлен атеросклероз коронарных артерий и сосудов мозга. Назовите липопротеины, концентрацию которых нужно контролировать в ходе лечения данного больного. Дайте характеристику этих транспортных форм липидов. Билет 7 ЛПОНП ЛПНП ЛПВП Билет 8. 1.Биологические мембраны, их структурные компоненты. Функции биологических мембран. Структурной основой всех мембран являются липиды, в частности фосфолипиды, представленные двумя соединениями фосфодиацилглициринами и сфингомиелинами. Фосфотидилглицерин - наиболее распространенный представитель фосфолипидов он присутствует в мембранах всех живых организмов и является производным фосфатидной кислоты. В основном это кислоты с длиной углеродной цепи 12-24 атома, либо полностью насыщенные либо имеющие одну или несколько несопряженных двойных связей. В структуре фосфолипидов заложена важная функциональная особенность: содержание длинной гидрофобной цепи и гидрофильной "головки" из фосфатидной кислоты. Сфингомиелины являются производными аминоспирта сфингозина. Они характерны только для мембран животных клеток. Наряду с этими компонентами мембраны содержат белки и связанные с ними углеводы. Мембраны представляют собой плоские образования толщиной в несколько молекул (60-100 Å). Основу составляет липидный бислой, где гидрофильные головки обращены к воде внутри и снаружи клетки, а гидрофобные хвосты из жирных кислот как бы выталкиваются из воды и сливаются между собой внутри мембраны (рис. 4.7.1.). Отдельные участки мембраны, липиды которых содержат больше насыщенных ЖК находятся в жестком состоянии, другие, где содержится больше ненасыщенных ЖК, в более расплавленном. Между ацилными цепями липидного бислоя содержится холестерол, он препятствует их кристаллизации, т.е. поддерживает состояние текучести. Мембрана не статическое образование, а благодаря жидкокристаллической структуре она является двухслойным раствором, в котором липиды способны диффундировать как параллельно поверхности мембраны, так и из одного монослоя в другой. В структуру мембран обязательно входят белки и их состав варьирует в зависимости от функции той или иной мембраны. В зависимости от прочности связи с мембраной различают периферические и интегральные белки. Интегральные белки располагаются между липидами монослоя или пронизывают весь бислой, часто возвышаясь над поверхностью мембраны.Периферические белки связаны с мембранами электростатическими и водородными связями и часто взаимодействуют таким образом с интегральными белками (рис. 4.7.1.). Белки выполняют следующие функции: 1) транспорт (трансмембранный перенос веществ); 2) преобразование энергии (ферменты дыхательной цепи); 3) коммуникативную (рецепторные белки связывают клетку с окружающей средой); 2. Патология углеводного обмена. Сахарный диабет. Нарушение углеводного и липидного обмена при этом заболевании. Сахарный диабет – группа обменных заболеваний, характеризующихся гипергликемией, которая является результатом дефекта секреции или действия инсулина или обоих процессов. •Сахарный диабет –тяжёлое распространённое эндокринное заболевание, связанное с абсолютным или относительным дефицитом инсулина, сопровождается нарушением всех видов обмена. Способствуют развитию сахарного диабета: •стрессы, •избыток углеводов и жиров в питании, •гиподинамия, •ожирение, •экологическое неблагополучие, •артериальная гипертензия. Дефицит инсулина возникает при: •поражении поджелудочной железы, •нарушении перехода проинсулина в инсулин, •нарушении молекулярной структуры инсулина, •дефекте рецепторов в органах-мишенях. •усиленном действии инсулиназы, •избытке контринсулярного гормона. Типы сахарного диабета •Сахарный диабет I типа–инсулинозависимый. Возникает при разрушении ß-клеток из-за аутоиммунных реакций. Абсолютный дефицит инсулина. •Сахарный диабет II типа–инсулиннезависимый. Возникает из-за повреждения механизмов передачи инсулинового сигнала в клетки-мишени или нарушения секреции инсулина. Характерные симптомы сахарного диабета 1. Гипергликемия вызвана: -нарушением проницаемости глюкозы в ткани, -усилением гликогенолиза, -усилением глюконеогенеза, -действием контринсулярных гормонов. 2. Глюкозурия. 3. Полиурия и полидипсия (жажда). 4. Кетонемия и кетонурия. 5. Азотемия и азотурия. 6. Снижение антиоксидантной защиты. Механизм развития кетоацидоза •Дефицит инсулина и резкое повышение концентрации всех контринсулярных гормонов –причина активации липолиза и мобилизации СЖК, что способствует активной продукции кетоновых тел. •Жиры используются в качестве источника энергии, ацетил-КоА идёт на синтез кетоновых тел. Диагностика сахарного диабета •анализ крови, слезы, •тест толерантности к глюкозе (ТТГ), •определение глюкозы и ацетона в моче. Тест толерантности к глюкозе –исследование способности использовать глюкозу при нагрузках. Методика проведения: 1.Натощак измеряют уровень сахара крови. 2.Испытуемый выпивает стакан сладкого чая (нагрузка). 1г глюкозы на 1 кг массы тела. 3.Через 2 часа вновь определяют уровень сахара крови. В норме уровень глюкозы в крови: •натощак 3,3-5,5 ммоль/л, •через 2 часа после приёма пищи менее 7,8 ммоль/л, в моче сахар отсутствует, •максимально поднимается (не более 80% от исходного) через 60 минут, затем снижается и через 3 часа нормализуется. При латентном сахарном диабете нарушена толерантность к глюкозе •уровень глюкозы натощак может быть в норме (менее 6,7 ммоль/л), •через 2 часа после приёма пищи уровень глюкозы в крови более 7,8 –11,1 ммоль/л, При явном сахарном диабете: •уровень глюкозы натощак повышен (более 6,7 ммоль/л), •через 2 часа после нагрузки – более 11,1 ммоль/л. Сахарная кривая 1.Фаза –рефлекторная. 2.Выраженная гипергликемия. 3.Инсулиновая фаза. 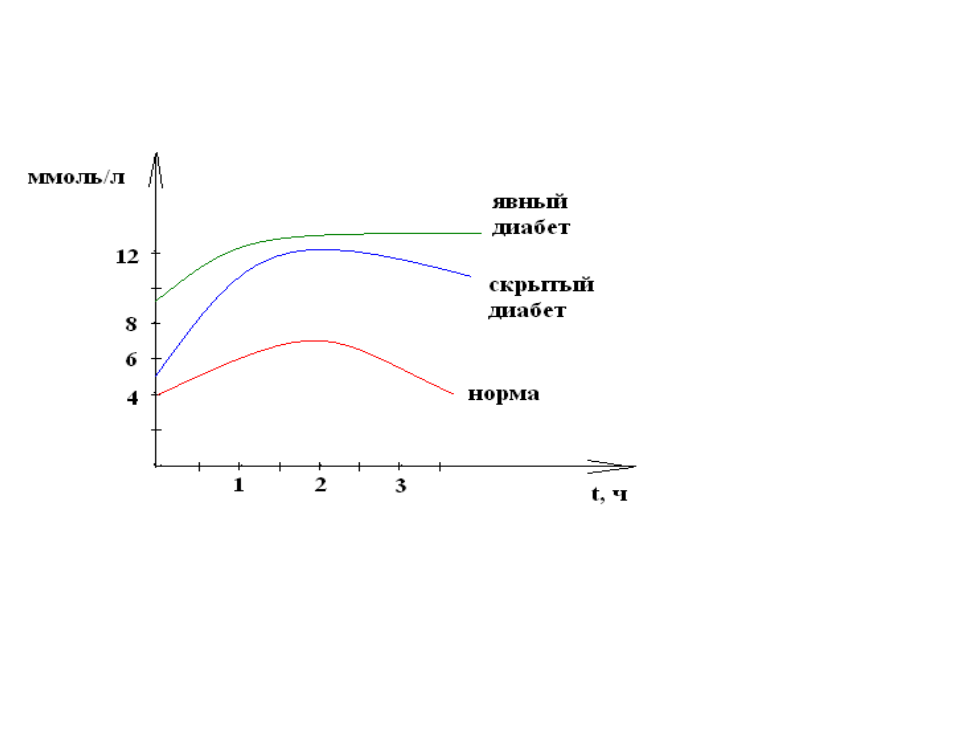 3. В крови больного повышена активность липазы, амилазы, трипсина. О какой патологии следует думать? Какие реакции катализируются данными ферментами? Билет8 амилаза -острый панкреотит трипсин- расщепление белков липаза -гидролиз липидов Билет 9. Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций. В основе классификации лежит тип катализируемой реакции. •Оксидоредуктазыкатализируют окислительно-восстановительные реакции. •Трансферазы-реакции с переносом групп. •Гидролазы -гидролитический разрыв связи СС, СN, СSс присоединением воды по месту разрыва. •Лиазы–реакции негидролитическогорасщепления с образованием двойных связей, некоторые обратные реакции синтеза. •Изомеразы–перенос групп внутри молекулы с образованием изомеров. •Лигазыкатализируют соединение двух молекул, сопряжённое с разрывом пирофосфатнойсвязи АТФ. Трансферазы Коферменты трансфераз: •ФП, •ТГФК, •АТФ, •ФАФС, •АДФ Трансферазы •фосфотрансферазы, •аминотрансферазы, •гликозилтрансферазы, •ацилтрансферазы, •переносчики одноуглеродных частиц, •переносчики кетонных и альдегидных групп. Трансферазы катализируют реакции переноса различных групп от одного субстрата (донор) к другому (акцептор), участвуют в реакциях взаимопревращения различных веществ, обезвреживания природных и чужеродных соединений. Коферментами являются пиридоксальфосфат,коэнзим А, тетрагидрофолиевая кислота, метилкобаламин. Класс подразделяется на 9 подклассов в зависимости от строения переносимых групп.Примером подклассов являются ферменты, переносящие одноуглеродные фрагменты, альдегидные или кетоостатки, ацильные остатки, азотсодержащие группы, фосфорсодержащие группы. селенсодержащие группы.На подподклассы деление производится в зависимости от вида переносимой группы – метил (2.1.1.), карбоксиметил или формил (2.1.2.), амино-группы (2.6.1.).Часто встречается рабочее название трансфераз – киназы. Это трансферазы, катализирующие перенос фосфата от АТФ на субстрат (моносахариды, белки и др), т.е. фосфотрансферазы. Напишите последовательность реакций превращения ацетил-КоА в мевалоновую кислоту в процессе синтеза холестерина. Укажите ферменты и коферменты. Синтез холестерина включает 35 реакций, идёт в 3 стадии: образование из ацетил-КоА мевалоновой кислоты, образование из мевалоновой кислоты сквалена, циклизация сквалена в холестерин. 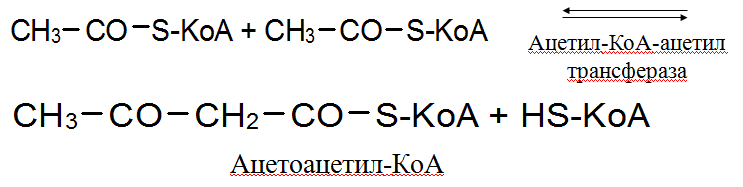    Биохимический анализ нормальной и патологической мочи. Глюкозурия, протеинурия, кетонурия, билирубинурия. Патологические компоненты мочи Пигменты Кроме указанных выше пигментов, в моче при патологиях может обнаруживаться еще пигмент – продукт распада гема билирубин. Клинико‑диагностическое значение Билирубинурия может развиться при инфекционных заболеваниях, диффузном токсическом зобе. При заболеваниях печени он появляется в моче в виде билирубина глюкуронида (прямой билирубин) – паренхиматозные желтухи при вирусных гепатитах или нарушение оттока желчи при механических желтухах. Для гемолитических желтух билирубинурия не характерна, т.к. непрямой билирубин не проходит через почечный фильтр. Белки В норме белок в моче практически отсутствует. Клинико‑диагностическое значение Появление белка в моче называется протеинурией. По степени потери белка различают от 0,003 до 1 г/сут, от 1 до 3 г/сут, от 3 г/сут и более. Самая большая потеря белка происходит при поражении гломерулярного аппарата. Почечнаяпротеинурия возникает при поражении почек: поражение почечного фильтра – повышение проницаемости гломерул (нарушение эндотелия, базальной мембраны, дефект подоцитов), снижение кровотока в почках (замедление, уменьшение объема крови). Внепочечныепротеинурии: данный вид протеинурия возникает при воспалении в мочеточниках, мочевом пузыре, уретре, предстательной железе. также в моче определяют белок Бенс-Джонса, что характерно для миеломной болезни, макроглобулинемии Вальденстрема. Функциональная почечная протеинурия (временная) – при стрессах, отрицательных эмоциях, при длительной физической нагрузке (маршевая), при длительном нахождении в положении стоя (чаще у детей), холодовая. Глюкоза Моча здорового человека содержит минимальное количество глюкозы, которое обычными лабораторными пробами не обнаруживается. Клинико‑диагностическое значение Появление глюкозы в моче называется глюкозурия. Для более достоверной оценки исследуют мочу, собранную за сутки. Существуют две основные причины, обуславливающие появление глюкозы в моче: гипергликемия, при которой концентрация глюкозы в ультрафильтрате превышает способность почек к ее реабсорбции (сахарный и стероидный диабет, тиреотоксикоз), нарушение канальцевой реабсорбции, при которой даже низкие количества глюкозы не реабсорбируются (нефроз, нефрит, нефротический синдром, ренальный диабет). Физиологическая глюкозурия наблюдается при употреблении большого количества сладостей (только при наличии нарушений в почках или инсулярного аппарата), при стрессе, после приема лекарств (кофеин, кортикостероидные гормоны). Кетоновые тела Клинико‑диагностическое значение Наличие кетоновых тел в моче называют кетонурией. Чаще всего наблюдают при тяжелом сахарном диабете, диабетической коме, голодании, тяжелых токсикозах. Определение кетонов в моче может использоваться для оценки эффективности диеты при снижении веса. Билет 10. Классификация и химическая структура липидов. Роль липидов в обеспечении жизнедеятельности организма. Переваривание и всасывание липидов, роль желчи в этом процессе, желчные кислоты. Ресинтез липидов в эпителии кишечника. 1) ЛИПИДЫ. Липиды - сложные эфиры ВЖК и спиртов (глицерин, инозит, сфингозин). Липиды не растворимы в воде Простые липиды представлены двухкомпонентными веществами - сложными эфирами вжк с глицерином. В эту группу относят: а) триацилглицерины - сложные эфиры ВЖК и глицерина. б) воска - сложные эфиры ВЖК и высших спиртов. в) стериды - сложные эфиры ВЖК и полициклических спиртов (холестерин). Сложные липиды - многокомпонентные вещества, состоящие из спиртов, ВЖК, остатка фосфорной кислоты, азотистых оснований, одного или нескольких остатков углеводов. Их подразделяют на фосфолипиды и гликолипиды. 1. Фосфолипиды представляют собой сложные эфиры многоатомных спиртов (глицерин, сфингозин, инозит) с ВЖК, содержащие в качестве добавочных групп остатки фосфорной группы и азотистых оснований. Выделяют: а) глицерофосфолипиды: лецитин, инозитфосфолипид. б) сфингофосфолипиды. Входят в состав всех тканей и клеток организма. Они легко образуют комплексы липидов с белками, облегчая транспорт липидов, участвуют в формировании плазматических и внутриклеточных мембран, обеспечивают проницаемость мембран. 2. Гликолипиды. В их состав входит галактоза или её производные, сфингозин и ВЖК. Они восстанавливают электровозбудимость мозговой ткани, вовлечены в процесс приема сигналов, поступающих в клетки, участвуют в рецепции пептидных гормонов, входят в состав мозговой и нервной ткани. БИОРОЛЬ: 1.Энергетическая (при окислении 1 грамма жира выделяется 9,3 ккал). 2.Пластическая (в комплексе с белком входят в состав биологических мембран клеток и клеточных органелл, обеспечивая их проницаемость). Участвуют в передаче нервного импульса.3.Жир, окружая внутренние органы своеобразной капсулой, предохраняет их от ударов и сотрясений.4.Входя в состав подкожной клетчатки, липиды выполняют функцию терморегуляции. 5.Являются источником жирорастворимых витаминов. Переваривание и всасывание липидов.Суточная потребность 80-100 г., из них 25 г. должно поступать растительных липидов. Переваривание липидов происходит в тех отделах пищеварительного тракта, где имеются следующие условия: 1. Наличие липаз-ферментов расщеляющих липиды. 2. Условия для проявления их оптимальной активности (рН=7,8-8). 3. Условия для эмульгирования липидов. Липаза может воздействовать только на эмульгированные жиры. Эмульсии-дисперсные системы двух несмешивающихся жидкостей, где одна жидкость находится в раздробленном состоянии (в виде капелек) в другой (жир-Н2О). Такими эмульгаторами для липидов в нашем организме являются соли желчных кислот. В ротовой полости переваривания липидов не происходит. В желудке липаза низкоактивна, т.к. рН среды в желудке 1,5-2,0. Исключение составляют новорожденные и грудные дети. У них в желудке рН среды =5-6, в этих условиях липаза расщепляет эмульгированный жир грудного молока. Основное место переваривания липидов у взрослого организма – тонкий отдел кишечника (12-перстная кишка), где имеются все необходимые условия. В этот отдел кишечника поступает сок поджелудочной железы, содержащий липазы, сюда же поступает из желчного пузыря желчь, составные компоненты которой (желчные кислоты) необходимы для переваривания липидов. Функции желчных кислот: 1. эмульгируют липиды 2. активируют липазы 3. способствуют всасыванию продуктов гидролиза липидов в стенку кишечника. Желчные кислоты образуются в печени из холестерина и являются производными холановой кислоты. В желчи человека содержатся, главным образом, парные желчные кислоты (т.е. желчная кислота взаимодействует с глицином или таурином). Н  апример: холевая кислота + глицин - гликохолевая; соответственно апример: холевая кислота + глицин - гликохолевая; соответственнотаурохолиевая кислота) и т.д. Гидролиз триацилглицерина в кишечнике идёт ступенчато. 40% жира гидролизуется полностью до глицерина и ВЖК. Таким образом, образующаяся в результате гидролиза липидов смесь содержит: жирные кислоты, моноацилглицерины, диацилглицерины, глицерин и другие компоненты липидов. Всасывание продуктов гидролиза липидов. Глицерин и жирные кислоты с короткой углеродной цепью уходят из кишечника через портальную систему кровообращения и поступают в печень. А жирные кислоты с количеством углеродных атомов больше 10, моноацил-глицерины, диацилглицерины всасываются с помощью желчных кислот (путем образования с ними мицелл), которые транспортируют их через слизистую оболочку кишечника в эпителий кишечника. Внутри стенки кишечника мицелла распадается, а желчные кислоты уходят в кровь и через систему воротной вены попадают в печень, а оттуда вновь в желчные протоки. Таким образом происходит постоянная циркуляция желчных кислот между печенью и кишечником. Установлено, что у человека общий пул желчных кислот составляет 2,8-3,5 г., при этом они совершают 6-8 оборотов в сутки. 0,3 г. желчных кислот теряется с калом. Нарушения желчеобразования или поступления желчи в кишечник приводит к тому, что жиры выделяются в непереваренном или частично переваренном виде с калом – стеаторея. Из продуктов гидролиза триацилглицеринов пищи в стенке кишечника происходит ресинтез жиров, специфичных для данного организма. Здесь же в стенке кишечника реситезированный жир формирует с белками липопротеидные комплексы - хиломикроны (ХМ), которые являются транспортной формой экзогенного жира. ХМ - это комплекс белка (2%) + липид (Тгл/90%) + ХС + фосфолипид. ХМ в силу больших размеров диффундируют в лимфатическую систему кишечника, а из нее - в грудной лимфатический проток, затем в кровяное русло. Захватываются они печенью и жировой тканью, где расщепляются липопротеидлипазой Витамины, их классификация. Витамин В12 и фолиевая кислота, участие в обмене веществ и признаки витаминной недостаточности. ВИТАМИНЫ. В12 И ФОЛИЕВАЯ КИСЛОТА. Витамины – это низкомолекулярные органические соединения, которые поступают в организм с пищей или синтезируются в относительно небольших количествах в кишечнике. Они участвуют в обменных процессах в составе коферментов. Их классифицируют по способности растворяться в воде или липидах: водорастворимые (РР, В1, В2, В6, В12, С) и жирорастворимые витамины (А, D, Е, К). Витамин В12 – цианкобаламин (антианемический фактор). СОДЕРЖИТСЯ: печени, мясе, рыбе.Витамин В12 синтезируют микроорганизмы. Биологическая роль: Витамин В12 участвует в: реакциях трансметилирования (переносит метильные группы при синтези митионина, холина, ацетата). реакциях изомеризации. восстановление рибонуклеотидов до дезоксирибонуклеотидов. синтезе ДНК и пролиферации кроветворных клеток. синтезе ГЕМа. окисление жирных кислот с нечетным числом углеродных атомов. Гипо- и авитаминоз В12 у человека может развиваться при недостаточном поступлении витамина с пищей и при нарушении его всасывания и усвоения, что приводит к злокачественную макроцитарную мегалобластическую анемию, нарушения нервной системы, снижение кислотности желудочного сока. ФОЛИЕВАЯ КИСЛОТА. Тетрагидрофолиевая кислота (ТГФК) образуется из витамина фолиевой кислоты при присоединении 4 атомов водорода к 5, 8 атомам азота и к 6, 7 атомам углерода за счет разрыва двух двойных связей. ФОЛИЕВАЯ К-ТА СОДЕРЖИТСЯ В салате, капусте, шпинате, петрушке, томате, злаках, печени, говядине, яичном желтке. При дефиците развивается Макроцитарная анемия. ТГФК участвует в ферментном катализе, связанном с переносом одноуглеродных остатков: формильного –СОН, метильного –СН3, метиленового –СН2–, гидроксиметильного –СН2ОН, метенильного >СН–, формиминового – CH=NH. Эти остатки присоединяются к ТГФК по 5 и(или) 10 атомам азота. Аметоптерин В комплексной терапии злокачественного острого лейкоза у детей назначают антиметаболит фолиевой кислоты аметоптерин (метотрексат). Аметоптерин конкурирует с фолиевой кислотой за фермент, так как похож на неё, но коферментом быть не может, поскольку отличается от нее. Он ингибирует перенос одноуглеродных остатков, необходимых для синтеза нуклеиновых кислот, содержащихся в большом количестве в клетках белой крови, и тем самым снижает их число, резко повышенное при ряде форм острого лейкоза. 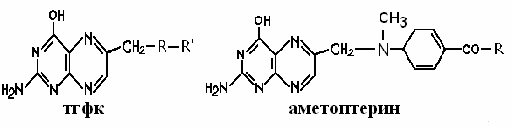 3.Какие изменения белкового спектра будут наблюдаться при остром воспалении? Что такое белки «острой фазы»? Диагностическое значение определения их концентрации в крови. Билет10 повышен. СРБ в 1000 раз БОФ –белки плазмы крови,кроме повыш. При воспалении явл-ся маркерами повреждения и воспаления. Повыш.при оухолях и беременности. Альфа 1-антитрипсин,церуллоплазмин,гаптоглобин,гетопексин,Срб,фибриноген. БИЛЕТ№11 1. Роль воды в организме. Водный баланс, его регуляция и патология. Макроэлементы: натрий, калий, хлор, магний. Роль и обмен воды Без воды человек может прожить 5 дней. Содержание воды в организме человека зависит от возраста, особенностей питания, пола и других факторов. Эмбрион человека 1,5 месяцев содержит 97.5% воды, 4-х месяцев - 91-92%, плод 7-8 месяцев - 83-85% воды, новорожденные дети 74-77%, взрослые мужчины - 60-65%, лица старше 81 года содержат около 50% воды. Функции воды в организме вода является растворителем, регулятор теплового баланса в организме, транспортная функция, обеспечивает тургор тканей, среда для химических реакций, участник химических реакций, в жидкой среде осуществляется переваривание и всасывание, структурная функция воды. Водный баланс У взрослого здорового человека водный баланс равен нулю. В норме количество потребляемой и образующейся в процессе метаболизма воды равно количеству выделяемой из организма воды.
Положительный водный баланс наблюдается при избыточном питье, массивных внутривенных введениях, почечной недостаточности, усилении выработки альдостерона, вазопрессина. Избыток воды приводит к перегрузке сердечно-сосудистой системы, вызывает изнуряющее потоотделение, сопровождающееся потерей солей и витаминов, ослаблением организма. Отрицательный водный баланс наблюдается при резком ограничении поступления воды в организм, при рвоте, диарее, при несахарном диабете. у ожоговых больных: при потере 10% воды развивается интоксикация, при потере 20% воды наступает гибель организма. Нарушение водно-электролитного баланса Дегидратация, недостаток воды в организме возникает, если не восполняются потребности в ней. При избытке воды возникает гипергидратация, может развиться водная интоксикация. При белковой диете увеличивается потребность в воде. Регуляция выделения воды осуществляется ЦНС, получающей информацию от натрио-, волюмо-, осморецепторов.  Антидиуретический гормон (вазопрессин) синтезируется в гипоталамусе, затем транспортируется в заднюю долю гипофиза, способствует увеличению реабсорбции воды в почечных канальцах, снижает диурез Биологическое действие АДГ в клетках почечных канальцев АДГ связывается с V2 –рецептором, вызывая активацию аденилатциклазы и образование цАМФ, цАМФ активирует протеинкиназу, фосфорилирующую белки, фосфорилированные белки индуцируют транскрипцию гена белка аквапорина, аквапорин встраивается в мембрану клетки почечного канальца, образуя водные каналы. Альдостерон синтезируется в коре надпочечников, минералокортикоид, увеличивает реабсорбцию воды и натрия. Стимулируют синтез альдостерона: ангиотензин II, АКТГ, простагландин Е, низкая концентрация ионов натрия, высокая концентрация ионов калия. Натрий В организме взрослого человека содержится 105 г натрия, из них во внеклеточном пространстве - 50%, в костной ткани - 40%, внутри клеток – 10%. В плазме крови взрослого человека содержание натрия 135 - 147 ммоль/л, у грудных детей – в 2 раза ниже. В сутки потребляется 3-6 г натрия, что превышает физиологическую потребность. Потребность зависит от климата, национальных традиций, привычки человека. Биологическая роль натрия Участник буферных систем. Поддерживает кислотно-щелочное равновесие 2. Обеспечивает постоянство осмотического давления во внеклеточной жидкости. 3. Участвует в возникновении нервного импульса вместе с калием.4. Обмен натрия – важное звено водно-солевого обмена. Одна молекула натрия связывает 400 молекул воды. 5. Влияет на состояние мышечной и сердечно-сосудистой системы. 6. Активатор ферментов. 7. Способен повышать основной обмен. 8. Сопрягающий ион в наружной мембране животной клетки 9. Опосредует развитие гипертонической болезни за счёт увеличения объема внеклеточной жидкости и повышения тонуса капилляров и артериол. Всасывание натрия происходит в тонком кишечнике. Выводится натрий: с мочой, с потом, с калом, с пищеварительными соками. Повышено выделение натрия при: потоотделении, ожогах, рвоте, асците. Причины гипонатриемии: недостаток натрия в пище, избыточное выведение натрия через почки (лечение диуретиками), кожу (ожоги, потоотделение), желудочно-кишечный тракт (рвота, понос), избыточное поступление воды, патологическая задержка воды в организме. Клинические проявления: слабость, головокружение, потеря веса, апатия, обмороки, тахикардия, гипотония, олигурия, снижение тургора и сухость кожи, снижение внутриглазного давления, дегидратация. Гипернатриемия Причины гипернатриемии: избыточное потребление натрия, осмотические перегрузки (при переедании с мочой выводится много азота и воды), несахарный диабет (при недостатке вазопресссина), гиперальдостеронизм. Клинические проявления: артериальная гипертония, гипергидратация. Калий – внутриклеточный катион: 98% калия находится в клетках, 2% - во внеклеточной жидкости. В плазме крови - 3,5 – 5,6 ммоль/л. В сутки в организм человека должно поступать с пищей 2- 4 г калия. Максимальная потребность в калии наблюдается у детей для построения тканей тела. Калий является незаменимым элементом питания Пищевые источники калия курага, картофель, бананы, морковь, цитрусовые, клюква, виноград, яблоки, калина, мёд, перец красный. Биологическая роль калия участвует в процессах нервно-мышечной возбудимости (недостаточность калия ведёт к мышечной слабости), вместе с натрием создаёт потенциал покоя и действия клетки, дефицит калия приводит к нарушению синтеза макроэргов, принимает участие в синтезе гликогена, белков, влияет на ритм сердечных сокращений (при дефиците калия снижается возбудимость миокарда), из-за низкого содержания калия в плазме роль в поддержании осмотического давления невелика. Причины гипокалиемии недостаток калия в пище, рвота, поносы, сахарный диабет, использование диуретиков, при усиленной продукции альдостерона калий теряется с мочой. Клинические проявления: нарушение нервно-мышечной передачи, слабость, гипотония, запоры, аритмии, нарушение функции почек, алкалоз, депрессия, обмороки. Признаки недостатка калия в организме снижение умственной деятельности, памяти, кожный зуд, понижение физической выносливости, повышение чувствительности к холоду, мозоли на подошвах ног, запоры, подверженность простудам, пропадает аппетит, тошнота, рвота, медленно заживают порезы и ушибы, кариес, угревая сыпь, судороги мышц, боли в суставах, плохой сон. Причины гиперкалиемии избыточное потребление калия: алиментарное, при парентеральном питании ,при переливании длительно хранившейся крови, выход калия из клеток при: массивном повреждении ткани, активном катаболическом процессе, системном ацидозе, недостаточности инсулина, уменьшение выделения калия при: острой почечной недостаточности, приёме калий-сохраняющих диуретиков, недостатке минералокортикоидов, болезни Аддисона, адреналэктомии.Клиника гиперкалиемии сонливость, брадикардия, гипотония, нарушения ритма сердечных сокращений, параличи, парезы. Хлор основной внеклеточный анион: 90% хлора находится во внеклеточной жидкости, содержание в сыворотке: 97-108 ммоль/л, Пищевые источники хлора: молоко, мясо, яйца. Хлор легко всасывается. Выделяется с мочой, потом, калом. Биологическая роль хлора поддерживает осмотическое давление внеклеточной жидкости, входит в состав соляной кислоты желудочного сока, активатор ферментов (амилаза), поддерживает кислотно-щелочное равновесие. Депо хлора кожа, соединительная ткань, подкожная клетчатка. Недостаток хлора возникает при рвоте, гиперацидных состояниях, повышенной потливости. Магний В организме взрослого человека содержится 140 г магния. Пищевые источники магния: зелёные овощи, соль, вода. Биологическая роль магния участие в обмене белков, жиров и углеводов, участие в синтезе белков и нуклеиновых кислот, участие в переносе, хранении, утилизации энергии, снижение возбудимости нейронов,замедление нейро-мышечной передачи,расслабление гладкой мускулатуры, снижение артериального давления, магний – кофактор ферментов. Гипермагнезиемия седативный эффект, снижение артериального давления, вялость, сонливость. Гипомагнезиемия дрожь, спазмы мышц, судороги, рвота, диарея, раздражительность, аритмии, иммунодефициты, ранняя седина, кожные язвы. 2. Биосинтез ДНК (репликация). Биосинтез РНК (транскрипция). Посттранскрипционный процессинг РНК. Основные положения аминокислотного кода. Обратная транскрипция. Репликация воспроизведение (удвоение) молекул ДНК в процессе деления клетки. процесс синтеза дочерней ДНК на матрице ДНК. Структура дочерней ДНК аналогична родительской ДНК. Механизм репликации ДНК– полуконсервативный. В каждой дочерней молекуле одна нить является старой, а другая – вновь синтезированной. Постулаты Корнберга (1955 г) Для синтеза ДНК нужны нуклеозидтрифосфаты. Реакция идёт только в присутствии уже готовой ДНК, выполняющей роль матрицы. Поскольку в молекуле ДНК нуклеотидные остатки образуют пары А-Т и Г-Ц, в реакции расходуются одинаковые количества dАТФ и ТТФ (стехиометричекий коэффициент m), dГТФ и dЦТФ(стехиометричекий коэффициент n) Требуется набор ферментов (реплисома). Инициация репликации происходит в нескольких точках хромосомы. Точки инициации репликации- ориджины репликации.  Во время миграции репликативной вилки происходит разделение цепей родительской ДНК с участием ДНК-хеликазы. 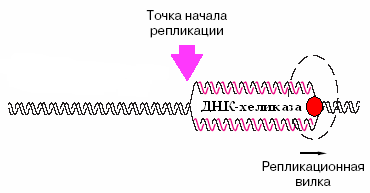 ДНК-полимераза α катализирует синтез короткого (до 10 нуклеотидов) олигонуклеотида, то есть праймера, с которого начинается синтез ДНК. Затем на конец одной цепи присоединяется ДНК-полимераза δ (дельта). Расположение оснований в двух нитях не только комплементарно, но и антипараллельно. Элонгация репликации – репликация обеих материнских цепей ДНК и связывание друг с другом фрагментов новообразованных цепей ДНК. Обе дочерние молекулы сохраняют связь с родительской. Хромосома имеет форму вилки. Обе цепи реплицируются одновременно, хотя имеют разное направление. Рост дочерних цепей должен происходить в противоположных направлениях. Синтез новых цепей идёт в направлении от 5`- к 3`- концу . На одной репликативной вилке синтезируются непрерывная нуклеотидная цепь, на другой – фрагменты Оказаки, которые потом соединяются ДНК-лигазой. Элонгация завершается отделением праймеров, формированием дочерней цепи ДНК. После завершения репликации происходит метилирование нуклеотидных остатков вновь образованных цепей ДНК. На каждом конце хромосомы присутствует специфическая нуклеотидная последовательность (GGG ТТА-теломерная ДНК). Это нужно для сохранения генетической информации. С каждым клеточным циклом ДНК хромосом будет последовательно укорачиваться. Ферменты репликации ДНК-топоизомераза (нуклеаза) разрывает цепь ДНК (3`-5`-фосфодиэфирную связь), а в конце репликации зашивает надрезы. ДНК-хеликаза расплетает двойную спираль ДНК. Белки, дестабилизирующие спираль, связываются с одноцепочечной ДНК и предотвращают комплементарное скручивание матричных цепей. Синтез ДНК на матрице РНК (обратная транскрипция) Фермент обратная транскриптаза (ревертаза, РНК-зависимая ДНК-полимераза) был обнаружен в 1970 году Балтимором и Теминым. Обратная транскриптаза Сначала синтезирует РНК-ДНК-гибрид. Затем фермент РНКаза Н удаляет РНК-цепь, оставшаяся ДНК- цепь служит матрицей длясинтеза второй цепи ДНК. Возникает двухцепочечная ДНК-копия, содержащая информацию, первично представленную в виде РНК-генома ретровируса. Транскрипция- биосинтез матричных РНК. Экспрессия генов (поток генетической информации) включает транскрипцию и трансляцию. Отличия транскрипции от репликации: не требует синтеза праймера, использует не всю молекулу ДНК, а отдельные её сегменты, требует наличия одной из цепей ДНК в качестве матрицы, которая полностью сохраняется, при транскрипции транскрибируются отдельные гены или группы генов, а при репликации кодируется вся родительская ДНК. м-РНК переносит информацию от ДНК в ядре до цитоплазмы, где она соединяется с рибосомами и служит матрицей, на которой происходит синтез белка, короткоживущая, локализована в ядре и цитоплазме, одноцепочечная, комплементарна одной из цепей ДНК.В транскрипции различают три фазы инициация, элонгация, терминация. Элонгация идёт в направлении от 5`- к 3`- концу антипараллельно матричной цепи ДНК. Активация промотора происходит с помощью белкового фактора – ТАТА. Транскриптон - участок ДНК, ограниченный промотором и сайтом терминации. У эукариотов в состав транскриптона входит один ген. Посттранскрипционный процессинг- ферментативные превращения транскриптов, после чего они стают активными. Процессинг включает: кэпирование, сплайсинг, полиаденилирование, метилирование. Кэпирование присоединение остатка 7-метилгуанозина к 5`- концу молекулы и-РНК, что защищает РНК от ферментативного распада. Полиаденилирование присоединение фрагментов АА УАА к 3`- концу и-РНК в ядре или цитоплазме. Это облегчает выход и-РНК из ядра и замедляет гидролиз в цитоплазме. Сплайсинг генов В ядре происходит сплайсинг генов – ферментативное присоединение одного гена или части гена к другому, а также процесс удаления интронов и соединения экзонов при синтезе м-РНК. Эукариотические гены имеют фрагментарное строение: они состоят из нескольких значащих участков (экзонов), разделённых нетранслируемыми вставками (интронами). Экзон – участок гена, транскрипт которого оказывается в зрелой м-РНК. Он кодирует участок цепи белка. Интрон – вставочная последовательность в гене, которая транскрибируется, но вырезается до трансляции. Регуляторные сигналы при транскрипции Энхансеры повышают уровень транскрипции. Силансеры ослабляют уровень транскрипции. Энхансеры и силансеры – участки в нетранскрибируемых последовательностях генома. Рибозимы катализируют сам сплайсинг. 3.При длительном приеме антибиотиков и сульфаниламидов угнетается микрофлора кишечника, способная синтезировать пиридоксин. В результате может возникнуть гиповитаминоз В6. Какие реакции превращения глутаминовой кислоты нарушаются в этом случае? Билет 11 Трансаминирование,обмен белков Билет 12. |
