Тец руководство. Руководство к практаческим занятиям по медицинской микробиологии, вирусологии и иммунологии под редакцией
 Скачать 2.14 Mb. Скачать 2.14 Mb.
|
|
Тема 2.3. МОРФОЛОГИЧЕСКИЕ ОСОБЕННОСТИ И УЛЬТРАСТРУКТУРА АКТИНОМИЦЕТОВ И СПИРОХЕТ Введение. Актиномицеты (Actinomyces) относятся к порядку Actinomycetales, включающему семейства Actinomycetaceae, Strep-tomycetaceae и Nocardiaceae. Актиномицеты имеют нитевидную форму. Они способны к ветвлению и могут образовывать структуры, напоминающие мицелий одноклеточных грибов (рис. 2.3.1). Встречаются также палочко- и кокковидные формы. Нити имеют длину 100—600 мкм и толщину 0,2—1,2 мкм. Актиномицеты неподвижны, лишены выраженной капсулы, жгутиков и пилей. Как и другие бактерии, актиномицеты окрашиваются простыми методами или по методу Грама. Актиномицеты относятся к фирмикутным бактериям и окрашиваются грамположительно. В отличие от других бактерий они способны размножаться не только поперечным делением, но и спорами. Спирохеты относятся к порядку Spirochaetales. Они представляют собой извитые подвижные бактерии. Патогенные спирохеты входят в семейство Spirochaetaceae и принадлежат к трем родам: Borrelia, Treponema и Leptospira. Их основные морфологические признаки представлены в табл. 2.3.1. Клетка спирохеты имеет форму нити, закрученной в виде спирали. Клеточная стенка обладает строением, типичным для грациликутных бактерий. В периплазматическом пространстве располагаются сократительные фибриллы — эндофлагеллы, которые прикрепляются к полюсам клетки с обоих концов, оплетают тело бактерии по направлению к центру клетки, где они переплетаются между собой. Фибриллы обладают сокра- 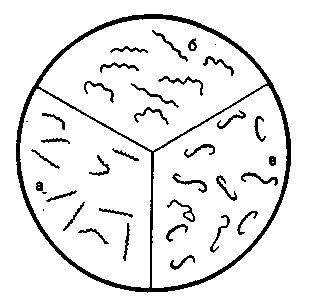
План Программа Определение формы актиномицетов в препарате, окрашенном по методу Грама. Методы изучения морфологии спирохет с дифференциацией по морфологическим признакам. Определение формы и подвижности спирохет в прижизненных препаратах. Исследование спирохет в окрашенных препаратах. Изучение электронограмм спирохет и спирилл. Демонстрация Препарат из чистой культуры актиномицетов. Окраскапо методу Грама. Подвижность лептоспир (темнопольная микроскопия). Боррелии в препарате толстой капли крови (окраска по методу Романовского-Гимзы). а Задание студентам Изучить морфологию актиномицетов в препарате. Зарисовать. Изучить морфологию лептоспир с помощью методатемнопольной микроскопии. Зарисовать. Изучить морфологию боррелий в препарате толстой капли крови. Зарисовать. Методические указания Морфологию спирохет изучают в нативных препаратах и в мазках, окрашенных по методу Романовского-Гимзы. Препараты исследуют с помощью темнопольной или фазово-кон-трастной микроскопии, наблюдая за активным и характерным движением спирохет и особенностями их формы. Приготовление мазка из крови. На чистое обезжиренное стекло ближе к одному из его концов поместить каплю крови. Другое предметное стекло со шлифованым краем прижать под углом 45° к капле крови, а затем скользящим движением передвинуть его к другому концу нижнего стекла. При этом кровь распределится по предметному стеклу тонким слоем. Высушить препарат на воздухе, фиксировать в жидком фиксаторе (метиловый спирт или смесь этилового спирта и эфира). Окраска препарата по методу Романовского-Гимзы (смесь метиленового синего, эозина и азура). На мазок нанести рабочий раствор красителя (2 капли красителя на 1 мл дистиллированной воды) на 10—20 мин. Затем препарат промыть водой и высушить на воздухе. Боррелии — возбудители возвратного тифа (B.recurrentis) окрашиваются в фиолетовый, эритроциты крови — в розово-коричневый, ядра лейкоцитов — в фиолетовый цвет. Трепонемы окрашиваются в бледно-розовый, лептоспиры — в розово-сиреневатый цвет.
План Программа 1. Изучение морфологии риккетсий, хламидий и мико-плазм. Демонстрация Хламидий в инфицированных клетках эпителия уретры, мазках-отпечатках из органов и культурах клеток. Электронограммы риккетсий, хламидий и микоплазм. Задание студентам Изучить морфологию риккетсий в препарате, окрашенном по Здродовскому. Изучить морфологию хламидий. 3. Изучить морфологию микоплазм. Методические указания Окраска риккетсий по методу Здродовского Окрасить мазок разведенным фуксином Циля (10—15 капель на 10 мл дистиллированной воды) в течение 5 мин. Промыть водой. Обработать мазок 0,5 % раствором лимонной кислоты или 0,01 % раствором хлористоводородной кислоты. Промыть водой. Окрасить метиленовым синим в течение 1 мин. Промыть водой и высушить препарат. Риккетсий, окрашенные по методу Здродовского, имеют красный цвет, цитоплазма клеток, в которых они паразитируют, — голубая, ядра — синие. Глава 3 ФИЗИОЛОГИЯ БАКТЕРИЙ Введение. Бактерии в ходе эволюции освоили различные экологические ниши и приспособились к соответствующим источникам неорганических и органических веществ, наличию кислорода, температуре и другим факторам окружающей среды. Создание условий, подходящих для выращивания (культивирования) микробов, необходимо для изучения их свойств и диагностики вызываемых ими заболеваний. Культивирование бактерий лежит в основе бактериологических методов исследования. Питательные среды. Применяют для выращивания (культивирования) микроорганизмов в лабораторных или промышленных условиях. Любая питательная среда должна отвечать сле дующим требованиям: — содержать все необходимые для роста и размножения бактерий вещества в легкоусвояемой форме; — иметь оптимальные для бактерий физико-химические свойства: рН, влажность, осмолярность и др. Компоненты питательных сред. Для построения органических компонентов микробной клетки необходимы азот, углерод, водород и кислород. Снабжение водородом и кислородом осуществляется за счет воды. В качестве источника углерода гетеротрофные микроорганизмы используют органические соединения, в первую очередь сахара, многоатомные спирты и органические кислоты. Источником азота могут служить неорганические соединения (соли аммония), а также олигопептиды и аминокислоты — продукты гидролиза белков различного происхождения (животного — мясо, рыба, казеин; растительного — соевые бобы, горох; микробного — дрожжи и др.). Поскольку в состав микробных клеток входят не только органические, но и минеральные соединения, питательные среды должны содержать неорганические вещества: соединения хлора, фосфора, серы, натрия, калия, кальция, магния и некоторые другие. Минеральные соли необходимы также для создания оптимальных для роста и размножения физико-химических условий (рН, ионная сила и т.д.). Микробам для нормального развития необходимы микроэлементы, преимущественно металлы (железо, медь, марганец и др.), которые входят в состав простетических групп молекул различных ферментов. Кроме основных компонентов питательной среды, для жизнедеятельности ауксотрофных микроорганизмов, к числу которых относятся многие патогенные бактерии, требуется присутствие факторов роста — органических соединений, входящих в состав микробной клетки, но не синтезируемых ею самостоятельно. В качестве факторов роста могут выступать определенные аминокислоты, азотистые основания, витамины и др. Большинство бактерий нуждается в таких факторах роста, как витамины группы В и никотиновая кислота. Для роста некоторых патогенных бактерий в питательные среды надо добавлять нативные белки (кровь, сыворотку). Для жизнедеятельности микробной клетки, безусловно, необходима вода как основной растворитель и среда для протекания всех биохимических реакций. В бактериологической практике используют среды, различные по происхождению. Синтетическими питательными средами называют такие, которые состоят из растворов химически чистых соединений в точно установленных дозировках. Преимуществом синтетических сред являются их строго постоянный состав и воспроизводимость. Полусинтетические среды включают наряду с химически чистыми соединениями перера-ботанные нативные компоненты неопределенного состава — гидролизаты мяса, дрожжевой экстракт и т.д. Натуральные питательные среды представляют собой неизмененные нативные (природные) компоненты (сыворотка крови, яичный белок и др.). Различные потребнрсти микробов отдельных видов обусловливают большое разнообразие питательных сред. По консистенции питательные среды могут быть жидкими, полужидкими, плотными. Для придания плотной консистенции к жидкой среде добавляют агар-агар, представляющий собой продукт переработки особого вида морских водорослей. Агар-агар плавится при 80—86 °С, затвердевает при температуре около 40 "С и в застывшем состоянии придает среде плотность. В плотные среды добавляют 1,5—2 %, в полужидкие — 0,3—0,7 % агар-агара. В некоторых случаях для получения плотных питательных сред используют нативные компоненты (свернувшаяся сыворотка крови, свернувшийся яичный белок), которые сами по себе являются плотными. Преимуществом плотных питательных сред является возможность получения чистых культур микроорганизмов, а также сообществ микроорганизмов (колоний, бактериальных газо- .s нов), имеющих макроскопические размеры. По целевому назначению питательные среды делят на основные, элективные и дифференциально-диагностические. К основным относятся среды, применяемые для выращивания многих бактерий. Это триптические гидролизаты мясных, рыбных продуктов, крови животных или казеина, из которых готовят жидкую среду — питательный бульон и плотную — питательный агар. Такие среды также служат основой для приготовления сложных питательных сред — сахарных, кровяных и др., удовлетворяющих пищевые потребности патогенных бактерий. Элективные питательные среды предназначены для избирательного выделения и накопления микроорганизмов определенного вида (или определенной группы) из материалов, содержащих разнообразную постороннюю микрофлору. При создании элективных питательных сред исходят из биологических особенностей, которые отличают данные микробы от большинства других. Например, избирательный рост стафилококков наблюдается при повышенной концентрации хлорида натрия, холерного вибриона — в щелочной среде и т.д. Дифференциально-диагностические питательные среды применяют для различения (дифференциации) отдельных видов (или групп) микробов. Принцип составления этих сред основан на различиях в биохимической активности бактерий разных видов вследствие неодинакового набора ферментов. В состав дифференциально-диагностической среды входят следующие компоненты: а) основная питательная среда, обеспечивающая размножение бактерий, б) определенный углевод (например, лактоза), способность использовать который является диагностическим признаком для данного вида, в) цветной индикатор (например, индикатор Андреде), изменение цвета которого свидетельствует о сдвиге рН среды в кислую сторону вследствие ферментации соответствующего углевода. Дифференциально-диагностические среды широко используют в лабораторных микробиологических диагностических исследованиях для дифференциации и идентификации бактерий. Культивирование бактерий применяют, в частности, для выделения и идентификации чистых культур (схема 3.1). а Выделение чистой культуры бактерий Выделение отдельных видов бактерий из исследуемого материала, содержащего, как правило, смесь различных микроорганизмов, является одним из этапов любого бактериологического исследования, проводимого с различными целями: диагностики заболеваний, определения микробной обсеменен-ности окружающей среды и т.д. Чистой культурой называется популяция бактерий одного вида или одной разновидности, выращенная на питательной среде. Многие виды бактерий подразделяют по одному признаку на биологические варианты — биовары. Биовары, различающиеся по биохимическим свойствам, называют хемовара-ми, по антигенным свойствам — сероварами, по чувствительности к фагу — фаговарами и т.д. Культуры микроорганизмов одного и того же вида или биовара, выделенные из различных источников либо в разное время из одного и того же источника, называют штаммами, которые обычно обозначают номерами или какими-либо символами. Колония представляет собой видимое изолированное сообщество микроорганизмов одного вида, образующееся в результате размножения одной бактериальной клетки на плотной питательной среде (на поверхности или в глубине ее). а Методы выделения чистой культуры Для выделения чистой культуры применяют методы, основанные на: механическом разобщении бактериальных клеток; предварительной обработке исследуемого материала физическими или химическими факторами, оказыва ющими избирательное антибактериальное действие; избирательном подавлении размножения сопутствую щей микрофлоры физическими или химическими факторами во время инкубации посевов; способности некоторых бактерий быстро размножать ся в организме чувствительных к ним лабораторных животных (биопробы). Задание студентам Ознакомиться с питательными средами и основными ингредиентами для их изготовления. Выполнить I этап выделения чистой культуры аэробов из исследуемого материала, содержащего смесь бактерий: а) приготовить мазок из исследуемого материала и окрасить его по методу Грама, микроскопировать, оценить морфологию присутствующих бактерий и их концентрацию; б) засеять материал на чашку Петри с МП А, нанося материал петлей и последовательно распределяя его шпателем; в) наметить ход дальнейшего исследования по выделению чистых культур аэробных бактерий. ЗАНЯТИЕ 2 Программа II этап выделения чистых культур аэробных бактерий. Особенности культивирования анаэробов; характер роста анаэробов на специальных питательных средах. Демонстрация Различные типы колоний аэробных бактерий. Рост чистых культур анаэробов на средах Кита-Тароцци, Вейнберга, Вильсона-Блера, молоке и тиогликолевом бульоне. Техника отсева культуры из колоний на скошенный агар. Задание студентам 1. Выполнить II этап выделения чистой культуры аэробов из материала, содержащего смесь бактерий: а) учесть результаты посева исследуемого материала на чашке Петри с МПА, отметить наличие или отсутствие колоний, в случае неудачи проанализировать ее причины; б) определить, сколько типов колоний имеется на чашке, и зарисовать их; в) описать по принятой схеме колонии всех типов; г) приготовить мазки из колоний каждого типа и окрасить их по методу Грама, микроскопировать и занести данные в протокол; д) произвести отсев чистой культуры из колонии каждого типа на скошенный агар; е) наметить план дальнейшей работы. 2. Составить план выделения чистой культуры анаэробов. Методические указания Основные среды. Пептоныыи бульон. Выпускается в сухом виде; состав (г/л): триптический гидролизат кильки — 10,05; натрия хлорид — 4,95. Питательный агар. Состав (г/л): ферментативный гидролизат кормовых дрожжей — 12,0; агар — 12,5; натрия хлорид - 5,5; рН 7,3+0,1. Основные сложные среды— кровяные, сывороточные и асцитические. Их готовят путем добавления к питательному агару 5—10 % дефибринированной крови или сыворотки крови либо 25 % асцитической жидкости. Для приготовления жидкой среды такие же количества сыворотки или асцитической жидкости добавляют к питательному бульону. Агар Мюллера-Хинтон (основная плотная питательная среда для определения чувствительности бактерий к антибиотикам методом дисков): на 1 л дистиллированной воды 300 г мясного настоя (из говядины), 17,5 г гидролизата казеина, 1,5 г крахмала, 17 г агар-агара. Элективные питательные среды. Пептонная вода 1 %, рН 8,0. Избирательная для холерного вибриона, который размножается быстро, опережая рост других микроорганизмов. Щелочная реакция среды не препятствует росту возбудителя холеры Vibrio cholerae, но тормозит рост других микроорганизмов. Щелочной агар (плотная среда): питательный агар, рН 7,8, аналогично предыдущей среде элективен для V.cholerae. Среда Леффлера. Смесь 1 части лошадиной сыворотки и 3 частей сахарного бульона, скошенная в пробирках при нагревании в аппарате Коха, элективна для возбудителя дифтерии Corynebacterium diphtheriae. Желточно-солевой агар (ЖСА). Содержит повышенные концентрации хлорида натрия (8—10 %), которые не препятствуют размножению стафилококков, что обеспечивает элективность среды для данных микроорганизмов. Среда позволяет дифференцировать стафилококки, продуцирующие ле-цитиназу, от стафилококков, не выделяющих этот фермент, по образованию зон помутнения с перламутровым оттенком вокруг колоний лецитиназоположительных видов (фермент расщепляет лецитин куриного желтка, который вносится в расплавленный и остуженный до 45 °С питательный солевой агар). Среды для культивирования анаэробов. Среда Вильсона— Блера (железосульфитный агар). Готовится из питательного агара, к которому добавляют глюкозу, Na2SO3, FeCl2. Анаэробные клостридии (C.perfringens) на этой среде образуют колонии черного цвета за счет восстановления Na2SO3 в Na2S, который, соединяясь с хлоридом железа, дает осадок сульфида железа (FeS) черного цвета. Среда Китта—Тароцци. Состоит из питательного бульона, 0,5 % глюкозы и кусочков печени или мясного фарша для адсорбции кислорода. Перед посевом среду прогревают в течение 10—15 мин на кипящей водяной бане для удаления воздуха. После посева среду заливают небольшим слоем вазелинового масла. Тиогликолевый бульон с гемином (жидкая элективная среда для культивирования неспорообразующих анаэробов — представителей родов Bacteroides, Prevotella, Porphyro-monas): на 1 л дистиллированной воды 17 г гидролизата казеина, 3 г соевого гидролизата, 6 г глюкозы, 2,5 г хлорида натрия, 0,5 г тиогликолата натрия, 0,25 г L-цистеина, 0,1 г сульфата натрия, 5 мг гемина. Дифференциально-диагностические среды. Среды Гисса. К 1 % пептонной воде добавляют 0,5 % раствор определенного углевода (глюкоза, лактоза, мальтоза, маннит и др.) и индикатор Андреде (кислый фуксин в 1 н. растворе NaOH), разливают по пробиркам. В пробирки помещают поплавок (трубка длиной около 3 см, один конец которой запаян) для улавливания газообразных продуктов, образующихся при разложении углеводов. Среда при рН 7,2—7,4 бесцветна. При разложении углеводов она приобретает красный цвет. Среда Ресселя. Применяется при изучении биохимических свойств энтеробактерий (шигелл, сальмонелл). Содержит питательный агар, лактозу, глюкозу и индикатор бромти-моловый синий. Приготавливают в пробирках по 6—8 мл в виде столбика со скошенной поверхностью. Цвет незасеянной среды травянисто-зеленый. Посев делают штрихом по скошенной поверхности и уколом в глубину столбика. Микроорганизмы , ферментирующие глюкозу до кислоты, вызывают изменение окраски столбика среды из первоначальной травянисто-зе-г леной в желтую; скошенная поверхность при этом приобретает синий цвет. Лактозоположительные микроорганизмы (Е. со//) изменяют цвет столбика и скошенной части среды в желтый, Микроорганизмы, образующие щелочь, изменяют цвет среды в синий. Газообразование отмечается в толще столбика среды. Среда Эндо. Выпускается в виде порошка, который состоит из высушенного питательного агара с 1 % лактозы и индикатора — основного фуксина, обесцвеченного сульфитом натрия. Свежеприготовленная среда бесцветна или бледно-розовая. При росте лактозоположительных бактерий их колонии окрашиваются в темно-красный цвет с металлическим блес-koivi; лактозоотрицательные бактерии образуют бесцветные колонии. Среда Плоскирева (б актоагар Ж). Выпускается в сухом виде и содержит питательный агар с лактозой, бриллиантовым зеленым, солями желчных кислот, минеральными солям: и и индикатором (нейтральный красный). Эта среда является не только дифференциально-диагностической, но и селективной, так как подавляет рост многих микроорганизмов (кишечная палочка и др.) и способствует лучшему росту некоторых патогенных бактерий (возбудители брюшного тифа, пара-тифов, дизентерии). Лактозоотрицательные бактерии образуют на этой среде бесцветные колонии, а лактозоположительные — красные. Висмут-сульфит агар. Выпускается в сухом виде; содержит триптический гидролизат кильки, глюкозу, неорганические соли, бриллиантовый зеленый, агар. Среда предназначена для выделения сальмонелл. Дифференцирующие свойства среды основаны на способности микроорганизмов продуцировать Н2S, который вступает в реакцию с цитратом висмута и образует соединение черного цвета — сульфит висмута. Среда резко угнетает рост сопутствующей микрофлоры за счет инги-бирующего действия бриллиантового зеленого и сульфита натрия. Техника посевов и пересевов культур микроорганизмов. Универсальным инструментом для производства посевов является бактериологическая петля (металлическая многоразовая или пластмассовая одноразовая). Кроме нее, для посева уколом применяют специальную бактериологическую иглу, а для посевов на чашки Петри — металлические, стеклянные или пластиковые шпатели. Для посевов жидких материалов наряду с петлей используют пастеровские и градуированные пипетки. Первые предварительно изготовляют из стерильных легкоплавких стеклянных трубочек, которые вытягивают на пламени в виде капилляров. Конец капилляра сразу же запаивают для сохранения стерильности. У пастеровских и градуированных пипеток широкий конец закрывают ватой, после чего их помещают в специальные пеналы или обертывают бумагой и стерилизуют. Все манипуляции с микробами осуществляют с помощью стерильных инструментов вблизи пламени горелки. Металлическую бактериологическую петлю перед использованием, после каждой манипуляции и по окончании работы стерилизуют путем прокаливания в пламени горелки. Культивирование микробов осуществляют посевом их на питательные среды с последующей инкубацией в оптимальных условиях температуры, влажности, газового состава атмосферы и т.д. С этой целью материал, содержащий микроорганизмы (материал от больного, из чистой культуры, из изолированной колонии и т.д.), помещают (засевают) в жидкие или на плотные среды. В последнем случае посев может быть произведен как на поверхность, так и в глубину агара уколом. Предварительно посуду (пробирку, чашки Петри и др.) надписывают, указывая Дату посева и характер посевного материала (номер исследования или название культуры). В зависимости от техники посева и концентрации микробов в посевном материале бактерии на поверхности плотной питательной среды могут давать равномерный сплошной рост — бактериальный газон, "сливной рост" (возникает при помещении большого количества микроорганизмов на ограниченный участок поверхности агара) или образовывать изолированные колонии. Техника посева материала на плотную питательную среду. Получение изолированных колоний. Образование изолированных колоний достигается путем механического разобщения микробов при посеве. С этой целью материал, взятый петлей, наносят на поверхность агара параллельными штрихами, чем достигается последовательное уменьшение концентрации бактерий вплоть до единичных клеток. Для снижения концентрации бактерий можно также зигзагообразными движениями густо нанести материал на небольшой участок агара в верхней части чашки Петри, после чего петлю стерилизуют, а материал распределяют параллельными штрихами по остальной части среды. Другой способ состоит в приготовлении суспензии с малой концентрацией бактерий. Одну каплю такой суспензии наносят петлей на поверхность питательного агара в чашку Петри и тщательно втирают стерильным шпателем в среду, равномерно распределяя материал по всей ее поверхности. Получение бактериального газона. Посевы "газоном" производят шпателем на питательный агар в чашке Петри. Для этого, приоткрыв левой рукой крышку, петлей или пипеткой наносят посевной материал на поверхность питательного агара. Затем проводят шпатель через пламя горелки, остужают его о внутреннюю сторону крышки и растирают материал по всей поверхности среды. После инкубации посева появляется равномерный сплошной рост бактерий. Получение сливного роста. В пробирку со скошенным агаром вносят петлю с посевным материалом, опуская ее до конденсата в нижней части среды, и зигзагообразным движением распределяют материал по скошенной поверхности агара. Вынув петлю, обжигают край пробирки и закрывают ее пробкой. Петлю стерилизуют в пламени горелки и ставят в штатив. Техника стерильной работы с пробиркой и бактериологической петлей описана в теме 2.1. Выделение чистых культур бактерий (ЧК) I этап — получение изолированных колоний бактерий из исследуемого материала. При выделении ЧК бактерий из испытуемого материала первоначально необходимо оценить концентрацию бактерий в материале. На I этапе выделения ЧК также осуществляют первоначальную идентификацию бактерий по морфологии и тинкториальным свойствам. Для решения этих задач из исследуемого материала готовят фиксированный мазок, окрашивают по методу Грама (или другими методами в зависимости от цели исследования) и микроскопируют. Если количество бактерий в поле зрения велико, исследуемый материал разводят в пробирке со стерильным изотоническим раствором хлорида натрия. При малом количестве бактерий в препарате весь объем образца засевают на жидкие среды обогащения с целью увеличения концентрации бактерий. При необходимости выделения определенного вида бактерий посев осуществляют на элективные среды. Для выделения ЧК бактерий из испытуемого материала необходимо сначала разобщить находящиеся в нем микробы разных видов. Обычно для этого посев материала производят на плотную питательную среду таким образом, чтобы получить изолированные колонии присутствующих в нем бактерий (см. выше). После посева чашку переворачивают дном кверху, подписывают и помещают в термостат при 37 °С на 18—24 ч. Иногда применяют метод пластинчатых разводок, который заключается в перемешивании различных разведений исследуемого материала с расплавленным и остуженным питательным агаром в колбе или пробирке. После этого агар разливают в чашки Петри и инкубируют в термостате. Разделение бактерий с использованием физических и химических факторов осуществляют следующим образом. Для выделения спорообразующих бактерий уничтожают неспорообразую-щие, прогревая исследуемый материал при 80 °С в течение 20 мин или подвергают кратковременному кипячению. Споры бактерий при этом сохраняются и при посеве прогретого материала на питательную среду прорастают. Если материал содержал только один вид спорообразующих бактерий, таким образом можно получить ЧК. Если материал содержал споры разных бактерий, дальнейшее выделение осуществляют стандартными методами. При выделении ЧК психрофильных бактерий используют инкубацию при низких температурах, задерживающих рост сопутствующей микрофлоры. Так, например, для выделения ЧК возбудителя чумы (Yersinia pestis) посевы инкубируют при температуре около 5 "С. В ряде случаев ЧК бактерий можно получить путем подавления размножения части микробов в исследуемом материале воздействием на них факторами, к которым выделяемый вид устойчив. С этой целью используют антимикробные препараты, химические вещества и бактериофаги. В питательную среду вносят соответствующее вещество или фаг в строго определенной концентрации, препятствующей размножению сопутствующих бактерий, но не оказывающей выраженного ингибиру-ющего действия на исследуемый микроорганизм. Кроме упомянутых, в бактериологической практике иногда применяют и другие методы. Например, для выделения чистой культуры бактерий рода Proteus (Proteus vulgaris) используют его способность к "ползучему" росту (метод Шукевича). При этом бактерии, засеянные в основание скошенного агара, за время культивирования распространяются по всей поверхности агара. II этап — накопление ЧК для ее дальнейшей идентификации. II этап начинают с оценки результатов первичного посева материала и изучения кулыпуральных признаков выросших бактерий — особенностей их роста на питательных средах. Морфология микробных колоний является наиболее информативным культуральным признаком. Колонии различаются по величине, форме, цвету, консистенции, контуру края, структуре и характеру поверхности (рис. 3.1.1). По величине колонии могут быть крупные (диаметр более 4—5 мм), средние (2—4 мм) и малые (1—2 мм), по форме — круглые, розеткооб-разные, листовидные и т.д. Цвет колонии зависит от выработки определенного пигмента — белого, желтого, красного и др. Колонии непигментирующих бактерий бесцветны. По консистенции различаются сухие, влажные, сочные или слизистые колонии. Поверхность колонии бывает гладкой, морщинистой, исчерченной, плоской, выпуклой, вдавленной. Край колонии может быть ровным, волнистым, бахромчатым. Колонии могут иметь аморфную, зернистую, волокнистую внутреннюю структуру. При получении микробного газона характер роста бактерий может быть сухим, влажным, "ползучим", складчатым, пигментированным. В жидкой питательной среде одни бактерии дают диффузное помутнение, другие характеризуются придонным или пристеночным ростом; некоторые культуры образуют пленки на поверхности среды, другие — осадок на дне пробирки, что преимущественно определяется потребностью в кислороде. Для оценки результатов первичного посева исследуемого материала чашки с посевами просматривают и изучают морфологию выросших колоний. Для определения морфологии бактерий и их тинкториальных свойств из материала колоний разных типов готовят мазки, окрашивают по методу Грама и микроскопируют. Необходимо помнить, что родственные бактерии могут отличаться по морфологии колоний и наоборот. Материал из изолированной колонии каждого типа пересевают в отдельные пробирки со скошенным агаром или какой-либо другой питательной средой. Для этого часть колонии снимают петлей, не задевая соседние колонии, и засевают штрихом на скошенную поверхность агара в пробирку. Для выделения и накопления чистой культуры выбирают колонии только тех бактерий, которые присутствовали в исследуемом материале. Появление колоний других бактерий может быть результатом контаминации (загрязнения) посева посторонними микробами  вследствие недостаточно строгого соблюдения стерильных условий работы. Особенности культивирования анаэробных бактерий. Все манипуляции со строгими анаэробами должны осуществляться в бескислородных условиях. Для этого используют герметичные настольные камеры с регулируемым газовым составом среды. Посевы производят на специальные обогатительные (элективные) среды для анаэробов (тиогликолевую, Китта—Тароцци). Посевы инкубируют в специальных СО2-инкубаторах или в анаэростатах (металлических или пластмассовых контейнерах, герметично закрывающихся крышкой, снабженной патрубками для заполнения газовой смесью нужного состава), которые помещают в обычный термостат. Для инкубации небольших по объему посевов (1—2 чашки Петри) применяют пластиковые пакеты, содержащие химические генераторы газовой смеси, которые обеспечивают полное удаление кислорода из воздушной среды в течение нескольких минут. |
