РУКОВОДСТВО ПО ОБЩЕЙ ХИРУРГИИ. Руководство по общей хирургии Учебное пособие. М. Оао Издательство Медицина
 Скачать 9.28 Mb. Скачать 9.28 Mb.
|
|
Диагностика. При клиническом исследовании крови выявляются анемия, увеличение СОЭ, лейкоцитоз (до 14—30 • 109/л), сдвиг лейкоцитарной формулы влево. При тяжелом течении перитонита нередко определяется лейкопения, что является неблагоприятным признаком. Естественной реакцией организма на проявления интоксикации являются изменения лейкоцитарной формулы крови, поэтому в 1941 г. врач-терапевт Я. Я. Кальф-Калиф предложил лейкоцитарный индекс интоксикации (ЛИИ), основанный на учете различных клеточных группировок лейкоцитарного ряда крови. Определяют ЛИИ по следующей формуле: — (4 мц + Зю + 2п + с) • (пл.кл. + 1) J,J/lJ/l (мон. + лимф.) • (э + 1) ' где мц. — миелоциты, ю. — юные, п. — палочкоядерные, с. — сегментоядерные, пл.кл. — плазматические клетки, мон. — моноциты, лимф. — лимфоциты, э. — эози-нофилы. В норме ЛИИ 0,3—1,5. Увеличение индекса до 3,0 у.е. свидетельствует о преимущественно ограниченном характере воспалительного процесса в брюшной полости. Повышение ЛИИ до 4,0 у.е. и более указывает на распространенный характер воспаления брюшины и выраженную эндогенную интоксикацию организма. Нетрудно заметить, что повышение ЛИИ связано с исчезновением эозинофилов, увеличением количества сегментоядерных, палочкоядерных, снижением числа лимфоцитов и моноцитов, появлением плазматических клеток, что свидетельствует об угнетении иммунных защитных сил, а появление в циркуляции молодых и незрелых форм свидетельствует о напряженности компенсаторных механизмов, обеспечивающих дезактивацию токсинов. Лейкоцитоз крови не всегда является достаточным критерием тяжести перитонита, поэтому следует обращать внимание на морфологическое и биохимическое исследования лейкоцитов, которые позволяют правильнее оценить состояние больного. К этим методам относится определение степени регенеративного сдвига форм нейтрофилов (ГСН), который рассчитывают по формуле: _ миелоциты + юные + палочкоядерные сегментоядерные В норме этот показатель равен 0,05—0,08. При тяжелых формах перитонита индекс достигает 1—2. При стертой клинической симптоматике, затруднениях клинической диагностики перитонита могут быть предприняты дополнительные исследования. При обзорном рентгенологическом исследовании в вертикальном положении больных с распространенным перитонитом обнаруживают признаки функциональной кишечной непроходимости: выраженное вздутие всех отделов желудочно-кишечного тракта и скопление жидкого содержимого в просвете желудка и кишечника и др. Важным признаком распространенного перитонита является наличие свободной жидкости в брюшной полости, которая выявляется на снимках, выполненных в горизонтальном положении больного, и характеризуется появлением однородных полигональных теней разных размеров, располагающихся между кишечными петлями, затемнением и расширением латеральных каналов. Рентгенологическое исследование органов грудной клетки выявляет смещение кверху и ограничение подвижности диафрагмы, дисковидные ателектазы в базальных отделах легких, особенно при распространении воспалительного процесса на верхний этаж брюшной полости. Эхографическое исследование позволяет объективно оценить динамику развития воспалительного процесса в брюшной полости В особо сложных случаях, особенно на ранних этапах развития перитонита, предпринимают диагностическую лапароскопию {рис. 17.16). Получае- 458 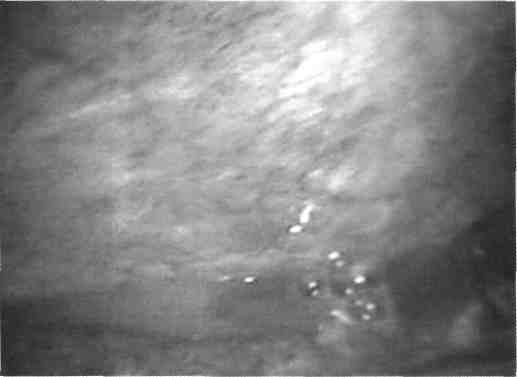 Рис. 17.16. Диагностическая видеолапароскопия — картина местного перитонита (распространение жидкости ограничивается подпеченочным пространством). мая при видеолапароскопия информация позволяет во всех случаях правильно поставить диагноз перитонита: выявляются экссудат и его характер (серозный, серозно-фибринозный, гнойный), а также изменения париетальной и висцеральной брюшины (гиперемия, отек, наложения фибрина) {рис. 17.17). Лечение. Основывается на применении комплекса мероприятий патогенетического воздействия: хирургическом вмешательстве; антибактериальной терапии; интенсивной инфузионной терапии, направленной на дезинтоксикацию, улучшение микроциркуляции, компенсацию водно-электролитных, белковых и энергетических потерь; гипербарической оксигенации; афферентных методах активной гемокоррекции; борьбе с парезами и кишечной недостаточностью; лечении послеоперационных осложнений. Оперативное лечение больных с перитонитом включает радикальное устранение источника перитонита, декомпрессию желудочно-кишечного тракта, тщательную санацию и рациональное дренирование брюшной полости. Операцию проводят под общим обезболиванием или перидуральной анестезией как на этапе самой операции, так и в послеоперационном периоде. Адекватным оперативным доступом является только срединная лапарото-мия.
459 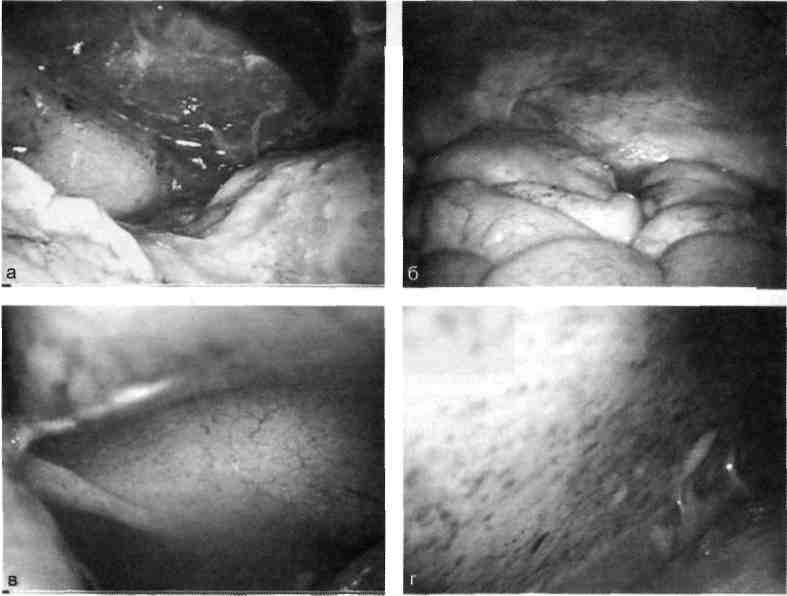 Рис. 17.17. Диагностическая видеолапароскопия (распространенный перитонит). Одновременное обнаружение экссудата в подпеченочном пространстве (а); правом боковом канале (б); малом тазе (в); левом боковом канале (г). При ревизии в первую очередь необходимо исключить наиболее частые причины возникновения перитонита, а именно прободную язву желудка или двенадцатиперстной кишки, острый деструктивный аппендицит, холецистит и панкреатит, повреждения полых органов. Для этого сначала поэтапно тщательно осматривают все органы верхнего этажа брюшной полости, а затем — нижнего. У женщин ревизию следует начинать с органов малого таза, осматривая матку и ее придатки, мочевой пузырь, сигмовидную кишку. Это позволяет подтвердить или исключить перитонит на почве гнойных гинекологических и онкологических заболеваний. После выявления источника распространенного перитонита приступают к его устранению с помощью наименее травматичного и технически легко исполнимого хирургического пособия. В случае если удалить источник перитонита не представляется возможным, его следует надежно отграничить тампонами, локализовав таким образом от свободной брюшной полости. Третьим вариантом ликвидации источника перитонита является его дренирование, показанием к которому служат неудалимый гнойно-некротический очаг в брюшной полости, распространение гнойно-некротического процесса на забрюшинную клетчатку. Заключительную санацию брюшной полости осуществляют одномоментно или методами «продленной санации». Она преследует двойную цель: механическое очищение с максимальным удалением инфицированного и ток- 460 сичного содержимого и лечебное (медикаментозное) воздействие. Для решения первой задачи применяют 6—12 л слабогипертонических растворов солей (раствор Рингера—Локка) и антисептиков (фурацилин 1:5000, 0,01— 0,02 % раствор хлоргексидина). Для усиления эффекта механического очищения в состав санирующих жидкостей включают раствор перекиси водорода (на 1,0 л жидкости добавляют 100,0 мл 3 % раствора перекиси водорода). На заключительном этапе санации брюшную полость орошают растворами антибиотиков (с учетом вида микрофлоры экссудата) в комбинации с препаратами группы метронидазола. В настоящее время достаточно широко применяют метод электрохимической детоксикации — брюшную полость после промывания растворами антисептиков тщательно осушают, после чего в нее однократно вливают 400—600 мл раствора гипохлорита натрия в концентрации 900—1200 мг/л. Брюшную полость дренируют полихлорвиниловыми трубками, которые перед вливанием раствора гипохлорита пережимают. Дренажи открывают через 1,5—2 ч после операции; в среднем требуются 2—3 таких сеанса. Непрямое электрохимическое окисление (НЭХО) крови относится к альтернативным, немедикаментозным методам лечения. Внутривенное введение 0,004 % гипохлорита натрия в количестве 10 мл на 1 кг массы тела больного оказывает выраженный детоксикационный эффект, способствует быстрому (в течение 3—7 сут) купированию воспалительного процесса в брюшной полости и симптомов вторичного иммунодефицита. Местное лечение перитонита осуществляют также сочетанным применением раствора гипохлорита натрия с лазеротерапией. Обязательным компонентом санации является удаление «обсемененных» микроорганизмами напластований фибрина с петель кишечника и брюшины. Применяют иммобилизованные ферменты (профезим, иммозимаза) с экспозицией на 6—8 ч для усиления протеолиза фибринных наложений, плотно фиксированных к брюшине. Качественной механической очистке париетальной и висцеральной брюшины от фибринозных наложений способствует применение низкочастотного ультразвука, пульсирующей струи антисептиков. В качестве озвучиваемой среды используют раствор фурацилина, водный раствор хлоргексидина, раствор фурагина или антибиотиков широкого спектра действия; озвучиванию подвергают все анатомические пространства брюшной полости поочередно, в течение 7—10 мин. Озонотерапия играет значительную роль в комплексном лечении перитонита. Механизм местного действия озонотерапии связан с активацией метаболизма и энергетики клеточных структур кишечника, усилением гликолиза, позволяющим сохранить жизнеспособность и структурную целостность энтероцитов. Однако даже самое тщательное интраоперационное промывание брюшной полости озонированными растворами не всегда достигает цели полной санации, так как между складками брюшины и петлями кишечника может остаться патогенная микрофлора. Поэтому санацию брюшной полости следует проводить и в послеоперационном периоде. Пролонгированный перитонеальный лаваж применяют, когда после первичного промывания в брюшной полости на петлях кишечника остаются фибринозные наложения, являющиеся хорошим адсорбентом токсинов и микроорганизмов. В послеоперационном периоде они могут вызвать про-грессирование перитонита и другие осложнения. Основными целями процедуры являются радикальное удаление источника перитонита и создание надежного герметизма брюшной полости. 461 Существуют две принципиальные схемы перитонеального лаважа: проточный (непрерывный) и фракционный (периодическое введение в брюшную полость определенных дозированных объемов раствора, который удаляют также через определенный промежуток времени). Диализирующий раствор готовят следующим образом: на 1000 мл дистиллированной воды берут один из антибиотиков (в соответствии с видовым составом микрофлоры), террилитин 10 мг, хлорофиллипт 10 % раствор 10 мг, диоксидин 1 % раствор 10 мл, трипсин или химотрипсин или химопсин 50 мг, 10 000 ЕД гепарина, 30 000—60 000 ЕД контрикала или 400 000 ЕД гордокса, а также хлорида натрия 12,2, хлорида калия 0,6, хлорида кальция 0,6, хлорида магния 0,2, гидрокарбоната натрия 0,6, глюкозы 12. Состав диализата может быть и другим. На 3—4-е сутки выводимый из брюшной полости раствор становится прозрачным, объем его совпадает с вводимым. Верхние (ирригационные) трубки удаляют на 5—6-е сутки, нижние (дренажные) трубки удаляют через 2—3 сут после удаления верхних. На сегодняшний день в арсенале хирурга находится несколько вариантов завершения оперативного вмешательства. Ушивание лапаротомной раны с дренированием — наиболее часто используемый вариант завершения операции при перитоните. Дренирование брюшной полости при распространенном перитоните является обязательным звеном оперативного вмешательства. Метод программированных релапаротомий осуществляется в послеоперационном периоде в определенные установленные сроки (чаще с перерывами в 1—3 дня), когда выполняют релапаротомию, тщательную санацию брюшной полости с последующим ее ушиванием с помощью особых швов. С целью повторных санаций брюшной полости при перитоните используют и малоинвазивные методы — санацию с помощью видеолапароскопической техники. Через наложенную гильзу при необходимости повторно вводят лапароскоп, накладывают пневмоперитонеум, промывают брюшную полость ги-похлоритом натрия и т. д. При открытом ведении брюшной полости при перитоните (лапаростомия) после основных этапов оперативного вмешательства лапаротомную рану не ушивают наглухо, чтобы в послеоперационный период проводить ее систематическую ревизию и повторную санацию. Брюшную полость окончательно закрывают и ушивают лапаротомную рану только после полного купирования перитонита. После завершения основных этапов операции по поводу перитонита петли кишечника защищают салфеткой с мазью или антисептиком, поролоном, а края раны только частично сводят редкими швами через все слои передней брюшной стенки или накладывают кольцевые швы, либо используются специальные сводящие рану приспособления: наложение кольцевидных швов; использование спиц Киршнера; вшивание «замка-молнии». Одним из важнейших этапов оперативного вмешательства при распространенном перитоните является декомпрессия желудочно-кишечного тракта. Оптимальным вариантом интубации кишечника является трансназальный способ. Принципы инфузионной терапии распространенного перитонита в послеоперационный период включают: • восполнение дефицита ОЦК, регуляция волемии и нормализация центральной гемодинамики; 462 Таблица 17.5. Специфическая антибактериальная терапия
* Фторхинолон (левофлоксацин, офлоксацин, пефлоксацин, ципрофлоксацин).
Специфическая антибактериальная терапия, не подменяя хирургическую санацию и другие компоненты медикаментозной терапии, существенно влияет на эффективность лечения перитонита (табл. 17.5). Основные принципы детоксикационной терапии и иммунокоррекции распространенного перитонита приведены в разделе «Эндогенная интоксикация в хирургии и принципы ее коррекции». 17.5.2. Эмпиема Эмпиема (греч. — гнойник) — скопление гноя в естественных, т. е. в анатомических и существующих полостях — плевральной, желчном пузыре, суставе. 463 Эмпиема плевры (empiema pleurae) (гнойный плеврит — pleuritis purulen-ta) — частный случай эмпием, воспаление висцеральной и париетальной плевры с накоплением гнойного экссудата или гнойно-фибринозных масс в образовавшейся между ними полости. Эмпиема плевры развивается как осложнение гнойно-деструктивных заболеваний легких (абсцессы, гангрена и др.), паразитарных или врожденных кист легкого, при распаде злокачественной опухоли легкого, кавернозном туберкулезе легких в случае прорыва каверны в плевральную полость, ранений и травм груди, после оперативных вмешательств на органах грудной клетки, сопровождавшихся массивной кровопотерей. Инфицирование плевральной полости может произойти лимфогенным или гематогенным путем из внелегочных очагов гнойной инфекции (деструктивный панкреатит, подциафрагмальный абсцесс и др.). Особенно часто это осложнение развивается у ослабленных больных, страдающих сахарным диабетом, хроническим алкоголизмом. Эмпиема плевры — полиэтиологическое заболевание. Различают неспецифическую, специфическую и смешанную эмпиему. Основными возбудителями эмпиемы, ассоциируемой с абсцессом легкого, являются анаэробы. Эмпиема как осложнение после хирургического вмешательства вызывается преимущественно аэробными грамотрицатель-ными бактериями или S. aureus. Специфические эмпиемы плевры вызываются туберкулезными палочками, реже грибковой флорой. Смешанной эмпиему считают в тех случаях, когда в экссудате находят и туберкулезные палочки, и другие микроорганизмы (S. aureus, S. pneumonie, S. pyogenes). Изменения в плевре могут нарастать остро или постепенно с развитием экссудативного, фибринозного или гнойно-фибринозного плеврита. При гнойно-деструктивных заболеваниях легких эмпиема чаще начинается с прорыва абсцесса в плевральную полость и протекает по типу пиопневмо-торакса с тяжелой клинической картиной вследствие раздражения огромного рецепторного поля плевры и значительного всасывания токсинов. При ранениях и травмах груди микробное загрязнение плевры из окружающей среды происходит в момент ранения (осколки, инородные тела, обрывки одежды) или в последующем через рану грудной стенки или поврежденные отделы бронхиального дерева. Чаще эмпиема развивается у раненых с открытым пневмотораксом, свернувшимся гемотораксом. После торакальных операций развитию эмпиемы плевры способствуют замедленное расправление легкого из-за негерметичности легочной паренхимы, ателектаза или наличия активного воспалительного процесса в оставшейся части легкого. Нередко эмпиема развивается как следствие первичной несостоятельности культи бронха, нагноения свернувшегося гемоторакса или раны грудной стенки. Эмпиемы классифицируют в зависимости от степени деструкции легкого; по характеру сообщения с внешней средой: закрытые и открытые эмпиемы; по распространенности гнойного процесса: отграниченные и распространенные; по длительности течения: острую и хроническую. Отграниченные эмпиемы могут иметь самую разную локализацию. Нередко встречаются многокамерные эмпиемы плевры. | ||||||||||||||||||||||||||||||||||||
