учебник. Учебник ФЛ - Виноградов, Каткова 2016. Учебник для медицинских и фармацевтических учреждений среднего профессионального образования Под
 Скачать 5.41 Mb. Скачать 5.41 Mb.
|
Противоаритмические средстваПротивоаритмические средства (ПАС) применяются при различных наруше- ниях ритма сердечных сокращений; при тахиаритмиях снижают возбудимость и автоматизм проводящей системы сердца, подавляют активность эктопических (гетеротопных) очагов возбуждения; при брадиаритмиях восстанавливают авто- матизм синусового узла и проводимость импульсов в миокарде. Нарушения ритма сердечных сокращений разного характера и локализации осложняют многие заболевания сердца (миокардит, кардиосклероз, пороки, ИБС, ИМ), операции на этом органе, на крупных сосудах и легких; могут возникать при тяжелой травме, интоксикации и в других критических ситуациях, а также при наркозе (галотаном и др.), применении ряда фармакологических препаратов (адреномиметики, сердечные гликозиды, кофеин, аминофиллин). Аритмии зна- чительно утяжеляют состояние и создают угрозу для жизни больного. В каждом конкретном случае вид аритмии определяется по данным ЭКГ. В за- висимости от локализации патологического очага выделяют аритмии: надже лу дочковые (суправентрикулярные); же лу дочковы е. По характеру нарушений ритма различают: тахиаритмии (экстрасистолии, пароксизмальные тахикардии, трепета- ние, фибрилляция предсердий или желудочков и т. п.); брадиаритмии (различные виды блокад, синдром слабости синусового узла). Встречаются и более сложные смешанные варианты аритмий. Особенно опас- ны аритмии желудочковые, которые требуют немедленной терапии. В основе патогенеза разнообразных тахиаритмий лежат два самостоятельных механизмаилиихсочетание: нарушения образования импульсов — возникновение дополнительных к синусовому узлу водителей ритма (эктопических или гетеротопных очагов воз- буждения) в результате локально возросшего автоматизма. С этим механизмом может быть связано появление предсердных и желудочковых экстрасистолий, трепетание и фибрилляция (мерцание) предсердий, постоянная тахикардия пред- сердий, постоянная атриовентрикулярная (узловая) тахикардия, пароксизмаль- ная тахикардия желудочков при ИМ, фибрилляция желудочков; нарушения проведения импульсов как результат однонаправленного блока проведения и рециркуляции («re-entry» — «повторного входа», или «кругового движения») возбуждения в структурах проводящей системы в результате несо- впадения по времени рефрактерных периодов соседних участков миокарда. По такому типу возникают пароксизмальная тахикардия предсердий, трепетание предсердий (сочетанный механизм), пароксизмальная атриовентрикулярная (уз- ловая) тахикардия, пароксизмальная тахикардия желудочков, не связанная с ИМ. Непосредственные причины нарушений ритма разнообразны, наиболее общи- ми, по-видимому, являются местные нарушения электролитного обмена (дефицит K+ и Mg2+, избыток Na+ и Ca2+), возникающие в миокарде под влиянием гипоксии, воспалительного процесса, токсического или аутоиммунного повреждения, повы- шения тонуса симпатической иннервации, избытка гормонов щитовидной железы и т. п. Для лечения нарушений сердечного ритма назначаются ПАС, которые преду- преждают или корригируют нарушения ионного баланса волокон миокарда и про- водящей системы и восстанавливают таким образом связанные с ними функции: автоматизм, проводимость, возбудимость. Для лучшего понимания механизма действия различных ПАС на клеточном уровне необходимо иметь четкие пред- ставления о том, как происходит генерация электрических импульсов в клетках проводящей системы сердца. Физиологическим водителем ритма сердца в норме является синусовый (сино- атриальный, СА) узел, расположенный в стенке правого предсердия около устья верхней полой вены. От синусового узла импульсы передаются на атриовентрику- лярный узел, далее — на пучок Гиса и его ветви, затем на волокна Пуркинье. Эти образования представляют собой проводящую систему сердца. По ней импульсы достигают мышечных волокон желудочков, которые синхронно сокращаются. Графически процесс формирования импульса (потенциала действия, ПД) пред- ставлен на рис. 20. 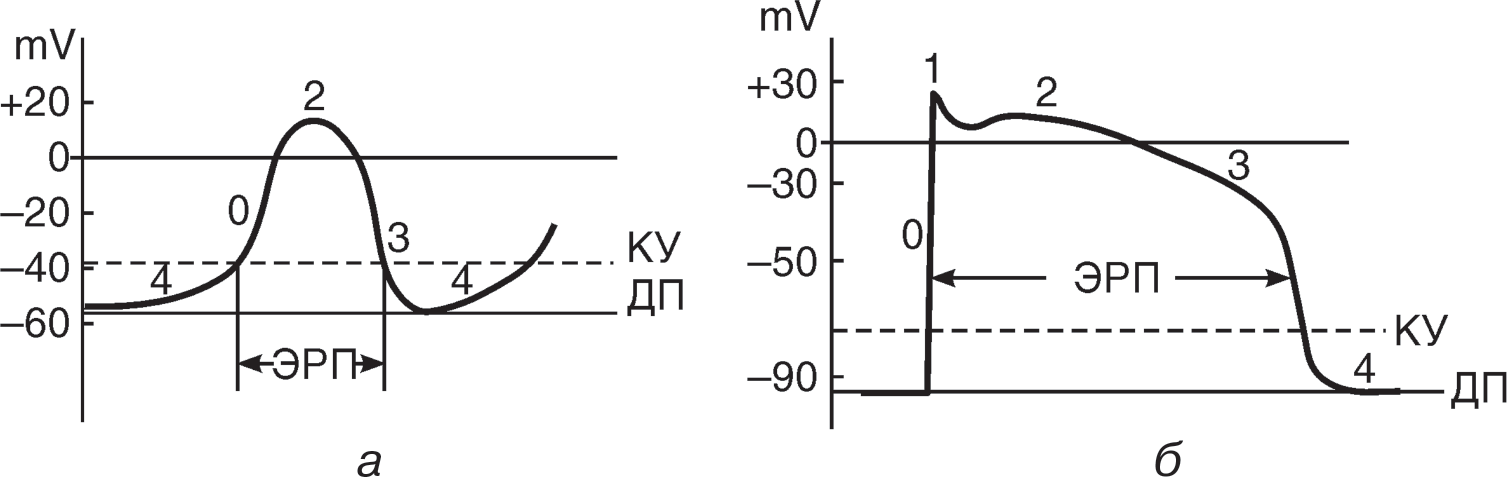 Рис. 20. Потенциал действия (ПД) клеток синусового узла (а) и клеток сократительного миокарда желудочков сердца (б) (объяснение в тексте): 4 — фаза спонтанной диастолической деполяризации (диастолы в желудочках); 0 — фаза быстрой де- поляризации; 1 — фаза начальной быстрой реполяризации (не выражена в синусовом узле); 2 — «пла- то»; 3 — фаза конечной быстрой реполяризации; КУ — критический уровень быстрой деполяризации; ДП — диастолический потенциал; ЭРП — эффективный рефрактерный период Клетки синусового узла обладают уникальной способностью к медленной спонтанной деполяризации (автоматизму) в период диастолы (фаза 4 потенциала действия); в других участках проводящей системы в норме функция автоматизма выражена слабее и подавлена более высоким автоматизмом СА-узла. Этот про- цесс в синусовом узле связан с вхождением ионов кальция по медленным кальци- евым каналам внутрь клетки во время диастолы. Как только диастолическая депо- ляризация достигает критической величины, происходит резкое скачкообразное увеличение проницаемости мембраны для ионов кальция (или натрия), развива- ется быстрая деполяризация (фаза 0 потенциала действия) и происходит распро- странение волны деполяризации на соседние участки мембраны. Вслед за этим развивается реполяризация клеточной мембраны, в которой выделяют три фазы: начальная быстрая реполяризация, связанная с выходом ионов калия (фаза 1), не выражена в клетках синусового узла; плато — вход ионов кальция и/или натрия на фоне продолжающегося вы- хода калия (фаза 2); конечнаябыстраяреполяризация(фаза 3), первоначально обусловленная ускоренным током калия из клетки, затем работой натрий-калиевого «насоса», восстанавливающего исходное соотношение ионов (потенциал покоя). Клетки сократительного миокарда имеют свои электрофизиологические осо- бенности (здесь в зарождении потенциала действия основную роль играет бы- стрый входящий ток ионов натрия, возникающий при поступлении импульса). Эти клетки названы клетками «быстрого ответа», в отличие от клеток синусового узла и отчасти атриовентрикулярного, характеризующихся «медленным отве- том». Возбуждение и сокращение миокарда в ответ на импульс возникает, если по- следний попадает в определенную фазу потенциала действия. В фазы 0, 1 и 2 воз- буждения не произойдет — это абсолютный рефрактерный период. Только в конце фазы 3 импульс повышенной мощности способен вызвать возбуждение. Время от начала потенциала действия до момента, когда может возникнуть следующий по- тенциал действия, обозначается как эффективный рефрактерный период (ЭРП). Рефрактерность препятствует круговому движению волны возбуждения по мио- карду, защищает миокард от слишком быстрого повторного возбуждения, кото- рое могло бы нарушить его сократительную функцию. Активирующее (ускоряющее) влияние на медленную деполяризацию мембра- ны (фаза 4 ПД), возникновение импульса и связанные с этим процессом функции миокарда (автоматизм, проводимость, возбудимость, сократимость) оказывает симпатическая иннервация (через бета1-адренорецепторы); тормозит автоматизм синусового узла и атриовентрикулярную проводимость, ослабляет сократимость предсердий — парасимпатическая (через М2-холинорецепторы). Фармакологические средства для лечения тахиаритмий различаются по спектру противоаритмического действия, механизмам развития эффекта, перено- симости больными и другим свойствам. По преобладающему механизму действия ПАС разделяются на четыре класса: I — мембраностабилизирующие (блокаторы натриевых каналов); II — бета-адреноблокаторы; III — замедляющие реполяризацию (блокаторы калиевых каналов); IV — блокаторы кальциевых каналов. Основные представители каждого класса ПАС представлены в табл. 73. В ряде случаев при тахиаритмиях применяются и другие средства: дигоксин, трифосаде- нин (натрия аденозинтрифосфат), магния сульфат, калия хлорид, калия и магния аспарагинат (панангин) и др. Таблица73 Классификация противоаритмических средств
Класс I — мембраностабилизирующие препараты. Общим свойством ПАС этого класса является способность блокировать потенциалзависимые натриевые каналы в мембранах волокон проводящей системы, через которые осуществля- ется вход ионов натрия в период деполяризации (фазы 0 и 4 ПД). В результате затягивается скорость развития потенциала действия. Препараты гораздо сильнее замедляют спонтанную деполяризацию и нарастание потенциала действия в оча- гах с частыми разрядами (в эктопических очагах возбуждения) и, подавляя их ав- томатизм, гасят аритмии. По характеру взаимодействия с натриевыми каналами ПАС I класса подразделяются на три группы: IA(хинидин, прокаинамид) — блокируют в основном активированные (откры- тые) натриевые каналы, замедляют преимущественно фазу 0 (быстрой деполяри- зации) и отчасти фазу 4; кроме того, блокируют калиевые каналы и замедляют процесс реполяризации (фаза 3), увеличивая таким образом продолжительность потенциала действия и эффективный рефрактерный период (время до возмож- ности начала очередного потенциала действия); I B (лидокаин и др.) — блокируют инактивированные (закрытые) натриевые каналы, быстро их освобождают и замедляют преимущественно фазу 4 (медлен- ной деполяризации), укорачивают фазу 2 (плато), при этом ускоряют реполяри- зацию и уменьшают длительность потенциала действия и эффективный рефрак- терный период (главным образом в волокнах Пуркинье и в мышце желудочков); IC(пропафенон,этацизини др.) — прочно связываются с активированными натриевыми каналами, очень медленно их освобождают и выраженно тормозят процесс деполяризации на всем протяжении (фазы 0 и 4), продолжительность по- тенциала действия существенно не изменяют. ПАС I A группы исторически были первыми (хинидинпредложен в 1918 г., прокаинамид— в 1950-е гг.), лучше других изучены в эксперименте и клинике. Отличаются высокой универсальностью и надежностью противоаритмического действия, но угнетают сократимость миокарда и дают наибольшее число побоч- ных и токсических реакций. Хинидин как более токсичный препарат сейчас в кли- нической практике не применяется. Противоаритмический эффект ПАС I А группы обусловлен способностью по- нижать возбудимость и автоматизм клеток в дополнительных (эктопических) очагах возбуждения, замедлять проводимость импульсов и удлинять эффектив- ный рефрактерный период. На автоматизм синусового узла препараты влияют слабее. Замедление проводимости главным образом в местах перехода волокон Пуркинье в мышечные волокна желудочков прерывает «круговое движение» вол- ны возбуждения. Умеренная холиноблокирующая активность, свойственная про- каинамиду и в большей степени хинидину, может привести к снятию вагусного тормозного влияния на синусовый узел, атриовентрикулярную проводимость и распространение предсердного ритма на желудочки, что, по-видимому, является одной из причин нередко наблюдающихся случаев усиления аритмии при лече- нии этими препаратами (аритмогенный эффект). ПоказаниямикприменениюпрепаратовIАгруппыявляются: различные виды желудочковых тахиаритмий; наджелудочковые аритмии (пароксизмальная тахикардия, фибрилляция предсердий и др.). Для ликвидации аритмии прокаинамид вводят внутривенно (медленно). Для поддерживающей терапии назначают внутрь. Дозы и схемы лечения подбирают индивидуально. Побочные эффекты: снижение сократимости миокарда и появление признаков сердечной недостаточности, понижение АД, в больших дозах может возникать атриовентрикулярная блокада; характерны также сухость во рту, нарушение зре- ния; при приеме внутрь тошнота, рвота. При длительном применении прокаина- мида могут быть и другие токсические явления — судороги, нервно-психические расстройства, состояние, похожее на системную красную волчанку. ПАС I B группы. Основными представителями группы являются местноане- стезирующие средства — лидокаини некоторые его аналоги (в РФ не применяют- ся). Обычно препараты хорошо переносятся больными, существенно не ухудшают сократимость миокарда и гемодинамику, отличаются высокой эффективностью при желудочковых тахиаритмиях. Механизм противоаритмического действия ПАС I B группы связан с подавле- нием автоматизма эктопических очагов возбуждения в желудочках за счет за- медления деполяризации в фазе 4. Они не оказывают отрицательного влияния на проведение потенциала действия и могут даже его ускорять (восстанавливать), устраняя «круговое движение» импульсов в желудочках. Не влияют в терапевти- ческих дозах на автоматизм синусового узла и сократимость миокарда. Лидокаин является препаратом выбора для лечения и профилактики различ- ных желудочковых тахиаритмий (экстрасистолии, тахикардии, фибрилляция), в том числе возникающих при ИМ, в послеоперационном периоде, при интокси- кации сердечными гликозидами. Для купирования желудочковой аритмии лидокаин вводят внутривенно сна- чала одномоментно (1,5 мг/кг за 2 мин), затем переходят на длительное капельное введение (1—4 мг/мин), действие препарата после инфузии сохраняется 2—3 ч. При оказании неотложной помощи больным ИМ, осложненным желудочковыми аритмиями, а также на период их эвакуации лидокаин (3,5—6 мг/кг с интервала- ми 3 ч) вводят внутримышечно, лучше в дельтовидную мышцу. Из побочных эффектов могут наблюдаться: головокружение, слабость, спутан- ность сознания, онемение языка и губ, понижение АД, очень редко блоки прове- дения, судорожные реакции. Поиск аналогов лидокаина с более длительным дей- ствием и удовлетворительно всасывающихся из кишечника ведется интенсивно. Из новых средств этой группы, назначаемых при желудочковых аритмиях внутрь, можно назвать мексилетин. ПАС I C группы — пропафенон, этацизин, лаппаконитина гидробромид (ал- лапинин)— по влиянию на натриевые каналы и электрофизиологические свой- ства миокарда отличаются от ПАС I А и I В групп. Пропафенон и этацизин незна- чительно блокируют и кальциевые каналы. ПАС I С группы характеризуются более избирательным подавляющим вли- янием на проводимость импульсов в атриовентрикулярном узле, системе Гиса — Пуркинье, желудочках, при этом практически не изменяют продолжительность потенциала действия и ЭРП. Пропафенон и этацизин могут незначительно сни- жать автоматизм синусового узла и сократимость миокарда. Препараты не пони- жают АД. Обладают высокой собственной аритмогенной активностью, поэтому применяются только при угрожающих жизни желудочковых и наджелудочковых тахиаритмиях, устойчивых к другим ПАС. Используют препараты под строгим врачебным контролем (мониторирование ЭКГ, АД и т. п.). Для купирования аритмий пропофенон вводят внутривенно ка- пельно, для поддерживающей терапии — внутрь. Этацизин и аллапинин назнача- ют внутрь. Побочные эффекты: тошнота, головокружение, атриовентрикулярная блокада, аритмии и др. Пропафенон проявляет М-холиноблокирующее и бета-адренобло- кирующее действие, может снижать сократимость миокарда. Класс II — бета-адреноблокаторы (пропранолол, метопролол и др.). По- мимо основного адреноблокирующего действия, некоторым из них (пропра- нолол) присуще сходное с ПАС I класса влияние на натриевую проницаемость мембраны в фазе 0 («хинидиноподобный» мембраностабилизирующий эффект). Однако при обычных клинических дозировках оно имеет второстепенное значе- ние. Основной же механизм противоаритмического действия связан с блокадой бета1-адренорецепторов в сердце и снятием аритмогенного действия катехола- минов (см. «Адреноблокаторы»). Бета-адреноблокаторы снижают кислородный запрос миокарда, выраженность ишемии и связанных с ней изменений электро- литного баланса, энергетического обмена и нарушений функциональных свойств клеточных мембран. Препятствуют тому ускорению спонтанной диастолической деполяризации, которое вызывают катехоламины, на процесс реполяризации практически не влияют. В результате подавляется автоматизм (фаза 4 ПД) сину- сового, атриовентрикулярного узлов и активность эктопических очагов возбуж- дения в желудочках. Снижение проводимости они вызывают преимущественно в атриовентрикулярном узле, что также обусловлено бета1-адреноблокирующим эффектом и доминированием тормозных влияний холинергической иннервации. Бета-адреноблокаторы особенно эффективны при наджелудочковых и желу- дочковых тахиаритмиях, обусловленных высоким симпатоадреналовым тонусом (нейрогенные, гормональные нарушения ритма, начальный период ИМ и т. п.). Применяются как для купирования (внутривенно), так и для поддерживающей терапии (внутрь) различных тахиаритмий. Недостатками препаратов являются снижение сократительной способности миокарда вплоть до ОСН, замедление проводимости — до атриовентрикуляр- ной блокады. Поэтому применение бета-адреноблокаторов может быть опасно в остром периоде ИМ при наличии признаков недостаточности сердца. Препара- ты неселективного действия (пропранолол) вызывают побочные эффекты, свя- занные с блокадой бета2-адренорецепторов других органов (бронхоспазм, похо- лодание конечностей из-за ухудшения периферического кровообращения и др.). Селективные бета1-адреноблокаторы (метопролол, атенолол и др.) таких ослож- нений практически не вызывают. Эсмолол— высокоселективный бета1-адреноблокатор, обладает ультракорот- ким хорошо управляемым действием (Т1/2 9 мин). Применяется для купирования тахиаритмии, в том числе во время и после операций. Вводится внутривенно ка- пельно под контролем ЭКГ и АД. Класс III — замедляющие реполяризацию (блокаторы калиевых кана- лов). Наибольший интерес из препаратов с таким действием представляет амио- дарон(кордарон). Он обладает широким спектром противоаритмической актив- ности, несколько более выраженной в отношении наджелудочковых аритмий. Ос- новной механизм противоаритмического действия связан с замедлением скорости реполяризации волокна (торможением выхода ионов калия в фазу 3 ПД) за счет блокады калиевых каналов, удлинением потенциала действия и значительным увеличением продолжительности эффективного рефрактерного периода. Амио- дарон проявляет также умеренное блокирующее действие на натриевые каналы, бета1-адренорецепторы в миокарде, слабо блокирует кальциевые каналы, т. е. от- части проявляет свойства ПАС I, II и IV классов. Обладает антиангинальным дей- ствием, оказывает альфа-адреноблокирующее действие, понижает АД. Как противоаритмическое средство амиодарон имеет ряд преимуществ: эф- фективность при различных видах наджелудочковых и желудочковых аритмий, возможность внутривенного и перорального введения, длительное действие (до 20—24 ч), отсутствие заметного отрицательного влияния на сократимость и про- водимость сердца, невысокий риск аритмогенного действия. При приеме внутрь максимальный терапевтический эффект наступает через 2—3 нед. и длительно сохраняется после отмены препарата. Т1/2 составляет в сред- нем 50 дней, препарат имеет склонность к кумуляции. При длительном приеме (месяцы) образуется желтовато-коричневый микроосадок в роговице глаза, ко- торый медленно рассасывается после прекращения приема. Возможны и другие побочные эффекты: головная боль, снижение АД, брадикардия, атаксия, паресте- зии, нарушения функций щитовидной железы (гипо- или гипертиреоз), печени, воспаление (пневмонит) и фиброз легких и др. Применяется в неотложных случаях при тяжелых тахиаритмиях (мерцатель- ная аритмия, фибрилляция предсердий, фибрилляция желудочков и т. п.) — вну- тривенно медленно; для поддерживающей терапии препарат назначают внутрь в таблетках. Дозы и схемы применения строго индивидуальны. Соталол— другой препарат класса III — обладает выраженной способностью блокировать калиевые каналы, а также свойствами неселективного бета-адрено- блокатора (II класс ПАС). Как и амиодарон, продлевает реполяризацию (фаза 3 ПД) и увеличивает рефрактерность во всех отделах сердца. Вместе с тем угнетает автоматизм синусового и атриовентрикулярного узлов, тормозит проводимость. Применяется при наджелудочковых и желудочковых тахиаритмиях. Назначают препарат внутрь для профилактики и поддерживающего лечения тахиаритмий. Т1/2 7—12 ч, длительность действия около 24 ч. В тяжелых случаях вводят внутри- венно. Побочныеэффектытакие же, как у неселективных бета-адреноблокаторов. Обладает собственным аритмогенным действием. Класс IV — блокаторы кальциевых каналов (верапамил, дилтиазем). Механизм их противоаритмического действия связан с блокадой «медленных» кальциевых каналов и угнетением входа кальция в клетку, вследствие чего замед- ляется кальцийзависимая деполяризация (фаза 4, отчасти фаза 0 ПД) в синусовом и в атриовентрикулярном узлах, подавляется автоматизм последних, замедляется атриовентрикулярная проводимость. Препараты понижают АД, обладают анти- ангинальной активностью. Верапамил и дилтиазем относятся к препаратам выбора для купирования наджелудочковых тахиаритмий (пароксизмальной наджелудочковой тахикар- дии, фибрилляции предсердий). Верапамил вводят внутривенно в дозе 5—10 мг за 2—3 мин (при необходимости повторяют через 30 мин), затем продолжают капельное введение (5 мкг/кг/мин) или назначают препарат внутрь (40—160 мг каждые 6 ч). При применении в высоких дозах верапамил (в меньшей степени дилтиазем) может снижать сократительную способность миокарда, сильно по- давлять активность синусового узла и вызывать атриовентрикулярную блокаду. К второстепенным побочным эффектам относятся запоры, отеки в области голе- ней, головная боль, утомляемость. Из других препаратов, используемых при тахиаритмиях, следует отметить следующие: аденозин— применяется исключительно для купирования приступов над- желудочковой тахикардии, в качестве препарата аденозина используется трифо- саденин (натрия аденозинтрифосфат); сердечный гликозид дигоксин—только при фибрилляции и трепетании предсердий; магниясульфат—вспомогательное средство при желудочковых тахиарит- миях; калияхлорид,калияи магнияаспарагинат(панангин,аспаркам)—при нару- шениях ритма на фоне гипокалиемии, при интоксикации сердечными гликозидами. Препараты для лечения брадиаритмий (различных видов блокад, синдро- ма слабости синусового узла). Непосредственными причинами брадиаритмий яв- ляются: атриовентрикулярный блок II—III степени (чаще всего); синоатриальный блок; блок пучка Гиса; предсердная асистолия с медленным замещающим узловым или желудоч- ковым ритмом. Эта патология обычно бывает следствием ИМ разной локализации, острых воспалительных и дистрофических процессов в миокарде, интоксикации сердеч- ными гликозидами и ПАС, холиномиметиками, солями калия. Крайнее выраже- ние брадиаритмии — приступы временной обратимой асистолии с остановками кровообращения и утратой сознания длительностью до 5 с и более (синдром Мор- ганьи — Адамса — Стокса). Тяжелая и упорная брадисистолия требует срочных мер лечения и применения искусственного водителя ритма. При наличии блокад в разных отделах проводящей системы с явлениями бра- дисистолии улучшить автоматизм и проводимость можно за счет снятия тормозных влияний вагуса атропином (0,1 % раствор по 0,5—1 мл в вену с интервалом 2—6 ч). Рассмотренные противоаритмические средства демонстрируют существую- щие представления о принципиальных подходах к лекарственному воздействию на аритмии. В табл. 74 в обобщенном виде приведены данные о выборе противо- аритмических препаратов при разных видах аритмий. Выбор препарата осущест- вляется с учетом его эффективности при определенном типе аритмии и наличия нередких противопоказаний (содержатся в справочниках, инструкциях к препа- ратам). Преимущества имеют препараты с минимальным проаритмогенным дей- ствием и низкой токсичностью. Таблица74 Выбор противоаритмических средств при разных видах аритмий
При острых, угрожающих жизни нарушениях ритма лечение проводится вну- тривенно, реже — внутримышечно. Оно осуществляется под постоянным (мони- торным) контролем за ритмом сердца (ЭКГ), уровнем АД и другими доступными в неотложной кардиологической практике показателями. Настойчивая и осто- рожная терапия продолжается до купирования аритмии или появления побочных реакций. Последние говорят о неэффективности данного ПАС и необходимости перехода на другой препарат или комбинацию или на электроимпульсное лече- ние. После ликвидации аритмии проводят поддерживающую терапию перораль- ным или иным способом, которую в зависимости от тенденции к рецидиву про- должают от нескольких дней до месяцев. Следует иметь в виду, что лечение аритмий — задача чрезвычайно трудная и ответственная. Наиболее квалифицированно она решается в специализирован- ных кардиологических (терапевтических и хирургических) клиниках. Далеко не всегда с устойчивой, рецидивирующей аритмией удается справиться с помощью ПАС, а при форсированном их применении возможен их собственный аритмоген- ный эффект и другие серьезные осложнения. Поэтому в трудных случаях, когда нарушение ритма сопровождается расстройствами внутрисердечной и общей ге- модинамики, в клиниках прибегают к электроимпульсной терапии под наркозом (кардиоверсия или дефибрилляция). Она, в частности, проводится при мерцании и трепетании предсердий, а в экстренном порядке в любых условиях — при фи- брилляции желудочков. Поскольку при последней происходит остановка крово- обращения, попытки лечить ее с помощью ПАС невозможны, а у врача остается лишь несколько минут на реанимацию. Поэтому задача фармакотерапии состоит лишь в предупреждении фибрилляции желудочков (например, при ИМ, передози- ровке сердечных гликозидов) и ее рецидивов после дефибрилляции. Показанием к лекарственной профилактике фибрилляции служит наличие ее предвестников: частые, особенно политопные (из разных очагов), экстрасистолии, желудочковая тахикардия и др. В специализированных кардиохирургических клиниках после сложной топи- ческой диагностики места аритмогенного очага, путей, обеспечивающих круговое движение возбуждения, через катетер может подводиться зонд, с помощью ко- торого осуществляется строго нацеленная точечная коагуляция очага путем воз- действия тока СВЧ или лазера. При этом в большинстве случаев удается добиться практически радикального устранения нарушений ритма. |
